La dehiscencia de anastomosis ocurre en 1 al 19% de los pacientes con cirugía colorrectal. El objetivo es presentar la primera serie de cirugía colorrectal en México en la que se utilizó la angiografía por fluorescencia con verde de indocianina para valorar la perfusión, previo a realizar la anastomosis.
Material y métodosEstudio retrospectivo, analítico y descriptivo. Se analizaron los expedientes de pacientes consecutivos con cirugía colorrectal de un mismo grupo de cirujanos colorrectales en los que se utilizó la angiografía con verde de indocianina.
ResultadosSe revisaron 21 expedientes de los cuales 11 (52.3%) eran mujeres, media de edad 57 años (38 a 82) y media de índice de masa corporal (IMC) 25 kg/m2(17 a 34). El diagnóstico fue enfermedad maligna en 15 (71.4%) pacientes. La angiografía cambió nuestra decisión terapéutica en tres (14.2%) casos. Dos anastomosis se hicieron colorrectales a menos de 5 cm del margen anal (14.2%), a menos de 5 cm del margen anal, 13 (61.9%) se hicieron a más de 5 cm, tres (14.2%) fueron ileo-colónicas, dos (9.5%) se hicieron colo-anales y una (4.7%) se hizo ileo-anal. Tuvimos seis (28.5%) complicaciones, no existió dehiscencia de anastomosis ni complicación asociada con el uso de verde de indocianina. Mortalidad de 0%.
ConclusiónPresentamos la primera serie de cirugía colorrectal en México en la que se utilizó la angiografía por fluorescencia con verde de indocianina con excelentes resultados.
Anastomotic leak occurs in 1-19% of colorrectal surgeries. Our objective was to present the first Mexican case series on colorrectal surgery using indocyanine green fluorescence angiography to evaluate perfusion prior to carrying out the anastomosis.
Materials and methodsA retrospective, analytic, descriptive study was conducted. We studied the case records of consecutive patients that underwent colorrectal surgery with indocyanine green angiography performed by the same group of colorrectal surgeons.
ResultsTwenty-one case records were reviewed. Eleven (52.3%) of the patients were women, mean patient age was 57 years (38-82), and mean body mass index was 25 kg/m2 (17-34). Fifteen (71.4%) patients were diagnosed with malignant disease. Indocyanine green angiography changed our therapeutic decision in three (14.2%) patients. Two colorrectal anastomoses (14.2%) were performed at fewer than 5 cm from the anal verge and 13 (61.9%) were performed at more than 5 cm from the anal verge. Three of the anastomoses were ileocolic (14.2%), two were coloanal (9.5%), and one was ileoanal (4.7%). There were six (28.5%) complications, no cases of anastomotic leak, and no complications associated with the use of indocyanine green. The mortality rate was 0%.
ConclusionThe present case series is the first on colorrectal surgery conducted in Mexico using indocyanine green fluorescence angiography, with excellent results.
La tasa de complicaciones en la cirugía de colon y recto es de 20 a 30% y la estancia intrahospitalaria varía entre seis y 12 días1–8. La dehiscencia de anastomosis (DA) es una de las complicaciones más temidas por los pacientes y cirujanos porque conlleva una alta tasa de morbilidad y mortalidad; además, se asocia con un mayor costo y estancia intrahospitalaria. La DA en enfermedad maligna colónica o rectal se ha vinculado con una tasa elevada de recurrencia y con menor sobrevida9–13. Ocurre en 1 al 19% de los pacientes con cirugía de colon y recto, y la incidencia es mayor entre más distal se confecciona la anastomosis1,10,12,14. La incidencia varía según la ubicación, reportada desde el 1 al 8% en anastomosis ileo-colónica, del 2 al 3% colo-colónica, del 3 al 7% ileo-rectal y del 5 a 19% colorrectal o colo-anal10. La mortalidad asociada con la DA está reportada entre el 6 al 22% de los casos14.
Se han descrito múltiples factores de riesgo para la DA, entre ellos: la técnica del cirujano, la ubicación de la anastomosis, las características de los pacientes, entre otras. Sin embargo, el factor de riesgo más asociado con la DA es la mala perfusión sanguínea10. Tradicionalmente, esta se evalúa de una anastomosis de manera subjetiva, valorando las características macroscópicas como la coloración de la serosa, el pulso palpable, los movimientos peristálticos o el sangrado activo de las arterias marginales10,12,14. Existe literatura que demuestra que el análisis macroscópico de la perfusión sanguínea colónica no evalúa de manera adecuada el riesgo de DA9,10,14.
La angiografía con fluorescencia con verde de indocianina (AFVI) se ha utilizado para valorar la perfusión en tiempo real, obteniendo una mejor evaluación de las asas a anastomosar y reduciendo la DA en la cirugía de colon y recto9,10.
ObjetivoPresentar la primera serie de cirugía de colon y recto en México en la que se utilizó la AFVI para valorar la perfusión, previo a realizar la anastomosis.
Material y métodosEl verde de indocianina es una tinción de cianina aprobada por la Administración de Medicamentos y Alimentos (FDA) para su uso como auxiliar en estudios diagnósticos de cardiología, oftalmología, gastroenterología, entre otros9,14,15. El verde de indocianina se inyecta de manera intravenosa y se une a proteínas plasmáticas con poca permeabilidad al intersticio. Se elimina casi exclusivamente por la vía hepática. Esta tinción se distingue por ser fluorescente al exponerse a luz infrarroja9,14.
Realizamos un estudio retrospectivo, descriptivo y analítico. Se incluyeron todos los pacientes con cirugía de colon y recto que requirieron anastomosis y en los que se usó la AFVI. Todas las personas firmaron un consentimiento informado y fueron operadas por un solo grupo de cirujanos coloproctólogos (Coloncare Hospital Ángeles Valle Oriente, Monterrey, Nuevo León, México).
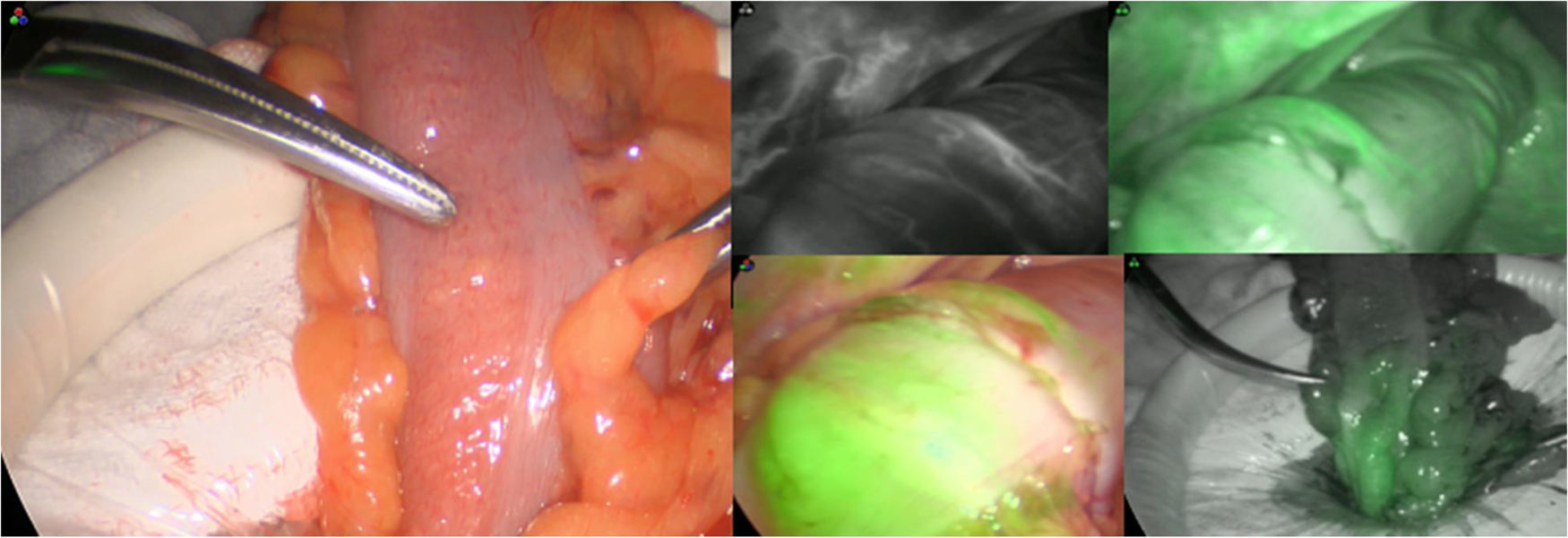
Los pacientes fueron casos seriados a partir de noviembre del 2019 hasta marzo del 2020. Utilizamos la plataforma de Stryker 1688. Incluimos casos con enfermedad benigna y maligna. En todos ellos se realizó, en un primer tiempo, la resección colónica o rectal y, posteriormente, se identificó el sitio con adecuada perfusión sanguínea de acuerdo con sus características macroscópicas. El sitio de anastomosis se elige con base en el aspecto de la mucosa y de la capa sero-muscular del colon y el sangrado evidenciado en el sitio de corte a criterio y experiencia del cirujano. Posteriormente, se diluyen 25 mg de verde de indocianina en 10 mililitros de agua inyectable y se administra a 0.2 mg/kg y se evalúa si el sitio elegido previamente para anastomosar presenta buena circulación por medio de la AFVI. El tiempo entre la inyección intravenosa y la aparición de la fluorescencia en el colon es variable entre 35 y 90 segundos. Los casos en los que la AFVI modificó la decisión del sitio para realizar la anastomosis se consideraron como cambios de decisión terapéutica (fig. 1). A continuación, se administró una segunda dosis (misma dosis) para valorar el segmento proximal y el distal del intestino a anastomosar. Posteriormente, se llevó a cabo la anastomosis en el sitio adecuado indicado por la AFVI. En todos los pacientes de rutina efectuamos la prueba neumática y visual vía rectosigmoidoscopía para evaluar el procedimiento. Además, en todos los casos en los que se realizó la anastomosis mecánica, se revisaron los rodetes completos en la grapadora. Dimos seguimiento mínimo de dos semanas a todos los pacientes.
Análisis estadísticoSe realizó un análisis plenamente descriptivo. Se obtuvieron medias con desviación estándar. No se realizó ninguna comparación entre grupos.
Consideraciones éticasProtección de personas y animales. No se realizaron experimentos en animales o en humanos. Fue un estudio retrospectivo. Todos los pacientes firmaron un consentimiento informado del procedimiento.
Confidencialidad de datos. Hemos seguido los protocolos de nuestro centro de trabajo sobre la publicación de datos de los pacientes que intervienen en el mismo y se ha preservado el anonimato de sus datos.
Todos los pacientes firmaron un consentimiento informado del procedimiento quirúrgico en el que se les explico los riesgos y beneficios del procedimiento a realizar.
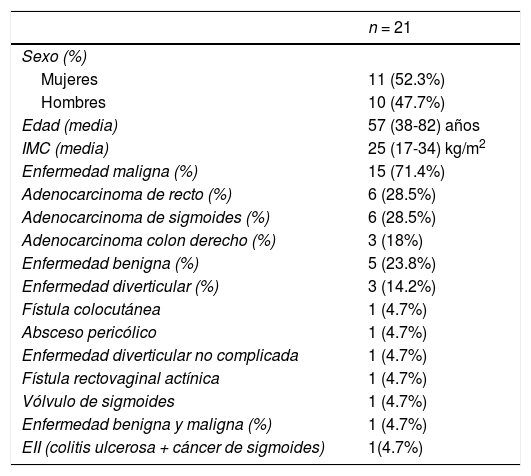
ResultadosSe estudiaron 21 personas de las cuales 11 (52.3%) fueron mujeres. La media de edad fue de 57 años (38 a 82), el índice de masa corporal (IMC) de 25 kg/m2 (17 a 34). De nuestros pacientes, 15 (71.4%) se operaron por enfermedad maligna, cinco (23.8%) por enfermedad benigna y un caso con colitis ulcerosa y cáncer de sigmoides (4.7%) (tabla 1). Las comorbilidades más frecuentes que encontramos en nuestro grupo fueron hipertensión arterial en siete (33.3%) pacientes, tabaquismo en cuatro (19%), diabetes mellitus en tres (14.2%) y una (4.7%) persona con antecedente de radioterapia a la pelvis por malignidad ginecológica. De nuestra serie, cinco (23.8%) casos recibieron quimioterapia y dos (9.5%) radioterapia neoadyuvante. Se observó enfermedad fistulizante en tres (14.2%) pacientes y dos (9.5%) se presentaron con un cuadro obstructivo parcial colónico sintomático (tabla 2).
Características demográficas
| n = 21 | |
|---|---|
| Sexo (%) | |
| Mujeres | 11 (52.3%) |
| Hombres | 10 (47.7%) |
| Edad (media) | 57 (38-82) años |
| IMC (media) | 25 (17-34) kg/m2 |
| Enfermedad maligna (%) | 15 (71.4%) |
| Adenocarcinoma de recto (%) | 6 (28.5%) |
| Adenocarcinoma de sigmoides (%) | 6 (28.5%) |
| Adenocarcinoma colon derecho (%) | 3 (18%) |
| Enfermedad benigna (%) | 5 (23.8%) |
| Enfermedad diverticular (%) | 3 (14.2%) |
| Fístula colocutánea | 1 (4.7%) |
| Absceso pericólico | 1 (4.7%) |
| Enfermedad diverticular no complicada | 1 (4.7%) |
| Fístula rectovaginal actínica | 1 (4.7%) |
| Vólvulo de sigmoides | 1 (4.7%) |
| Enfermedad benigna y maligna (%) | 1 (4.7%) |
| EII (colitis ulcerosa + cáncer de sigmoides) | 1(4.7%) |
EII: enfermedad inflamatoria intestinal; IMC: índice de masa corporal.
Comorbilidades y presentación clínica
| n= 21 | |
|---|---|
| Comorbilidades | |
| Hipertensión arterial (%) | 7 (33.3%) |
| Tabaquismo (%) | 4 (19%) |
| Diabetes mellitus (%) | 3 (14.2%) |
| Radioterapia previa (%)Enfermedades cardiovasculares (%) | 1 (4.7%)0 (0%) |
| Presentación clínica | |
| QT NA (%)Enfermedad fistulizante (%)RT NA (%) | 5 (23.8%)3 (14.2%)2 (9.5%) |
| Obstrucción colónica parcial sintomática (%) | 2 (9.5%) |
QT NA: quimioterapia neoadyuvante; RT NA: radioterapia neoadyuvante.
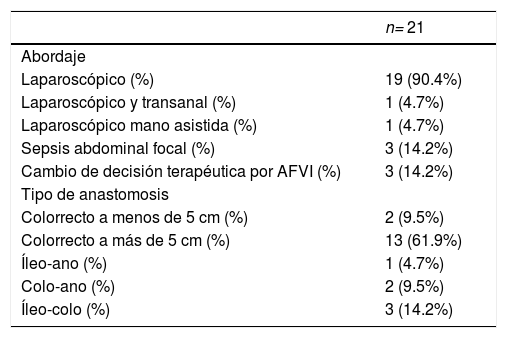
Se realizaron 19 (90.4%) cirugías completamente laparoscópicas, una (4.7%) con abordaje laparoscópico-transanal y una (4.7%) laparoscópica mano-asistida. Encontramos sepsis abdominal focal en tres (14.2%) de nuestros pacientes con enfermedad fistulizante y ninguno presentó peritonitis diseminada. A los casos con diagnóstico de cáncer de colon se les realizó una ligadura del pedículo central (raíz de la arteria). Las anastomosis anales se hicieron vía endoanal y el resto se confeccionaron intracorpóreas. Todos los pacientes a los que se les realizó una escisión total del mesorecto se les movilizó el ángulo esplénico. Ninguno recibió transfusiones intraoperatorias. La AFVI cambió nuestra decisión terapéutica en tres (14.2%) de los casos. Dos (9.5%) de las anastomosis fueron colorrectales a menos de 5 cm del margen anal, 13 (61.9%) se hicieron a más de 5 cm del margen anal. Se hicieron tres (14.2%) anastomosis ileo-colónicas, dos (9.5%) fueron colo-anales y una (4.7%) ileo-anal (tabla 3). Por protocolo, los pacientes que recibieron quimioterapia o radioterapia neoadyuvante y aquellos con anastomosis ileo-anal se les realizó ileostomía en asa de protección, la cual se cerró seis semanas posteriores a la primera intervención.
Abordaje y hallazgos transquirúrgicos y cambio de decisión terapéutica por AFVI
| n= 21 | |
|---|---|
| Abordaje | |
| Laparoscópico (%) | 19 (90.4%) |
| Laparoscópico y transanal (%) | 1 (4.7%) |
| Laparoscópico mano asistida (%) | 1 (4.7%) |
| Sepsis abdominal focal (%) | 3 (14.2%) |
| Cambio de decisión terapéutica por AFVI (%) | 3 (14.2%) |
| Tipo de anastomosis | |
| Colorrecto a menos de 5 cm (%) | 2 (9.5%) |
| Colorrecto a más de 5 cm (%) | 13 (61.9%) |
| Íleo-ano (%) | 1 (4.7%) |
| Colo-ano (%) | 2 (9.5%) |
| Íleo-colo (%) | 3 (14.2%) |
AFVI: angiografía con fluorescencia con verde de indocianina.
Nuestro grupo presentó seis (28.5%) complicaciones de las cuales tres (14.2%) se clasificaron como Clavien-Dindo I (ileo post-quirúrgico) y tres (14.2%) se clasificaron como Clavien-Dindo II (neumonía, infección de catéter venoso central e infección de herida quirúrgica). No tuvimos ninguna DA y ninguna complicación asociada con el uso de AFVI. Reportamos una mortalidad de 0% (tabla 4).
Discusión y conclusiónPresentamos la primera serie en México de pacientes con cirugía de colon y recto para enfermedad benigna y maligna en los que se utilizó la AFVI para valorar perfusión, previo a realizar la anastomosis.
La AFVI ha demostrado ser un procedimiento seguro sin incrementar la morbilidad o la mortalidad a los pacientes. En nuestra serie, no hubo ninguna complicación asociada con el uso de verde de indocianina. Boni et al. presentaron 107 pacientes con enfermedad maligna y benigna y no encontraron complicaciones relacionadas con la AFVI14 así como tampoco las hallaron en el grupo de Santi9. Además de ser muy segura, la AFVI es fácilmente replicable y no requiere de una curva de aprendizaje para ser aplicada con el mayor éxito.
Existen, en la literatura, múltiples estudios que han demostrado que la AFVI disminuye la DA en la cirugía de colon y recto en la enfermedad benigna y particularmente en la enfermedad maligna. La escisión total del meso en cirugía para malignidad está asociada con una peor perfusión en la nueva anastomosis confeccionada y, por lo tanto, es en este escenario en el que se ha encontrado un mayor beneficio del uso de la AFVI. Boni et al. reportaron 3.7% de cambio de decisión terapéutica al usar este procedimiento. Solo reportan una DA y la vinculan con mala técnica quirúrgica14.
Santi et al. reportaron un cambio de decisión terapéutica al usar AFVI en 38 pacientes. Este mismo grupo informó sobre tres complicaciones y una DA relacionada con un problema con la grapadora mecánica9. Wada et al. reportaron un grupo de 149 pacientes con resección anterior baja. Hicieron un pareamiento por puntaje de propensión y observaron DA de 8.8%, utilizando AFVI contra 14.7% sin AFVI. Encontraron, además, que mayor IMC, haber recibido quimioterapia preoperatoria y la disección lateral ganglionar se relaciona con la DA16.
Kudszuz et al. exponen un cambio de decisión terapéutica en el 13.9% y la reducción de la DA por 4% al utilizar AFVI17. El estudio PILLAR-II trial reportó un cambio de decisión terapéutica en el 7.9% de los casos con AFVI18.
En el meta-análisis por Blanco et al. se incluyeron 555 pacientes en el grupo con AFVI y 747 en el grupo de control sin AFVI. Se incluyeron personas con cirugía de colon y recto para enfermedad benigna y maligna. La DA se reportó en 5.4% y no hubo diferencia estadísticamente significativa entre el grupo con AFVI y el grupo de control. Sin embargo, cuando se consideraron los pacientes con enfermedad maligna se encontró una disminución estadísticamente significativa de la DA al utilizar AFVI. Se reportó un cambio de decisión terapéutica en 7.4% de todos los casos (benignos y malignos)10. Shen et al. realizaron un meta-análisis de pacientes con cáncer de colon y recto comparando un grupo con AFVI y el grupo de control, y también encontraron que el uso de AFVI disminuye la DA en personas con cáncer de colon y de recto, de manera estadísticamente significativa19.
Se ha utilizado también la AFVI en la cirugía robótica de colon y de recto, y los hallazgos son similares. Hellan et al. reportan un grupo de 40 pacientes con resecciones rectales o de colon izquierdo por robot, utilizando AFVI. Tuvieron un cambio de decisión terapéutica en el 40% de los pacientes y 5% de DA13. Jafari et al. presentan una serie de casos con resecciones rectales por robot, comparando un grupo con AFVI contra un grupo de control. Demostraron un cambio de decisión terapéutica en el 19% y disminución de DA del 18 a 6% al utilizar AFVI20. Kim et al. informaron una serie de proctectomías con robot, reduciendo la DA al usar AFVI de 5.2% a 0.6%21.
El uso de la AFVI disminuye la DA y, por lo tanto, se ha hecho muy atractiva también para los protocolos de recuperación acelerada (ERAS). Brescia et al. estudiaron a 182 pacientes con cirugía de colon o recto con protocolo ERAS y a 75 se les hizo AFVI. En esos 75 casos, hubo cambio de decisión terapéutica en 6.7%. No existió DA en el grupo con AFVI mientras que en el grupo de control se presentó DA en 5.6%. No hubo diferencia estadísticamente significativa en la estancia intrahospitalaria entre los grupos1.
El costo de la AFVI ha sido otro tema repetitivo en la literatura. Considerando que los pacientes con DA requieren re-operación, cuidados en terapia intensiva y aumento de la estancia intrahospitalaria, entonces la AFVI es una terapéutica mucho más económica. La DA aumenta el costo por cinco de un paciente sin esta complicación22.
La AFVI se ha usado también para estudiar la perfusión de la neoplasia, previo a la resección de colon o recto. Santi et al. utilizaron esta técnica para diferenciar la tumoración colónica del uréter derecho y no lesionarlo en un caso. Asimismo, han usado AFVI en resecciones colónicas para identificar el pedículo vascular nutricio del tumor9.
Aun con AFVI siguen reportándose fugas de anastomosis, lo que nos hace pensar que debemos buscar una manera más objetiva para analizar la fluorescencia23. La intensidad de la fluorescencia es dependiente de la distancia a la que se coloca la luz y de si se realiza de manera intraabdominal o externamente. La valoración de la fluorescencia continúa siendo subjetiva. Cuando la concentración del verde de indocianina es baja se logra una buena relación entre esta y la intensidad reflejada. Sin embargo, cuando aumentamos la concentración se pierde la proporcionalidad. Por esta razón se ha recomendado mantener niveles bajos13. Es evidente que la AFVI continúa siendo un estudio subjetivo interpretado por el cirujano.
Wada et al. midieron de manera cuantitativa la fluorescencia, utilizando un software de análisis, evaluando el tiempo a máxima fluorescencia y encontraron menores curvas en los pacientes que presentaron DA al compararlos con el grupo sin DA16. El futuro de la AFVI está en poder medir, de manera cuantitativa, la fluorescencia y así quitar por completo la subjetividad del análisis de perfusión de las asas en cirugía de colon y recto.
En conclusión, presentamos la primera serie de cirugía colorrectal en México en la que se usó AFVI con excelentes resultados. En nuestro estudio no existió DA ni complicaciones asociadas con el uso de verde de indocianina.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesEl Dr. Luis Enrique Salgado Cruz ha participado como consultor para Stryker.