El cáncer gástrico es una de las principales causas de cáncer a nivel mundial. No existe una estrategia global de tamizaje. La endoscopia se ha convertido en el método de elección para tamizaje, sin embargo, no existe un método estandarizado. El uso de la endoscopia sistemática alfanumérica codificada puede aumentar la detección de lesiones gástricas. El objetivo es comparar la utilidad del sistema de endoscopia alfanumérica codificada con la endoscopia convencional para la detección de lesiones premalignas y cáncer gástrico temprano en sujetos con riesgo promedio de cáncer gástrico.
Material y métodosEstudio de corte transversal, comparativo, prospectivo y aleatorizado, en pacientes con riesgo promedio para cáncer gástrico (40-50 años, sin historia de infección por H. pylori, metaplasia intestinal, atrofia gástrica ni cirugía gastrointestinal). Antes de la endoscopia recibieron preparación gástrica (200mg de acetilcisteína oral o 50mg de dimeticona oral). Se realizó cromoendoscopia convencional con índigo carmín para realzar el contraste.
ResultadosFueron 50 casos consecutivos (edad promedio de 44.4 ± 3.34 años, el 60% mujeres 60%, con IMC de 27.6 ± 5.82 kg/cm2). La calidad de la imagen endoscópica fue satisfactoria en todos los casos, sin diferencias entre métodos (p = 0.817). El índice de detección de lesiones premalignas y de cáncer gástrico temprano fue del 14% (6 metaplasias intestinales y un adenocarcinoma gástrico). La Sn, Sp, VPP, VPN y la exactitud diagnóstica fueron del 100, 95, 80, 100 y 96%, respectivamente para la endoscopia sistemática alfanumérica codificada y para la endoscopia convencional 100, 45, 20, 100 y 52%, respectivamente. La endoscopia sistemática alfanumérica codificada fue mejor que la endoscopia convencional para la detección de lesiones (p = 0.003; RM = 12).
ConclusiónAmbas técnicas fueron efectivas; sin embargo, el sistema alfanumérico codificado disminuye significativamente la tasa de falsos positivos.
Gastric cancer is one of the main causes of cancer worldwide, but there is currently no global screening strategy for the disease. Endoscopy is the screening method of choice in some Asian countries, but no standardized technique has been recognized. Systematic alphanumeric-coded endoscopy can increase gastric lesion detection. The aim of the present article was to compare the usefulness of systematic alphanumeric-coded endoscopy with conventional endoscopy for the detection of premalignant lesions and early gastric cancer in subjects at average risk for gastric cancer.
Materials and methodsA cross-sectional, comparative, prospective, randomized study was conducted on patients at average risk for gastric cancer (40-50 years of age, no history of H. pylori infection, intestinal metaplasia, gastric atrophy, or gastrointestinal surgery). Before undergoing endoscopy, the patients had gastric preparation (200mg of oral acetylcysteine or 50mg of oral dimethicone). Conventional chromoendoscopy was performed with indigo carmine dye for contrast enhancement.
ResultsFifty consecutive cases (mean age 44.4 ± 3.34 years, 60% women, BMI 27.6 ± 5.82 kg/m2) were evaluated. Endoscopic imaging quality was satisfactory in all the cases, with no differences between methods (p = 0.817). The detection rate of premalignant lesions and early gastric cancer was 14% (6 cases of intestinal metaplasia and one case of gastric adenocarcinoma). Sensitivity, specificity, positive predictive value, negative predictive value, and diagnostic accuracy were 100, 95, 80, 100 and 96%, respectively, for systematic alphanumeric-coded endoscopy, and 100, 45, 20, 100, and 52%, respectively, for conventional endoscopy. Lesion detection through systematic alphanumeric-coded endoscopy was superior to that of conventional endoscopy (p = 0.003; OR = 12).
ConclusionBoth techniques were effective, but systematic alphanumeric-coded endoscopy significantly reduced the false positive rate.
El cáncer gástrico es la tercera causa de muerte por cáncer (723,000 muertes/año); en 2002 se reportaron 870,000 nuevos casos1,2. En la actualidad no existe una estrategia aceptada universalmente para el tamizaje de lesiones premalignas3. Se han propuesto técnicas no invasivas (radiológicas, serología de H. pylori, pepsinógeno i, pepsinógeno ii y gastrina sérica) e invasivas (endoscopia, magnificación, cromoendoscopia, imagen de banda estrecha, autofluorescencia y endomicroscopia confocal)3.
Las metaplasia intestinal, la atrofia y la displasia gástricas incrementan el riesgo de cáncer4. Se ha aceptado universalmente la Clasificación de París como una forma unificada para clasificar las lesiones gástricas5. La tasa de cáncer gástrico de intervalo (23.1%) ha sido relacionada con el tamaño de las lesiones y la presencia de metaplasia intestinal6-8. Una exploración minuciosa y la adecuada limpieza de la mucosa gástrica son indispensables en sujetos con riesgo para detectar estas lesiones9.
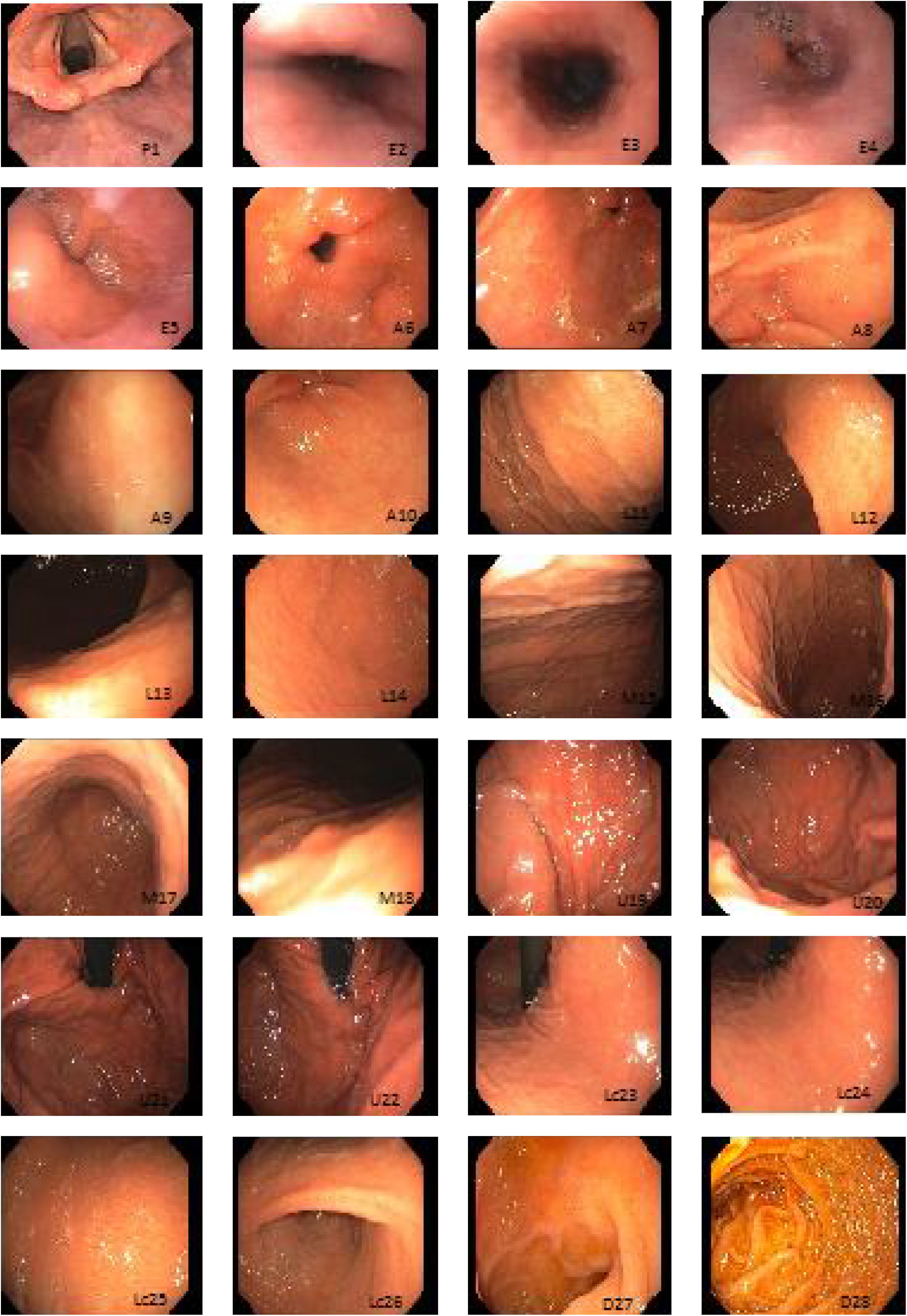
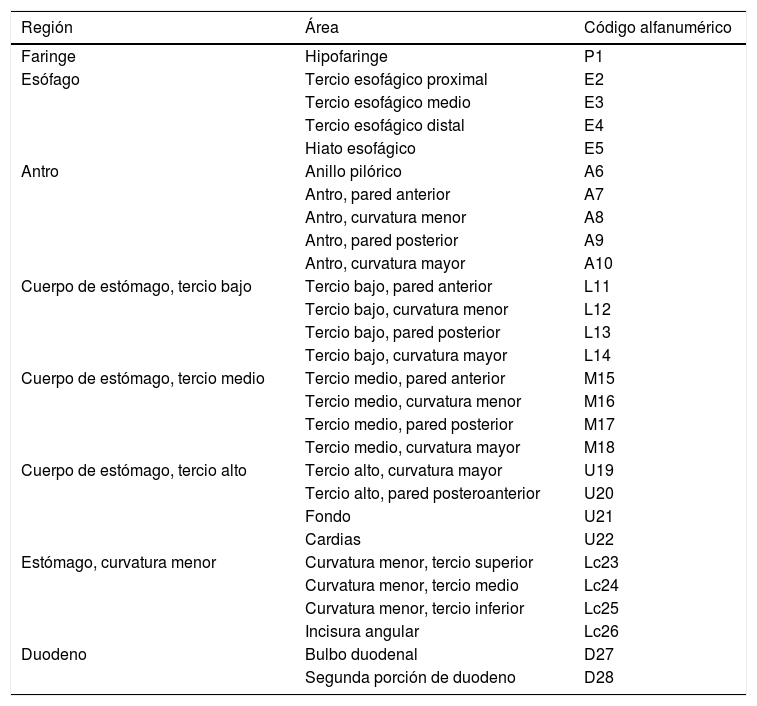
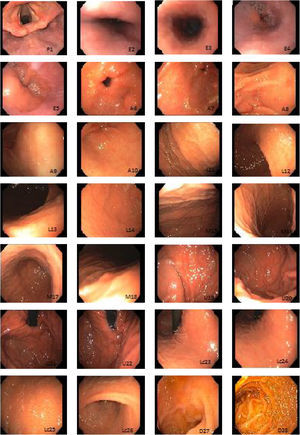
La endoscopia sistemática alfanumérica codificada (ESAC) es un método de evaluación de la mucosa gástrica que divide el tracto digestivo superior en 8 regiones y 28 áreas (tabla 1, fig. 1) y permite explorar la totalidad de la superficie con un sistema de coordenadas basado en la identificación de ciertos ejes naturales, paredes, curvaturas y puntos de referencia anatómicos que evita áreas ciegas, lo cual puede tener impacto significativo sobre la tasa de detección de lesiones premalignas y la disminución del cáncer de intervalo9-11.
Endoscopia sistemática alfanumérica codificada
| Región | Área | Código alfanumérico |
|---|---|---|
| Faringe | Hipofaringe | P1 |
| Esófago | Tercio esofágico proximal | E2 |
| Tercio esofágico medio | E3 | |
| Tercio esofágico distal | E4 | |
| Hiato esofágico | E5 | |
| Antro | Anillo pilórico | A6 |
| Antro, pared anterior | A7 | |
| Antro, curvatura menor | A8 | |
| Antro, pared posterior | A9 | |
| Antro, curvatura mayor | A10 | |
| Cuerpo de estómago, tercio bajo | Tercio bajo, pared anterior | L11 |
| Tercio bajo, curvatura menor | L12 | |
| Tercio bajo, pared posterior | L13 | |
| Tercio bajo, curvatura mayor | L14 | |
| Cuerpo de estómago, tercio medio | Tercio medio, pared anterior | M15 |
| Tercio medio, curvatura menor | M16 | |
| Tercio medio, pared posterior | M17 | |
| Tercio medio, curvatura mayor | M18 | |
| Cuerpo de estómago, tercio alto | Tercio alto, curvatura mayor | U19 |
| Tercio alto, pared posteroanterior | U20 | |
| Fondo | U21 | |
| Cardias | U22 | |
| Estómago, curvatura menor | Curvatura menor, tercio superior | Lc23 |
| Curvatura menor, tercio medio | Lc24 | |
| Curvatura menor, tercio inferior | Lc25 | |
| Incisura angular | Lc26 | |
| Duodeno | Bulbo duodenal | D27 |
| Segunda porción de duodeno | D28 |
El objetivo del estudio es comparar la utilidad de la ESAC con la endoscopia convencional en la detección de lesiones premalignas y cáncer gástrico temprano en sujetos con riesgo promedio de cáncer gástrico. Definimos como riesgo promedio el de aquellos pacientes con rango de edad entre 40 y 50 años sin ningún factor asociado que incremente el riesgo de cáncer.
Material y métodosSe realizó un estudio de corte transversal, prospectivo con asignación aleatorizada en sujetos con riesgo promedio de cáncer gástrico en el Hospital General de México Dr. Eduardo Liceaga.
Criterios de selección: a) inclusión: sujetos sanos de entre 40 y 50 años, de ambos sexos y con consentimiento informado por escrito; b) exclusión: antecedente de infección por H. pylori, metaplasia intestinal, atrofia o displasia gástricas, cirugía gástrica resectiva, oclusión intestinal, hipertensión portal y hemorragia digestiva.
PremedicaciónTodos tuvieron limpieza gástrica preendoscópica (asignación aleatoria) mediante la ingesta oral (20-30 min antes del procedimiento) de dimeticona suspensión (Espaven pediátrico®; 50mg) o N-acetilcisteína (Lysomucil® granulado de 200mg) diluidos en 100ml de agua. La calidad de la limpieza gástrica se evaluó otorgando una puntuación: 0 = sin residuos, se puede valorar completamente la mucosa; 1 = algunos residuos que se pueden aspirar con el endoscopio; 2 = residuos líquidos y espesos, para los cuales es necesario irrigar con agua para disolverlos y después aspirarlos completamente; 3 = residuos líquidos espesos, para los cuales es necesario irrigar con agua para disolverlos y después aspirarlos, sin poder aspirarlos por completo; 4 = residuos sólidos que no pueden ser aspirados. Se registró el tiempo promedio requerido para la exploración endoscópica.
Mediante un aleatorización simple (tabla de números aleatorios) fueron asignados a uno de los siguientes grupos para la exploración gástrica: 1) endoscopia convencional o 2) ESAC.
Equipo de endoscopiaVideogastroscopios GIF-Q145 (Japón 2000) y GIF-Q150 (Japón 2006), procesador EVIS EXERA-II.
Cromoendoscopia y toma de biopsiaLos estudios fueron realizados por médicos en entrenamiento en endoscopia, supervisados por médicos adscritos. En el grupo de ESAC, la captura de imágenes se realizó a la entrada, después de completar con limpieza adicional de la cámara gástrica (en caso de ser necesaria) para exponer el 100% de la mucosa, siguiendo la codificación ya previamente referida (tabla 1, fig. 1). En caso de detectar alguna lesión sospechosa de premalignidad —lo cual se definió como aquella que mostrara alguna de las siguientes características: polipoidea o ulcerosa, lesiones parís 0-iia y 0-iic, cambio de coloración (rojiza o blanquecina), áreas de mucosa pálida plana sin márgenes bien definidos o áreas de mucosa con el patrón mucoso francamente alterado— se aplicó índigo carmín al 0.3% con aspersor, con posterior toma de biopsias, las cuales fueron inmediatamente fijadas en formaldehido al 10% y evaluadas por patólogos del hospital. En caso de no detectar alteraciones sugestivas de lesiones premalignas, pero sí evidencia de gastropatía crónica (gastritis difusa antral, gastritis atrófica corporal difusa o gastritis atrófica multifocal) se tomaron biopsias sistemáticas de acuerdo con el protocolo de Sydney12.
Análisis estadísticoSe calculó el índice de detección de lesiones.Se realizó estadística descriptiva para frecuencias y proporciones. Se empleó la prueba de chi cuadrado (variables categóricas) y la de la t de Student (variables cuantitativas) con nivel de significancia 0.05. Se calculó el tamaño del efecto (razón de momios [RM] con IC 95%). El tamaño de la muestra fue calculado con la fórmula de proporciones (a = 0.05, ß = 0.2, poder 0.8, d = 0.4) con 23 sujetos por grupo.
El protocolo fue revisado y aceptado por el Comité de Ética e Investigación del hospital (DI/16/107/03/032) y se siguieron las buenas prácticas clínicas.
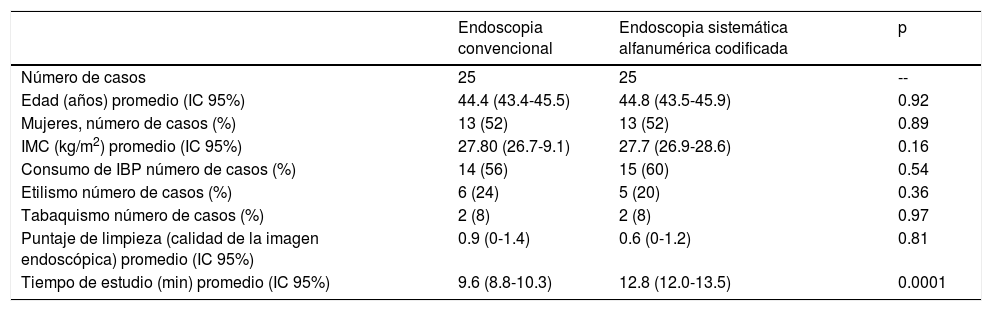
ResultadosFueron 50 casos consecutivos con edad promedio de 44.4 ± 3.34 años, un 52% de mujeres, con IMC de 27.6 ± 5.82 kg/cm2. Antecedentes: consumo de IBP (58%), etilismo (22%) y tabaquismo (8%). No hubo diferencias para edad (p = 0.92) ni IMC (p = 0.16) entre los grupos. La calidad de la imagen endoscópica para evaluar la morfología para diferenciar las lesiones premalignas fue satisfactoria en todos los casos. No observamos diferencias entre la calidad de la imagen endoscópica en ambos grupos (p = 0.817).
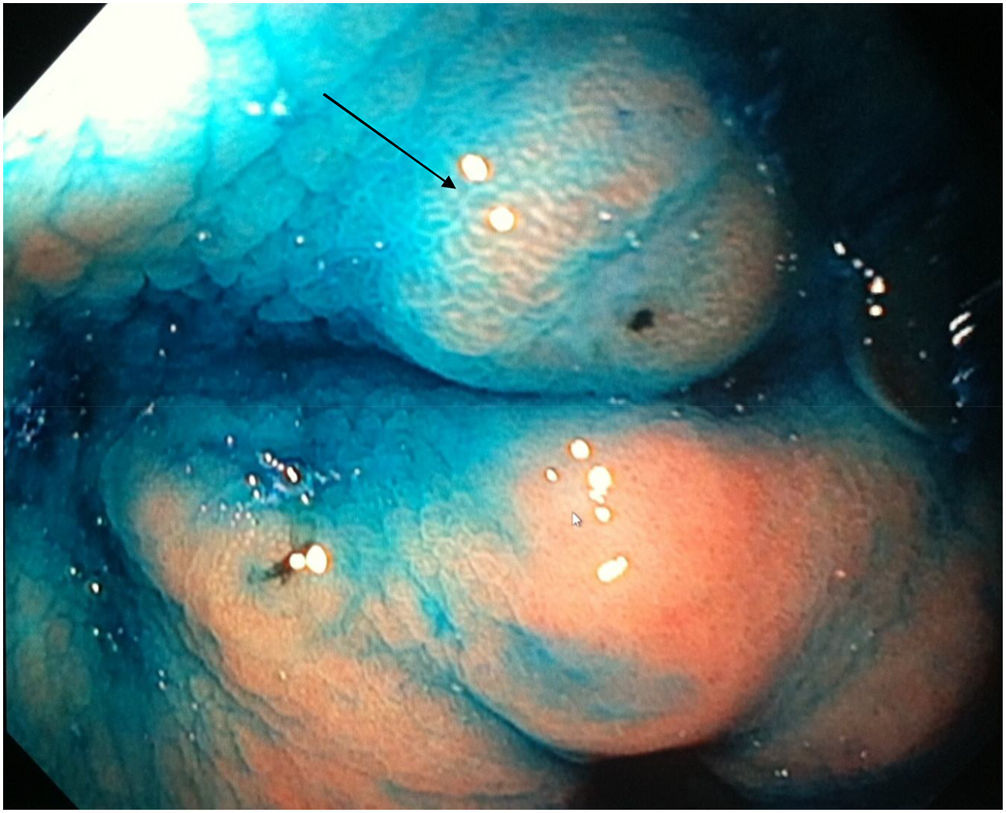
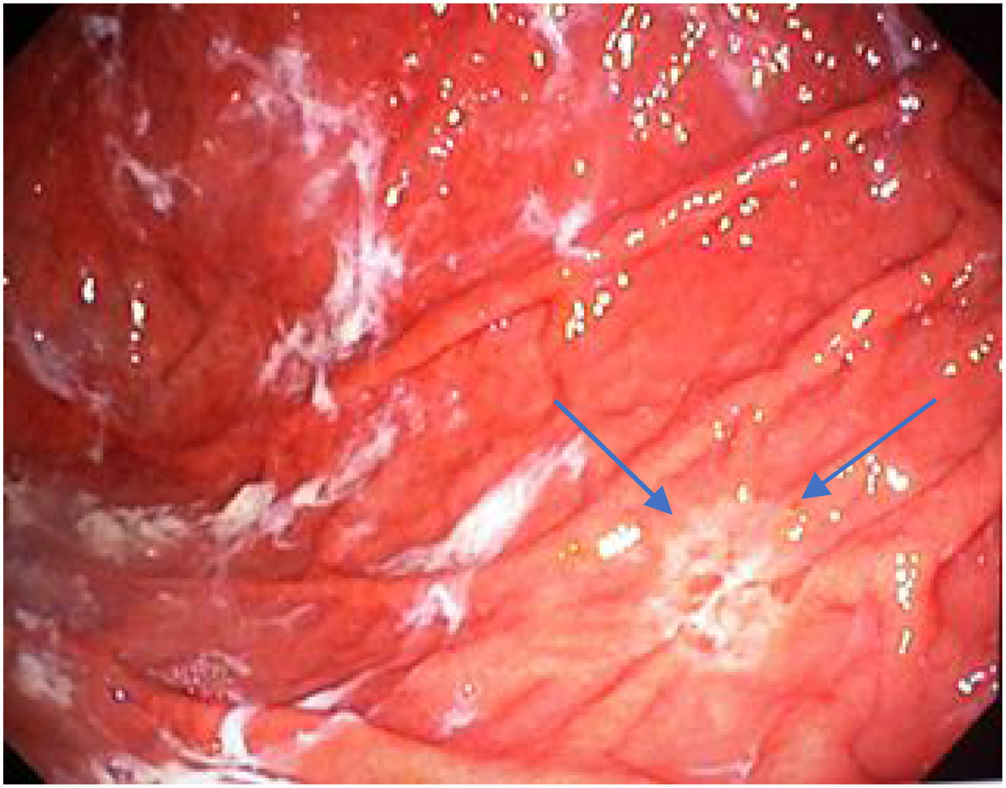
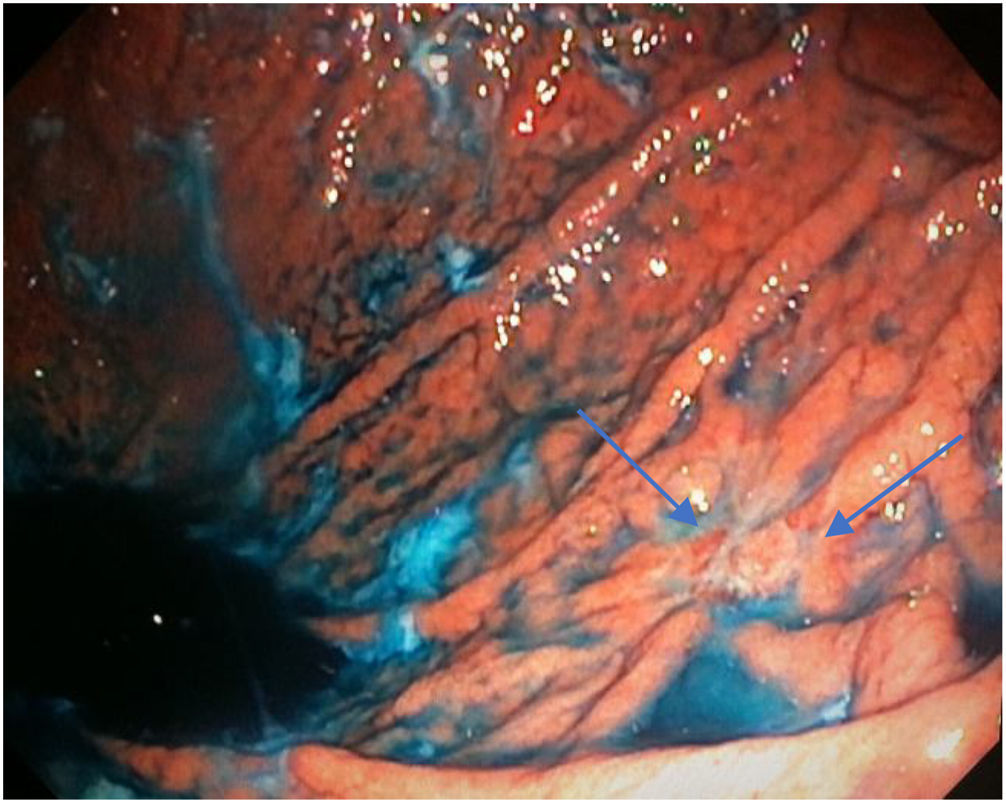
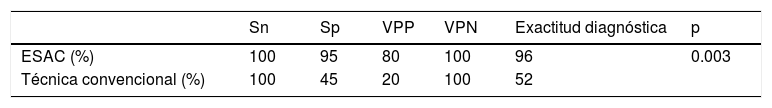
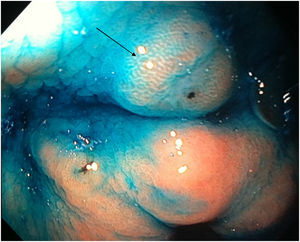
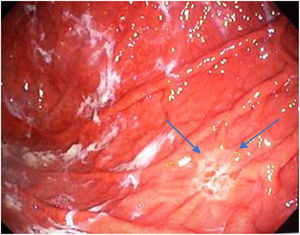
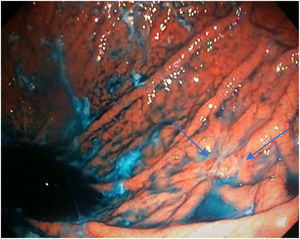
El tiempo promedio (minutos) para la exploración de la mucosa fue significativamente mayor con ESAC (12.8 ± 2.6, IC 95%: 12.09-13.51 versus 9.6 ± 2.42, IC 95%: 8.88-10.31; p = 0.0001) (tabla 2). Hallazgos endoscópicos (confirmación histológica): 18% (9/50) mucosa normal, 20% (10/50) gastritis crónica asociada a H. pylori, 6% (3/50) gastritis reactiva y 56% (28/50) gastritis crónica. Se detectaron 6 casos de metaplasia intestinal sin displasia (figs. 2 y 3) y un caso de adenocarcinoma poco diferenciado (difuso de la clasificación de Lauren), que se mostró como una lesión plana ulcerada (fig. 4, tabla 3). El índice de detección de lesiones premalignas y cáncer gástrico temprano fue del 14%. La región y las áreas con mayor frecuencia de lesiones fueron el antro y la curvatura menor. Para la ESAC la sensibilidad (Sn), especificidad (Sp), valor predictivo positivo (VPP), valor predictivo negativo (VPN) y exactitud diagnóstica fueron 100, 95, 80, 100 y 96%, respectivamente. Para la endoscopia convencional la Sn, Sp, VPP, VPN y la exactitud diagnóstica fueron 100, 45, 20, 100 y 52%, respectivamente. La exploración endoscópica con el uso de la ESAC fue mejor que el sistema convencional para la detección de lesiones preneoplásicas (p = 0.03, RM = 12) (tabla 4). La concordancia interobservador fue baja (kappa 0.4).
Características demográficas de la población
| Endoscopia convencional | Endoscopia sistemática alfanumérica codificada | p | |
|---|---|---|---|
| Número de casos | 25 | 25 | -- |
| Edad (años) promedio (IC 95%) | 44.4 (43.4-45.5) | 44.8 (43.5-45.9) | 0.92 |
| Mujeres, número de casos (%) | 13 (52) | 13 (52) | 0.89 |
| IMC (kg/m2) promedio (IC 95%) | 27.80 (26.7-9.1) | 27.7 (26.9-28.6) | 0.16 |
| Consumo de IBP número de casos (%) | 14 (56) | 15 (60) | 0.54 |
| Etilismo número de casos (%) | 6 (24) | 5 (20) | 0.36 |
| Tabaquismo número de casos (%) | 2 (8) | 2 (8) | 0.97 |
| Puntaje de limpieza (calidad de la imagen endoscópica) promedio (IC 95%) | 0.9 (0-1.4) | 0.6 (0-1.2) | 0.81 |
| Tiempo de estudio (min) promedio (IC 95%) | 9.6 (8.8-10.3) | 12.8 (12.0-13.5) | 0.0001 |
IBP: inhibidores de bomba de protones; IC: intervalo de confianza; IMC: índice de masa corporal.
Casos con lesiones preneoplásicas
| Paciente | Tipo de lesión | Área | Técnica endoscópica | Morfología de la lesión |
|---|---|---|---|---|
| 1 | Metaplasia intestinal | Antro (A6) | Convencional | Plana |
| 2 | Metaplasia intestinal | Antro (A6) | ESAC | Plana |
| 3 | Metaplasia intestinal | Antro (A6) | Convencional | Polipoidea |
| 4 | Metaplasia intestinal | Curvatura menor (Lc25) | ESAC | Plana |
| 5 | Metaplasia intestinal | Curvatura menor (L12) | ESAC | Plana |
| 6 | Metaplasia intestinal | Cuerpo y fondo (M15-U22) | ESAC | Plana |
| 7 | Adenocarcinoma poco diferenciado | Cuerpo curvatura mayor (M18) | Convencional | Úlcera |
ESAC: endoscopia sistemática alfanumérica codificada.
Comparación entre las técnicas diagnósticas
| Sn | Sp | VPP | VPN | Exactitud diagnóstica | p | |
|---|---|---|---|---|---|---|
| ESAC (%) | 100 | 95 | 80 | 100 | 96 | 0.003 |
| Técnica convencional (%) | 100 | 45 | 20 | 100 | 52 |
ESAC: endoscopia sistemática alfanumérica codificada; Sn: sensibilidad; Sp: especificidad; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
El cáncer gástrico es una de las principales causas de muertes relacionadas con el cáncer a nivel mundial. La mayor parte de los casos se diagnostica en estadios avanzados y con mal pronóstico. Las lesiones precancerosas incluyen la metaplasia intestinal y la atrofia gástrica. En un estudio danés, demostraron que estas lesiones incrementan el riesgo de cáncer: el 0.1% es para atrofia gástrica, el 0.25% para metaplasia intestinal, el 0.6% para displasia moderada y el 6% para displasia severa a los 5 años4. A pesar de esta prevalencia, no existe una estrategia global de tamizaje3. En algunas de estas zonas con alta prevalencia, se propone iniciar el tamizaje en hombres y mujeres mayores de 40 años; sin embargo, se debe ajustar este rango de edad en poblaciones específicas, según la incidencia de cáncer gástrico y los factores de riesgo individuales13,14. En áreas no endémicas, se recomienda iniciar el tamizaje a los 40-45 años de edad15.
La endoscopia se ha convertido en el método de elección en zonas como Japón y Corea, con un costo-beneficio razonable. Sin embargo, el costo sigue siendo un problema en países en vías de desarrollo, además de los riesgos inherentes a un estudio invasivo. Nuevas técnicas de imagen como la cromoendoscopia digital, magnificación, imagen de banda estrecha, autofluroescencia, endomicroscopia confocal o endocistoscopia pueden mejorar la detección de lesiones premalignas16-20; sin embargo, estas técnicas no están disponibles en la mayoría de las unidades de endoscopia. La detección de estas lesiones depende de la destreza y conocimiento del endoscopista, por lo que estandarizar una técnica y un adecuado entrenamiento son importantes21. Hosokawa et al. reportaron tasas de falso negativo en la detección de cáncer gástrico temprano con endoscopia de hasta el 25.8%; Aida et al. mostraron datos en los que las lesiones correspondientes a cáncer gástrico no se detectaron en una endoscopia previa en el 23.1% de los casos7,22. En un estudio en el que evaluaron los factores relacionados con el desarrollo de cáncer gástrico de intervalo (cáncer detectado dentro de los 2 años de una endoscopia negativa), las lesiones más pequeñas (1.3 vs. 1.8 cm) y la presencia de metaplasia intestinal fueron los que en análisis multivariado mostraron significación estadística8, por lo que una adecuada exploración endoscópica es necesaria para detectar este tipo de lesiones.
En el protocolo propuesto por Emura et al., la ESAC es un método sistemático del tracto gastrointestinal alto basado en la fotodocumentación secuencial de imágenes parcialmente superpuestas que, usando una nomenclatura alfanumérica endoluminal compuesta de 8 regiones y 28 áreas, proporciona el cubrimiento total de la superficie gastrointestinal alta. Incorpora un sistema sencillo de coordenadas basado en la identificación de ciertos ejes naturales, paredes, curvaturas y puntos de referencia anatómicos (tabla 1, fig. 1). La efectividad de esta técnica fue demostrada en un estudio de tamizaje en voluntarios sanos, con riesgo promedio, entre 40 y 70 años, en los que diagnosticaron cáncer gástrico temprano en 2/650 (0.3%)22. Este sistema de evaluación endoscópica no ha sido evaluado en nuestra población. Idealmente, un examen de tamizaje debe incluir premedicación intraluminal, equipos de alta definición, cromoendoscopia digital y endoscopistas con experiencia visual en la identificación de imágenes23. En esta serie se utilizó premedicación con dimeticona o acetilcisteína para quitar el moco adherido y la espuma generada por secreciones, lo que favoreció la adecuada evaluación de la superficie mucosa gástrica. Se analizaron las 2preparaciones (datos no mostrados) y se demostró mejor calidad de la imagen endoscópica en el grupo de dimeticona. Se utilizó cromoendoscopia convencional con índigo carmín (0.3%), el cual es un colorante no absorbible ni tóxico que ha mostrado mejorar la detección de lesiones preneoplásicas, facilitar la caracterización de las lesiones, de los bordes y del tamaño23. En nuestro estudio la prevalencia de lesiones premalignas y cáncer gástrico temprano fue del 14%, cifra menor que la reportada en poblaciones como Colombia (30%)9 —que se consideran de alta prevalencia— y que es similar a la reportada por otros países como Turquía, en donde han reportado una prevalencia del 13%24. Se considera a México como una población de baja prevalencia de metaplasia intestinal y cáncer gástrico. Ambas técnicas endoscópicas fueron eficaces para detectar casos (100%), sin embargo, la evaluación con el método convencional tuvo una alta tasa de falsos positivos (Sn 95 vs. 45%) y un VPP muy bajo (80 vs. 20%). La técnica ESAC fue más efectiva que la convencional en la detección de lesiones premalignas y cancer gástrico temprano de estómago (p = 0.003; RM = 12; IC 95%). Las limitaciones del estudio son la baja prevalencia de este tipo de lesiones en la población estudiada, no emplear endoscopios con alta definición para la caracterización de las lesiones y la baja concordancia interobservador. Además, no fue un estudio cruzado con el paciente como propio control para determinar la tasa de lesiones no detectadas en ambas técnicas. Las fortalezas del estudio se basan en su metodología (diseño de corte transversal con asignación aleatorizada). Según nuestro conocimiento, este es el único estudio de tamizaje que evalúa el rendimiento de la ESAC en México. Idealmente los centros endoscópicos deberían utilizar equipos de alta definición y cromoendoscopia electrónica en el tamizaje de sujetos con riesgo promedio y alto para cáncer gástrico. Sin embargo, la evaluación sistemática es una herramienta que puede tener un impacto significativo en la omisión de lesiones y la reducción del cáncer de intervalo.
En conclusión, las técnicas endoscópicas ESAC y convencional fueron ambas efectivas para detectar lesiones premalignas; sin embargo, el uso del sistema alfanumérico codificado disminuye significativamente la tasa de falsos positivos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo/estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos a todos los médicos adscritos, residentes y enfermeras que participaron e hicieron posible la realización de este estudio.