El adenocarcinoma colorrectal es infrecuente en niños y jóvenes y suele presentarse con signos y síntomas inespecíficos, lo que lleva a diagnósticos tardíos.
ObjetivosDescribir la presentación clínica y evolución de los niños y adolescentes con adenocarcinoma colorrectal atendidos en nuestro hospital, y detectar posibles condiciones predisponentes de esta enfermedad.
Materiales y métodosSe presentan 8 pacientes con adenocarcinoma colorrectal seguidos en el Hospital Posadas entre enero de 2000 y diciembre de 2021. Buscamos enfermedades predisponentes a esta patología.
ResultadosEdad mediana: 16 años (entre 11 y 17 años). Presentación clínica: dolor abdominal 8 pacientes (dolor en hipocondrio derecho: 4), tumor abdominal en 3, sangrado rectal en 4 y pérdida de peso en 3. Duración media de los síntomas: 9 semanas (rango: 1-24). Ningún paciente mostró enfermedades predisponentes. Un paciente presentó poliposis, sin otros casos familiares. La histología presentó adenocarcinoma mucinoso en todos los pacientes,con células tipo anillo de sello en 4. El tumor primario se ubicó en el colon derecho en 6. Estadificación según la clasificación de Dukes modificada, al diagnóstico: I:1; IIb: 1; IIIb: 1; IIIc: 1; IV: 4. Todos los pacientes, excepto dos, recibieron quimioterapia, y uno, radioterapia. La supervivencia global fue del 25% a los 3 años.
Conclusiones1. Todos los pacientes presentaban adenocarcinoma mucinoso. 2. No encontramos ninguna enfermedad predisponente. 3. La evolución de los niños con cáncer colorrectal fue muy mala. 4. Se debe considerar el diagnóstico de cáncer colorrectal en niños con dolor abdominal agudo, tumor abdominal o hemorragia digestiva baja, particularmente si tienen pérdida de peso.
Colorectal adenocarcinoma is rare in children and adolescents and tends to present with nonspecific signs and symptoms, leading to late diagnoses.
ObjectivesOur aim was to describe the clinical presentation and progression in children and adolescents with colorectal adenocarcinoma treated at our hospital and detect possible predisposing conditions of this disease.
Materials and methodsEight patients with colorectal adenocarcinoma were followed at the Hospital Posadas within the time frame of January 2000 and December 2021. We searched for diseases predisposing to this cancer.
ResultsThe mean patient age was 16 years (between 11 and 17 years of age). Clinical presentation was abdominal pain in the 8 patients; 4 of them had pain in the right hypochondrium, 3 had abdominal tumor, 4 had rectal bleeding, and 3 had weight loss. Mean symptom duration was 9 weeks (range: 1-24 weeks). None of the patients showed predisposing illnesses. One patient presented with polyposis, with no cases in any other family member. Histology showed mucinous adenocarcinoma in all the patients, 4 of whom had the signet ring cell subtype. The primary tumor was located in the right colon in 6 patients. At diagnosis, staging according to the modified Dukes classification was: I: one patient; IIb: one patient; IIIb: one patient; IIIc: one patient; and IV: 4 patients. All patients except 2 received chemotherapy and one patient received radiotherapy. Overall survival at 3 years was 25%.
ConclusionsAll patients presented with mucinous adenocarcinoma, no predisposing diseases were found, and the children with colorectal cancer had a very poor prognosis. Colorectal cancer diagnosis should be considered in children presenting with acute abdominal pain, abdominal tumor, or lower gastrointestinal bleeding, especially if there is weight loss.
El cáncer colorrectal es extremadamente raro en la población pediátrica, con una tasa de incidencia anual según datos del programa Surveillance, Epidemiology and End Results (SEER) de 0.12/1,000,000 en población de 0 a 14años, y aumenta a 1.78/1,000,000 entre 15 y 19años1-3. En Argentina, en la población adulta, se presentan cada año cerca de 10,300 nuevos casos de cáncer colorrectal; con base en estas cifras, esta enfermedad representa la tercera enfermedad oncológica más frecuente, precedida por el cáncer de mama como primera malignidad, y es la causa más común de mortalidad después del cáncer de pulmón4,5. En el Registro Oncopediátrico Hospitalario Argentino (ROHA), desde el año 2000 se han registrado 199 casos de cáncer del tracto gastrointestinal, y 68 de ellos son cáncer colorrectal3.
El carcinoma mucinoso es el tipo histopatológico más frecuente en pacientes pediátricos, mientras que en la población adulta representa solo el 15%5. También es más común en el colon derecho en niños y en adultos jóvenes. Esos factores y el bajo índice de sospecha entre los pediatras son los responsables de la mala evolución de esta condición6.
En niños, el cáncer colorrectal suele estar asociado a trastornos hereditarios, mientras que el 90% de los casos en adultos son esporádicos7-9.
El Hospital Posadas es centro de referencia en gastroenterología y hematooncología pediátrica.
El objetivo de este estudio es describir las formas de presentación más frecuentes del cáncer colorrectal en niños y adolescentes atendidos en nuestro hospital y detectar posibles condiciones predisponentes de esta enfermedad.
Materiales y métodosEstudio analítico, observacional, retrospectivo. Se utilizó la lista de verificación STROBE Checklist.
Se revisaron las historias clínicas de los pacientes de 17 años o menores con diagnóstico confirmado histopatológicamente de cáncer de colon atendidos en el Hospital Nacional Profesor Alejandro Posadas entre enero de 2000 y diciembre de 2021. Los datos analizados incluyen signos y síntomas de presentación, duración de los síntomas, tiempo de diagnóstico, ubicación del tumor primario, hallazgos patológicos, modalidad de tratamiento, seguimiento y resultado.
La evaluación incluyó antecedentes personales completos, antecedentes familiares, examen físico, exámenes de laboratorio, Rx de abdomen, ecografía abdominal, colonoscopia y tomografía computarizada de cuerpo entero10.
Estudios diagnósticos realizados: Rx de abdomen de pie, ecografía abdominal, TAC de tórax, abdomen y pelvis con contraste endovenoso, colonoscopia.
Análisis estadísticoLas variables cualitativas se describen con recuento de casos y porcentajes. Las variables numéricas se expresan a través de medidas de tendencia central y dispersión respetando la distribución de los datos.
Las variables del estudio son: sexo, edad, signos y síntomas, antecedentes personales completos, antecedentes familiares, examen físico, exámenes de laboratorio, colonoscopia y tomografía computarizada de cuerpo entero, duración de los síntomas, tiempo de diagnóstico, ubicación del tumor, hallazgos patológicos, modalidad de tratamiento, seguimiento, evolución en el tiempo.
Consideraciones éticasEl protocolo del trabajo fue aprobado por el comité de ética en investigación del Hospital Nacional Profesor Alejandro Posadas. El mismo está inscripto con el código de registro para el CEIHP, ref.: 801 LUPOSO/23.
El proyecto respeta las guías de la CIOMS (2016), la resolución del Ministerio de Salud de la Nación N.° 1480/11 y la Disposición 6677/10 de la ANMAT.
El consentimiento informado no se solicitó para la publicación de este trabajo, porque en el presente artículo no se publican datos personales que permitan identificar al paciente. Se preserva el anonimato de los datos de los mismos de acuerdo con la legislación actual de habeas data y siguiendo las normas de investigación en seres humanos.
ResultadosDe 12 pacientes con cáncer colorrectal, 8 fueron adenocarcinoma, 2 linfomas, 1 tumor estromal y 1 tumor tipo Ewing.
El grupo con adenocarcinoma consistió en 8 pacientes: 5 mujeres y 3 hombres, de 11 a 17 años. La mediana de edad fue de 16 años. La mediana de duración de los síntomas hasta el diagnóstico fue de 9 semanas (rango 1-24 semanas).
Sus perfiles clínicos se resumen en la tabla 1.
Pacientes
| Edad/Sexo | Presentación clínica | Duración de los síntomas | Localización del tumor | Cirugía | Anatomía patológica | Seguimiento |
|---|---|---|---|---|---|---|
| 13/F | Torsión de ovario | 1 semana | CarcinomatosisColon izquierdo | Colostomía paliativa | Carcinoma. Células en anillo de selloEstadio IV | Sospecha síndrome de LynchFalleció 7 meses después de la cirugía |
| 16/F | Invaginación.Dolor abdominal.Sangrado rectal | 1 semana | Colon izquierdo | Hemicolectomía izquierda. Colectomía total | Carcinoma. Células en anillo de sello.Estadio IIIB | ¿Poliposis adenomatosa familiar?Falleció 6 años después del diagnóstico |
| 16/F | Sospecha de apendicitis | 6 semanas | Colon derecho | Apendicectomía. Hemicolectomía derecha | Adenocarcinoma moderadamente diferenciado. Estadio IV | Falleció 36 meses después del diagnóstico. Metástasis cerebrales |
| 16/M | Sospecha de apendicitis | 12 semanas | Colon derecho | Apendicectomía. Hemicolectomía derecha | Adenocarcinoma bien diferenciado. Estadio IIB | Vivo 10 años después del diagnóstico sin evidencia de recurrencia |
| 17/F | Dolor abdominal, vómitos, debilidad y sangrado rectal | 12 semanas | Colon derecho. Metástasis hepáticas | Colostomía paliativa | Carcinoma. Células en anillo de sello. Enfermedad metastásica.Estadio IV | Falleció 6 meses después del diagnóstico |
| 11/M | Sospecha de apendicitis | 9 semanas | Colon derecho | Hemicolectomía derecha | Adenocarcinoma moderadamente diferenciado. Estadio IIIC | Falleció 4 meses después del diagnóstico |
| 11/M | Dolor abdominal. Sangrado rectal | 9 semanas | Colon izquierdo | Hemicolectomía izquierda | Células en anillo de sello. Carcinomatosis peritoneal.Estadio IV | Falleció 6 meses después del diagnóstico |
| 12/F | Dolor abdominal. Sangrado rectal | 24 semanas | Colon derecho | Hemicolectomía derecha | Adenocarcinoma bien diferenciado. Estadio I | Viva 3 años después del diagnóstico |
La sintomatología que predominó al momento del diagnóstico en los pacientes con adenocarcinoma fue dolor abdominal en los 8 pacientes, vómitos en 5, hematoquezia en 4, pérdida de peso en 3 y tumor abdominal en 3.
Cuatro pacientes comenzaron con dolor abdominal en cuadrante inferior derecho; en 3 de ellos se sospechó apendicitis y fueron operados, y posteriormente (después de 6-12 semanas) fueron reintervenidos por oclusión intestinal; el tumor se observó en esta segunda cirugía y solo uno en la primera cirugía.
Laboratorio: presentaron anemia 5 pacientes (con Hb menor de 11.5g/dl), hipoalbuminemia (albúmina menor 3.5g/dl) 4 pacientes, y en cuanto al antígeno carcinoembrionario, 5 pacientes presentaban aumento, con un valor medio de 48.2ng/ml.
En 6 niños, el tumor primario estaba en el colon derecho.
Solo 2 pacientes tenían colonoscopia previa, y el diagnóstico se realizó antes de la cirugía. El diagnóstico de los otros 6 pacientes fue en la cirugía; eso fue porque esta enfermedad no fue pensada. Los 6 pacientes se sometieron a una colonoscopia después de la cirugía para la evaluación de la estadificación, y sus familias se incluyeron en el programa de detección11,12.
Los hallazgos histopatológicos incluyeron adenocarcinoma mucinoso en los 8 pacientes, con células tipo anillo de sello en 4 casos.
Para la estadificación del tumor utilizamos la clasificación de Dukes modificada: un paciente tenía enfermedad en estadioI, uno estadioIIb, un paciente estadioIIIb y uno estadioIIIc, y los otros 4 tuvieron estadioIV (sitios metastásicos: paciente 1 hígado, carcinomatosis peritoneal y cerebro, paciente 2 hígado y pulmón, paciente 3 hígado y carcinomatosis peritoneal, paciente 4 hígado).
Tras completar el diagnóstico y la estadificación, el tratamiento consistió en cirugía, quimioterapia, inmunoquimioterapia y/o radioterapia.
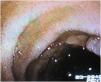
La cirugía primaria en 3 pacientes fue una colostomía paliativa; a uno de ellos se le realizó hemicolectomía izquierda (fig. 1), a 4 de los pacientes se les realizó hemicolectomía derecha, y al otro paciente, con diagnóstico endoscópico de poliposis adenomatosa, se le realizó una colectomía total en la segunda cirugía.
Todos los pacientes, excepto 2, recibieron quimioterapia adyuvante: FOLFOX-4 (oxaliplatino, fluorouracilo, leucovorina) en cuatro pacientes, 5-FLU +LV (fluorouracilo, leucovorina) en un paciente y mFOLFOX-6 en un paciente. Además, 2 pacientes recibieron bevacizumab (inhibidor del receptor del factor de crecimiento endotelial vascular) y otros 2 pacientes recibieron cetuximab (inhibidor del receptor del factor de crecimiento epidérmico). Un paciente presentó metástasis cerebrales un año después de hemicolectomía derecha, y se administró radio y quimioterapia adyuvante con cetuximab y capecitabina (fluoropirimidina oral).
La evolución de nuestros pacientes fue la siguiente: uno de nuestros pacientes está libre de enfermedad 8 años después del diagnóstico y uno está libre de enfermedad 3 años después del diagnóstico. Seis de los niños murieron de enfermedad progresiva.
Condiciones predisponentes: la madre de una niña que tenía un diagnóstico de carcinoma de ovario al mismo tiempo que el cáncer colorrectal murió de cáncer gástrico, por lo que no fue posible una evaluación de marcadores de cáncer colorrectal no polipósico hereditario (CCNPH)13,14.
No se pudo realizar el estudio genético en nuestros pacientes.
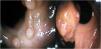
Una paciente presentaba 9 pólipos hiperplásicos en la primera cirugía, y en las siguientes endoscopias se observaron varios pólipos adenomatosos en duodeno y colon, pero no presentaba ningún caso familiar de poliposis adenomatosa familiar (PAF) (figs. 2 y 3).
Ninguno de nuestros pacientes presentó colitis ulcerosa.
Discusión y conclusionesEl cáncer colorrectal es muy poco frecuente en la población pediátrica.
Por lo general, se consideraba que el cáncer de colon era una enfermedad del colon izquierdo o distal. Sin embargo, el 40-60% de los pacientes menores de 20 años desarrollan un tumor primario de colon en el colon derecho, como ocurrió en nuestro grupo, donde 4 de los tumores se localizaron en el colon proximal6.
En adultos, a pesar de los numerosos ensayos clínicos realizados en todo el mundo, la supervivencia global a los 5 años se mantiene sin cambios en aproximadamente un 50-60%4. La transición de la mucosa colónica normal al pólipo adenomatoso y al cáncer colorrectal puede demorar más de una década. Su lento crecimiento y epidemiología justifican enfoques de detección agresivos, que generalmente faltan, y el 85% de los casos nuevos se diagnostican a medida que se examinan los síntomas. El cribado sistemático puede reducir tanto las tasas de incidencia como las tasas de morbimortalidad, por lo que un diagnóstico precoz puede mejorar la tasa de supervivencia global a los 5 años hasta aproximadamente un 90%15,16. Sin embargo, esto no se suele hacer en niños debido a la baja prevalencia de este tumor7.
En pediatría, la supervivencia global estimada a los 5 y 10 años según los datos del programa SEER es del 40% y del 31%, respectivamente. La supervivencia libre de eventos (SSC) a los 10 años es del 17.7%. Estos valores difieren de la población adulta, cuya supervivencia global a los 5 y 10 años es del 60% y del 54%, respectivamente (p<0.001)15.
Los niños cuyos antecedentes familiares y exámenes físicos predicen un alto riesgo hereditario de cáncer de colon deben incluirse en los programas de detección3,10,11.
Las guías de Bethesda y Ámsterdam constituyen un enfoque útil para identificar a los pacientes con riesgo de CCNPH. Los familiares de primer grado de los pacientes cumplen criterios de tamizaje, por lo que deben ser seguidos por cáncer colorrectal17-21.
El pronóstico del cáncer colorrectal informado en niños sigue siendo muy malo, a pesar de las herramientas de diagnóstico avanzadas, los procedimientos quirúrgicos y la quimiorradioterapia mejorada. La mayoría de los casos informados de cáncer colorrectal en la infancia se caracterizan por una etapa avanzada de la enfermedad en la presentación debido a un retraso en el diagnóstico y al comportamiento biológico agresivo del tumor, en lugar del índice de crecimiento lento que se observa en los adultos. Esto se atribuye a la alta tasa de histología mucinosa, que tiene una baja respuesta a la quimioterapia. El carcinoma mucinoso de colon representa solo del 5 al 15% de todos los casos de cáncer colorrectal en adultos. En cambio, se ha reportado en más del 50% de los casos en niños3,7,8. Todos nuestros pacientes tenían este tipo de cáncer, y 4 de ellos también tenían el tipo de células en anillo de sello, lo que empeoró el pronóstico. En un artículo del National Cancer Database de Estados Unidos también vieron el mismo tipo de histología, concluyendo que aumentaba la mortalidad5,22.
Existen muy pocos reportes de cáncer colorrectal en población pediátrica. Ferrari et al.23 reportaron siete pacientes, y Cortez-Pinto et al.24 describieron cinco pacientes, confirmando la baja prevalencia y el mal pronóstico de esta enfermedad en niños y en adolescentes. Kravarusic et al.25 reportaron 7 casos y señalaron el comportamiento tumoral agresivo y el diagnóstico tardío en pacientes pediátricos. En ambos trabajos los síntomas fueron similares a los de nuestro grupo. Lo que no fue reportado en la literatura fue el dolor abdominal agudo, presente en 3 de nuestros pacientes, lo que hizo sospechar apendicitis. El único reporte de nuestro país es un trabajo de Chantada et al.26 en 14 pacientes menores de 20 años de tres hospitales pediátricos y 7 pacientes de 21 a 30 años de dos centros de adultos. En este estudio, los pacientes más jóvenes tenían peor pronóstico que el grupo de mayor edad. En los cuatro estudios, el resultado de los pacientes fue similar al de nuestro grupo, y se consideraron los mismos hechos para el mal pronóstico en pacientes jóvenes en comparación con pacientes adultos.
En un artículo de Sultan et al.27, con datos del SEER y con 159 niños y adolescentes, el adenocarcinoma era el histiotipo más común; sin embargo, los niños/adolescentes tenían histiotipos más desfavorables (es decir, adenocarcinoma mucinoso [22%] y células en anillo de sello, carcinoma [18%]) en comparación con los adultos (10% y 1%, respectivamente).
Wu et al.28 analizaron 284 pacientes pediátricos con cáncer colorrectal, y tuvieron peor pronóstico los que tenían adenocarcinoma mucinoso y con células en anillo de sello (p<0.001). Estos hallazgos coinciden con los de nuestros pacientes.
Hill et al.29 presentóaron77 pacientes de 7 a 19 años derivados al St. Jude Children Research Hospital entre 1964 y 2003, donde sugieren que la biología del cáncer colorrectal (con una mayor prevalencia de histología mucinosa) difiere en pacientes pediátricos y adultos y puede contribuir a un mal resultado. Argumentan que el estadio de la enfermedad fue un predictor significativo de la supervivencia, así como que los tumores no mucinosos tuvieron una ventaja significativa en la supervivencia; y los tumores con una proporción de células en anillo de sello de más del 10% también se asociaron significativamente con malos resultados. La supervivencia a 10 años para todos los pacientes fue del 20.1% en este trabajo.
En las últimas publicaciones se observa una incidencia creciente de cáncer colorrectal entre la población más joven, menor de 50 años30-32.
En la infancia, el cáncer de colon suele asociarse a trastornos hereditarios y antecedentes familiares, a diferencia de los casos adultos; sin embargo, en nuestra población no pudimos encontrar asociación ni con PAF ni con colitis ulcerosa. En el paciente con sospecha de síndrome de Lynch (CCNPH) no pudimos evaluar marcadores para esta enfermedad3,12.
Perrott et al.33 mostraron una asociación positiva entre la exposición a antibióticos en la infancia y cáncer de colon en jóvenes, en especial de colon derecho en un estudio presentado en la European Society for Medical Oncology (ESMO) en 2021.
Los síntomas más comunes en nuestros pacientes fueron dolor abdominal, vómitos, pérdida de peso, masa abdominal y proctorragia, los cuales son inespecíficos y comunes a varias enfermedades gastrointestinales; esto explica la poca concienciación de los pediatras34.
En nuestra población la duración media de los síntomas antes del diagnóstico fue de 9 semanas. No pudimos medir la pérdida de peso de nuestros pacientes debido a que la mayoría eran adolescentes que no fueron llevados a control pediátrico, por lo que se consideró este síntoma en base al relato de sus padres.
La cirugía adecuada es el pilar del tratamiento, complementado con quimio y radioterapia, pero el estado avanzado de la enfermedad en la mayoría de nuestros pacientes imposibilitó el uso de cirugía radical para obtener mejores resultados, de manera similar a lo encontrado en los diversos reportes de la literatura.
Aunque el número de pacientes es similar a lo reportado en la literatura, no es suficiente para sacar conclusiones definitivas, por lo que será importante realizar más estudios multicéntricos.
Concluimos que el cáncer colorrectal es una patología infrecuente y de muy mal pronóstico en la edad pediátrica. Un hallazgo de sangrado rectal persistente, masa abdominal o dolor abdominal inexplicable no debe subestimarse en pacientes pediátricos, particularmente si tienen pérdida de peso. El diagnóstico precoz y un abordaje multidisciplinario para el tratamiento y el seguimiento son importantes para mejorar el pronóstico.
FinanciaciónNo se recibió financiamiento de ningún tipo.
Conflicto de interesesLos autores declaramos que no tenemos ningún conflicto de intereses.