Existen anormalidades en el esfínter pilórico que pueden ser detectadas en la gastroparesia. La inyección de toxina botulínica tipo A (BoNT/A) en el píloro ha sido utilizada en el tratamiento de gastroparesia con diversos resultados. El objetivo del presente artículo fue evaluar si existía correlación entre las características del esfínter pilórico observadas con el catéter luminal de imagen funcional (EndoFLIP®) con planimetría por impedancia en pacientes con gastroparesia, y síntomas, vaciamiento gástrico y respuesta terapéutica tras inyección de BoNT/A en esfínter pilórico.
MétodosEl estudio con EndoFLIP® se llevó a cabo en pacientes en tratamiento para gastroparesia con BoNT/A. Se utilizó el índice de síntoma cardinal de gastroparesia (GSCI por sus siglas en inglés) antes del tratamiento y a las 2, 4, 8 y 12 semanas después del tratamiento.
ResultadosSe reclutó a 44 pacientes (30 con gastroparesia idiopática, 14 con gastroparesia diabética). Se encontró correlación entre menor diámetro pilórico, área de sección transversal (AST) y distensibilidad, y vómito y arcadas más intensos en la evaluación basal. También se observó una tendencia a correlacionar de mayor retención gástrica con el AST y una distensibilidad pilórica disminuidas. El tratamiento con BoNT/A dio como resultado una disminución significativa en el GSCI a las 2 y 4 semanas después del tratamiento, pero no a las 8 o 12 semanas después. La náusea, la saciedad temprana, la plenitud posprandial y el dolor abdominal superior mejoraron hasta 12 semanas, mientras que la pérdida de apetito, la plenitud gástrica y el estómago visiblemente más grande mejoraron solo hasta 4 semanas. Las arcadas y el vómito no mejoraron. La elasticidad pilórica basal correlacionó con un mayor grado de mejora de saciedad temprana y náuseas a las 8 semanas, y la mayor distensibilidad pilórica correlacionó con una mejora en el dolor abdominal.
ConclusionesLas características del píloro observadas con EndoFLIP® proporcionaron información fisiopatológica importante relacionada a síntomas, vaciamiento gástrico y predicción de respuesta a tratamiento dirigido al píloro en pacientes con gastroparesia.
Pyloric sphincter abnormalities may be detected in gastroparesis. Botulinum toxin A (BoNT/A) injection into the pylorus has been used to treat gastroparesis with varying results. The aim of the present article was to assess whether pyloric sphincter characteristics using the endoscopic functional lumen imaging probe (EndoFLIP®) with impedance planimetry in patients with gastroparesis correlated with symptoms, gastric emptying, and therapeutic response to pyloric sphincter BoNT/A injection.
MethodsEndoFLIP® study was performed on patients undergoing gastroparesis treatment with BoNT/A. The gastroparesis cardinal symptom index (GCSI) was applied prior to treatment and at post-treatment weeks 2, 4, 8, and 12.
ResultsForty-four patients were enrolled (30 with idiopathic gastroparesis, 14 with diabetic gastroparesis). Smaller pyloric diameter, cross-sectional area (CSA), and distensibility correlated with worse vomiting and retching severity at baseline. Greater gastric retention tended to correlate with decreased CSA and pyloric distensibility. BoNT/A treatment resulted in a significant decrease in the GCSI score at 2 and 4 weeks after treatment, but not at post-treatment weeks 8 or 12. Nausea, early satiety, postprandial fullness, and upper abdominal pain improved up to 12 weeks, whereas loss of appetite, stomach fullness, and stomach visibly larger improved only up to 4 weeks. Retching and vomiting failed to improve. Greater pyloric compliance at baseline correlated with greater improvement in early satiety and náusea at 8 weeks and greater pyloric distensibility correlated with improvement in upper abdominal pain.
ConclusionsEndoFLIP® characteristics of the pylorus provided important pathophysiologic information in patients with gastroparesis, in relation to symptoms, gastric emptying, and predicting the response to treatment directed at the pylorus.
La gastroparesia es un trastorno en el que se presenta retraso en el vaciamiento gástrico en ausencia de obstrucción mecánica1. La gastroparesia generalmente tiene 3tipos de etiología: diabética, idiopática y postoperatoria. Los síntomas de náuseas, saciedad temprana y plenitud posprandial atribuidas a la gastroparesia se correlacionan, aunque débilmente, al vaciamiento gástrico retardado2,3.
Aunque se asocia la hipomotilidad antral con el vaciamiento gástrico retardado4, es la apertura del esfínter pilórico lo que finalmente permite que el vaciamiento gástrico ocurra. El píloro es un esfínter relativamente poco estudiado y su fisiopatología en la gastroparesia no está bien comprendida. Estudios previos han analizado la presión del esfínter pilórico utilizando manometría con agua5, manometría de alta resolución6 y, más recientemente, el catéter luminal de imagen funcional (EndoFLIP®, modelo EF325N, Crospon Ltd., Galway, Irlanda)7-9. Se ha observado que pacientes con gastroparesia diabética tienen periodos prolongados de tono pilórico elevado y contracciones fásicas llamados «piloroespasmo»10. Algunos tratamientos de gastroparesia están dirigidos al píloro: inyecciones de toxina botulínica tipo A (BoNT/A) al píloro11,12, piloroplastia/piloromiotomía13 y colocación de stent en píloro14. La inyección de BoNT/A al píloro ha sido utilizada para tratar la gastroparesia con diversos resultados11,12,15,16, pero no han sido superiores al placebo en estudios con control17,18. La identificación de los pacientes que podrían beneficiarse del tratamiento al píloro no es clara.
El EndoFLIP® es una tecnología que ha sido utilizada para evaluar el esfínter esofágico inferior (EEI) en acalasia y enfermedad por reflujo gastroesofágico (ERGE)19-21. Actualmente, se utiliza como auxiliar en la evaluación de pacientes elegibles y como guía para tratamientos quirúrgicos de EEI, tales como la funduplicatura de Nissen en ERGE y esofagomiotomía para acalasia22,23. El EndoFLIP® usa un globo con 16 sensores, el cual es inflado dentro de un esfínter y evalúa su diámetro, área de sección transversal (AST), presión, distensibilidad y elasticidad. La utilización de EndoFLIP® en el esfínter pilórico es relativamente nueva. Se ha demostrado una mayor presión y menor elasticidad del esfínter pilórico en pacientes con gastroparesia en comparación con pacientes voluntarios normales a través de mediciones con el EndoFLIP®7.
El objetivo de este estudio fue medir la presión pilórica, el AST, la elasticidad y la distensibilidad utilizando la impedancia por planimetría de EndoFLIP® en pacientes con gastroparesia. Reclutamos a pacientes con gastroparesia en tratamiento de inyección de BoNT/A al píloro para nuestro estudio de prueba de concepto y buscar correlación entre características basales del esfínter pilórico, síntomas, vaciamiento gástrico y respuesta a inyecciones de BoNT/A en esfínter pilórico.
MétodosSe solicitó a pacientes con gastroparesia a los que se les estuviera realizando endoscopia superior por tratamiento de inyección de BoNT/A al píloro que participaran en el presente análisis del esfínter pilórico utilizando EndoFLIP®. El Comité Institucional de Ética de la Universidad de Temple aprobó el estudio y uno de los investigadores obtuvo el consentimiento informado de los pacientes. Previo al procedimiento, cada paciente contestó el cuestionario para la evaluación del paciente de síntomas gastrointestinales superiores (PAGI-SYM por sus siglas en inglés)24, el cual incluye el GCSI25, para evaluar la gravedad de sus síntomas de gastroparesia.
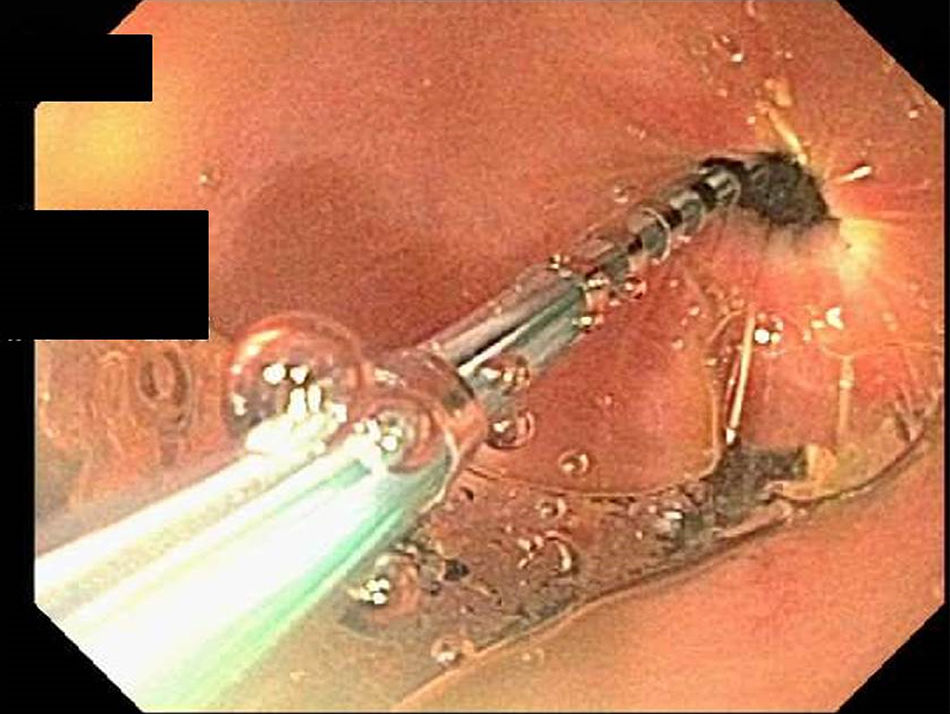
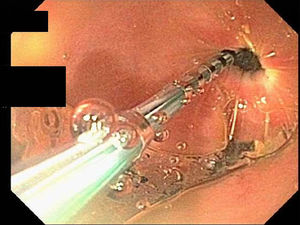
ProcedimientoLos pacientes realizaron ayuno la noche anterior al examen. La endoscopia fue realizada de acuerdo con el protocolo clínico estándar de la unidad de Gastroenterología del Hospital de la Universidad de Temple. Se colocó al paciente en posición decúbito lateral izquierda y fue sedado con propofol utilizando cuidado anestésico monitorizado. Se insertó un endoscopio terapéutico de diámetro grande (modelo Olympus GIF-1TH190) oralmente en el esófago y luego en el estómago. Se realizó el examen endoscópico inicial hasta el antro sin cruzar el píloro. A continuación, se pasó el catéter EndoFLIP® (modelo EF325N, Crospon Ltd., Galway, Irlanda) a través del canal de biopsia del endoscopio terapéutico de diámetro grande (como auxiliar en el paso del catéter al píloro); todo bajo visualización endoscópica directa (fig. 1), como hemos reportado previamente8.
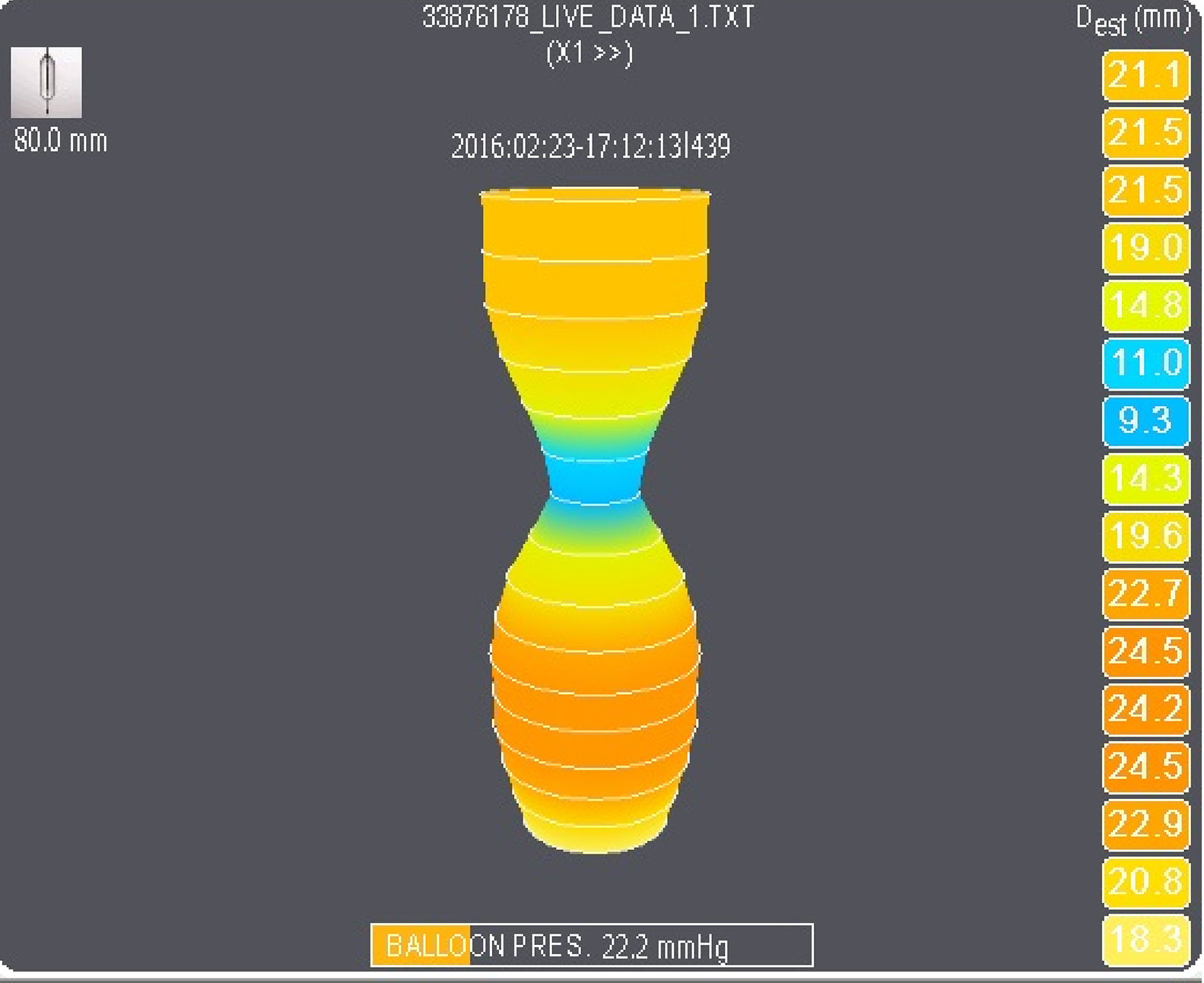
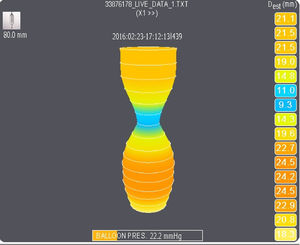
Con el catéter de globo EndoFLIP® en el píloro, se infló el globo a un ritmo de 1 cc/s hasta llegar a 30ml. El píloro fue evaluado utilizando las dimensiones del globo EndoFLIP® a 30 cc y después a 40 cc. El píloro fue medido utilizando el sistema EndoFLIP® modelo EF-100 con software Revision y el catéter EndoFLIP® EF-325N. La presión fue medida con el transductor de presión ubicado dentro del globo (fig. 2). El área (A) fue medida utilizando impedancia por planimetría, basada en la ley de Ohm, y el diámetro fue derivado como la raíz cuadrada de 4 A/π. La distensibilidad fue calculada como la mínima AST dividida entre la presión de cada volumen de llenado del globo. Estas mediciones fueron realizadas después de inflado el globo en cada distención del mismo por un mínimo de 5 s. La elasticidad y la distensibilidad están relacionadas con la habilidad del esfínter para estirarse. La distensibilidad es calculada tomando el punto más angosto del esfínter, midiendo su AST y dividiéndolo entre su presión. Es una medida de qué tan fácilmente se estira el punto más angosto del esfínter. La elasticidad es calculada tomando el volumen de entre 1 cm arriba y 1 cm abajo del punto más angosto del esfínter y dividiendo ese volumen entre la presión de distención. La elasticidad proporciona información sobre la facilidad de estiramiento dentro de la totalidad del esfínter (2cm de longitud) y no solamente en un punto (el más angosto). La mayoría de los reportes en la literatura relevante utilizan la distensibilidad.
Una vez realizada la evaluación del píloro con el EndoFLIP®, se retiró el catéter a través del canal de biopsia. A continuación, se intubó el píloro con el endoscopio para completar la endoscopia superior, para realizar la inyección circunferencial de 200 unidades (5 inyecciones de 40 U) de BoNT/A (BOTOX®, Allergan plc, Dublín, Irlanda) en el píloro11,12,18.
Evaluaciones de seguimientoSe aplicó el cuestionario PAGI-SYM en seguimiento de 2, 4, 8 y 12 semanas24. El paciente también respondió la escala de valoración del paciente clínico (CPGAS por sus siglas en inglés) en las mismas visitas para evaluar la respuesta clínica al tratamiento de los síntomas generales de gastroparesia en una escala de 0 (sin cambio) a 7 (completa mejoría)26,27. Se revisó la prueba de vaciamiento gástrico previa del paciente.
Análisis de datosLos datos fueron reportados como cuentas o porcentajes para las variables categóricas y media ± SD (o mediana [rango o rango intercuartil]) para las variables continuas para los pacientes con gastroparesia en general, al igual que por grupo (diabéticos vs. idiopáticos). Se utilizó el coeficiente de correlación de Spearman para evaluar la asociación de las medidas EndoFLIP®, en cada volumen de llenado del globo, con la gravedad de los síntomas de acuerdo con los resultados en el PAGI-SYM, el GCSI o de vaciamiento gástrico en línea base o las mejoras subsiguientes después del tratamiento en las citas de seguimiento, en relación con gastroparesia en general, al igual que con el tipo de enfermedad, según correspondiera. Los efectos del tratamiento con inyección de BoNT/A sobre los síntomas en CPGAS, CGSI y algunos de PAGI-SYM fueron reportados utilizando cambios en el resultado (resultado en seguimiento menos resultado de línea base) en las semanas 2, 4, 8 y 12 de las visitas de seguimiento. Un cambio expresado en un número negativo en la escala de síntomas representó una mejoría en los síntomas. La prueba de rangos con signo Wilcoxon fue utilizada para evaluar si existió una mejora estadísticamente significativa en cualquiera de las medidas antes mencionadas y la prueba exacta de Fisher fue utilizada para comparar una variable categórica en 2grupos de pacientes (p. ej., tipos de enfermedad). No se realizaron múltiples ajustes a las pruebas, debido a la naturaleza exploratoria del estudio. Los valores de p de menos de 0.05 fueron considerados estadísticamente significativos. Se utilizó la versión 9.3 del software SAS (SAS Institute Inc., Cary, NC, EE. UU.) para todos los análisis estadísticos.
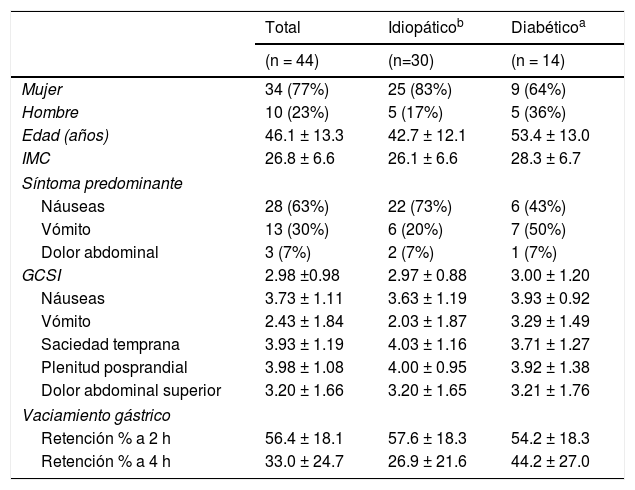
ResultadosPacientesEn la tabla 1 se muestra toda la información demográfica de los 44 pacientes con gastroparesia a quienes se les realizó la inyección pilórica con BoNT/A y la medición de píloro con EndoFLIP®. Treinta y cuatropacientes (77%) fueron mujeres y 10 (23%) fueron hombres. La media ± SD de la edad de los pacientes fue 46.1 ± 13.3 y el índice de masa corporal fue 26.8 ± 6.6. Treinta (68%) pacientes tenían gastroparesia idiopática y 14 (32%) pacientes tenían gastroparesia diabética.
Características demográficas y de la enfermedad de los pacientes de gastroparesia en línea base (n = 44)†
| Total | Idiopáticob | Diabéticoa | |
|---|---|---|---|
| (n = 44) | (n=30) | (n = 14) | |
| Mujer | 34 (77%) | 25 (83%) | 9 (64%) |
| Hombre | 10 (23%) | 5 (17%) | 5 (36%) |
| Edad (años) | 46.1 ± 13.3 | 42.7 ± 12.1 | 53.4 ± 13.0 |
| IMC | 26.8 ± 6.6 | 26.1 ± 6.6 | 28.3 ± 6.7 |
| Síntoma predominante | |||
| Náuseas | 28 (63%) | 22 (73%) | 6 (43%) |
| Vómito | 13 (30%) | 6 (20%) | 7 (50%) |
| Dolor abdominal | 3 (7%) | 2 (7%) | 1 (7%) |
| GCSI | 2.98 ±0.98 | 2.97 ± 0.88 | 3.00 ± 1.20 |
| Náuseas | 3.73 ± 1.11 | 3.63 ± 1.19 | 3.93 ± 0.92 |
| Vómito | 2.43 ± 1.84 | 2.03 ± 1.87 | 3.29 ± 1.49 |
| Saciedad temprana | 3.93 ± 1.19 | 4.03 ± 1.16 | 3.71 ± 1.27 |
| Plenitud posprandial | 3.98 ± 1.08 | 4.00 ± 0.95 | 3.92 ± 1.38 |
| Dolor abdominal superior | 3.20 ± 1.66 | 3.20 ± 1.65 | 3.21 ± 1.76 |
| Vaciamiento gástrico | |||
| Retención % a 2 h | 56.4 ± 18.1 | 57.6 ± 18.3 | 54.2 ± 18.3 |
| Retención % a 4 h | 33.0 ± 24.7 | 26.9 ± 21.6 | 44.2 ± 27.0 |
† Resultados expresados como ± SD media para una variable continua o conteo (%) para una variable categórica.
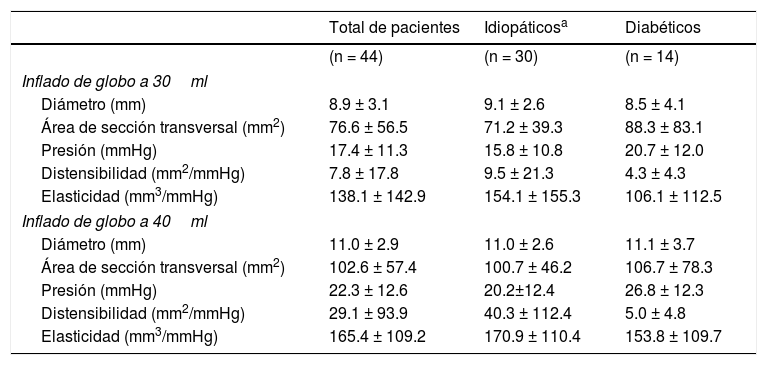
La figura 1 muestra la colocación del catéter de globo del EndoFLIP® en el esfínter pilórico. En la figura 2 se observan una imagen de muestra de las grabaciones con inflado del catéter del globo del EndoFLIP®. Las medidas del esfínter pilórico obtenidas con el EndoFLIP® se muestran en la tabla 2. La mejor observación del contorno del esfínter pilórico fue en la distensión del globo a 40 cc. Las medidas en dicho volumen de inflado fueron: diámetro pilórico 11.0 ± 2.9mm, AST 103 ± 57mm2, presión 22.3 ± 12.6mmHg, distensibilidad 29.1 ± 93.9mm2/mmHg y elasticidad 165 ± 109mm3/mmHg. Las medidas del EndoFLIP® tuvieron un amplio rango. A una distensión del globo de 30 cc los rangos fueron: diámetros pilóricos de 2.7 a 18.8mm, presiones de 0 a 61.9, AST de 20 a 278, elasticidad de 15.5 a 800.6 y distensibilidad de 0.7 a 118.5. Una distensibilidad baja indica un píloro «rígido», mientras que una distensibilidad alta indica un píloro «abierto» o «blando». De los 44 pacientes, 7 tuvieron distensibilidad pilórica ≥ 10mm2/mmHg (6 de ellos con gastroparesia idiopática y uno con gastroparesia diabética). No existieron diferencias estadísticamente significativas en las características pilóricas entre pacientes con gastroparesia idiopática y los de gastroparesia diabética (tabla 2).
Características EndoFLIP de paciente previo a tratamiento de gastroparesia (n = 44)†
| Total de pacientes | Idiopáticosa | Diabéticos | |
|---|---|---|---|
| (n = 44) | (n = 30) | (n = 14) | |
| Inflado de globo a 30ml | |||
| Diámetro (mm) | 8.9 ± 3.1 | 9.1 ± 2.6 | 8.5 ± 4.1 |
| Área de sección transversal (mm2) | 76.6 ± 56.5 | 71.2 ± 39.3 | 88.3 ± 83.1 |
| Presión (mmHg) | 17.4 ± 11.3 | 15.8 ± 10.8 | 20.7 ± 12.0 |
| Distensibilidad (mm2/mmHg) | 7.8 ± 17.8 | 9.5 ± 21.3 | 4.3 ± 4.3 |
| Elasticidad (mm3/mmHg) | 138.1 ± 142.9 | 154.1 ± 155.3 | 106.1 ± 112.5 |
| Inflado de globo a 40ml | |||
| Diámetro (mm) | 11.0 ± 2.9 | 11.0 ± 2.6 | 11.1 ± 3.7 |
| Área de sección transversal (mm2) | 102.6 ± 57.4 | 100.7 ± 46.2 | 106.7 ± 78.3 |
| Presión (mmHg) | 22.3 ± 12.6 | 20.2±12.4 | 26.8 ± 12.3 |
| Distensibilidad (mm2/mmHg) | 29.1 ± 93.9 | 40.3 ± 112.4 | 5.0 ± 4.8 |
| Elasticidad (mm3/mmHg) | 165.4 ± 109.2 | 170.9 ± 110.4 | 153.8 ± 109.7 |
† Resultados expresados como media ± SD para una variable continua.
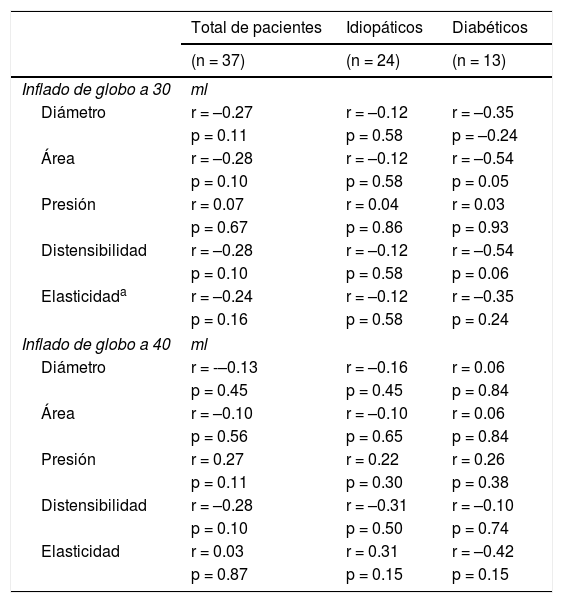
Todos los pacientes en el presente estudio tenían gastroparesia con vaciamiento gástrico retardado. Los porcentajes de retención a las 2 h promediaron 56.4 ± 18.1% (normal < 60%). Los promedios de retención a las 4 h promediaron 33.0 ± 24.7% (normal < 10%) (tabla 1). La tabla 3 muestra las correlaciones de retención gástrica a las 4 h con medidas de EndoFLIP®. La retención gástrica a las 4 h tendió a correlacionar débilmente con distensibilidad con un valor r negativo, utilizando inflados a 30 cc y 40 cc (n = 37; r = –0.28, p = 0.097 y r = –0.28, p = 0.099). Por consiguiente, la distensibilidad pilórica disminuida pareció correlacionar con una mayor retención gástrica en línea base. La correlación con distensibilidad con un valor r negativo fue más prominente en el subgrupo diabético utilizando el inflado a 30 cc (n = 13, r = –0.54, p = 0.06), pero no llegó a ser estadísticamente significativo, posiblemente debido al pequeño tamaño del grupo. La retención gástrica a las 4 h también tendió a correlacionar débil y marginalmente con el AST con un valor r negativo a un inflado de 30 cc (n = 37, r = –0.28, p = 0.098). También la correlación con el AST pilórica con un valor r negativo fue más prominente en el subgrupo diabético (n = 13, r = –0.54, p = 0.054). Por consiguiente, se asoció un píloro más pequeño a una retención gástrica elevada.
Correlación de medidas EndoFLIP con vaciamiento gástrico (retención % a 4 horas) en línea base†
| Total de pacientes | Idiopáticos | Diabéticos | |
|---|---|---|---|
| (n = 37) | (n = 24) | (n = 13) | |
| Inflado de globo a 30ml | |||
| Diámetro | r = –0.27 | r = –0.12 | r = –0.35 |
| p = 0.11 | p = 0.58 | p = –0.24 | |
| Área | r = –0.28 | r = –0.12 | r = –0.54 |
| p = 0.10 | p = 0.58 | p = 0.05 | |
| Presión | r = 0.07 | r = 0.04 | r = 0.03 |
| p = 0.67 | p = 0.86 | p = 0.93 | |
| Distensibilidad | r = –0.28 | r = –0.12 | r = –0.54 |
| p = 0.10 | p = 0.58 | p = 0.06 | |
| Elasticidada | r = –0.24 | r = –0.12 | r = –0.35 |
| p = 0.16 | p = 0.58 | p = 0.24 | |
| Inflado de globo a 40ml | |||
| Diámetro | r = -–0.13 | r = –0.16 | r = 0.06 |
| p = 0.45 | p = 0.45 | p = 0.84 | |
| Área | r = –0.10 | r = –0.10 | r = 0.06 |
| p = 0.56 | p = 0.65 | p = 0.84 | |
| Presión | r = 0.27 | r = 0.22 | r = 0.26 |
| p = 0.11 | p = 0.30 | p = 0.38 | |
| Distensibilidad | r = –0.28 | r = –0.31 | r = –0.10 |
| p = 0.10 | p = 0.50 | p = 0.74 | |
| Elasticidad | r = 0.03 | r = 0.31 | r = –0.42 |
| p = 0.87 | p = 0.15 | p = 0.15 | |
†Resultados expresados como coeficiente de correlación de Spearman (r) y valor-p.
Para caracterizar la gravedad de síntomas en gastroparesia se utilizó el PAGI-SYN (tabla 1). La gravedad de los síntomas en gastroparesia en orden descendente fue: plenitud posprandial (gravedad de síntoma de 4.0 ± 1.1), incapacidad de terminar una comida de tamaño normal (3.9 ± 1.2), náuseas (3.7 ± 1.1), pérdida de apetito (3.7 ± 1.3), plenitud gástrica (3.6 ± 1.3), distensión (3.5 ± 1.5), estómago visiblemente más grande (3.2 ± 1.6), dolor abdominal superior (3.2 ± 1.7), vómito (2.4 ± 1.8) y arcadas (2.3 ± 1.7).
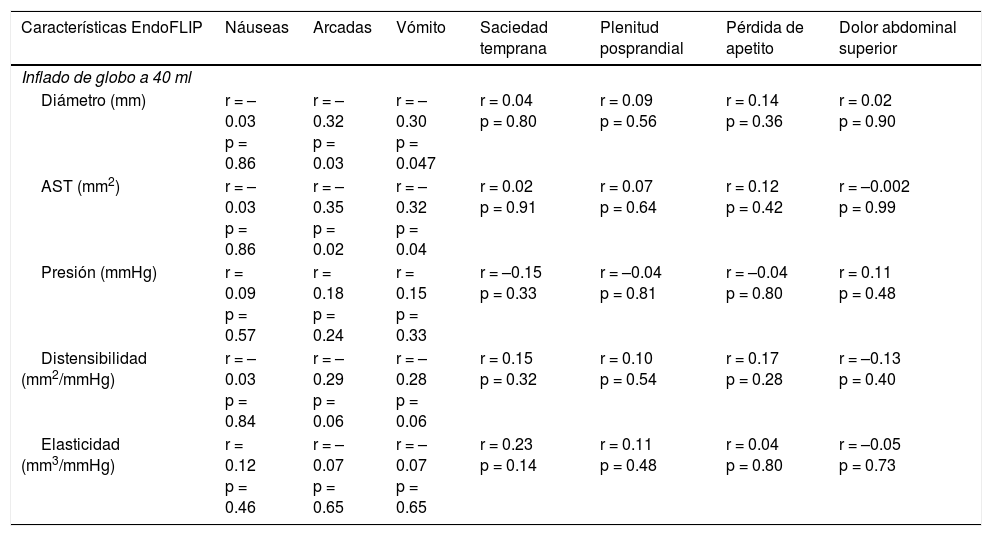
La tabla 4 muestra las correlaciones de varias medidas con EndoFLIP® en línea base utilizando inflado de globo a 40ml con algunos síntomas del PAGI-SYM en línea base. Inflado a 40 cc, el diámetro pilórico y AST menores correlacionaron con una mayor gravedad de vómito (r = –0.30, p = 0.047 y r = –0.32, p = 0.04) y arcadas (r = –0.32, p = 0.03 y r = –0.35, p = 0.02). La distensibilidad pilórica tendió a asociarse con la gravedad de vómito (r = –0.28, p = 0.06) y arcadas (r = –0.29, p = 0.06) en línea base, con valores r negativos, es decir, una menor distensión pilórica (píloro rígido) fue asociada con mayor gravedad de vómito y arcadas.
Correlación de características EndoFLIP utilizando inflado de globo a 40ml con resultados de síntomas específicos en línea base en todos los pacientes (n = 44)†
| Características EndoFLIP | Náuseas | Arcadas | Vómito | Saciedad temprana | Plenitud posprandial | Pérdida de apetito | Dolor abdominal superior |
|---|---|---|---|---|---|---|---|
| Inflado de globo a 40 ml | |||||||
| Diámetro (mm) | r = –0.03 p = 0.86 | r = –0.32 p = 0.03 | r = –0.30 p = 0.047 | r = 0.04 p = 0.80 | r = 0.09 p = 0.56 | r = 0.14 p = 0.36 | r = 0.02 p = 0.90 |
| AST (mm2) | r = –0.03 p = 0.86 | r = –0.35 p = 0.02 | r = –0.32 p = 0.04 | r = 0.02 p = 0.91 | r = 0.07 p = 0.64 | r = 0.12 p = 0.42 | r = –0.002 p = 0.99 |
| Presión (mmHg) | r = 0.09 p = 0.57 | r = 0.18 p = 0.24 | r = 0.15 p = 0.33 | r = –0.15 p = 0.33 | r = –0.04 p = 0.81 | r = –0.04 p = 0.80 | r = 0.11 p = 0.48 |
| Distensibilidad (mm2/mmHg) | r = –0.03 p = 0.84 | r = –0.29 p = 0.06 | r = –0.28 p = 0.06 | r = 0.15 p = 0.32 | r = 0.10 p = 0.54 | r = 0.17 p = 0.28 | r = –0.13 p = 0.40 |
| Elasticidad (mm3/mmHg) | r = 0.12 p = 0.46 | r = –0.07 p = 0.65 | r = –0.07 p = 0.65 | r = 0.23 p = 0.14 | r = 0.11 p = 0.48 | r = 0.04 p = 0.80 | r = –0.05 p = 0.73 |
† Resultados expresados como coeficiente de correlación Spearman (r) y valor-p.
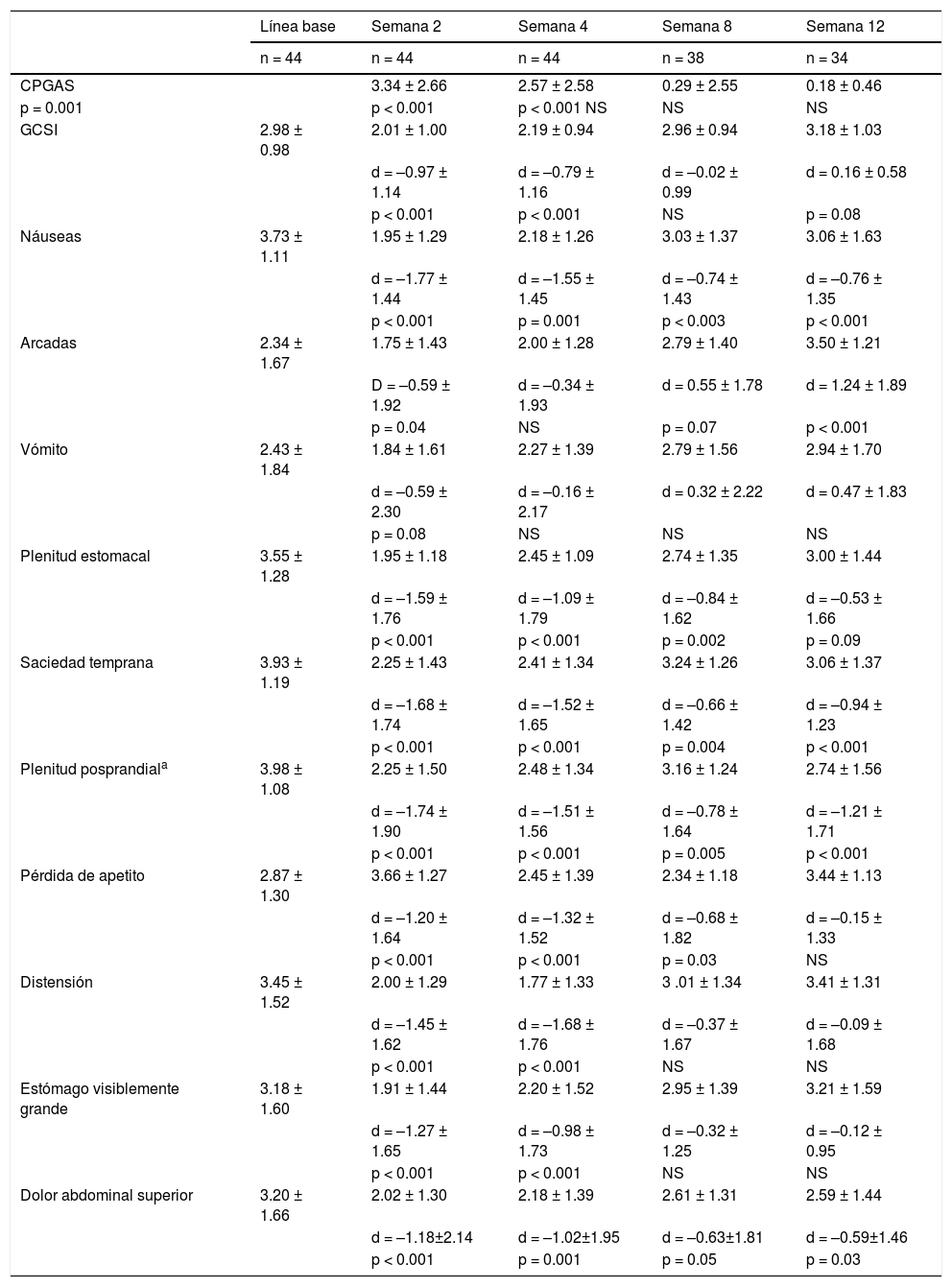
Se observó mejora en los síntomas generales de gastroparesia después de las inyecciones de toxina botulínica al píloro a la semana 4 postinyección, pero no se mantuvo a las semanas 8 y 12 (tabla 5).
Resultados en síntomas específicos en línea base y cambios post tratamiento†
| Línea base | Semana 2 | Semana 4 | Semana 8 | Semana 12 | |
|---|---|---|---|---|---|
| n = 44 | n = 44 | n = 44 | n = 38 | n = 34 | |
| CPGAS | 3.34 ± 2.66 | 2.57 ± 2.58 | 0.29 ± 2.55 | 0.18 ± 0.46 | |
| p = 0.001 | p < 0.001 | p < 0.001 NS | NS | NS | |
| GCSI | 2.98 ± 0.98 | 2.01 ± 1.00 | 2.19 ± 0.94 | 2.96 ± 0.94 | 3.18 ± 1.03 |
| d = –0.97 ± 1.14 | d = –0.79 ± 1.16 | d = –0.02 ± 0.99 | d = 0.16 ± 0.58 | ||
| p < 0.001 | p < 0.001 | NS | p = 0.08 | ||
| Náuseas | 3.73 ± 1.11 | 1.95 ± 1.29 | 2.18 ± 1.26 | 3.03 ± 1.37 | 3.06 ± 1.63 |
| d = –1.77 ± 1.44 | d = –1.55 ± 1.45 | d = –0.74 ± 1.43 | d = –0.76 ± 1.35 | ||
| p < 0.001 | p = 0.001 | p < 0.003 | p < 0.001 | ||
| Arcadas | 2.34 ± 1.67 | 1.75 ± 1.43 | 2.00 ± 1.28 | 2.79 ± 1.40 | 3.50 ± 1.21 |
| D = –0.59 ± 1.92 | d = –0.34 ± 1.93 | d = 0.55 ± 1.78 | d = 1.24 ± 1.89 | ||
| p = 0.04 | NS | p = 0.07 | p < 0.001 | ||
| Vómito | 2.43 ± 1.84 | 1.84 ± 1.61 | 2.27 ± 1.39 | 2.79 ± 1.56 | 2.94 ± 1.70 |
| d = –0.59 ± 2.30 | d = –0.16 ± 2.17 | d = 0.32 ± 2.22 | d = 0.47 ± 1.83 | ||
| p = 0.08 | NS | NS | NS | ||
| Plenitud estomacal | 3.55 ± 1.28 | 1.95 ± 1.18 | 2.45 ± 1.09 | 2.74 ± 1.35 | 3.00 ± 1.44 |
| d = –1.59 ± 1.76 | d = –1.09 ± 1.79 | d = –0.84 ± 1.62 | d = –0.53 ± 1.66 | ||
| p < 0.001 | p < 0.001 | p = 0.002 | p = 0.09 | ||
| Saciedad temprana | 3.93 ± 1.19 | 2.25 ± 1.43 | 2.41 ± 1.34 | 3.24 ± 1.26 | 3.06 ± 1.37 |
| d = –1.68 ± 1.74 | d = –1.52 ± 1.65 | d = –0.66 ± 1.42 | d = –0.94 ± 1.23 | ||
| p < 0.001 | p < 0.001 | p = 0.004 | p < 0.001 | ||
| Plenitud posprandiala | 3.98 ± 1.08 | 2.25 ± 1.50 | 2.48 ± 1.34 | 3.16 ± 1.24 | 2.74 ± 1.56 |
| d = –1.74 ± 1.90 | d = –1.51 ± 1.56 | d = –0.78 ± 1.64 | d = –1.21 ± 1.71 | ||
| p < 0.001 | p < 0.001 | p = 0.005 | p < 0.001 | ||
| Pérdida de apetito | 2.87 ± 1.30 | 3.66 ± 1.27 | 2.45 ± 1.39 | 2.34 ± 1.18 | 3.44 ± 1.13 |
| d = –1.20 ± 1.64 | d = –1.32 ± 1.52 | d = –0.68 ± 1.82 | d = –0.15 ± 1.33 | ||
| p < 0.001 | p < 0.001 | p = 0.03 | NS | ||
| Distensión | 3.45 ± 1.52 | 2.00 ± 1.29 | 1.77 ± 1.33 | 3 .01 ± 1.34 | 3.41 ± 1.31 |
| d = –1.45 ± 1.62 | d = –1.68 ± 1.76 | d = –0.37 ± 1.67 | d = –0.09 ± 1.68 | ||
| p < 0.001 | p < 0.001 | NS | NS | ||
| Estómago visiblemente grande | 3.18 ± 1.60 | 1.91 ± 1.44 | 2.20 ± 1.52 | 2.95 ± 1.39 | 3.21 ± 1.59 |
| d = –1.27 ± 1.65 | d = –0.98 ± 1.73 | d = –0.32 ± 1.25 | d = –0.12 ± 0.95 | ||
| p < 0.001 | p < 0.001 | NS | NS | ||
| Dolor abdominal superior | 3.20 ± 1.66 | 2.02 ± 1.30 | 2.18 ± 1.39 | 2.61 ± 1.31 | 2.59 ± 1.44 |
| d = –1.18±2.14 | d = –1.02±1.95 | d = –0.63±1.81 | d = –0.59±1.46 | ||
| p < 0.001 | p = 0.001 | p = 0.05 | p = 0.03 |
Resultados reportados como media ± SD, con el cambio en línea base (d) y el valor-p asociado por media de cambio = 0.
El resultado en CPGAS, con el que los pacientes evaluaron la mejoría en los síntomas, fue de 3.34 ± 2.66 en gastroparesia en general a las 2 semanas (p < 0.001 contra 0 [sin mejoría]) y 2.57 ± 2.58 a las 4 semanas (p < 0.001), pero no se observó mejoría en promedio a las 8 semanas (0.29 ± 2.55; p > 0.10) o 12 semanas (0.18 ± 0.46; p > 0.10). En el grupo de gastroparesia idiopática, el resultado en CPGAS a las 2 semanas fue 3.30 ± 2.81, 2.30 ± 2.64 a las 4 semanas, –0.33 ± 1.81 a las 8 semanas y 0.14 ± 0.35 a las 12 semanas. En el grupo de gastroparesia diabética, los resultados en CPGAS fueron 3.43 ± 2.41 a las 2 semanas, 3.14 ± 2.44 a las 4 semanas, 1.36 ± 3.27 a las 8 semanas y 0.25 ± 0.62 a las 12 semanas.
Los resultados en CPGAS mostraron mejoría en los síntomas generales de gastroparesia a las 4 semanas en 33 de los 44 pacientes (75%). La respuesta a la semana 4 fue similar en gastroparesia diabética (10/14 = 71%) y en gastroparesia idiopática (23/30 = 77%, p = 0.72). Sin embargo, la tasa de respuesta a la semana 8 fue mayor en gastroparesia diabética (8/14 = 57%) en comparación con gastroparesia idiopática (3/24 = 13%, p = 0.008).
Los resultados en GSCI (media ± SD) fueron significativamente más bajos a las semanas 2 y 4 (2.01 ± 1.00, p < 0.001 y 2.19 ± 0.94, p < 0.001, respectivamente) en comparación con los resultados en línea base (2.98 ± 0.98) (tabla 5). Los resultados en GSCI prácticamente volvieron a sus valores de línea base pretratamiento a las 8 y 12 semanas postratamiento.
Las inyecciones de BoNT/A produjeron una mejoría significativa en los síntomas de náusea, dolor abdominal superior, saciedad temprana y plenitud posprandial a través de las 12 semanas de seguimiento, mientras que se produjo una mejoría significativa en los síntomas de eructo, pérdida de apetito, plenitud estomacal y estómago visiblemente distendido solo hasta las 4 semanas, pero no se mantuvo a las 12 semanas (tabla 5). Las inyecciones de BoNT/A no lograron mejorar los síntomas de vómito y arcadas. Las arcadas fueron peores a la semana 12 de seguimiento, en comparación con los valores basales (una diferencia de 1.2 ± 1.9).
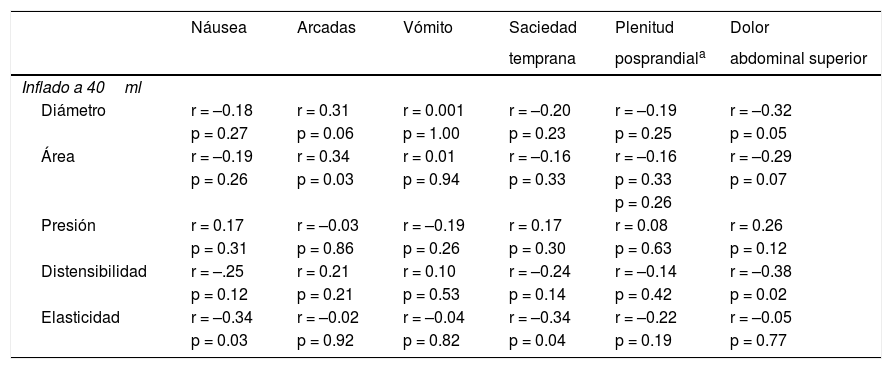
Respuesta clínica y correlaciones con EndoFLIP®Correlacionamos los cambios en los resultados (semana 8-línea base) en gravedad de síntomas 8 semanas después de la inyección con BoNT/A en píloro con las características EndoFLIP® antes de la inyección para evaluar predictores de respuesta sostenida (2 meses) (tabla 6). La elasticidad pilórica utilizando el inflado a 40 cc previa al tratamiento con toxina botulínica fue asociada con una mejora en náusea (r = –0.34, p = 0.03) y saciedad temprana (r = –0.34, p = 0.04) a las 8 semanas con valores de r negativos. En consecuencia, una mayor elasticidad pilórica en línea base estuvo correlacionada con un mayor grado de mejora en saciedad temprana y náuseas con tratamiento con BoNT/A a las 8 semanas. La distensibilidad pilórica en línea base estuvo relacionada con mejoría en el dolor abdominal superior (r = –0.38, p = 0.02), con un valor de r negativo, es decir, una distensibilidad pilórica mayor en línea base estuvo relacionada con un mayor grado de mejoría en el dolor abdominal superior a las 8 semanas. El diámetro pilórico y el área mayores en la línea base parecieron estar relacionados con un empeoramiento en las arcadas con el tratamiento con toxina botulínica (r = 0.31; p = 0.06 y r = 0.34; p = 0.03). Estas relaciones de mejoría en síntomas con los parámetros de línea base con EndoFLIP® estuvieron presentes en uno o ambos subgrupos (datos no incluidos). Por ejemplo, en los pacientes con gastroparesia idiopática (n = 24), se relacionó una mayor elasticidad pilórica en línea base con un mayor grado de mejoría en náusea (r = –0.41, p = 0.046) y en saciedad temprana (r = –0.39, p = 0.06) a las 8 semanas después del tratamiento. Además, una mayor distensibilidad pilórica en línea base estuvo marginalmente relacionada con un mayor grado de mejoría en dolor abdominal superior (r = –0.36, p = 0.08). En los pacientes diabéticos (n = 14), el diámetro pilórico y el área mayores utilizando inflado de globo a 40 cc estuvieron asociados a un mayor grado de mejoría en dolor abdominal superior (r = –0.60, p = 0.02 y r = –0.59, p = 0.03, respectivamente) a las 8 semanas (tabla 6).
Correlación de características EndoFLIP con mejoría en resultados de síntomas específicos a 8 semanas (resultados a 8 semanas-línea base) en todos los pacientes con datos de seguimiento (n = 38)†
| Náusea | Arcadas | Vómito | Saciedad | Plenitud | Dolor | |
|---|---|---|---|---|---|---|
| temprana | posprandiala | abdominal superior | ||||
| Inflado a 40ml | ||||||
| Diámetro | r = –0.18 | r = 0.31 | r = 0.001 | r = –0.20 | r = –0.19 | r = –0.32 |
| p = 0.27 | p = 0.06 | p = 1.00 | p = 0.23 | p = 0.25 | p = 0.05 | |
| Área | r = –0.19 | r = 0.34 | r = 0.01 | r = –0.16 | r = –0.16 | r = –0.29 |
| p = 0.26 | p = 0.03 | p = 0.94 | p = 0.33 | p = 0.33 | p = 0.07 | |
| p = 0.26 | ||||||
| Presión | r = 0.17 | r = –0.03 | r = –0.19 | r = 0.17 | r = 0.08 | r = 0.26 |
| p = 0.31 | p = 0.86 | p = 0.26 | p = 0.30 | p = 0.63 | p = 0.12 | |
| Distensibilidad | r = –.25 | r = 0.21 | r = 0.10 | r = –0.24 | r = –0.14 | r = –0.38 |
| p = 0.12 | p = 0.21 | p = 0.53 | p = 0.14 | p = 0.42 | p = 0.02 | |
| Elasticidad | r = –0.34 | r = –0.02 | r = –0.04 | r = –0.34 | r = –0.22 | r = –0.05 |
| p = 0.03 | p = 0.92 | p = 0.82 | p = 0.04 | p = 0.19 | p = 0.77 | |
† Resultados expresados como coeficiente de correlación Spearman (r) y valor-p.
La gastroparesia es un trastorno difícil de tratar y no es conocido el porqué algunos pacientes responden a ciertas terapias y otros no. Recientemente, los tratamientos para la gastroparesia están siendo dirigidos al píloro, aunque con resultados diversos. La planimetría por impedancia con EndoFLIP® para caracterizar la fisiopatología pilórica en pacientes en tratamiento para gastroparesia fue el núcleo de nuestro estudio. Quisimos evaluar si la fisiopatología pilórica se relacionaba con síntomas y vaciamiento gástrico, y si esto nos ayudaría a predecir qué pacientes podrían responder a la terapia dirigida al esfínter pilórico. En este estudio de prueba de concepto se utilizó el tratamiento con inyecciones de BoNT/A. La retención gástrica a las 4 h tendió a correlacionar negativamente con el AST y la distensibilidad pilórica, con valores r negativos. El diámetro pilórico, el AST y la distensibilidad estuvieron asociados con gravedad de síntoma de arcadas y vómito. Es decir, los síntomas de arcadas y vómito fueron más graves mientras más pequeño y rígido era el píloro.
En el presente estudio, la inyección de BoNT/A en píloro mejoró principalmente los síntomas de náusea, saciedad temprana, plenitud posprandial y dolor abdominal superior en el curso de 4 a 12 semanas, pero los síntomas de arcadas y vómito no mejoraron. De manera interesante, un diámetro pilórico y un área mayores en la línea base parecieron estar relacionados con un empeoramiento en arcadas en el tratamiento con BoNT/A. Una mayor elasticidad pilórica en la línea base estuvo relacionada con un mayor grado de mejoría en náuseas y saciedad temprana. Gourcerol et al. encontraron que la dilación pilórica en pacientes con gastroparesia con elasticidad pilórica baja mejoró sus síntomas gástricos7.
Los parámetros obtenidos con EndoFLIP® en nuestros pacientes fueron muy similares a los obtenidos en el estudio de Gourcerol et al.7, el cual mostró que la distensibilidad pilórica era de 25.2 ± 2.5mm2/mmHg en sujetos normales. La distensibilidad fue anormal si era menor de 10mm2/mmHg. El estudio mencionado anteriormente evaluó el vaciamiento gástrico con prueba de aliento, mientras que en nuestro estudio el vaciamiento gástrico se evaluó por medio de gammagrafía.
Nuestro estudio indica que las características pilóricas evaluadas con EndoFLIP® podrían proporcionar medidas de utilidad para predecir la respuesta de síntomas de gastroparesia a terapias dirigidas al píloro. En este estudio de prueba de concepto, utilizamos inyección de BoNT/A al píloro. Esta ha sido utilizada para tratar la gastroparesia con diversos resultados: parcialmente favorables en estudios abiertos9,10,13,14, pero no superiores a placebo en estudios con control15,16. En el presente estudio encontramos que el tratamiento con BoNT/A resultó en síntomas de gastroparesia disminuidos de acuerdo con el GSCI a las semanas 2 y 4 después del tratamiento, pero esa disminución no se mantuvo a las 8 y 12 semanas después de la inyección. En consecuencia, y de acuerdo con las guías para gastroparesia1, el tratamiento con BoNT/A no es una opción de tratamiento a largo plazo para muchos de los pacientes.
Entre las limitaciones del presente estudio estuvo el hecho de que todos los pacientes recibieron tratamiento con inyecciones de BoNT/A en el píloro; no contamos con un grupo control con placebo. De igual manera, no estudiamos con EndoFLIP® a sujetos normales, lo cual sí fue realizado en el estudio previo realizado por Goucerol et al.7. Sin embargo, demostramos parámetros objetivos del píloro evaluados a través del EndoFLIP® y los correlacionamos con síntomas, vaciamiento gástrico y mejoría en síntomas. Las mediciones con EndoFLIP® fueron realizadas bajo anestesia con propofol, lo que podría tener un efecto en el tono y contractilidad del píloro. Nuestro estudio fue realizado en una sola locación y la cohorte incluyó a 44 pacientes, lo cual puede haber limitado algunas de las relaciones estadísticas, especialmente aquellas en las que los subgrupos de gastroparesia idiopática y gastroparesia diabética fueron analizados. Otras limitaciones incluyen la ausencia de seguimiento EndoFLIP® y vaciamiento gástrico después del tratamiento con BoNT/A, el diseño de estudio abierto y una posible falta de poder estadístico para realizar un análisis más profundo de los subgrupos.
En conclusión, el presente estudio mostró que la planimetría por impedancia del píloro utilizando EndoFLIP® proporcionó información fisiopatológica importante en pacientes con gastroparesia en relación con los síntomas, vaciamiento gástrico y respuesta a tratamiento dirigido al píloro. El área pilórica y la distensibilidad correlacionaron con retención gástrica, al igual que con síntomas de arcadas y vómito. La BoNT/A mejoró los síntomas de náuseas, saciedad temprana, plenitud posprandial y dolor abdominal superior. La elasticidad pilórica correlacionó con mejoría en síntomas de saciedad temprana y náuseas. En consecuencia, el EndoFLIP®, principalmente con el globo inflado a 40 cc, podría proporcionar información fisiopatológica importante sobre el píloro en pacientes con gastroparesia. Dicha información podría ayudar a mejorar nuestra comprensión de la función pilórica y auxiliar a identificar a aquellos pacientes que se podrían beneficiar de las terapias dirigidas al píloro. Nuestro estudio estuvo específicamente relacionado con la utilización de EndoFLIP® para predecir la respuesta a la inyección intrapilórica de BoNT/A. Se requieren más estudios para evaluar el píloro en pacientes con otras causas de gastroparesia y para observar cómo responde el píloro a diferentes tratamientos como la piloromiotomía.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste trabajo no recibió ninguna forma de financiamiento.
AutoríaMohammed Saadi, MD: diseño y concepto del estudio; registro de datos; análisis e interpretación de datos; análisis estadístico; redacción de borrador.
Daohai Yu, PHD: diseño del estudio; análisis e interpretación de datos; análisis estadístico; revisión crítica del manuscrito por contenido intelectual importante.
Zubair Malik, MD: Diseño y concepto de estudio; revisión crítica del manuscrito por contenido intelectual importante.
Henry Parkman, MD: diseño y concepto del estudio; análisis e interpretación de datos; revisión crítica del manuscrito por contenido intelectual importante, supervisión del estudio.
Ron Schey, MD: diseño y concepto del estudio; análisis e interpretación de datos; revisión crítica del manuscrito por contenido intelectual importante.
Conflicto de interesesTodos los autores declaran no tener conflictos de interés.