La última década se ha caracterizado por cambios frecuentes en diversos aspectos relacionados con el carcinoma hepatocelular (CHC). A continuación se comentan algunos temas relevantes en el área presentados en congresos internacionales de la especialidad durante el último año.
Vigilancia. Es claro el beneficio de la vigilancia de los grupos con alto riesgo para desarrollar CHC. Aunque este beneficio fue puesto en duda recientemente, continúa presentándose evidencia que lo confirma. Ahmed et al.1 en el Reino Unido evaluaron el estadio y resultado del tratamiento cuando el diagnóstico se realiza mediante programas de vigilancia vs. ausencia de vigilancia. De los 189 casos de CHC (2009-2012) se incluyeron 169, de los cuales 37 (22%) fueron diagnosticados mediante vigilancia y 132 (78%) no. El diagnóstico se estableció en estadio temprano (BCLC A) en 29.7% en el grupo bajo vigilancia vs. 6.1% en el no sometido a vigilancia (p = 0.0003), y fueron susceptibles a tratamiento curativo (trasplante o resección) más frecuentemente que en el grupo diagnosticado sin vigilancia (13.5% vs. 2.3%, p = 0.01); en consecuencia, la supervivencia también fue mayor (p = 0.02). Llama la atención la baja frecuencia de vigilancia a la población con alto riesgo (22%), similar a la reportada en diversas publicaciones que han evaluado esta práctica. No observaremos una diferencia clara en la supervivencia si no aplicamos la vigilancia de acuerdo a las normas vigentes, y en consecuencia ofrezcamos un tratamiento acorde al estadio.
Hígado graso con/sin cirrosis. Resulta cada vez más evidente el papel que juega el hígado graso no alcohólico (HGNA) como tercera causa de cirrosis y sus complicaciones, precedido por las virales y el alcohol. Davila et al.2 identificaron individuos con CHC procedentes de la Administración de Veteranos en los Estados Unidos durante 2005 a 2011. Excluyeron los causados por virus y alcohol y analizaron diferentes variables en los que denominaron idiopáticos. De 1,200 CHC, 22% fueron catalogados como idiopáticos, la frecuencia de los cuales aumentó de 18% en 2004-2005 a 35% en 2009-2011 (p = 0.03). DM y/o HGNA estuvieron presentes en 60% de estos casos. Este grupo fue sometido menos frecuentemente a programas de vigilancia (p < 0.01), diagnosticado en estadios más avanzados y menos frecuentemente sometido a tratamiento específico. Con una metodología más depurada, Rubayat et al.3 de la Universidad de Missouri analizaron los casos de CHC obtenidos en la base de datos SEER (Surveillance, Epidemiology and End Results) de Medicare desde 1993 a 2007. De 17,895 casos, 2,863 (16%) fueron secundarios a HGNA confirmado; 1,832 (64%) presentaban cirrosis y 1,031 (36%) no; de estos, 18% presentaban únicamente esteatosis. También fue la causa más común después de la infecciosa y el alcohol, y presentó un aumento a partir de 1993. Con base en lo anterior, debemos alertar la posibilidad de investigar enfermedad hepática crónica en este grupo de pacientes (HGNA), desgraciadamente cada vez más frecuente en México y en caso de estar presente, considerar la necesidad de vigilancia a esta población.
Modelos predictivos de desarrollo de CHC. En un interesante trabajo realizado en Canadá, Sharma et al.4 pretendieron identificar variables asociadas al desarrollo de CHC y desarrollar un sistema de puntaje que permita predecir su desarrollo. Utilizaron variables preexistentes en una cohorte de 2,229 cirróticos, de los cuales 374 desarrollaron CHC y habían sido vigilados durante 10 años antes del CHC. Las variables identificadas asociadas fueron: Edad, género, etiología de la cirrosis y puntaje de APRI. La suma de los puntos otorgados por cada variable determinó el riesgo de desarrollar CHC. Ningún individuo con un puntaje < 12 presentó CHC, y 48% de los que tenían > 32 lo presentaron a 10 años (p < 0.0001).
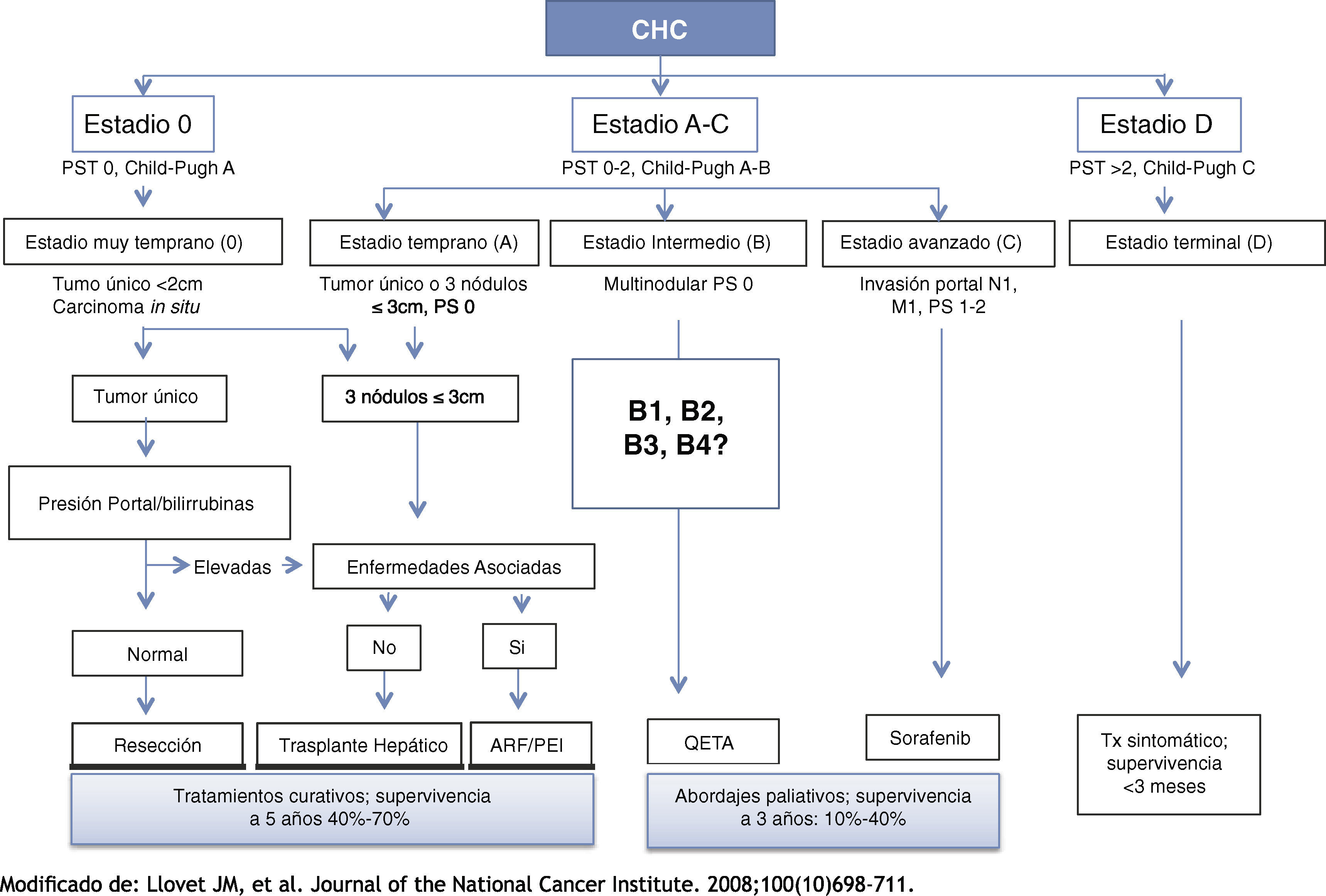
Tratamiento en estadio temprano (BCLC 0 y A). Estos pacientes ameritan abordajes terapéuticos con intención curativa que incluyen resección hepática, trasplante hepático y/o ablación local (fig. 1). Quizás lo más relevante en esta área incluya la apertura de las guías de práctica clínica europeas sobre manejo del CHC5, tanto a la posibilidad de expansión de criterios pretrasplante («up-to-seven») más allá de los tradicionales de Milán, como a la aplicación de tratamientos locorregionales (ablación por radiofrecuencia [ARF] y/o quimioembolización transarterial [QETA]) en lista de espera de trasplante, cuando se estima que ésta sea mayor a 6 meses. En cuanto a la disminución de estadiaje («down-staging»), sugieren se evalúe en estudios prospectivos enfocados a supervivencia y progresión de la enfermedad.
Estadios intermedio y avanzado (BCLC B y C). Las terapias aceptadas incluyen QETA –estrategia también puesta en duda recientemente6 – o quimioembolización con partículas sólidas (deb-TACE) para el estadio intermedio (BCLC B) y terapia sistémica con sorafenib para el estadio avanzado (BCLC C) (fig. 1). El estadio intermedio (BCLC B) es un grupo muy heterogéneo, con una amplia variabilidad en las características del tumor (pero no resecable) y en estadio de Child-Pugh (5 a 9 puntos). Se ha propuesto dividir este estadio en 4 sub estadios (B1-B4)7. Piscaglia et al.8 validaron clínicamente la propuesta en una base de datos existente denominada ITALICA (ITAlian LIver CAncer) usando el método de Kaplan-Meier y una prueba de rango logarítmico para un seguimiento a 60 meses. Fueron divididos 391 pacientes estadio BCLC B en los 4 subgrupos propuestos. La supervivencia global por grupos fue: B1: 34 m, B2: 24 m, B3: 15 m y B4: 12 m (p < 0.0001 entre grupos). La supervivencia a 5 años fue: B1: 39.5%, B2: 32.4%, B3: 10.7% y B4: 13.8% (p < 0.001). Indudablemente un refinamiento en la clasificación permitirá determinar el mejor abordaje terapéutico para cada uno de los subgrupos, y aquí es donde deberán evaluarse diferentes estrategias. Tal es el caso de la radioembolización9, la cual ha mostrado utilidad, pero aún no se determina con claridad al grupo de pacientes más beneficiados con este tratamiento. Kolling et al.10 y Gaia et al.11 compararon radioembolización vs. QETA y sorafenib «cara a cara», respectivamente, en estadios intermedio y avanzado sin encontrar diferencias significativas en supervivencia con las estrategias evaluadas.
Manejo combinado. Un estudio retrospectivo de cohortes realizado en 3 centros alemanes12 comparó la supervivencia de 134 pacientes en estadio avanzado (BCLC C) sometidos a una de 3 estrategias: a) sorafenib + QETA (n = 50), b) QETA (n = 50) o c) sorafenib (n = 34). La supervivencia por grupos fue: a) 17 m, b) 10.5 m y c) 8 m. Fu et al.13 evaluaron los resultados del manejo combinado con sorafenib y QETA en una revisión sistemática y meta-análisis y los compararon con los obtenidos con QETA. 9 estudios con 900 pacientes reunieron criterios y fueron incluidos. Los resultados demostraron que efectivamente se prolongó la supervivencia durante el primer año de tratamiento combinado, pero no hubo diferencia a 2 años. No debemos perder de vista que los pacientes en estos estadios quedan fuera de tratamiento con intención curativa.
Finalmente, seguimos sin contar con un tratamiento sistémico de segunda línea aprobado para individuos en estadio BCLC C, aparte de sorafenib. Brivanib (inhibidor selectivo del VEGFR y de FGFR) no cumplió el objetivo primario en los estudios fase III como primera y segunda línea de tratamiento. Moléculas como los inhibidores mTor (everolimus) y los inhibidores HGF/c-MET (tivantinib) se encuentran en fases avanzadas de evaluación14.
FinanciamientoNo hubo financiamiento para la realización de este trabajo.
Conflictos de InterésLa autora no tiene conflicto de interés, en relación con el artículo que se remite para publicación.