El tratamiento endoscópico por medio de la colangiopancreatografía retrógrada endoscópica (CPRE) en pacientes con anatomía modificada representa un reto en la actualidad. Existen 2 técnicas básicas: la CPRE guiada por enteroscopia (entero-CPRE) y la CPRE guiada por laparoscopia (CPRE-LAP)1. La primera tiene una baja tasa de éxito (<70%) y la segunda presenta eventos adversos serios de hasta un 14,3%, lo que limita su uso2.
Recientemente se ha descrito una técnica que utiliza el ultrasonido endoscópico y que permite la anastomosis entre el reservorio gástrico con el estómago excluido utilizando una endoprótesis de aposición luminal, para posteriormente poder realizar la CPRE de forma convencional; se conoce como endoscopic ultrasound-directed transgastric ERCP (EDGE)3.
Presentamos el caso de un hombre de 63 años con diagnóstico de coledocolitiasis y antecedente de by-pass gástrico en Y de Roux hace 5 años. El paciente inició con fiebre, dolor abdominal, ictericia, náuseas y vómitos. Los laboratorios demostraron hiperbilirrubinemia directa, colestasis y leucocitosis, por lo cual se realizó una colangiorresonancia magnética donde se documentó coledocolitiasis (fig. 1A). Se explicaron ampliamente los riesgos y beneficios del procedimiento y previa firma de consentimiento informado se propuso la realización de la técnica EDGE.
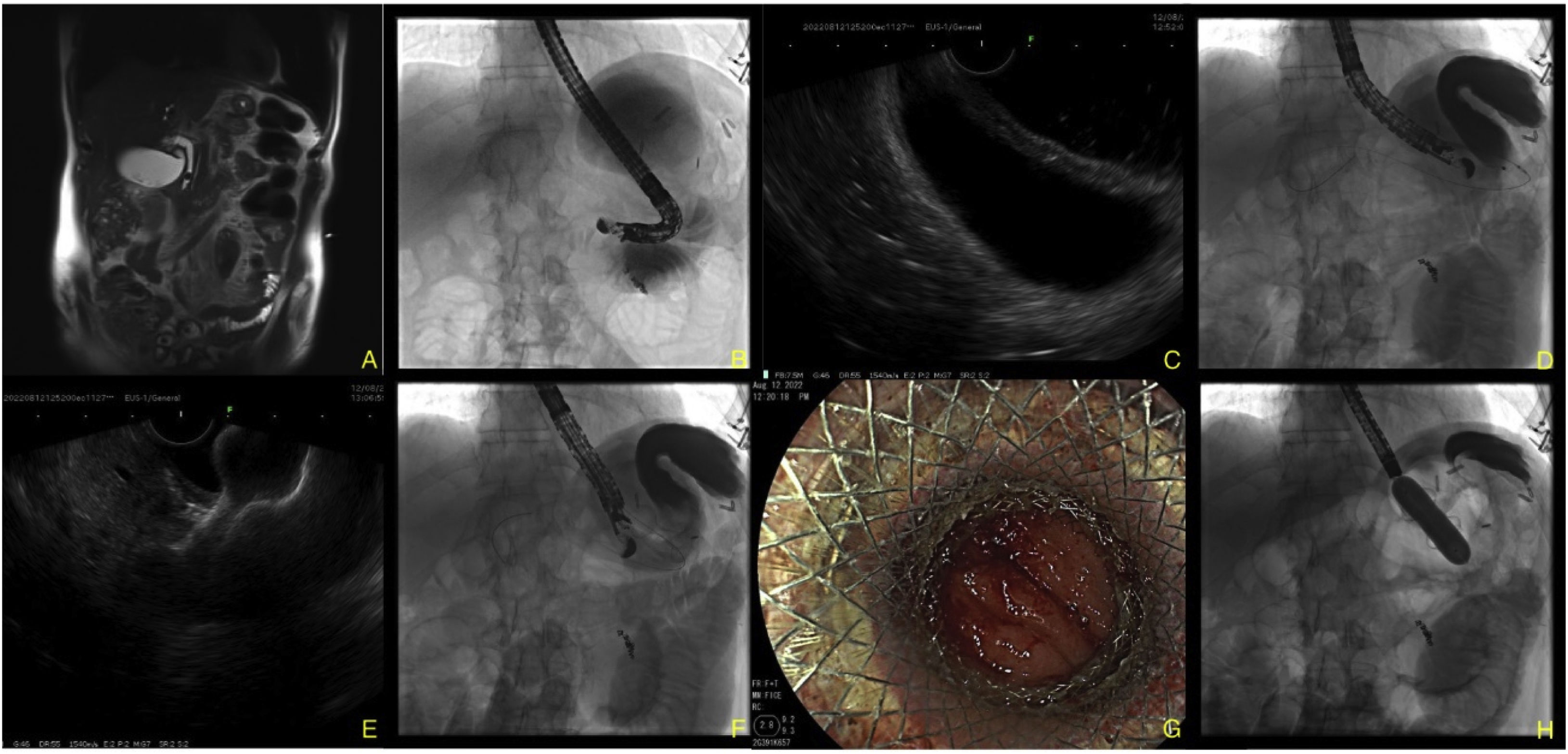
A. Imagen por resonancia magnética que demuestra un lito en tercio distal. B. Distensión del estómago excluido visto por fluoroscopia. C. Visión por ultrasonido endoscópico (USE) de ambas paredes gástricas. D. Punción con FNA 19G del remanente gástrico al estómago excluido y avance de guía hidrofílica 0.035” hacia el antro del estómago excluido. E. Imagen por USE de colocación de endoprótesis tipo Hot AXIOS™. F. Imagen fluoroscópica de colocación. G. Imagen endoscópica de la gastroyeyuno anastomosis. H. Dilatación a 18mm con balón CRE™ de la anastomosis a través del cuerpo de la prótesis.
Se realizó una revisión endoscópica convencional al remanente gástrico y a la gastroyeyuno anastomosis, posteriormente se instiló agua inyectable combinada con medio contraste hidrosoluble al 50% por vía retrógrada y con ello se logró el llenado del estómago excluido a través del asa yeyunal aferente. Se corroboró por fluoroscopia y endosonografía lineal (EG-580UT, Fujinon, Tokio, Japón), donde se visualizaron ambas paredes gástricas (fig. 1B y C). Se realizó una punción del remanente gástrico con aguja fina de 19G (Expect™, Boston Scientific, Marlborough, MA, EE. UU.) y se pasó una guía de 0.035” (Jagwire™, Boston Scientific, Marlborough, MA, EE. UU.), corroborando una adecuada posición hacia el antro gástrico (fig. 1D). Posteriormente se colocó la endoprótesis de aposición tipo Hot AXIOS™ de 20×10mm (Boston Scientific, Marlborough, MA, EE. UU.) y se aplicó una corriente de corte puro (AutoCut 120W, ERBE VIO® 3, Tübingen, Alemania)3. Se logró realizar una anastomosis gastro-gástrica (fig. 1E-G). Se realizó una dilatación con balón hidrostático hasta 18mm (CRE™, Boston Scientific, Marlborough, MA, EE. UU.) (fig. 1H). Posteriormente, se procedió a realizar la CPRE de forma convencional con un duodenoscopio (ED-580XT, Fujinon, Tokio, Japón), el cual se introdujo por vía oral previa lubricación con aceite mineral, llegando a la segunda porción del duodeno a través de la endoprótesis luminal (fig. 2A). Se canuló la vía biliar de forma selectiva confirmando la presencia de varios defectos de llenado en el tercio distal de colédoco y salida de material purulento de la vía biliar (fig. 2B). Se realizó esfinterotomía (fig. 2C y D) y la posterior extracción de litos sin complicaciones (fig. 2E y F). Se extrajo la endoprótesis con pinza de cuerpo extraño y finalmente decidimos realizar un cierre del sitio de la fístula gastro-gástrica con clip OVESCO tipo GC (OTSC®, Tübingen, Alemania) de forma satisfactoria (fig. 2G y H). La evolución del paciente fue favorable y se egresó a las 48h posprocedimiento.
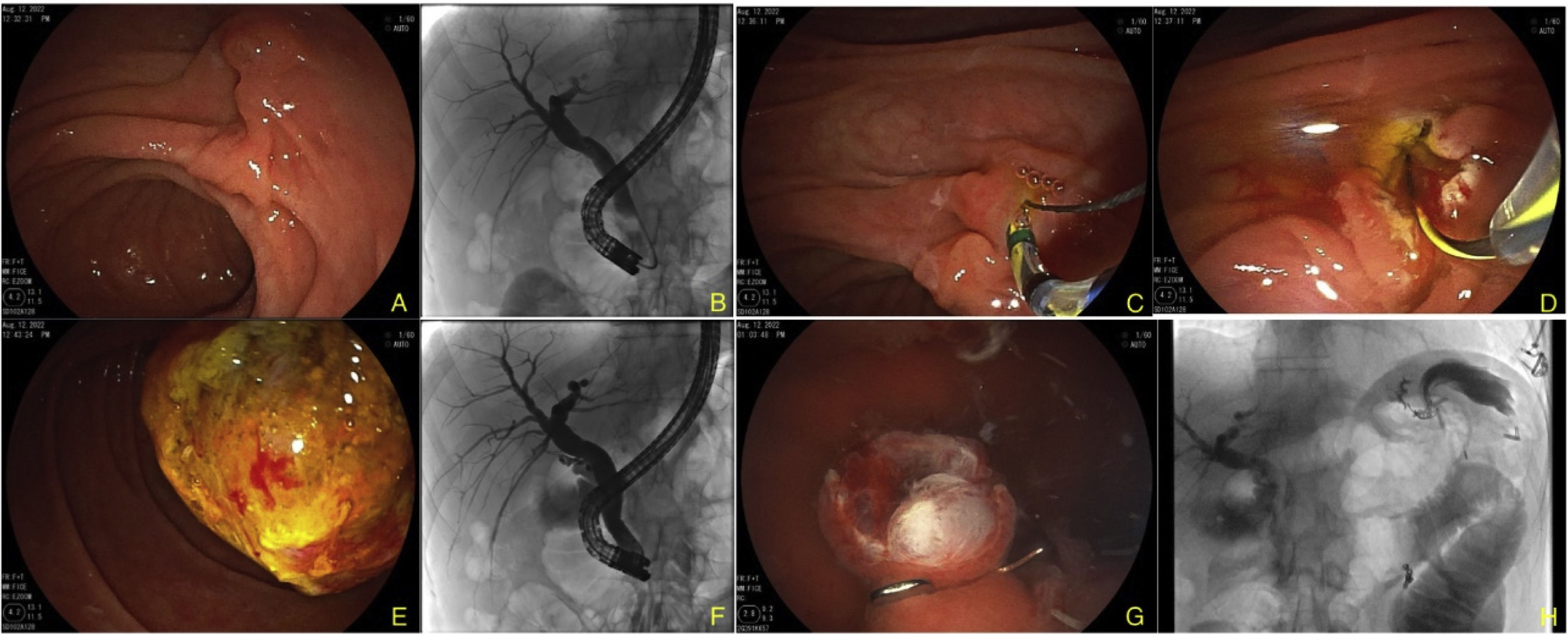
A. Imagen de la ampolla de Vater con duodenoscopio. B. Imagen fluoroscópica que muestra el duodenoscopio a través de la endoprótesis, al inyectar medio de contraste existe dilatación de la vía biliar y defectos de llenado en su interior. C. Esfinterotomía biliar. D. Paso de la guía. E. Extracción de litos. F. Visión fluoroscópica donde ya no se evidencian litos en la vía biliar. G. Imagen endoscópica de cierre con clip OTSC®. H. Imagen fluoroscópica que corrobora adecuado cierre y sin evidencia de fuga.
La cirugía de by-pass gástrico en Y de Roux es frecuente debido a la alta prevalencia de sobrepeso y obesidad a nivel mundial. Sin embargo, en caso de enfermedad biliopancreática el abordaje en ellos es complejo. El EDGE, descrito por Kedia et al.4 en 2014, permite la creación de una gastro-gastro anastomosis temporal guiada por ultrasonido endoscópico para abordaje de enfermedad pancreatobiliar. El éxito técnico y clínico descritos actualmente son del 100 y el 91%, respectivamente (similar a la CPRE-LAP, pero mayor que la entero-CPRE)5,6. Shah-Khan et al.7 demostraron que el EDGE representa una opción terapéutica más popular comparada con otras opciones (86% EDGE, 56% CPRE-LAP, 19% enteroscopia); un 67% la consideraron como estándar de tratamiento. La técnica realizada en nuestro centro es similar a la descrita por otros autores, que puede ser realizada en una o 2 sesiones; en nuestro caso se realizó en una sesión, a causa de la colangitis que presentaba nuestro paciente, y al igual que otros autores, no tuvimos eventos secundarios. Sin embargo, algunos autores están a favor de 2 sesiones (creación de gastroyeyuno anastomosis y la CPRE en segundo tiempo, para la maduración de la fístula), o incluso 3 (incluyendo una más para el cierre), con el argumento de una potencial disminución en el riesgo de perforación4,5,7. Prakash et al.8 evaluaron retrospectivamente el EDGE en una sesión y documentaron menor tiempo, costos y sin diferencias en cuanto a eventos adversos con respecto a más sesiones. Los eventos adversos en su mayoría son leves (18%) y algunos potencialmente graves (migración=11%, perforación=5%). Shinn et al.9, en una serie retrospectiva de 128 pacientes, demostraron que el diámetro<15mm se asoció a un mayor riesgo de migración (OR=5.36, IC 95% 1.29-22.24; p<0.02), pero no la dilatación, la colocación de prótesis de doble cola o el sitio para la anastomosis (p=NS). Finalmente, existe controversia con respecto al cierre de la fístula ya que su realización solo podría prevenir una potencial reganancia de peso en estos pacientes, pero sin diferencias significativas en la prevención de eventos adversos10. En nuestro caso, debido a la dificultad técnica del procedimiento, la manipulación de la vía biliar con la prótesis de aposición como punto de apoyo y la dilatación a 18mm, decidimos realizar el cierre primario con clip tipo GC.
En conclusión, el EDGE es una técnica segura, efectiva y con una aceptable tasa de eventos adversos (<20%), para el abordaje de pacientes con anatomía modificada y que presentan enfermedad pancreatobiliar, de forma que representa una alternativa viable y que debe ser considerada de primera instancia en este grupo de pacientes en nuestro medio.
Consideraciones éticasLos autores declaran que se solicitó la firma del consentimiento informado correspondiente y las imágenes presentadas preservan el anonimato del paciente.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses para la realización del presente trabajo.