La detección y el diagnóstico oportuno del virus de la hepatitis C (VHC) implica identificar la población susceptible de tratamiento, prevenir, limitar complicaciones y evitar contagios. El objetivo de este estudio fue analizar y describir los factores de riesgo asociados a la detección de anticuerpos contra el VHC (anti-VHC) en la población con acceso a la seguridad social que participó en programa nacional de tamizaje.
Material y métodosEstudio transversal/analítico que utilizó datos relacionados con pruebas rápidas realizadas entre septiembre de 2021 y octubre de 2022 en 26 de las 32 entidades federativas de México. Se seleccionaron los reactivos anti-VHC para analizar y comparar, según sexo y edad, los posibles factores de riesgo mediante estadística descriptiva e inferencial. Se analizó la distribución y la densidad geográfica del programa de tamizaje a nivel de la entidad federativa y del municipio.
ResultadosSe realizaron 75,185 detecciones anti-VHC; 2,052 reactivos (2.7%), promedio 44.3 años (±15.1). Ocupación: 32.3% empleado, 19% ama de casa y 18.2% trabajador de sector salud. Hasta 5 de cada 10 pacientes no indicaron factores de riesgo, pero en comparación con las mujeres, los varones con antecedente de accidente con material punzocortante o uso de sustancias psicoactivas intravenosas mostraron 1.4 y 5 veces más probabilidad de detección anti-VHC. Según el lugar de residencia, el 80% de los reactivos se concentró en Estado de México, CDMX y Guanajuato.
ConclusionesLa evidencia sugiere cuál es la población y los factores de riesgo en los que se debe focalizar la estrategia de microeliminación del VHC, mediante el continuo tamizaje, diagnóstico, acceso a tratamiento médico y seguimiento epidemiológico.
Timely detection and diagnosis of hepatitis C virus (HCV) involves identifying the population that is predisposed to treatment and prevention, thus limiting complications and preventing infection. The aim of this study was to analyze and describe risk factors associated with anti-HCV antibody detection in a population with access to public healthcare that participated in a national screening program.
Material and methodsAn analytic cross-sectional study was conducted that utilized data related to rapid tests carried out between September 2021 and October 2022 in 26 of the 32 states of Mexico. Anti-HCV reactive tests were selected, according to age and sex, for analyzing and comparing possible risk factors through descriptive and inferential statistics. The geographic distribution and density of the screening program at the state and municipal levels was analyzed.
ResultsThere were 75,185 anti-HCV antibody detections, 2,052 reactive tests, and mean participant age was 44.3 years (±15.1). Occupation: 32.3% were employees, 19% were housewives, and 18.2% were healthcare workers. Five out of every 10 cases had no indication of risk factors, but there was a 1.4 and 5-times greater likelihood of anti-HCV detection in men with a history of sharps injury or intravenous psychoactive substance use, compared with women. Regarding place of residence, 80% of the reactive tests were concentrated in the State of Mexico, Mexico City, and Guanajuato.
ConclusionsThe evidence herein helps determine the population and risk factors that should be focused on in carrying out the HCV microelimination strategy of continuous screening, diagnosis, medical treatment access, and epidemiologic surveillance.
La infección por el virus de la hepatitis C (VHC), en la actualidad, continúa siendo un problema de salud pública, tanto en los países de altos ingresos como en aquellos de bajos ingresos, debido al espectro de consecuencias sanitarias, sociales y económicas atribuibles a tal enfermedad1,2. Según un informe reciente, durante el año 2020 se reportaron una tasa de incidencia en México del 0.28%3, mientras que la prevalencia fue del 1.4%4. La diferencia en ambas cifras podría ser explicada por las rutas de contagio y/o diferentes factores de riesgo que han sido reportados en la población mexicana. En este sentido, la exposición a sangre contaminada ha sido el principal mecanismo de contagio reportado en diferentes artículos científicos2,5 (exposición al compartir agujas para el uso de sustancias psicoactivas intravenosa, accidentes punzocortantes en trabajadores de instituciones de salud, transfusiones). Sin embargo, también se han identificado mecanismos de tipo sexual (múltiples parejas o relaciones sexuales de riesgo) e intrauterina (madre a hijo)6.
La hepatitis C, causada por el VHC, se reconoce como una inflamación del hígado; se puede manifestar como una infección aguda que suele ser asintomática, pero evoluciona a una forma crónica que puede presentar complicaciones7. Por lo anterior, aproximadamente un 30% de las personas con diagnóstico eliminan el virus espontáneamente en los 6 meses siguientes a la infección, sin tratamiento necesario2, mientras que en el 70% la enfermedad tiende a evolucionar a la cronicidad6,8. Debido a que los síntomas clínicos del VHC son inespecíficos, hasta 8 de cada 10 personas desconocen su diagnóstico1 y, por consiguiente, no tienen acceso a tratamiento de manera oportuna. Más aun, las consecuencias de la enfermedad pueden ser cirrosis, carcinoma hepatocelular o insuficiencia hepática6.
Respecto al VHC, se han reconocido grupos poblacionales con mayor riesgo de infección, por ejemplo, la población migrante de países con endemicidad intermedia y alta, algunos grupos indígenas, al igual que usuarios de sustancias psicoactivas inyectables o intranasales, personas con antecedente de transfusiones antes del año 1995 o antecedente de lugares de reclusión, hombres que tienen sexo con hombres, trabajadores/as sexuales, personas viviendo con virus de inmunodeficiencia humana (VIH) e hijos de madres con infección crónica por hepatitis B o C, principalmente si tienen diagnóstico de VIH9.
Es por lo anterior que los programas de tamizaje representan una estrategia útil en términos de salud pública, no solo por el hecho de realizar detecciones e identificar la población que requiere diagnóstico clínico, sino también para definir a la población susceptible de recibir tratamiento médico, limitar cadenas de contagio y, eventualmente, eliminar la infección por el VHC, en alineación con la estrategia de la Organización Mundial de la Salud (OMS) para los 5 virus de hepatitis (A, B, C, D y E)10, y que implica reducir tanto la incidencia como la mortalidad. Algo que es factible también gracias a la disponibilidad de nuevos tratamientos médicos11. En este sentido, la OMS recomienda que el tamizaje se realice principalmente en la población con factores y/o conductas de riesgo asociadas a esta enfermedad2,3,12, con la finalidad de incrementar el número de diagnósticos clínicamente oportunos13. Es por lo anterior que el objetivo de este estudio fue analizar y describir los factores de riesgo asociados a la detección de anticuerpos contra el VHC (anti-VHC) en la población con acceso a la seguridad social que participó en un programa nacional, realizado en México durante septiembre de 2021 y octubre de 2022.
Material y métodosSe realizó un estudio transversal/analítico, por lo que se utilizó la lista de verificación correspondiente para estudios observacionales, esto es, STROBE checklist transversal (retrospectivo). En este contexto, el estudio incluyó datos obtenidos mediante un sistema de información en salud relacionado con una estrategia institucional de microeliminación del VHC. Esta estrategia ha sido implementada desde septiembre de 2021 a través de unidades médicas de primero y segundo nivel de atención del Instituto Mexicano del Seguro Social (IMSS), distribuidas en las 32 entidades federativas de México, y en la cual ha participado voluntariamente la población con acceso a la seguridad social (población derechohabiente y trabajadores del IMSS). Brevemente, uno de los componentes fundamentales de la estrategia institucional de microeliminación del VHC es el tamizaje, el cual implica utilizar un cuestionario (tabla 1) con preguntas dicotómicas orientadas a identificar los factores y las conductas de riesgo, después, la población que decide participar, previo consentimiento informado, se realiza pruebas de detección de anti-VHC mediante Advanced QualityTM (InTec Products, Inc., Fujian, China), cuya especificidad ha sido reportada del 97-99% y sensibilidad del 100%. Aquellas pruebas que resultan reactivas son vinculadas para realizar estudio confirmatorio y poder establecer el diagnóstico correspondiente, garantizar acceso al tratamiento médico necesario, llevar a cabo vigilancia y el seguimiento epidemiológico correspondiente hasta asegurar la eliminación y la curación del VHC.
Frecuencias absolutas y relativas de los factores de riesgo reportados por la población con acceso a la seguridad social que participó en el programa institucional de tamizaje de anticuerpos contra VHC (anti-VHC), 2021-2022
| No | Sí | ||
|---|---|---|---|
| n (%) | n (%) | ||
| 1 | ¿Comparte o ha compartido hojas de afeitar, rastrillos o cepillo de dientes? | 1,619 (78.9%) | 433 (21.1%) |
| 2 | ¿Tiene o ha tenido tatuajes, piercings, delineado permanente o microblading? | 1,166 (56.8%) | 886 (43.2%) |
| 3 | ¿Usa o ha usado sustancias psicoactivas intravenosas, aunque haya sido una sola vez (drogas)? | 1,953 (95.2%) | 99 (4.8%) |
| 4 | ¿Usa o ha usado sustancias psicoactivas intranasales (drogas)? | 1,924 (93.8%) | 128 (6.2%) |
| 5 | ¿Recibió transfusión de sangre o productos sanguíneos (plasma plaquetas) antes de 1995? | 1,796 (87.5%) | 256 (12.5%) |
| 6 | ¿Recibió algún tipo de trasplante antes de 1995? | 2,034 (99.1%) | 18 (0.9%) |
| 7 | ¿Usted vive con infección por VIH? | 1,923 (93.7%) | 129 (6.3%) |
| 8 | ¿Al momento de su nacimiento, su mama presentó o tenía diagnóstico de hepatitis C? | 2,015 (98.2%) | 37 (1.8%) |
| 9 | ¿Tiene o ha tenido prácticas sexuales de alto riesgo (múltiples contactos sexuales)? | 1,575 (76.8%) | 477 (23.2%) |
| 10 | ¿Tiene o ha tenido contactos sexuales sin protección? | 705 (34.4%) | 1,347 (65.6%) |
| 11 | ¿Tiene o ha tenido alguna pareja sexual con infección por virus de hepatitis C? | 1,983 (96.6%) | 69 (3.4%) |
| 12 | ¿Tiene o ha tenido antecedente de enfermedades de transmisión sexual? | 1,887 (92%) | 165 (8%) |
| 13 | ¿Usted usa o ha usado sustancias psicoactivas con fines sexuales (chemsex)? | 2,020 (98.4%) | 32 (1.6%) |
| 14 | ¿Usted ha estado en prisión? | 2,005 (97.7%) | 47 (2.3%) |
| 15 | ¿Recibe o ha recibido hemodiálisis? | 2,024 (98.6%) | 28 (1.4%) |
| 16 | ¿Ha tenido accidentes con material punzocortante?a | 280 (13.6%) | 337 (16.4%) |
| 17 | ¿Ha sufrido exposición de mucosas, heridas o lesión con objetos punzocortantes provenientes de personas infectadas por hepatitis C?a | 524 (25.5%) | 85 (4.1%) |
| 18 | ¿Está en contacto con equipo médico como catéteres y endoscopios?a | 395 (19.2%) | 214 (10.4%) |
VHC: virus de la hepatitis C; VIH: virus de la inmunodeficiencia humana.
En función de la fuente secundaria, durante el periodo septiembre 2021/octubre 2022 se realizaron 75,185 detecciones a nivel nacional; para realizar este estudio se seleccionaron solo los reactivos anti-VHC que fueron reportados en el mismo periodo, cuyos datos estaban completos y disponibles para el análisis. Adicionalmente, se recolectaron las características sexo, edad, ocupación, lugar de residencia, al igual que las siguientes variables dicotómicas, reportadas como factores de riesgo en otras publicaciones3,7,10,14: uso compartido de hojas de afeitar, rastrillo o cepillo dental; antecedente de tatuajes, piercings, delineado permanente o maquillaje semipermanente —microblading—; uso de sustancias psicoactivas intravenosas o intranasales (drogas); antecedente de transfusión de sangre, productos sanguíneos o trasplante antes de 1995; diagnóstico del VIH; antecedente de diagnóstico materno del VHC en el nacimiento; múltiples parejas sexuales; múltiples contactos sexuales sin protección; pareja sexual con diagnóstico del VHC; antecedente de enfermedades de transmisión sexual; uso de sustancias psicoactivas con fines sexuales (chemsex); antecedente de prisión; antecedente de hemodiálisis; accidentes con material punzocortante; exposición de mucosas, heridas o lesiones con objetos punzocortantes utilizados por personas con VHC; contacto con equipo médico como catéteres y endoscopios.
Análisis estadístico y geográficoLas variables fueron analizadas mediante estadística descriptiva e inferencial en función de su naturaleza. Particularmente la variable ocupación fue sujeta a un análisis de frecuencias, cuyos resultados se mostraron mediante una nube de palabras, en cambio, para la edad de los participantes se obtuvieron medidas resumen (promedio, desviación estándar, mediana, valor máximo y mínimo), mientras que para las variables dicotómicas se calcularon frecuencias absolutas y relativas.
En complemento, se realizó análisis bivariado para identificar las variables asociadas a detección anti-VHC, las cuales fueron consideradas en el modelo final mediante regresión logística, ajustadas por sexo y edad, según los factores de riesgo, lo que implicó obtener medidas de asociación tipo odds ratio (OR), coeficientes (B0, B1) y, por consiguiente, las variables estadísticamente significativas (p<0.05). Los modelos en referencia se generaron en el Programa Estadístico para las Ciencias Sociales (SPSS®, por sus siglas en inglés, v.27 Windows).
Una siguiente etapa consistió en realizar un proceso de geolocalización con base en el lugar de residencia de los casos reactivos del programa de tamizaje, preservando el anonimato y la confidencialidad, con el propósito de generar un mapa para visualizar la distribución y la densidad espacial de las detecciones anti-VHC a nivel entidad federativa y municipal.
Consideraciones éticasEste estudio se ajustó a la normativa vigente en términos de investigación en salud y bioética, específicamente lo que establece la Ley General de Salud15 y respectivo Reglamento en materia de Investigación para la Salud16. Así, el estudio se clasificó sin riesgo, porque no se realizaron experimentos en animales o humanos, utilizó una fuente secundaria para la obtención de los datos, los cuales fueron anónimos, confidenciales y no permitieron identificar nominalmente ningún paciente. Por lo anterior, no fue necesario solicitar consentimiento informado de pacientes, según lo establecido en la normatividad antes referida.
ResultadosSe analizaron 2,052 reactivos (2.7%) anti-VHC; el 67.3% (n=1,381) de la población que participó en las pruebas de tamizaje fueron mujeres. Además, el promedio de edad fue de 44.3 años (± 15.1), mediana de 42, el rango de edades fue de 15 a 95. Referente a la ocupación, la categoría con mayor frecuencia fue empleado (n=664, 32.3%), seguida de ama de casa (n=389, 19%) y profesional de la salud (n=374, 18.2%), esto es, medicina, enfermería y trabajo social como las principales ocupaciones reportadas (fig. 1).
En la nube de palabras se presentan los resultados del análisis de frecuencia según la ocupación que fue reportada por la población con acceso a la seguridad social (población general y trabajadores de institución de salud), los cuales participaron en el programa institucional de tamizaje de anticuerpos contra VHC (anti-VHC), correspondiente a septiembre 2021 y octubre 2022.Fuente: elaboración de los autores con base en registros institucionales de las detecciones de anticuerpos contra VHC (anti-VHC) en la población con acceso a la seguridad social, 2021 y 2022.
En la tabla 1 se presentan las frecuencias absolutas y relativas de los factores examinados en la población que participó en el tamizaje. Aunque la mayoría de estos indicaron una respuesta negativa, un menor porcentaje reportó factores de riesgo como tatuajes, piercings, delineado permanente o microblading (43.2%), múltiples contactos sexuales (23.2%), uso compartido de hojas de afeitar, rastrillos o cepillo dental (21.2%), entre otros más.
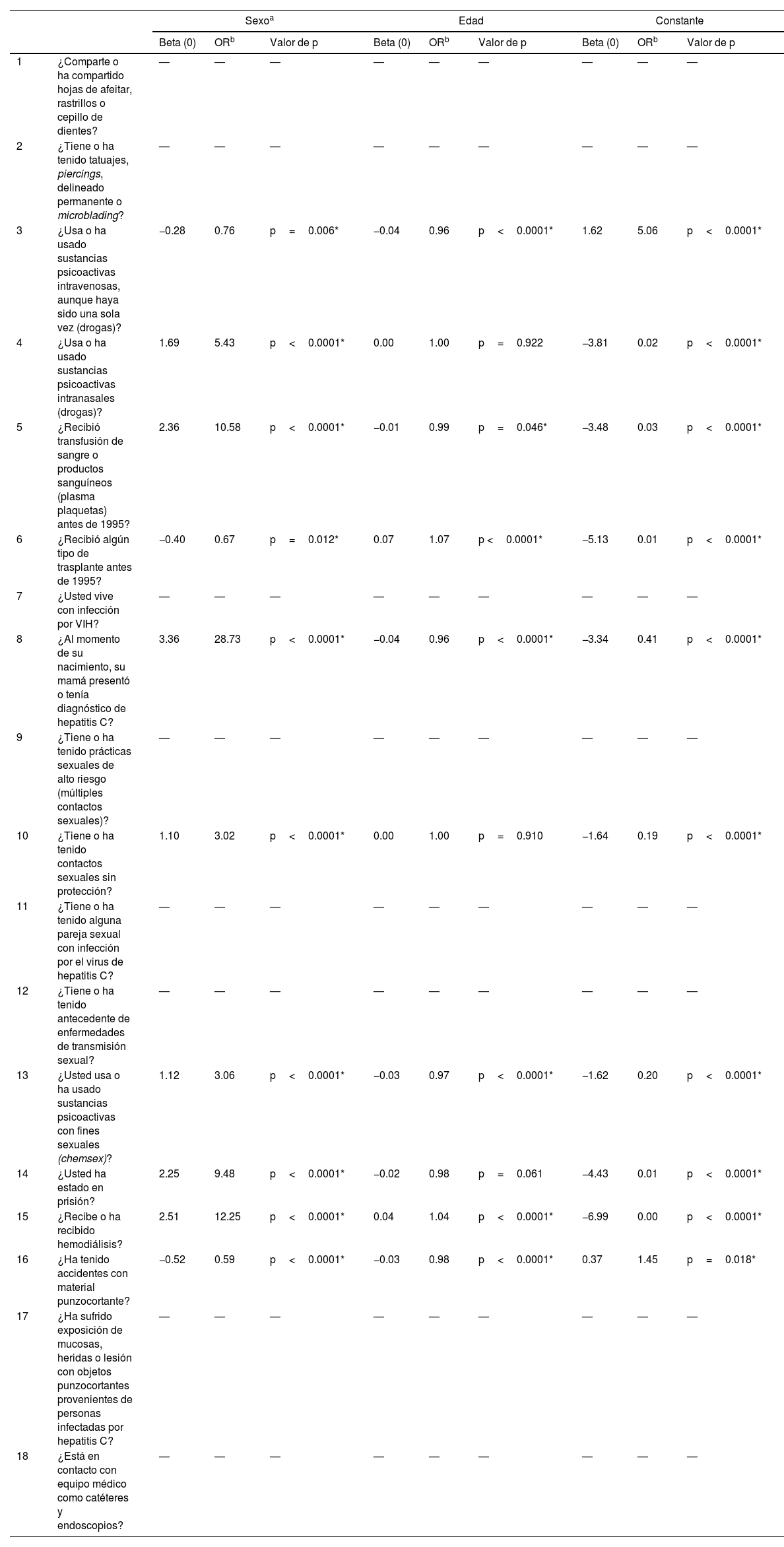
En la tabla 2 se presentan los factores de riesgo calculados por medio de modelos de regresión logística ajustados para características sociodemográficas. Aun cuando la edad no fue significativa, se identificó que los varones mostraron una probabilidad entre 3 y 28 veces mayor (p<0.0001), en comparación con las mujeres, respecto a los siguientes factores: antecedente de diagnóstico de hepatitis C de mamá al momento del nacimiento; antecedente de hemodiálisis; antecedente de transfusión de sangre o productos sanguíneos antes del año 1995; antecedente de prisión; uso de sustancias psicoactivas intranasales o con fines sexuales (chemsex); contactos sexuales sin protección. En tanto que otros factores como accidentes con material punzocortante y uso de sustancias psicoactivas intravenosas incrementaron 1.4 y 5 veces, respectivamente, la probabilidad de detección anti-VHC (p<0.05) en comparación con las mujeres (tabla 2).
Factores de riesgo de la población con acceso a la seguridad social que participó en el programa institucional de tamizaje de anticuerpos contra VHC (anti-VHC), 2021-2022, ajustados por características sociodemográficas
| Sexoa | Edad | Constante | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Beta (0) | ORb | Valor de p | Beta (0) | ORb | Valor de p | Beta (0) | ORb | Valor de p | ||
| 1 | ¿Comparte o ha compartido hojas de afeitar, rastrillos o cepillo de dientes? | — | — | — | — | — | — | — | — | — |
| 2 | ¿Tiene o ha tenido tatuajes, piercings, delineado permanente o microblading? | — | — | — | — | — | — | — | — | — |
| 3 | ¿Usa o ha usado sustancias psicoactivas intravenosas, aunque haya sido una sola vez (drogas)? | −0.28 | 0.76 | p=0.006* | −0.04 | 0.96 | p<0.0001* | 1.62 | 5.06 | p<0.0001* |
| 4 | ¿Usa o ha usado sustancias psicoactivas intranasales (drogas)? | 1.69 | 5.43 | p<0.0001* | 0.00 | 1.00 | p=0.922 | −3.81 | 0.02 | p<0.0001* |
| 5 | ¿Recibió transfusión de sangre o productos sanguíneos (plasma plaquetas) antes de 1995? | 2.36 | 10.58 | p<0.0001* | −0.01 | 0.99 | p=0.046* | −3.48 | 0.03 | p<0.0001* |
| 6 | ¿Recibió algún tipo de trasplante antes de 1995? | −0.40 | 0.67 | p=0.012* | 0.07 | 1.07 | p <0.0001* | −5.13 | 0.01 | p<0.0001* |
| 7 | ¿Usted vive con infección por VIH? | — | — | — | — | — | — | — | — | — |
| 8 | ¿Al momento de su nacimiento, su mamá presentó o tenía diagnóstico de hepatitis C? | 3.36 | 28.73 | p<0.0001* | −0.04 | 0.96 | p<0.0001* | −3.34 | 0.41 | p<0.0001* |
| 9 | ¿Tiene o ha tenido prácticas sexuales de alto riesgo (múltiples contactos sexuales)? | — | — | — | — | — | — | — | — | — |
| 10 | ¿Tiene o ha tenido contactos sexuales sin protección? | 1.10 | 3.02 | p<0.0001* | 0.00 | 1.00 | p=0.910 | −1.64 | 0.19 | p<0.0001* |
| 11 | ¿Tiene o ha tenido alguna pareja sexual con infección por el virus de hepatitis C? | — | — | — | — | — | — | — | — | — |
| 12 | ¿Tiene o ha tenido antecedente de enfermedades de transmisión sexual? | — | — | — | — | — | — | — | — | — |
| 13 | ¿Usted usa o ha usado sustancias psicoactivas con fines sexuales (chemsex)? | 1.12 | 3.06 | p<0.0001* | −0.03 | 0.97 | p<0.0001* | −1.62 | 0.20 | p<0.0001* |
| 14 | ¿Usted ha estado en prisión? | 2.25 | 9.48 | p<0.0001* | −0.02 | 0.98 | p=0.061 | −4.43 | 0.01 | p<0.0001* |
| 15 | ¿Recibe o ha recibido hemodiálisis? | 2.51 | 12.25 | p<0.0001* | 0.04 | 1.04 | p<0.0001* | −6.99 | 0.00 | p<0.0001* |
| 16 | ¿Ha tenido accidentes con material punzocortante? | −0.52 | 0.59 | p<0.0001* | −0.03 | 0.98 | p<0.0001* | 0.37 | 1.45 | p=0.018* |
| 17 | ¿Ha sufrido exposición de mucosas, heridas o lesión con objetos punzocortantes provenientes de personas infectadas por hepatitis C? | — | — | — | — | — | — | — | — | — |
| 18 | ¿Está en contacto con equipo médico como catéteres y endoscopios? | — | — | — | — | — | — | — | — | — |
VHC: virus de la hepatitis C; VIH: virus de la inmunodeficiencia humana.
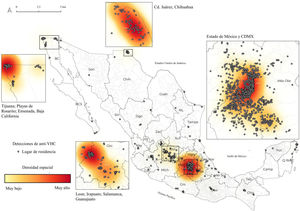
Por otra parte, en la figura 2 se muestra la localización y distribución de los reactivos anti-VHC, según el lugar de residencia, reportados en el programa de tamizaje institucional. Así, las entidades federativas donde se concentró una mayor cantidad fueron Estado de México (45.4%, n=931), CDMX (26%, n=531) y Guanajuato (12.1%, n=249); mientras que, a nivel municipal, la mayor densidad espacial de reactivos se observó en Ecatepec de Morelos (Estado de México), Gustavo A. Madero (CDMX), León (Guanajuato), Nezahualcóyotl (Estado de México) y Chalco (Estado de México). Ahora bien, según la cantidad de detecciones (tabla 3), los valores más altos se registraron en los siguientes estados, por ese orden: CDMX (32.5%, n=24,444), Estado de México (16.6%, n=12,475), Veracruz (12.2%, n=9,138), Chihuahua (5.4%, n=4,081) y Baja California (4.9%, n=3,686). Sin embargo, no se identificó relación estadística entre el número de detecciones y reactivos reportados según entidad federativa (datos no presentados).
Se observa la distribución y la densidad espacial de las detecciones de anti-VHC según el lugar de residencia que reportó la población con acceso a seguridad social (población general y trabajadores de institución de salud), los cuales participaron en el programa institucional de tamizaje, correspondiente a septiembre 2021 y octubre 2022. Así, la mayor intensidad de las tonalidades representa una mayor concentración de detecciones reactivas, por lo que puede sugerir los municipios y entidades federativas donde las tasas de incidencia podrían ser mayor en comparación con otros lugares de México.Fuente: elaboración de los autores con base en registros institucionales de las detecciones de anticuerpos contra VHC (anti-VHC) en población con acceso a seguridad social, 2021 y 2022.
Frecuencias absolutas y relativas de detecciones de anticuerpos contra VHC (anti-VHC) en la población con acceso a la seguridad social que participó en el programa institucional de tamizaje, 2021-2022
| Entidad federativa | Detecciones (n) | % | Reactivos (n) | % | No reactivos (n) | % |
|---|---|---|---|---|---|---|
| Aguascalientes | 580 | 0.77 | 48 | 2.34 | 534 | 0.73 |
| Baja California | 3,686 | 4.90 | 72 | 3.51 | 3,618 | 4.95 |
| Baja California Sur | 11 | 0.01 | 0 | 0.00 | 11 | 0.02 |
| Campeche | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Chiapas | 755 | 1.00 | 8 | 0.39 | 749 | 1.02 |
| Chihuahua | 4,081 | 5.43 | 95 | 4.64 | 3,986 | 5.45 |
| Coahuila | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Colima | 291 | 0.39 | 0 | 0.00 | 291 | 0.40 |
| CDMX | 24,444 | 32.51 | 531 | 25.88 | 23,879 | 32.65 |
| Durango | 257 | 0.34 | 2 | 0.10 | 255 | 0.35 |
| Edo. de México | 12,475 | 16.59 | 931 | 45.37 | 11,590 | 15.85 |
| Guanajuato | 2,301 | 3.06 | 249 | 12.13 | 2,024 | 2.77 |
| Guerrero | 2,383 | 3.17 | 9 | 0.44 | 2,376 | 3.25 |
| Hidalgo | 1 | 0.00 | 0 | 0.00 | 1 | 0.00 |
| Jalisco | 2,539 | 3.38 | 30 | 1.46 | 2,512 | 3.44 |
| Michoacán | 2 | 0.00 | 0 | 0.00 | 2 | 0.00 |
| Morelos | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Nayarit | 574 | 0.76 | 3 | 0.15 | 571 | 0.78 |
| Nuevo León | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Oaxaca | 2,573 | 3.42 | 15 | 0.73 | 2,560 | 3.50 |
| Puebla | 2,408 | 3.20 | 19 | 0.91 | 2,389 | 3.27 |
| Querétaro | 1 | 0.00 | 0 | 0.00 | 1 | 0.00 |
| Quintana Roo | 2,701 | 3.59 | 21 | 1.02 | 2,680 | 3.66 |
| San Luis Potosí | 1 | 0.00 | 0 | 0.00 | 1 | 0.00 |
| Sinaloa | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Sonora | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 |
| Tabasco | 2 | 0.00 | 0 | 0.00 | 2 | 0.00 |
| Tamaulipas | 1,658 | 2.21 | 8 | 0.39 | 1,651 | 2.26 |
| Tlaxcala | 829 | 1.10 | 0 | 0.00 | 829 | 1.13 |
| Veracruz | 9,138 | 12.15 | 9 | 0.44 | 9,130 | 12.48 |
| Yucatán | 1,492 | 1.98 | 2 | 0.10 | 1,490 | 2.04 |
| Zacatecas | 2 | 0.00 | 0 | 0.00 | 2 | 0.00 |
| Total | 75,185 | 2,052 | 73,133 |
Fuente: elaboración de los autores con base en registros institucionales de las detecciones de anticuerpos contra VHC (anti-VHC) en la población con acceso a la seguridad social, 2021 y 2022.
La detección anti-VHC se realizó principalmente en <45 años y en la población femenina. Aunque más del 50% de la población que participó en el programa de tamizaje no indicó factores de riesgo, los accidentes con material punzocortante y uso de sustancias psicoactivas intravenosas aumentaron la probabilidad de detección anti-VHC en los varones en comparación con las mujeres, independientemente de la ocupación. Considerando que la población incluida en el programa de tamizaje institucional tiene acceso a la seguridad social, se recomienda que el IMSS, a través de los recursos materiales, humanos y unidades médicas disponibles, garantice el continuum tamizaje, diagnóstico, acceso a tratamiento médico y seguimiento epidemiológico; a fin de hacer factible la eliminación de la infección de VHC y contribuir a reducir la carga de morbilidad que representa en México.
En este sentido, respecto a la seroprevalencia en población mexicana, un estudio reciente realizado en el occidente de México reportó un valor del 3.9%12, esto es, una cifra mayor en comparación, por ejemplo, con países de altos ingresos, como EE. UU. (2.1%)6 o Polonia (0.9-1.9%)17. La Encuesta Nacional de Salud y Nutrición (ENSANUT), por otro lado, reportó una seroprevalencia más alta en hombres que en mujeres, esto es, 0.49 (IC 95%: 0.24-0.59) y 0.29% (IC 95%: 0.14-0.63), respectivamente11,18; en tanto que otras investigaciones no han identificado diferencias significativas entre sexos, o bien, la seroprevalencia reportada ha sido aún mayor, hasta un 6%1. Particularmente en trabajadores de la salud, la seroprevalencia reportada en México ha oscilado entre el 0.5 y el 1.3%19. Sin embargo, las diferencias entre los valores citados podrían ser explicadas, entre otras razones, porque la mayoría de los estudios han incluido poblaciones que se ciñen a hospitales y no han sido representativas11, excepto la seroprevalencia reportada por la ENSANUT18. Las diferencias en cuanto a la seroprevalencia también podrían ser atribuibles a la prueba utilizada en la detección de anti-VHC, el tipo de población que participa en los programas de tamizaje, ya sea población abierta, trabajadores de instituciones del sector salud, donadores de sangre y hemoderivados, diferencias en el acceso a servicios de salud, disponibilidad de tratamientos médicos17, así como por el riesgo de infección atribuible a algunos grupos poblaciones específicos; mismos que deben ser prioritarios en las estrategias de microeliminación del VHC y atendiendo factores de riesgo conocidos.
Por otra parte, la evidencia ha mostrado mayor consenso respecto a los factores de riesgo del VHC en la población general, por ejemplo, antecedente de hemodiálisis, receptor de transfusión de sangre previo a la realización de cribado del VHC, uso de fármacos, usuarios de sustancias psicoactivas intravenosas o intranasales y factores de tipo sexual3,6,7. En tanto que otros estudios realizados en trabajadores del sector salud han reportado como factores de riesgo los accidentes con material punzocortante (66.7%), intervenciones médicas u odontológicas (58.6%)4,5,19. En nuestro estudio, que incluyó la población del sector salud y con acceso a seguridad social, se identificó que el antecedente de uso de sustancias psicoactivas intravenosas y accidentes con material punzocortante incrementaron la probabilidad de detección anti-VHC, con mayor frecuencia en la población <45 años. Además de que los factores identificados en este estudio coinciden con los reportados en otras publicaciones, son prevenibles y susceptibles de modificar. Por lo tanto, estos resultados resaltan la necesidad, por un lado, de reforzar la difusión de información sobre cómo prevenir la infección por VHC, atribuible a prácticas de riesgo ampliamente reconocidas, como tatuajes, uso de piercings, drogas inyectables, procedimientos cosméticos o de embellecimiento3,17. Por otro lado, se hace necesario reforzar normas de seguridad y medidas de protección tanto para trabajadores del sector salud como población general, particularmente referente a intervenciones médicas invasivas, inyecciones y suministro seguro de productos sanguíneos10, con el propósito de evitar accidentes con material biológico infeccioso, punzocortante y reducir el riesgo ocupacional5. Toda vez que el VHC representa una de las infecciones ocupacionales más comunes10,20 y una de las principales causas de enfermedades crónicas del hígado6,10,17. Adicionalmente, estos resultados contribuyen a reforzar la evidencia disponible respecto a cuál es la población a la que se deben dirigir los programas de tamizaje, dada una mayor probabilidad de detección según lugar de residencia, sexo, edad, ocupación o factores de riesgo17. Por lo que, en función de ello, es posible adaptar y focalizar las acciones de detección, confirmación diagnóstica, vigilancia y seguimiento epidemiológico, con el objetivo de incrementar el impacto del programa de eliminación del VHC.
Desde una perspectiva geográfica, en años previos se reportó una mayor incidencia del VHC en entidades federativas caracterizadas por alta densidad poblacional y flujos migratorios constantes, como son norte (Baja California), occidente (Sinaloa, Jalisco) y centro de México (Estado de México y CDMX)3, en comparación con la zona sur6. Los resultados aquí reportados indicaron una detección anti-VHC más alta en las entidades federativas en referencia, lo que a su vez podría demostrar que la infección por el VHC ha aumentado en los años recientes. En relación con la estrategia institucional de microeliminación del VHC en el IMSS, existe la posibilidad que, conforme aumente el número de detecciones, aumente la cantidad de reactivos, particularmente en CDMX, Chihuahua y Baja California. Por lo anterior, consideramos que esta evidencia puede ser utilizada en términos de planeación e implementación de acciones para tal programa. Dado que muestra las entidades federativas donde la prevalencia de VHC podría ser mayor a nivel nacional y, por tanto, prioritarias para focalizar estrategias de tamizaje, en caso de ser necesario, realizar vigilancia y seguimiento epidemiológico. Por otro lado, también es pertinente demostrar extender la cobertura territorial de la estrategia institucional de microeliminación en estados del norte (Coahuila, Nuevo León, Sinaloa, Sonora) y sureste (Campeche) del país, donde, según los resultados presentados, se identificó menor cantidad de detecciones (tabla 3).
Por otra parte, es necesario considerar algunas limitaciones en este estudio. En principio, aunque la estrategia de tamizaje de anti-VHC se implementó a nivel nacional, la cobertura territorial se asoció a 26 entidades federativas (81.2%), por lo que los resultados no son representativos. Más aún, en la frontera norte del país (Tijuana, Baja California), occidente (León, Guanajuato) y centro (Estado de México y CDMX) se reportó una mayor cantidad de reactivos anti-VHC, pero estos lugares también concentran más recursos materiales, humanos y de infraestructura de salud en comparación con otros, por consiguiente, este resultado podría sobrerrepresentar la detección de anti-VHC. Aunado a ello, el espectro de factores de riesgo estudiados fue limitado y no fue posible descartar la asociación causal con otros factores de infección en los casos que fueron detectados a través de la estrategia institucional. No obstante, el 100% de las personas reactivas fueron vinculadas a estudio confirmatorio mediante la prueba transcriptasa reversa reacción en cadena de la polimerasa (RT-PCR, por sus siglas en inglés). También es pertinente destacar que los resultados provienen de una estrategia institucional de microeliminación del VHC, implementada en una de las instituciones de seguridad social que tiene más de 54 millones de derechohabientes en el país. Por lo tanto, no solo es evidencia útil para el IMSS, sino también complementa aquellas estrategias de salud pública implementadas por el Sistema Nacional de Salud en México, como lo es el Programa Nacional de Eliminación de la Hepatitis C de la Secretaría de Salud, que incluye tamizaje, prueba diagnóstica y, de ser necesario, tratamiento médico21. Así, la evidencia de nuestro estudio resalta, por un lado, hacia donde extender la cobertura territorial para incrementar las posibilidades de detección del VHC a nivel nacional y, por otro, hipotetizar sobre los lugares (municipios y entidades federativas) que podrían registrar la mayor carga de infección del VHC en la actualidad, al igual que establecer donde se requiere continuar con programas de tamizaje, garantizar el medicamento para los casos reactivos y confirmados.
A manera de conclusión, este estudio sugiere que la actualización, el conocimiento de los factores y las conductas de riesgo a nivel poblacional resulta importante para reforzar y difundir las medidas preventivas pertinentes, a fin de evitar infecciones por el VHC en la población general. En relación con la implementación del programa de microeliminación del VHC en el IMSS, se identificaron características y grupos de población en riesgo (sexo, edad, ocupación), previamente reportados en la literatura, que deberían ser prioritarios, en alineación con los objetivos estratégicos establecidos, tanto a nivel internacional10 como nacional21. Esto es, mediante la implementación de cuestionarios para identificar factores de riesgo, tamizaje, estudios de confirmación diagnóstica, acceso a tratamiento médico, vigilancia y seguimiento epidemiológico. Y de esta manera hacer factible el control y la eventual eliminación de la infección por VHC en la población derechohabiente del IMSS.
Consideraciones éticasEste estudio cumple con la normativa vigente en México en términos de investigación en salud y bioética. Esto quiere decir que se ajusta a lo establecido en la Ley General de Salud y respectivo Reglamento en materia de Investigación para la Salud. Por lo tanto, el estudio se clasificó sin riesgo, toda vez que no se realizaron experimentos en animales ni humanos (protección de personas y animales); utilizó, además, una fuente secundaria para la obtención de los datos, los cuales no permitieron identificar nominalmente a ningún paciente, y así garantizar que los datos fueran anónimos y confidenciales (derecho de la privacidad y consentimiento informado). Por lo que el consentimiento informado no se solicitó para publicación de este estudio, porque en él no se publican datos personales que permitan identificar ningún paciente, según lo establecido en la normatividad antes referida.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial/privado o entidades sin ánimo de lucro. Esto quiere decir que no fue necesario utilizar ningún tipo de plan de financiación.
Conflicto de interesesLos autores declaran que, para la investigación y redacción de este estudio, no tienen ninguna relación financiera o personal con otras personas u organizaciones que pudieran dar lugar a algún conflicto de intereses en relación con el artículo que se remite para su publicación.
Los autores desean expresar su agradecimiento a la población que voluntariamente participó en los programas de tamizaje y que, eventualmente, contribuyó a disponer de datos para el análisis presentado en este manuscrito, lo cual, a su vez, debe colaborar para mejorar el impacto del Programa Nacional de Eliminación de la Hepatitis C en México.