Los casos de pancreatitis aguda recurrente (PAR) y pancreatitis crónica (PC) se han incrementado en la edad pediátrica en los últimos años. La PAR, que se caracteriza por 2 o más eventos documentados de pancreatitis aguda (PA), ocurre en el 10-30% de los casos de PA; y la PC es la etapa final de una inflamación progresiva que se manifiesta como fibrosis del parénquima pancreático y eventualmente disfunción exocrina y/o endocrina1,2.
En niños, usualmente existe más de un factor identificado que contribuye a su desarrollo, y se relacionan con un amplio espectro de etiologías (genéticas, anatómicas, obstructivas, farmacotóxicas, traumáticas, metabólicas [errores innatos del metabolismo], sistémicas, infecciosas, autoinmunes e idiopáticas)3. Dichas condiciones se relacionan con morbilidades, ingresos a urgencias y hospitalizaciones4.
Realizamos la descripción de 6 pacientes con PAR y 5 pacientes con PC en los que se realizó el estudio de factores de riesgo identificados en el desarrollo de PAR y de PC propuesto por el grupo INSPPIRE5,6. Se realizó secuenciación masiva con la plataforma Illumina®. Las características de los casos de PAR y PC se describen en la tabla 1 y la tabla 2, respectivamente. Los factores de riesgo para desarrollar PAR y PC son similares entre sí y las causas genéticas se han identificado en>50% de los casos de PAR y en ∼75% de aquellos con PC, y el 17% presenta más de una variante patogénica, según el reporte INSPPIRE3,5.
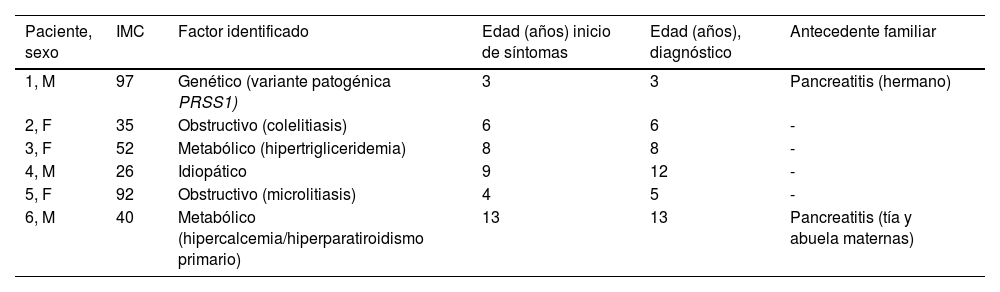
Características clínicas, factores identificados y hallazgos radiológicos en el grupo de pancreatitis aguda recurrente
| Paciente, sexo | IMC | Factor identificado | Edad (años) inicio de síntomas | Edad (años), diagnóstico | Antecedente familiar |
|---|---|---|---|---|---|
| 1, M | 97 | Genético (variante patogénica PRSS1) | 3 | 3 | Pancreatitis (hermano) |
| 2, F | 35 | Obstructivo (colelitiasis) | 6 | 6 | - |
| 3, F | 52 | Metabólico (hipertrigliceridemia) | 8 | 8 | - |
| 4, M | 26 | Idiopático | 9 | 12 | - |
| 5, F | 92 | Obstructivo (microlitiasis) | 4 | 5 | - |
| 6, M | 40 | Metabólico (hipercalcemia/hiperparatiroidismo primario) | 13 | 13 | Pancreatitis (tía y abuela maternas) |
IMC: índice de masa corporal expresado en percentiles por la Centers for Disease Control and Prevention; F: femenino; M: masculino; PRSS1: tripsinógeno catiónico.
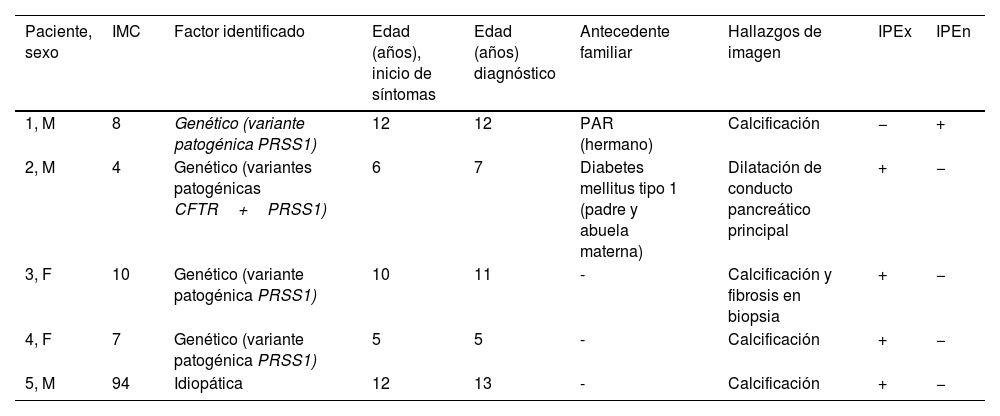
Características clínicas, factores identificados y hallazgos radiológicos en el grupo de pancreatitis crónica
| Paciente, sexo | IMC | Factor identificado | Edad (años), inicio de síntomas | Edad (años) diagnóstico | Antecedente familiar | Hallazgos de imagen | IPEx | IPEn |
|---|---|---|---|---|---|---|---|---|
| 1, M | 8 | Genético (variante patogénica PRSS1) | 12 | 12 | PAR (hermano) | Calcificación | − | + |
| 2, M | 4 | Genético (variantes patogénicas CFTR+PRSS1) | 6 | 7 | Diabetes mellitus tipo 1 (padre y abuela materna) | Dilatación de conducto pancreático principal | + | − |
| 3, F | 10 | Genético (variante patogénica PRSS1) | 10 | 11 | - | Calcificación y fibrosis en biopsia | + | − |
| 4, F | 7 | Genético (variante patogénica PRSS1) | 5 | 5 | - | Calcificación | + | − |
| 5, M | 94 | Idiopática | 12 | 13 | - | Calcificación | + | − |
CFTR: proteína del regulador de conductabilidad transmembrana de la fibrosis quística; F: femenino; IMC: índice de masa corporal expresado en percentiles por la Centers for Disease Control and Prevention; IPEn: insuficiencia pancreática endocrina; IPEx: insuficiencia pancreática exocrina; M: masculino; PAR: pancreatitis aguda recurrente; PRSS1: tripsinógeno catiónico.
La mediana de edad en el momento del diagnóstico fue de 8 años (rango intercuartil [RIQ] 5-12). La mediana de visitas a urgencias antes del diagnóstico fue de 3 (RIQ 2-5). La mediana de hospitalizaciones en el último año fue de 2 (RIQ 0-2).
En un estudio reciente, evaluaron en 479 niños variables demográficas, factores de riesgo y tratamiento en PAR y PC, e identificaron que las variantes genéticas son el factor de riesgo dominante7. En nuestro reporte, documentamos en un 45.4% una variante genética, siendo un porcentaje mayor a lo publicado por Saito et al. (39.1%)8. En el trabajo de Vue et al., donde el 33% (n=30/91) de los pacientes incluidos fueron hispanos, se evidenció al menos una mutación en el 36%1.
En una serie de 115 niños que incluyó a 20 con PAR (17%), a 16 de ellos se les realizó estudio genético, y en 6 encontraron una variante patogénica en uno de los 4 paneles de genes (tripsinógeno catiónico [PRSS1], inhibidor de la tripsina Kazal-tipo 1 [SPINK1], proteína del regulador de conductabilidad transmembrana de la fibrosis quística [CFTR] y quimiotripsina C [CTRC]), siendo el CFTR la variante genética más encontrada, seguido de PRSS1 y SPINK19. Esto difiere de nuestros hallazgos, posiblemente por nuestro tamaño limitado de pacientes y mayor prevalencia de la mutación CFTR en población caucásica. En población mexicana, Sánchez-Ramírez et al. identificaron en 55 pacientes (65.5% con PA, 34.5% con PAR) una frecuencia del 1.8% para variante patogénica en el CFTR, correspondiente a un paciente del subgrupo de PAR. Sin embargo, ninguno de los niños fue estudiado para variantes en PRSS1 o SPINK1 y no se incluyeron casos de PC10.
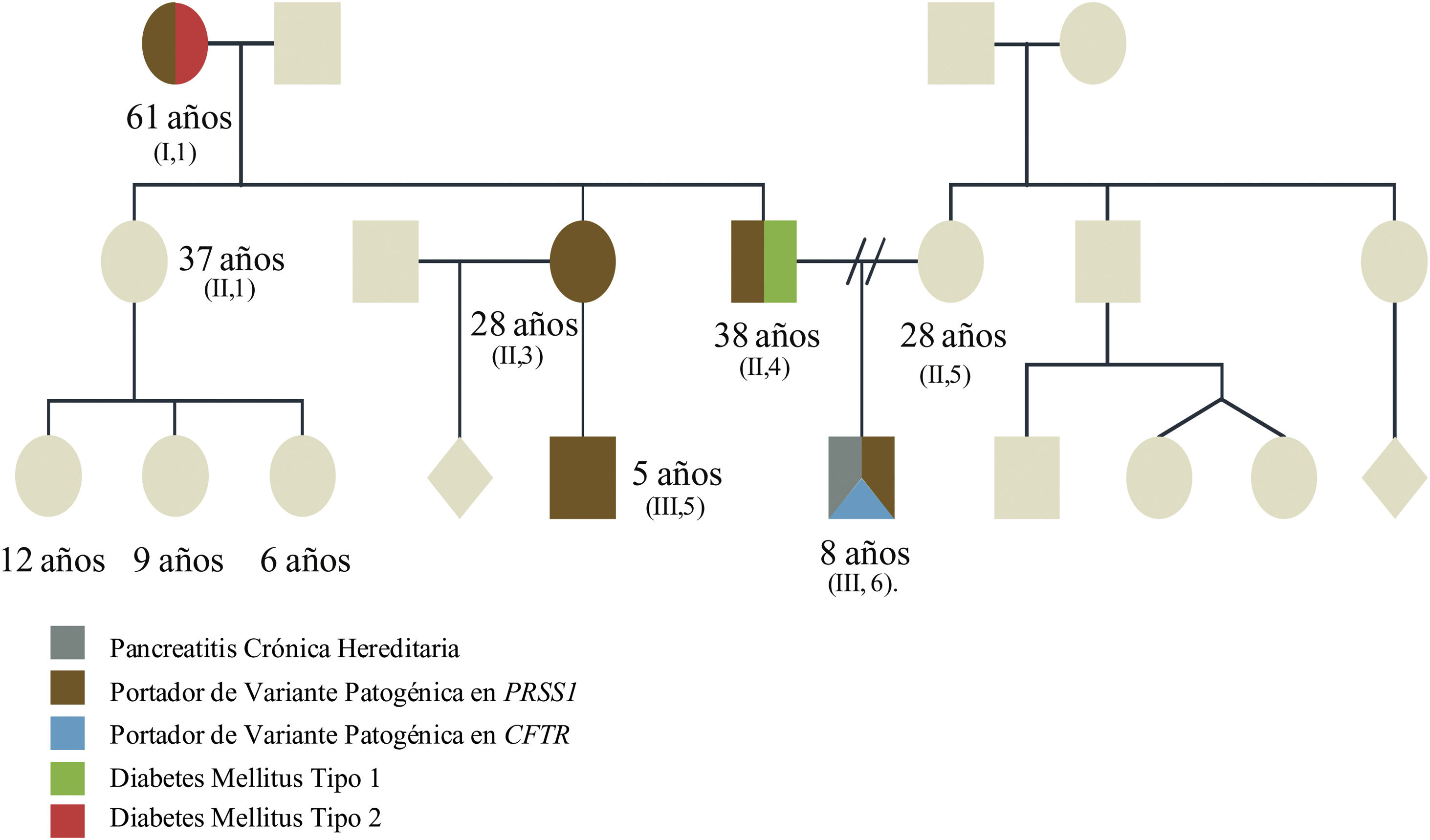
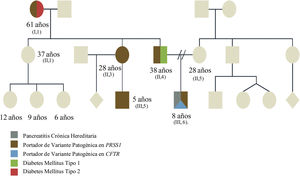
Presentaron variantes patogénicas heterocigotas en el PRSS1 (duplicación completa de la región codificante) 4/5 de nuestros pacientes con PC, y un paciente presentó 2 variantes patogénicas heterocigotas (CFTR [p.Phe508del] y PRSS1 [duplicación completa de la región codificante]). En este sentido, la presencia de ciertas variantes patogénicas en PRSS1 (p.N29I o R122H) se ha relacionado con una mayor probabilidad de una enfermedad progresiva que evoluciona a PC y, posteriormente, incluso a cáncer pancreático11. En la figura 1 ejemplificamos cómo una variante puede heredarse en la familia y expresarse de formas distintas. Llama la atención que todos los pacientes analizados presentan la misma variante patogénica en PRSS1, lo que nos hace sospechar que pudieran tener un ancestro en común.
Se describe a los familiares con manifestaciones de diabetes mellitus tipo 1 y pancreatitis, así como a los familiares asintomáticos. El caso del propósito presenta una evolución tórpida al ser portador no solo de la duplicación en PRSS1, sino también de una variante heterocigota en CFTR, con lo que se espera tenga una expresión y una progresión tórpidas.
Se ha descrito que una historia familiar positiva de pancreatitis es más frecuente en aquellos casos con variantes patogénicas, y un 30% de los pacientes con PAR o PC presenta algún antecedente familiar de pancreatitis, semejante a nuestro reporte (27.2%)1,7.
Reportamos 2 pacientes (subgrupo de PAR) con factor obstructivo. Saraswat et al. describieron en adultos con PAR que el 75% de los estudios microscópicos de la vesícula biliar presentaban cristales de colesterol y gránulos de bilirrubinato de calcio, los cuales se asocian con microlitiasis, y 30 meses después del tratamiento de microlitiasis (ácido ursodesoxicólico, esfinterotomía o colecistectomía) los pacientes se encontraban asintomáticos12.
En pediatría los factores de riesgo metabólico para PAR y PC se relacionan con cetoacidosis diabética, hipertrigliceridemia, hipercalcemia asociada a hiperparatiroidismo y, de forma menos frecuente, a errores innatos del metabolismo13. Encontramos que 2 pacientes con PAR presentaron un factor metabólico: un paciente presentó hipertrigliceridemia (niveles>1,000mg/dL; la presencia de niveles séricos>1,000mg/dL es un factor de riesgo absoluto para el desarrollo de PA); otro de nuestros pacientes presentó adenoma de paratiroides. El adenoma de paratiroides es la causa más común de hipercalcemia (>10.7mg/dL)14.
Los pacientes con factor metabólico tuvieron una edad media de presentación más tardía que los pacientes con PAR y sin factor metabólico (10.5 vs. 7.16 años), hallazgo similar a lo reportado por Husain et al.14.
En ocasiones estos pacientes no son sometidos a una evaluación diagnóstica extensa, por lo que debemos impulsar una postura proactiva desde el diagnóstico de PAR, enfatizando y priorizando la evaluación genética.
Recomendamos someter a consejo genético a los pacientes pediátricos sin etiología identificable; una tipificación temprana de los factores de riesgo podría mejorar el enfoque terapéutico9,13.
Consideraciones éticasLos autores declaran que se revisó el expediente clínico para la recogida de los datos, que se manejaron de forma confidencial y, por lo tanto, no permiten identificar a los pacientes incluidos de forma individual. No fue necesario obtener autorización del Comité de Ética y tampoco la firma de consentimiento informado.
FinanciaciónEl presente trabajo no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no haber tenido ningún tipo de conflicto de intereses.