El valor de las pruebas de filtración durante resecciones colorrectales para identificar fuga o sangrado de anastomosis no está establecido. Nuestro objetivo es comparar el impacto de la colonoscopia intraoperatoria (CIO) versus insuflación con jeringa como prueba de fuga en resección anterior baja para cáncer de recto, con respecto a la incidencia de filtración postoperatoria (FP).
Materiales y métodosEstudio retrospectivo sobre base de datos prospectiva de 426 pacientes con cáncer de recto sometidos a resección anterior baja electiva desde enero de 2015 hasta diciembre de 2019. La prueba de fuga anastomótica se realizó a criterio del cirujano. La incidencia de FP se comparó entre pacientes sometidos a CIO y prueba con jeringa, utilizando el análisis de regresión logística, incluido el análisis de emparejamiento por puntaje estimado de propensión.
ResultadosLas características clínicas y morbimortalidad no mostraron diferencias significativas entre los grupos. En total fueron 422 pacientes, una vez excluidos 4. Se compararon 70 pacientes CIO frente a 352 con prueba con jeringa. La incidencia de FP fue del 5.7% en CIO y del 12.2% en el grupo control (p=0.001). Después del emparejamiento por puntaje de propensión (n=221), equilibrando las características entre los grupos, la incidencia de FP fue del 5.7% en CIO y del 13.9% en el grupo con jeringa (p=0.001).
ConclusiónLa CIO es un método seguro para evaluar la integridad de la anastomosis colorrectal y se asocia con un mayor porcentaje de estoma de protección, lo que parece disminuir el riesgo de FP.
The value of leakage testing during colorectal resections to identify anastomotic leaks or bleeding has not been established. Our aim was to compare the impact of intraoperative colonoscopy (IOC) versus insufflation with a syringe, as leakage testing in lower anterior resection for rectal cancer, with respect to the incidence of postoperative leakage (PL).
Materials and methodsA retrospective study utilizing a prospective database of 426 patients with rectal cancer that underwent elective lower anterior resection, within the time frame of January 2015 and December 2019, was conducted. The anastomotic leak test was chosen by the surgeon. The incidence of PL was compared between patients that underwent IOC and those that had the syringe leak test, utilizing the logistic regression analysis. Propensity score matching was included.
ResultsThere were no significant differences in the clinical characteristics or morbidity and mortality rates between the 2 groups. Four patients were excluded, leaving a patient total of 422. Seventy patients with IOC were compared with 352 that had the syringe leak test. The incidence of PL was 5.7% in the IOC group and 12.2% in the control group (P=.001). After propensity score matching (n=221), balancing the characteristics between the groups, the incidence of PL was 5.7% in the IOC group and 13.9% in the syringe leak test group (P=.001).
ConclusionIOC was shown to be a safe method for evaluating the integrity of colorectal anastomosis and was associated with a higher percentage of protective stoma use, appearing to reduce the risk for PL.
La filtración de la anastomosis es la más devastadora complicación de una resección intestinal con anastomosis colorrectal, con una incidencia general de hasta el 30%. Esta no solo aumenta significativamente la tasa de morbimortalidad, sino que también conduce a malos resultados oncológicos al aumentar la tasa de recurrencia del cáncer tanto local como a distancia, y retrasa el inicio del tratamiento adyuvante1,2. La duración media de la hospitalización y los costos de atención médica para pacientes con filtración postoperatoria (FP) son entre 4 y 5 veces mayores a los de pacientes sin filtración3.
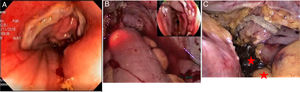
Las pruebas de fuga para anastomosis (PFA) se han implementado con el fin de disminuir el riesgo de complicaciones asociadas a la FP4,5; entre ellas se encuentra la colonoscopia intraoperatoria (CIO), que además de valorar la anastomosis colorrectal, ha sido usada para localizar lesiones no palpables que, en caso de ser obstructivas, permitan descartar lesiones sincrónicas y lavar el colon proximal a la obstrucción. Se han generado algunas dudas sobre si la CIO impide, por la distensión del colon, la manipulación y disección laparoscópica. El aire que se insufla en la CIO directamente sobre la anastomosis tiene una presión constante y posteriormente puede extraerse; durante esta evaluación directa se pueden identificar no solo fallas del grapado, sino también sangrado y la condición de la mucosa (isquemia)6–8, permitiendo reparaciones primarias y/o estomas de protección. Varios estudios han demostrado que este procedimiento es seguro y que no aumenta la tasa de conversión a cirugía abierta, el tiempo quirúrgico o la estancia hospitalaria7,9,10. La prueba estándar se realizó inyectando con una jeringa de 50cc aire o una mezcla de solución salina con azul de metileno o solución yodada a través del ano.
En las últimas décadas, se han propuesto otras PFA, como el uso de verde de indocianina (ICG por sus siglas en inglés), para evaluar la integridad del suministro de sangre a la anastomosis11. Varios estudios han reportado resultados prometedores con ICG y tasas reducidas de FP12,13; sin embargo, no hay consenso sobre su uso rutinario.
El presente estudio tiene como objetivo comparar la utilidad de la CIO frente a la prueba estándar de insuflación con jeringa como prueba diagnóstica de fuga anastomótica intraoperatoria, permitiendo un tratamiento precoz de la misma, en una resección anterior por cáncer de recto, y que pueda disminuir el riesgo de FP.
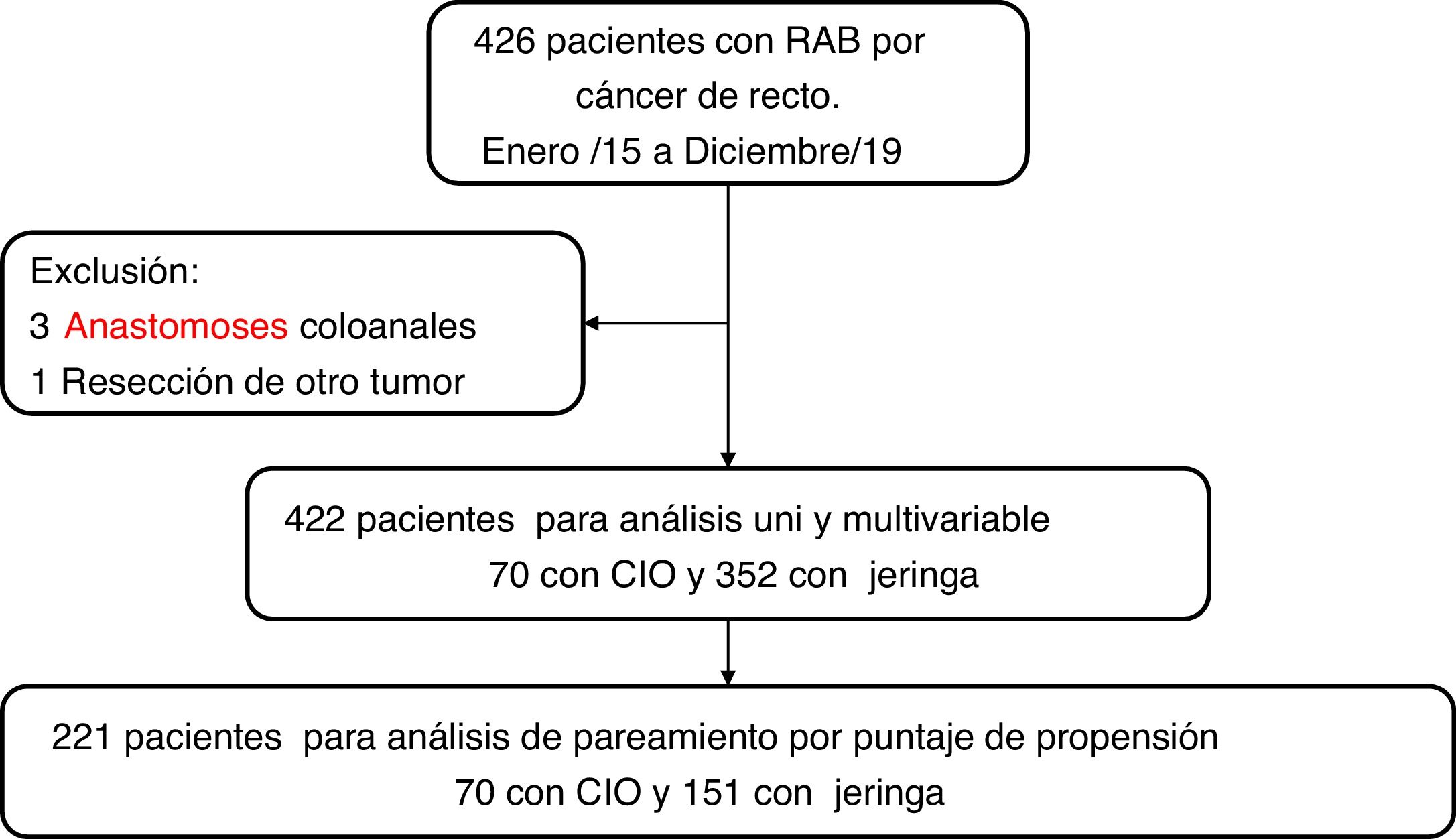
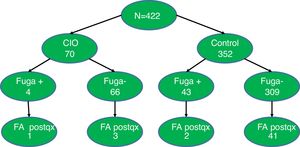
Material y métodosPoblaciónSe revisaron y analizaron 426 historias clínicas de pacientes con cáncer de recto en una base de datos prospectiva del Servicio de Cirugía Gastrointestinal del Instituto de Cancerología Las Américas-AUNA y la Clínica del Rosario en Medellín, Antioquia, de enero de 2015 a diciembre de 2019. Se incluyeron pacientes mayores de 18 años a quienes se realizó una resección anterior baja de recto por laparoscopia y anastomosis intestinal con grapadora. Se excluyeron 4 pacientes, 3 a quienes se realizó anastomosis coloanal y un paciente a quien se resecó de forma simultánea otro cáncer primario. En total 422 pacientes ingresaron al estudio (fig. 1). Todas las intervenciones fueron realizadas por un equipo quirúrgico especializado en cirugía oncológica, gastrointestinal o colorrectal.
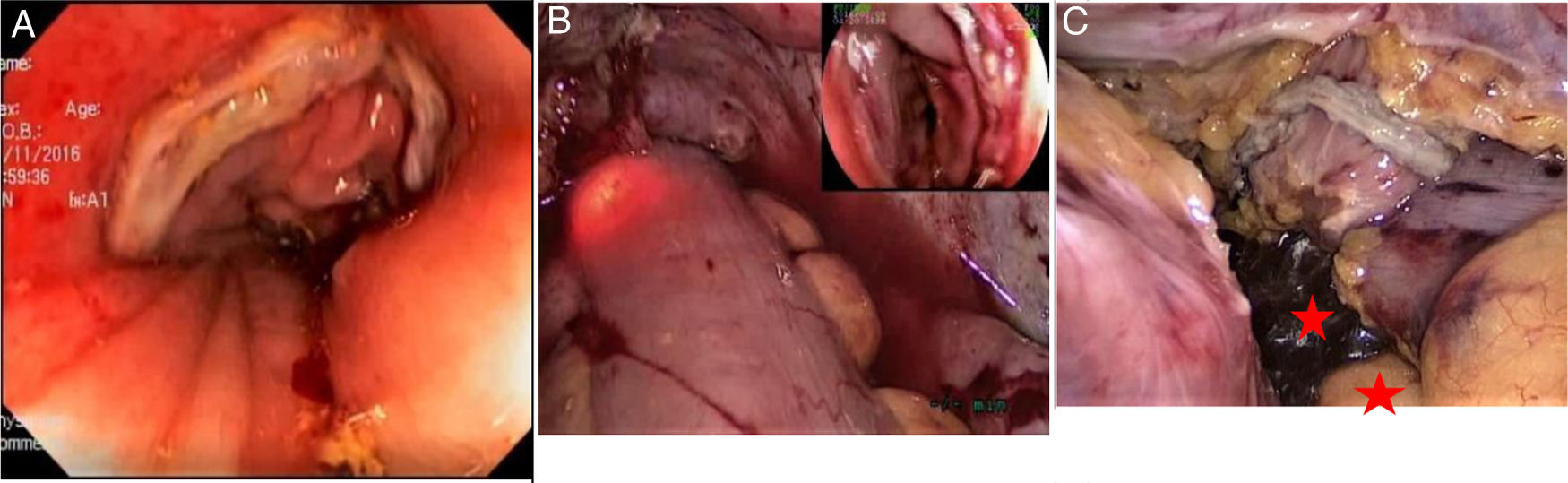
Valoración de la integridad de la anastomosisDespués de la anastomosis colorrectal con grapadora circular, se pinzó el intestino proximal a la anastomosis con una pinza atraumática y se llenó la cavidad pélvica con solución salina al 0.9% tibia. Al mismo tiempo, un cirujano con entrenamiento endoscópico insertó el colonoscopio a través del ano hasta visualizar la línea de anastomosis. Se realizó insuflación sostenida con el colonoscopio; además, se observó si presentaba sangrado o isquemia. En el grupo control se inyectó con una jeringa de 50cc a través del ano aire o una mezcla de solución salina con azul de metileno o solución yodada, de acuerdo con las preferencias del cirujano (fig. 2). La salida de burbujas de aire o de la solución inyectada a la cavidad pélvica se consideró positivo para fuga de anastomosis. En este caso, a todos los pacientes se les realizó ileostomía de protección. Otros manejos adicionales fueron sutura intracorpórea o sutura transanal. No se realizó nueva anastomosis en ninguno de los casos.
Filtración postoperatoriaEl diagnóstico de FP se sospechó por la presencia de dolor abdominal, fiebre, taquicardia y/o drenaje de materia fecal, gas o pus por la herida quirúrgica o por la sonda para drenaje pélvico si la tenía. El diagnóstico se confirmó mediante tomografía computarizada de abdomen y pelvis con contraste hidrosoluble oral y/o rectal, rectoscopia o reexploración quirúrgicas. La gravedad de la complicación se definió según la clasificación extendida de complicaciones quirúrgicas de Clavien-Dindo14. Una filtración de anastomosis posquirúrgica clasificada como Clavien-Dindo≥II en los primeros 30 días postoperatorios se definió como una FP sintomática.
Análisis estadísticoEl objetivo principal de este estudio fue comparar la CIO frente a la prueba estándar de insuflación con jeringa para el diagnóstico de fuga de anastomosis intraoperatoria, dando un tratamiento precoz que pueda reducir el riesgo de incidencia de FP sintomática después de la cirugía laparoscópica colorrectal. Teniendo en cuenta que la incidencia de FP fue baja en general y que la asignación de pacientes al grupo de insuflación con jeringa o CIO no fue aleatoria, se utilizó un enfoque de puntuación de propensión para ajustar los posibles factores de confusión y garantizar la comparabilidad. El puntaje de propensión se estimó utilizando un modelo de regresión logística. La variable de resultado fue la conducta de CIO, y las variables de confusión de base plausibles se incluyeron como covariables. La edad y la distancia entre el sitio anastomótico y el margen anal se consideraron como variables continuas. Se utilizó el tamaño del tumor con transformación logarítmica. Las otras covariables se dicotomizaron de acuerdo con sus valores de corte clínicamente apropiados.
Los pacientes que se sometieron a CIO se compararon con aquellos que se sometieron a PFA con jeringa en una proporción de 1:2. El desequilibrio de las características de los pacientes antes y después del emparejamiento se examinó mediante histogramas y diagramas del puntaje estimado de propensión (PEP) y las diferencias estandarizadas. Para el conjunto de pacientes pareados, las razones de probabilidad y sus intervalos de confianza del 95% (IC 95%) se estimaron mediante el análisis de regresión logística univariable (condicional). Las razones de riesgo y sus IC 95% se estimaron utilizando modelos incondicionales de la misma manera.
Realizamos un análisis de regresión logística multivariable mediante selección por pasos con un nivel de significación del 5%, ajustado por las mismas variables que en la estimación de los análisis del puntaje de propensión. Además, se aplicó un modelo logístico simple ajustado para PEP. Finalmente aplicamos modelos de regresión logística estratificada. Se construyeron 5 estratos de manera post hoc: 5 grupos ecualizados clasificados de acuerdo con los quintiles del PEP.
Se utilizó el software SAS®, versión 9.4 (SAS Institute, Cary, NC, EE. UU.) para todos los análisis. Todos los valores de p se informan de 2 colas.
Consideraciones éticasEl protocolo se elaboró según las normas éticas internacionales y la legislación colombiana, y tanto este como la ejecución del estudio fueron aprobados y vigilados por el Comité de Ética Independiente Clínica Rosario Tesoro, el cual cumple con las normas de Buenas Prácticas Clínicas en todas sus actividades.
Los autores declaran que este artículo no contiene información personal que permita identificar a los pacientes. Para esta investigación no se han realizado experimentos en seres humanos ni en animales, por lo que no fue necesario conseguir el consentimiento informado de los pacientes.
ResultadosEn total, a 422 pacientes con cáncer de recto se les realizó una resección anterior baja laparoscópica de forma electiva. A todos los pacientes se le realizó PFA, sea por CIO o por PFA con jeringa. Los 2 grupos de pacientes fueron comparables en términos de edad, sexo, índice de masa corporal y clasificación de la American Society of Anesthesiologists, entre otras características del paciente y del tumor.
La CIO se realizó en 70 pacientes (16.4%) y la PFA con jeringa se realizó en 352 pacientes (83.4%) (grupo control). Las características antes y después de la correspondencia de PEP se resumen en la tabla 1. Antes del emparejamiento de PEP (n=422), el grupo CIO tenía una mayor frecuencia de antecedentes de tabaquismo (p=0.03), estadio clínico avanzado (p=0.007), quimiorradioterapia preoperatoria (p=0.01) y ostomía protectora (p<0.0001) que el grupo de control. Después de la coincidencia de PEP (n=221), todas las covariables de ajuste estaban bien equilibradas, lo que resultó en una disminución de las diferencias estandarizadas a menos de 0.10.
Comparación de las características de la cohorte total (n=422) y pareada (n=221)
| Cohorte total (n=422) | Cohorte pareada (n=221) | |||||
|---|---|---|---|---|---|---|
| Variables | Grupo CIO | Grupo jeringa (n=352) | p | Grupo CIO | Grupo jeringa (n=151) | p |
| Sexo, n (%) | ||||||
| Masculino | 39 (54) | 185 (52.6) | 0.18 | 39 (54) | 80 (52.9) | 0.48 |
| Femenino | 31 (46) | 167 (47.4) | 31 (46) | 71 (47.1) | ||
| Edad en años, mediana (RIQ) | 61 (47-72) | 63 (49-74) | 0.82 | 61 (47-72) | 62 (54-66) | 0.66 |
| IMC, mediana (RIQ) | ||||||
| >25 | 52 (74.3) | 271 (76.9) | 0.76 | 52 (74.3) | 108 (71.5) | 0.88 |
| <25 | 18 (25.7) | 81 (23.1) | 18 (25.7) | 43 (38.5) | ||
| ASA, n (%) | ||||||
| I | 24 (34.2) | 123 (39.4) | 0.09 | 24 (34.2) | 45 (29.8) | 0.68 |
| II-III | 46 (65.8) | 229 (60.6) | 46 (65.8) | 106 (70.2) | ||
| Estadio, n (%) | ||||||
| I-II | 17 (24.3) | 82 (23.3) | 0.01 | 17 (24.3) | 31 (20.5) | 0.63 |
| III-IV | 53 (75.7) | 270 (76.7) | 53 (75.7) | 120 (79.5) | ||
| QRT preoperatoria, n (%) | ||||||
| Sí | 63 (90) | 318 (90.3) | 0.35 | 63 (90) | 129 (85.4) | 0.79 |
| No | 7 (10) | 34 (9.7) | 7 (10) | 22 (14.6) | ||
| Uso de dren pélvico | ||||||
| Sí | 22 (31.4) | 135 (38.3) | 0.07 | 22 (31.4) | 54 (35.7) | 0.07 |
| No | 48 (68.6) | 217 (61.7) | 48 (68.6) | 97 (64.3) | ||
| Ostomía, n (%) | ||||||
| Sí | 54 (77.1) | 181 (51.4) | 0 | 54 (77.1) | 78 (51.4) | 0.52 |
| No | 16 (22.9) | 171 (48.6) | 16 (22.9) | 73 (48.6) | ||
ASA: clasificación de la American Society of Anesthesiologists; IMC: índice de masa corporal; QRT: quimiorradioterapia; RIQ: rango intercuartílico.
La incidencia general de fuga anastomótica fue del 11.1% (47/422) y del 11.3% (25/221) en las cohortes completas y emparejadas con PEP, respectivamente. La incidencia de FP fue significativamente menor en el grupo con CIO que en el grupo control tanto en la cohorte completa (4/70, 5.7% vs. 55/352, 12.2%; p=0.001) como en la cohorte emparejada con PEP (4/70, 5.7% vs. 21/151, 13.9%; p=0.001). Hubo una muerte en cada grupo.
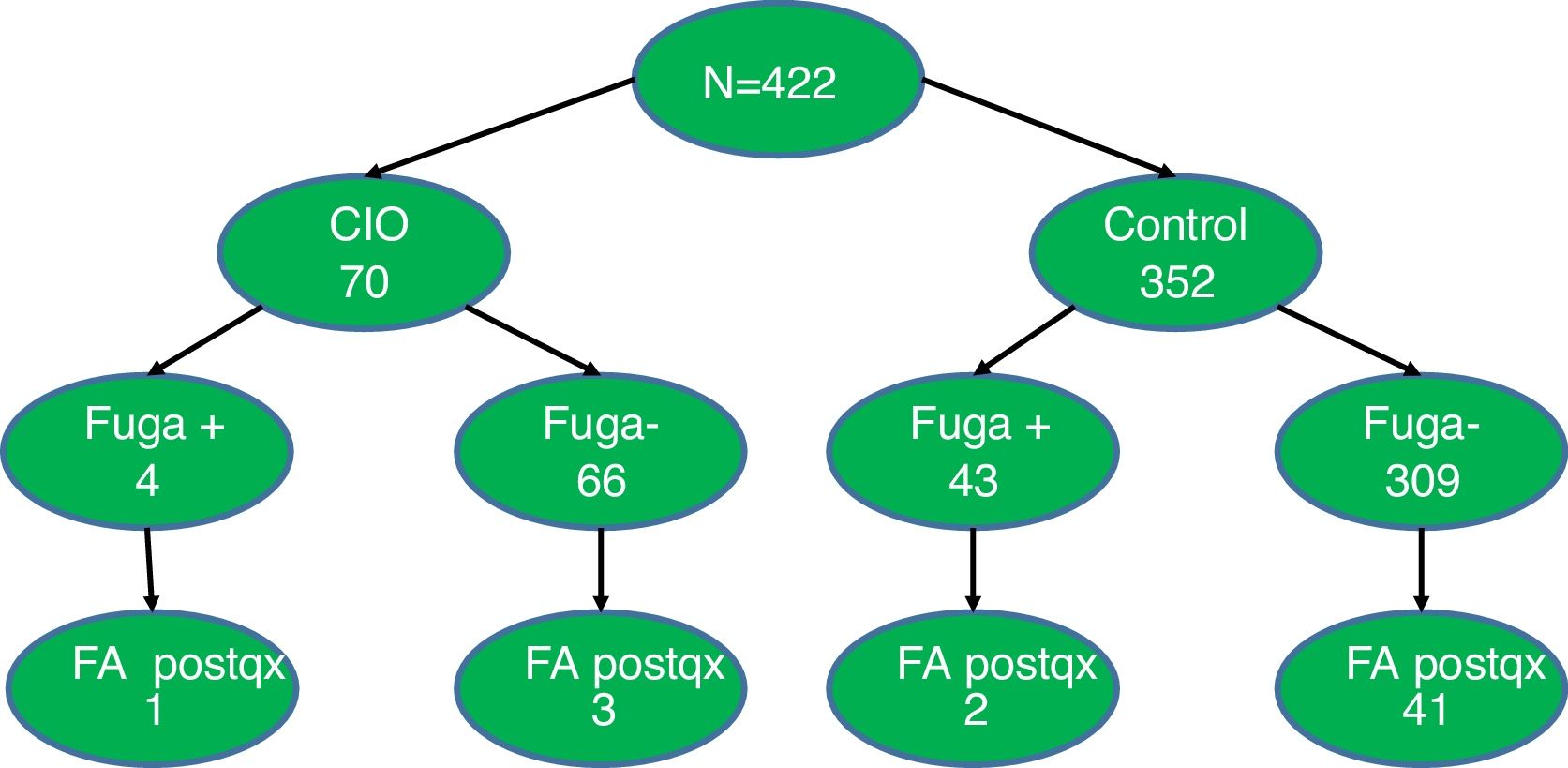
En el grupo de CIO, 4 pacientes presentaron FP; en 3 de ellos la PFA había sido negativa durante la cirugía (3/66, 4.5%). En la figura 3 se describen las tasas de FP de los pacientes a quienes se realizó CIO comparadas con las de los pacientes a quienes se realizó PFA con jeringa.
En el análisis de regresión logística univariable, la CIO redujo significativamente el riesgo de FP (OR 0.21; IC 95% 0.075-0.57, p=0.002). En el análisis de regresión logística multivariable ajustado y sin eliminación para las mismas variables que en la estimación del análisis PEP, la CIO redujo significativamente el riesgo de FP (OR 0.17; IC 95% 0.061-0.50, p=0.001). En el análisis de regresión logística multivariable con selección por etapas, la CIO redujo significativamente el riesgo de FP (OR 0.16; IC 95% 0.057-0.45, p=0.001). En el análisis de regresión logística univariable incondicional para la cohorte compatible con PEP, la CIO redujo significativamente el riesgo de FP (OR 0.19; IC 95% 0.065-0.53, p=0.002). En el análisis de regresión logística multivariable ajustado para PEP, la CIO redujo significativamente el riesgo de FP (OR 0.20; IC 95% 0.070-0.55, p=0.002). Finalmente, en el análisis de regresión logística univariable estratificado en 5 grupos construidos por PEP, la CIO redujo significativamente el riesgo de FP (OR 0.19; IC 95% 0.067-0.53, p=0.002). La CIO redujo fuerte y consistentemente el riesgo de FP con proporciones impares más bajas (OR 0.16-0.23) en todos los análisis de regresión usando PEP.
Las implicaciones clínicas tras un mes de evolución en el grupo con CIO y la cohorte evaluada de PFA con jeringa y estandarizada con PEP se recogen y comparan para los 2 grupos en la tabla 2.
Evolución postoperatoria de los pacientes con CIO y la cohorte evaluada de PFA con jeringa y estandarizada con PEP (n=221)
| Evolución | CIO (n=70) | Jeringa (n=151) | p |
|---|---|---|---|
| Total de fugas | 4 | 21 | 0.001 |
| Íleos | 11 | 16 | 0.234 |
| Sepsis abdominal o pélvica | 1 | 6 | 0.21 |
| Nueva cirugía | 1 | 5 | 0.43 |
| Estancia hospitalaria, días | 17 | 21 | 0.34 |
| Mortalidad | 1 | 1 | 0.91 |
CIO: colonoscopia intraoperatoria; PEP: puntaje estimado de propensión; PFA: prueba de fuga anastomótica.
La FP está influida por muchos factores, relacionados con el paciente, el tumor y el cirujano. En la tabla 3 se describen los factores asociados a las FP.
Factores asociados a las filtraciones postoperatorias
| Preoperatorio | Intraoperatorio | ||
|---|---|---|---|
| No modificables | Modificables | Alto riesgo | Protectores |
| Sexo | Fumador | Contaminación | Antibióticos intravenosos |
| Anastomosis distal | Obesidad | Cirugía mayor de 4h | Monitorización cardíaca |
| Tumor>3cm | Alcoholismo | Inotrópicos | Técnica operatoria |
| Estadio>2 | Esteroides | Pérdida de sangre | Grapado |
| Metástasis | Bevacizumab | Transfusión | Prueba de fugas |
| Radioterapia | Infliximab | Altura del tumor | Ostomía |
| ASA>II | Tacrolimus | ||
| Diabetes | Everolimus | ||
| EPOC-exfumador | Azatioprina | ||
| Enfermedad vascular | Micofenolato | ||
| Cirugía de urgencia | Desnutrición | ||
| Enfermedad renal | |||
ASA: clasificación de la American Society of Anesthesiologists; EPOC: enfermedad pulmonar obstructiva crónica.
Fuente: modificada de McDermott et al.15.
La PFA se considera un factor que disminuye el riesgo de presentar filtración intestinal posquirúrgica en la medida en que permite realizar una intervención temprana para corregirla y/o protegerla.
Gilbert y Trapnell16 reportaron la instilación intrarrectal de solución salina como prueba de fugas después de una anastomosis intestinal, usando una presión de distensión de 25cmH2O. La fuga (24%) fue tratada mediante sutura y solo un paciente desarrolló filtración en el postoperatorio. Los autores concluyeron que este era un buen método, ya que el sitio de la fuga se puede ver y tratar en comparación con la insuflación de aire. Esta prueba se consideró simple y efectiva17; incluso algunos estudios plantean que es seguro evitar el estoma de protección en pacientes con prueba de fuga negativa18. En las pruebas de fuga con agua o gas se debe controlar la presión de instilación, ya que el exceso puede provocar disrupción anastomótica.
También se ha utilizado la combinación de solución salina y azul de metileno para evaluar la integridad anastomótica, al identificar el sitio de filtración por la salida del colorante. En una serie de 229 pacientes a quienes se realizó PFA con azul de metileno, la prueba fue positiva en el 7% de los casos y todas fueron corregidas mediante sutura o rehaciendo la anastomosis. Los autores consideraron que la fuga de azul de metileno puede ser más fácil de detectar en comparación con las pruebas de aire/agua19. En un estudio reciente, Yang et al.20 compararon el rendimiento de la CIO con la PFA con jeringa en 430 pacientes en cirugía por cáncer rectal, encontrando que la tasa de FP fue del 11.7% en el grupo con PFA con jeringa negativa comparado con el 4.3% en el grupo con CIO negativa, lo que muestra que la CIO presenta mejor rendimiento comparada con otras pruebas para evidenciar fuga anastomótica. La realización de estoma de protección tras la prueba de fugas positiva fue significativamente mayor en el grupo con CIO que en el grupo sin CIO (4.65 frente a 0.93%). Otros autores cuestionan la efectividad de la prueba de fugas para disminuir el riesgo de FP. Wu et al.21 reportaron que la realización de la prueba de fuga intraoperatoria no redujo la incidencia de FP.
En esta serie se realizó PFA de forma rutinaria en todos los pacientes sometidos a resección anterior baja de recto, sin embargo, la elección de uno u otro tipo de prueba de fuga depende de las preferencias o entrenamiento de cada cirujano (cirujano oncólogo, cirujano gastrointestinal o coloproctólogo). Se comparó el grupo a quienes se realizó CIO y el grupo sin CIO en términos de impactar la incidencia de FP, la incidencia de sangrado inmediato y tardío y la necesidad de estoma de protección, buscando aclarar si la PFA intraoperatoria con CIO es un método más confiable para detectar defectos técnicos en las anastomosis comparada con el método convencional con jeringa y así disminuir el riesgo de FP. Hubo resultados interesantes en la tasa de FP entre los 2 métodos empleados. La tasa de FP fue menor en el grupo de CIO, aunque la incidencia de estoma de protección fue mayor en este grupo. Partiendo de la premisa de que no hubo diferencia en la técnica quirúrgica de la anastomosis entre los 2 grupos, la mayor tasa de prueba de filtración intraoperatoria positiva en el grupo con CIO puede indicar que la PFA con CIO puede ser un método más eficaz para detectar pequeños defectos en la anastomosis.
Se encontró que un paciente con CIO y PFA negativa presentó FP. La FP siempre podrá ser un desenlace; si bien la técnica quirúrgica es un factor importante para filtración, en la FP están involucrados otros factores, como las comorbilidades, el estado nutricional o las alteraciones vasculares, entre otras características del paciente.
Existen preocupaciones sobre la seguridad y las potenciales complicaciones relacionadas con la CIO. Se especula que la CIO puede dañar la anastomosis por elevación de la presión intraluminal. Se considera que este es un procedimiento seguro, ya que algunos estudios han mostrado que la presión máxima en el neorrecto después de la resección y anastomosis colorrectal puede ser de hasta 200mmHg. La presión de aire máxima generada por la fuente del colonoscopio varía entre 300 y 375mmHg, y la presión de aire en la punta del colonoscopio es de 72 a 166mmHg, un valor menor que el producido por la fuente debido a la fuga de aire a través del canal y de la conexión con la fuente de luz22,23. Kozarek y Sanowski22 demostraron que la presión media sostenida de aire intraluminal durante la colonoscopia diagnóstica fue de 22mmHg (rango 9-57mmHg). Se recomienda que la CIO sea realizada por endoscopistas quirúrgicos capacitados y con experiencia.
Estudios anteriores han informado sobre la eficacia de la imagen de fluorescencia con ICG para valorar la perfusión en la anastomosis13. En nuestros pacientes, la isquemia puede haber sido la principal causa de la fuga anastomótica postoperatoria, porque se detectaron 3 pacientes con FP de 66 pacientes con PFA negativas por CIO. La evaluación intraoperatoria de la integridad mecánica con CIO junto con el ICG podría contribuir en gran medida a una disminución en la incidencia de fuga anastomótica.
El presente estudio muestra algunas limitaciones. Fue un estudio retrospectivo no aleatorizado, el número de pacientes en el grupo con CIO fue pequeño, la decisión de realizar PFA usando CIO dependía de las preferencias de los cirujanos; sin embargo, brinda información útil y da pie a realizarlo con estudios controlados, aleatorizados a mayor escala que proporcionen una evidencia más fuerte frente a la utilidad de la CIO y así poder recomendarla. Adicionalmente, se deben tener en cuenta la curva de aprendizaje para la realización del procedimiento y el aumento de los costos de la cirugía.
Consideramos que la PFA con CIO es una opción válida en casos en los que se considere necesario realizar CIO para otro fin, o en los lugares en donde se disponga de esta técnica sin generar un aumento en los costos.
En conclusión, la evaluación anastomótica por medio de CIO es una técnica segura y se asoció con una reducción significativa en la incidencia de FP en pacientes sometidos a cirugía de cáncer rectal, que pudiera ser secundaria a la mayor realización de estoma de protección y eventualmente el uso de drenes en la cavidad pélvica. La visualización directa de la anastomosis por colonoscopia, además de proporcionar información útil, puede ayudar a realizar el tratamiento intraoperatorio necesario para prevenir la FP. Los resultados de este artículo plantean la necesidad de nuevos estudios de metodología más rigurosa sobre la identificación y el tratamiento intraoperatorio de la filtración anastomótica y su impacto clínico, que puedan llevar a un mejor desenlace para los pacientes.
Conflicto de interesesLos autores no presentan ningún conflicto de intereses.
FinanciaciónEste estudio se realizó con el apoyo de proyecto de sostenibilidad de la Vicerrectoría de Investigación de la Universidad de Antioquia, Medellín, Colombia.
Al bioestadístico y epidemiólogo Víctor Calvo por su colaboración.