El síndrome de rumiación es un trastorno funcional gastrointestinal que se caracteriza por la regurgitación posprandial sin esfuerzo de los alimentos ingeridos hasta la boca, en el que la contracción posprandial no percibida de la pared abdominal sería un mecanismo clave. En estos pacientes, el flujo retrógrado del contenido gástrico ingerido hasta la boca se produce debido a la combinación de una presión intraabdominal elevada con una presión intratorácica negativa. La prevalencia estimada es de alrededor del 2% en la población general adulta. Las características clínicas principales incluyen: a) regurgitación posprandial precoz; b) el material regurgitado sin esfuerzo es similar al alimento ingerido; c) el material regurgitado se escupe o se vuelve a tragar. El diagnóstico clínico del síndrome de rumiación requiere el cumplimiento de los criterios clínicos. Las pruebas de manometría esofágica de alta resolución idealmente con impedancia pueden representar un complemento importante para el diagnóstico clínico. Su manejo se basa en la instrucción acerca de la naturaleza del trastorno, la educación en respiración diafragmática posprandial y la evaluación de posible comorbilidad psiquiátrica. El uso del baclofeno se reserva como segunda línea para pacientes con síntomas refractarios.
Rumination syndrome is a functional gastrointestinal disorder characterized by effortless postprandial regurgitation of ingested food into the mouth. An unperceived postprandial contraction of the abdominal wall could be a key mechanism. In those patients, retrograde flow of the ingested gastric content into the mouth is produced due to a simultaneous combination of elevated intra-abdominal pressure and negative intrathoracic pressure. The estimated prevalence is around 2% in the general adult population. The main clinical characteristics include: a) early postprandial regurgitation, b) the effortlessly regurgitated material is similar to the ingested food, c) the regurgitated material is spit out or swallowed again. The clinical diagnosis of rumination syndrome relies on the clinical criteria. High resolution esophageal manometry, ideally including impedance monitoring, can be an important adjunct for making the clinical diagnosis. Its management is based on instruction as to the nature of the pathology, education in postprandial diaphragmatic breathing, and the assessment of possible psychiatric comorbidity. Baclofen use is reserved for second-line treatment in patients with refractory symptoms.
El término rumiación, que se aplica tanto al ser humano como a los animales, deriva del latín ruminor, que significa ‘traer desde la garganta o masticar lo regurgitado’1. Es un proceso normal en algunos grupos de animales como las vacas, ovejas y cabras2, los que se conocen como rumiantes.
El síndrome de rumiación es un trastorno funcional digestivo caracterizado por la regurgitación repetitiva y sin esfuerzo de comida recientemente ingerida hacia la boca, seguida de un nuevo episodio de masticación y deglución o expulsión del bolo alimenticio, el cual típicamente no presenta un sabor ácido o amargo, ya que ocurre pocos minutos después de comer. Representan características habituales y claves en el diagnóstico: a) el episodio suele repetirse hasta que el material regurgitado se vuelve ácido y b) el material regurgitado suele resultar placentero para el paciente2.
Afecta tanto a la población pediátrica como a la población adulta2-4. El síndrome de rumiación con frecuencia es mal diagnosticado como enfermedad de reflujo gastroesofágico refractario o vómitos recurrentes, lo que suele resultar en un prolongado retraso en el diagnóstico5.
Este síndrome se encuentra descrito y clasificado dentro de los trastornos funcionales gastroduodenales y presenta criterios establecidos dentro de la Clasificación de Roma IV6, los que se describen en la tabla 1.
Criterios diagnósticos del síndrome de rumiación
| Debe incluir lo siguiente:Regurgitación persistente o recurrente de comida recientemente ingerida con expulsión oral, o con remasticación y redeglución subsecuenteLa regurgitación no es precedida por arcadasLos criterios se cumplen por los últimos 3 meses con comienzo de síntomas, al menos 6 meses previo al diagnósticoObservaciones que apoyan el diagnóstico:Los eventos de regurgitación sin esfuerzo no van precedidos de náuseasEl material regurgitado contiene comida reconocible, que puede tener un sabor agradableEl proceso tiende a cesar cuando el contenido regurgitado se vuelve ácido |
Extraído de Stanghellini et al.6
Existen escasos datos acerca de la incidencia y prevalencia en adultos. Si bien se considera como un trastorno infrecuente, es probable que su prevalencia real esté subestimada, dada la falta de reconocimiento de esta enfermedad por parte del clínico y de los pacientes. En un estudio canadiense, al utilizar los criterios diagnósticos de Roma II, se reportó una prevalencia en población general del 0.8% (IC95%: 0.3-1.3) mediante la aplicación de cuestionarios7. Por otro lado, en un estudio multicéntrico reciente se estableció la prevalencia global de enfermedades funcionales gastrointestinales de acuerdo con los criterios de Roma IV y se describió una prevalencia del síndrome de rumiación del 2.8% (3.1% en mujeres, 2.5% en hombres) mediante encuesta en línea y de un 1.1% (1.4% mujeres, 0.8% hombres) de prevalencia mediante entrevista personal8. En pacientes con fibromialgia o trastornos de la alimentación, la prevalencia del síndrome de rumiación es mayor y puede llegar al 7-8%9,10.
En población pediátrica, en un estudio que encuestó a 2,163 niños y adolescentes, con edades comprendidas entre los 10 y 16 años, de 4 provincias de Sri Lanka, utilizando los criterios de Roma III, se reportó una prevalencia mediante la aplicación de un cuestionario del 5.1%, que era similar en hombres y mujeres (5.1% y 5%, respectivamente). De los pacientes afectados, un 12% de ellos tenían síntomas suficientemente graves para causar ausentismo escolar11.
FisiopatologíaLa fisiopatología no es aún del todo conocida, sin embargo, la activación no percibida de la pared abdominal en el periodo posprandial parece ser una característica patogénica cardinal dentro del proceso fisiopatológico. Se ha podido observar mediante manometría gastroduodenal y, más recientemente, con la introducción de la técnica de manometría esofágica de alta resolución con impedancia, que el flujo retrógrado del contenido gástrico que logra llegar a la cavidad bucal en los pacientes con síndrome de rumiación se produce debido a la combinación de una presión intraabdominal elevada junto con una presión intratorácica negativa, lo que da lugar a un gradiente esofagogástrico en dirección oral. En la manometría esofágica de alta resolución con impedancia en periodo posprandial, los fenómenos de rumiación siguen a presurizaciones gástricas con presiones típicamente superiores a 30mmHg en la mayoría de los episodios de reflujo proximal12, lo que se asocia con una relajación del esfínter esofágico inferior y superior en el momento de la presurización gástrica. Estas observaciones revelan que el aumento de presión intraabdominal no puede explicar por sí solo el fenómeno de rumiación y que es probable que la relajación de los esfínteres esofágicos superior e inferior también desempeñe un rol central en este proceso13,14. En los estudios manométricos, el aumento de presión de la musculatura abdominal se observa de manera simultánea en todos los sensores, lo que se reconoce en el trazado como «onda R». En ese mismo sentido, al comparar a los pacientes con síndrome de rumiación con los pacientes con enfermedad por reflujo gastroesofágico, los primeros alcanzan un pico de presiones abdominales con una mediana de 43mmHg, la cual resulta significativamente mayor que la del grupo de enfermedad por reflujo gastroesofágico, cuyo pico de presión abdominal resulta en una mediana de 6mmHg12.
Al comparar a pacientes con síndrome de rumiación y a controles con la prueba del baróstato gástrico, se observó que los pacientes con síndrome de rumiación presentaban más náuseas y sensación de distensión abdominal que los controles. También se observó que, a 4 y 8mmHg de presión de distensión gástrica, el tono del esfínter esofágico inferior se reducía más en estos pacientes que en los controles. Esto plantea una mayor sensibilidad gástrica y relajación del esfínter esofágico inferior durante la maniobra de distensión gástrica. Sin embargo, la mayoría de los pacientes con síndrome de rumiación parecen presentar los fenómenos de acomodación y vaciado gástrico dentro de rangos normales15.
Estudios con electromiografía de la musculatura abdominal muestran que la regurgitación del contenido gástrico se produciría por una maniobra coordinada consistente en una contracción súbita de los músculos intercostales junto a una contracción de los músculos abdominales anteriores16.
En un grupo de 5pacientes con síndrome de rumiación, diagnosticados por criterios de Roma III, que fueron monitorizados con impedancia, manometría esofágica de alta resolución y grabación videofluoroscópica para evaluar la barrera de la unión gastroesofágica en episodios de rumiación, se observó un ascenso de la unión gastroesofágica desde la cavidad abdominal hacia la cavidad torácica, lo que generaba una «pseudohernia» con contenido gástrico y aéreo. Sin embargo, la importancia de esta observación sigue siendo debatida, en particular, porque también se ha descrito en personas sanas durante la actividad física17. En cuanto a la hernia hiatal por deslizamiento, se observó en una cohorte una prevalencia de un 50% tanto en el grupo de síndrome de rumiación como en el grupo de comparación de los pacientes con enfermedad por reflujo gastroesofágico12.
Según los patrones observados en manometría esofágica de alta resolución con impedancia, se han descrito 3variantes de rumiación12:
Rumiación primaria: caracterizada por aumento de la presión abdominal, que precede el flujo retrógrado gástrico hacia el esófago.
Rumiación secundaria: similar a la primaria, pero el aumento de presión abdominal ocurre luego de un evento de reflujo gastroesofágico.
Rumiación asociada a eructos supragástricos: se produce por un mecanismo similar al eructo supragástrico, en el que el movimiento aboral del diafragma crea una presión subatmosférica en el cuerpo esofágico y se relaja el esfínter esofágico superior. Luego se produce entrada de aire al cuerpo esofágico, que se puede ver como un aumento de impedancia en dirección oral, luego y rápidamente (menos de un segundo) el aire es expulsado del cuerpo esofágico, lo que se manifiesta como un retorno a la impedancia basal. El aumento de la presión abdominal se produce durante la expulsión de aire y precede al flujo retrógrado del contenido gástrico.
De forma adicional a los mecanismos fisiopatológicos descritos, se plantea que pacientes con síndrome de rumiación pueden presentar un impulso premonitorio, similar a lo que ocurre en pacientes con tics motores o vocales: es una experiencia somatosensorial aversiva y desagradable que la persona experimenta antes y que se ve aliviada tras el evento de rumiación, lo que reforzaría la contracción abdominal. Este modelo de mecanismos múltiples, o «modelo de mantención», recientemente descrito propone que algunos pacientes pueden presentar mecanismos psicológicos o fisiopatológicos secundarios que contribuyesen al proceso de refuerzo que se produce en respuesta al mecanismo primario, que mantendría la contracción habitual de la pared abdominal18:
- -
Vía de mantenimiento primaria: los fenómenos de rumiación pueden representar un hábito o un reflejo que se desarrolla a través de una respuesta condicionada a estímulos, en este caso, la comida. Se ha formulado la hipótesis de que cuando el material se regurgita el impulso premonitorio se resuelve temporalmente, lo que refuerza la contracción de la pared abdominal.
- -
Posibles mecanismos psicológicos secundarios: el síndrome de rumiación puede mantenerse de forma secundaria por mecanismos ambientales, cognitivos y conductuales, que reforzarían las regurgitaciones continuas. En primer lugar, algunos individuos informan de una alta probabilidad de regurgitación después de comer determinados alimentos. En segundo lugar, algunos individuos describen dificultades para tolerar el impulso premonitorio y permitirán que se produzcan regurgitaciones para aliviar temporalmente sus molestias. En tercer lugar, algunos individuos presentan una preocupación por la forma/peso corporal que podría mantener parcialmente los síntomas, pero que no son atribuibles a un trastorno alimentario. En cuarto lugar, la regurgitación repetitiva podría cumplir una función positiva, al aliviar la ansiedad o proporcionar una sensación de alivio o placer; esto último se ha descrito en niños y adultos con trastornos del desarrollo.
- -
Posibles mecanismos fisiopatológicos secundarios: ciertas comorbilidades podrían contribuir al mantenimiento de la rumiación. El síndrome de rumiación puede darse en el contexto de otras condiciones que presentan regurgitación y vómitos, como la gastroparesia y la enfermedad de reflujo gastroesofágico18.
Un grupo de investigadores estudió el tono vagal en pacientes con síndrome de rumiación y voluntarios sanos a través de la variabilidad de la frecuencia cardiaca, el cual se midió basalmente, durante y después de las comidas. En el momento basal, el tono vagal fue similar y si bien en episodios posprandiales hubo tendencia a mayor tono vagal en el grupo de rumiación, este no fue estadísticamente significativo19.
Desde el punto de vista histopatológico, un estudio de Halland et al.20 en el que se analizaron biopsias duodenales de 22 pacientes con diagnóstico de síndrome de rumiación y se compararon con 10 pacientes controles mostró que el número de linfocitos intraepiteliales fue significativamente mayor en el grupo de rumiación (promedio 15, rango de 8-29 y 2 casos con ≥25 linfocitos intraepiteliales/100 enterocitos), en comparación con el grupo control (promedio 11, rango 11-18). Además, los pacientes con síndrome de rumiación tenían un promedio de conteo eosinofílico significativamente mayor que los controles, con 26 por mm2versus 18 por mm2 (p=0.006). No se observaron patógenos en la histología de ningún grupo, tampoco atrofia vellositaria ni otras características de enfermedad celíaca20. Los autores especulan que los mecanismos musculares que llevan a la rumiación podrían estar en un contexto de inflamación de bajo grado, pero que se requiere mayor investigación para comprobar dicha hipótesis20.
Características clínicasCuando nos enfrentamos a un paciente con sospecha de rumiación, el síntoma predominante es la rápida aparición de regurgitación posprandial y sin esfuerzo, típicamente dentro de los 10minutos de finalizar una comida6,21. Puede producirse luego de cada comida o en la mayoría de las comidas y, en general, ocurre mientras el paciente está comiendo o pocos minutos después de terminar la ingesta, lo que permite que el sabor de la comida sea similar a la comida recién ingerida21. Puede producirse incluso al ingerir solo líquidos, lo que favorecería la regurgitación de alimentos sólidos previamente ingeridos22. Los episodios suelen persistir durante una o 2horas después de la comida, y aun si ocurren con esta temporalidad, el material regurgitado consiste en alimentos parcialmente digeridos que son reconocibles por su sabor. A menudo se desencadena por una sensación de malestar (presión, dolor, ardor) en el abdomen.
Existe dificultad para reconocer esta condición, ya que tanto el paciente como los clínicos no familiarizados con esta enfermedad confunden la rumiación con vómito o reflujo gastroesofágico refractario, lo que retrasa el diagnóstico21, con un aumento de los estudios adicionales y los costos asociados. Para diferenciar de los vómitos, los episodios de regurgitación que se experimentan en el síndrome de rumiación, en general, no van precedidos de náuseas. Además, cuando un paciente vomita, el contenido es difícil de mantener en la boca debido a la intensidad del impulso, que rápidamente elimina hacia el exterior. Sin embargo, podrían existir fenómenos de rumiación incluso varias horas después de la alimentación, ser de mal sabor y tener contenido biliar o ácido21. Los pacientes con rumiación pueden volver a masticar el contenido, escupirlo o volver a tragarlo, según las circunstancias. Este hábito puede llevarlos a limitar sus actividades sociales, sobre todo el comer en presencia de terceros, en restaurantes o lugares de trabajo23.
Algunos individuos con síndrome de rumiación reportan síntomas dispépticos posprandiales que incluyen la plenitud o la sensación de ardor epigástrico24; se ha descrito la presencia de saciedad precoz en alrededor de 3/4 de los pacientes20. Otros síntomas como pirosis, dolor abdominal, diarrea o constipación (estreñimiento) son menos frecuentes, pero no descartan el diagnóstico. Por otro lado, la regurgitación nocturna, la disfagia o los síntomas que ocurren alejados de comidas hacen menos probable el diagnóstico22. Algunos pacientes con síntomas de enfermedad por reflujo gastroesofágico, como pirosis o regurgitación, no responden a inhibidores de la bomba de protones y llegan a cifras cercanas al 50%, con mayor riesgo en sexo femenino, raza latina o pacientes jóvenes25. En ese aspecto, algunos de estos pacientes catalogados como refractarios a enfermedad por reflujo gastroesofágico, con regurgitación como síntoma predominante, podrían corresponder realmente a pacientes con síndrome de rumiación. De hecho, en algunas series, hasta el 100% de los pacientes con síndrome de rumiación se encuentran usando inhibidores de la bomba de protones20.
De la misma manera, ciertos pacientes con otras enfermedades, como acalasia y trastornos de la acomodación o vaciamiento gástrico, refieren síntomas similares, los cuales deberían ser evaluados con estudios pertinentes, según el grado de sospecha23.
En algunos pacientes se describe la presencia de un evento incitante previo al diagnóstico de síndrome de rumiación, como enfermedad o estresor psicosocial (divorcio, muerte familiar, problemas escolares o laborales)26.
Dentro de las complicaciones asociadas al síndrome de rumiación, en niños se ha detectado que hasta el 77% presentan erosiones dentales27 y se ha descrito la halitosis como motivo de derivación28. También en adolescentes y adultos se describe baja de peso como un síntoma asociado en alrededor del 40% de los casos2. En casos graves de compromiso nutricional, se han manejado incluso con yeyunostomía para estabilizar a los pacientes26.
ComorbilidadesEl síndrome de rumiación se ha asociado con la presencia de trastornos de salud mental, como cuadros de ansiedad, depresión, trastornos somatomorfos y trastornos de adaptación, entre otros, de los que la comorbilidad psiquiátrica es un hallazgo bastante frecuente (más del 90% en una serie). Además, un 13% de los pacientes con diagnóstico de un trastorno de evacuación rectal tienen de manera concomitante síndrome de rumiación2,5,26. También algunas series destacan la restricción alimentaria por miedo a escupir o la historia previa de trastornos de alimentación (7-17%), así como el antecedente de abuso (33%)5,29,30.
Aunque algunos estudios han señalado que el síndrome de rumiación se produce predominantemente entre niños y adultos con retraso en el desarrollo, esto no ha sido corroborado por otros estudios: en algunas series la población presentaba inteligencia normal13,16,24.
Proceso diagnósticoEl diagnóstico de síndrome de rumiación es clínico. Debe sospecharse en pacientes que presentan regurgitación posprandial sin esfuerzo y sin arcadas. La presencia de «reflujo refractario» con regurgitación como síntoma predominante indica una rumiación subyacente, que es más frecuente en el subgrupo de mujeres jóvenes31. Los pacientes ven como media a 5 médicos y tienen síntomas cerca de 3 años antes del diagnóstico2. Este retraso puede también tener un rol deletéreo en su estado emocional y muchas veces, por el contexto del paciente, es difícil aceptar el diagnóstico de un trastorno funcional digestivo; también muchas veces resulta de ayuda el apoyo de una prueba diagnóstica objetiva. La confianza en el diagnóstico y una sólida relación médico-paciente es de suma importancia para lograr una buena adherencia al tratamiento y que el paciente acepte su enfermedad.
Las claves diagnósticas de la evaluación clínica inicial deben centrarse en establecer si los síntomas posprandiales son vómitos (como a menudo informan los pacientes) o regurgitación. La regurgitación, como se explicó antes, a diferencia del vómito, no requiere esfuerzo, puede no estar asociada a las náuseas y no está precedida por arcadas ni espasmos. También algunos pacientes pueden referirse a la regurgitación como eructo, por lo que es importante una anamnesis detallada para interpretar correctamente el síntoma. Los pacientes con el síndrome de rumiación a menudo informan de un evento desencadenante antes de la aparición de los síntomas de rumiación32.
En la práctica clínica habitual, en pacientes con sospecha de síndrome de rumiación, se suele excluir una obstrucción mecánica mediante estudio endoscópico alto con biopsias para excluir otros trastornos (por ejemplo, gastroenteritis eosinofílica, enfermedad celíaca o infección por Helicobacterpylori, entre otros) y técnicas de enterografía (enteroclisis por tomografía computada o por resonancia nuclear magnética). La endoscopia digestiva alta suele ser normal en pacientes con síndrome de rumiación, excepto por el hallazgo de esofagitis, que en algunas series se reporta en alrededor del 10%12.
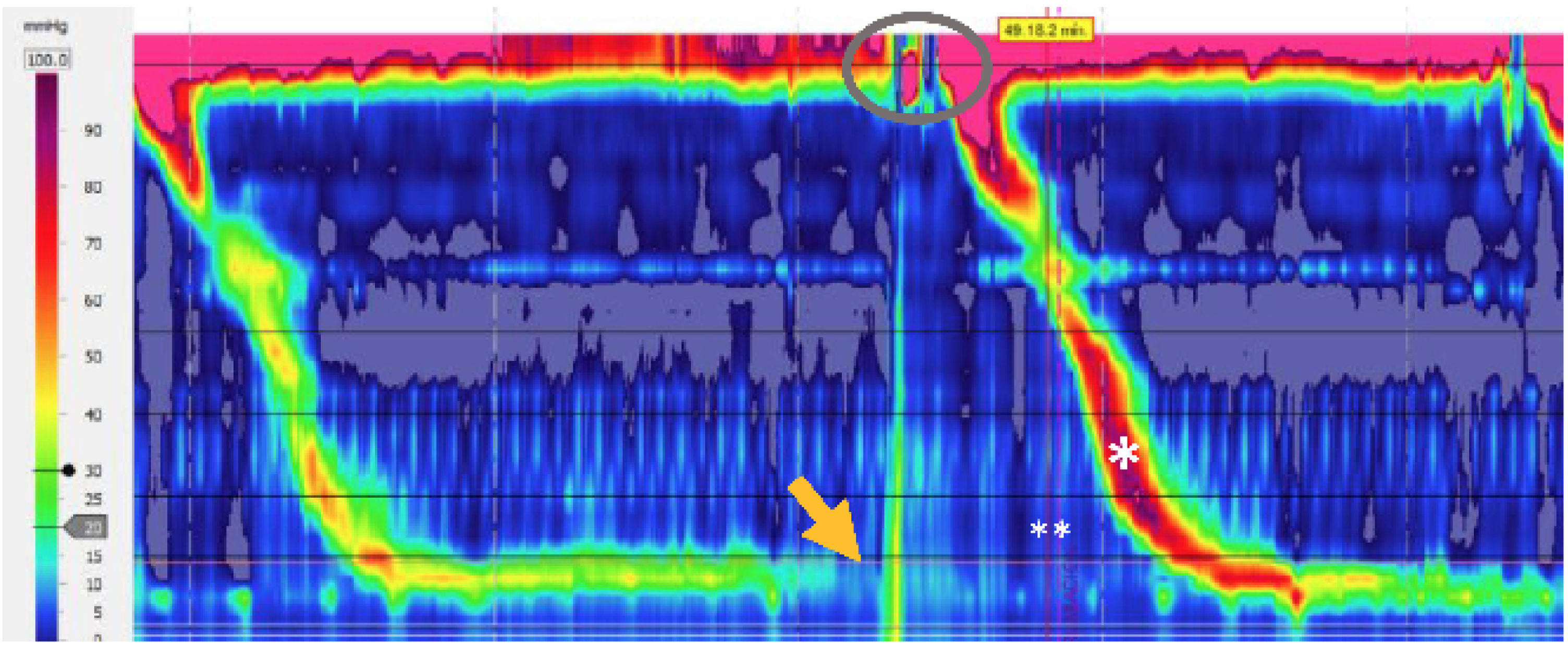
Para casos seleccionados se puede utilizar la manometría antroduodenal o manometría esofágica de alta resolución, idealmente con impedancia en periodo posprandial6. Esta última es considerada como el estándar de oro en algunos estudios, aunque aún no se han establecido valores normativos31. Ambas técnicas diagnósticas son escasas en nuestro medio y se limitan a centros especializados. Los criterios diagnósticos de la manometría esofágica de alta resolución con impedancia para síndrome de rumiación se basan en la presencia de reflujo hasta el esófago proximal asociado a una presurización gástrica mayor a 30mmHg12. Al ser analizada en periodo posprandial luego de una comida estandarizada23, permite caracterizar la presencia de reflujo gastroesofágico mediante las relajaciones transitorias del esfínter esofágico inferior, eructos supragástricos o fenómenos de rumiación. Al evaluar el rendimiento de esta técnica, hasta el 20% de los pacientes con síntomas de enfermedad por reflujo gastroesofágico catalogados como refractarios a inhibidores de bomba de protones presentan criterios de rumiación33. En la figura 1 se observa una manometría esofágica de alta resolución con hallazgos motores posprandiales característicos del síndrome de rumiación.
La motilidad del cuerpo esofágico suele observarse preservada; no obstante, existe el reporte de un caso de síndrome de rumiación asociado a motilidad esofágica inefectiva34.
Además de la manometría esofágica de alta resolución, se ha probado la utilidad del uso de la pH-metría de 24 h con impedancia para el diagnóstico de rumiación. En un estudio reciente, Nakagawa et al.31 evaluaron las características que presentan los pacientes por esa técnica, comparados con la manometría esofágica de alta resolución con impedancia, que se consideró el estándar de oro. Se observó que los pacientes con rumiación presentan de forma excepcional episodios de reflujo en posición acostada y que los episodios de reflujo de extensión proximal son significativamente mayores en pacientes con rumiación. A diferencia de los pacientes con enfermedad por reflujo gastroesofágico, los pacientes con rumiación tienen nadir de pH mayor al poco tiempo de comer y a medida que va transcurriendo el tiempo se va acidificando. El tiempo desde que se detecta reflujo mediante la impedancia y la aparición de síntomas es significativamente menor en pacientes con síndrome de rumiación que en enfermedad por reflujo gastroesofágico31.
En el mismo estudio, para el diagnóstico de rumiación de 0 a 2 puntos mediante el uso de pH-metría de 24 h con impedancia se propone el siguiente puntaje:
El número de reflujos no ácidos posprandiales (hasta un hora poscomida) con valor de corte de 3/h: 1 punto.
Índice de síntomas posprandiales con valor de corte de 60%: 1 punto.
Se hace el diagnóstico de síndrome de rumiación con 1 o 2 puntos, con una sensibilidad de 91.7% y 58% y una especificidad de 78.6% y 93%, respectivamente.
En la figura 2, se observa un ejemplo de trazado de pH-impedancia de 24 h con el protocolo de análisis antes descrito, compatible con síndrome de rumiación.
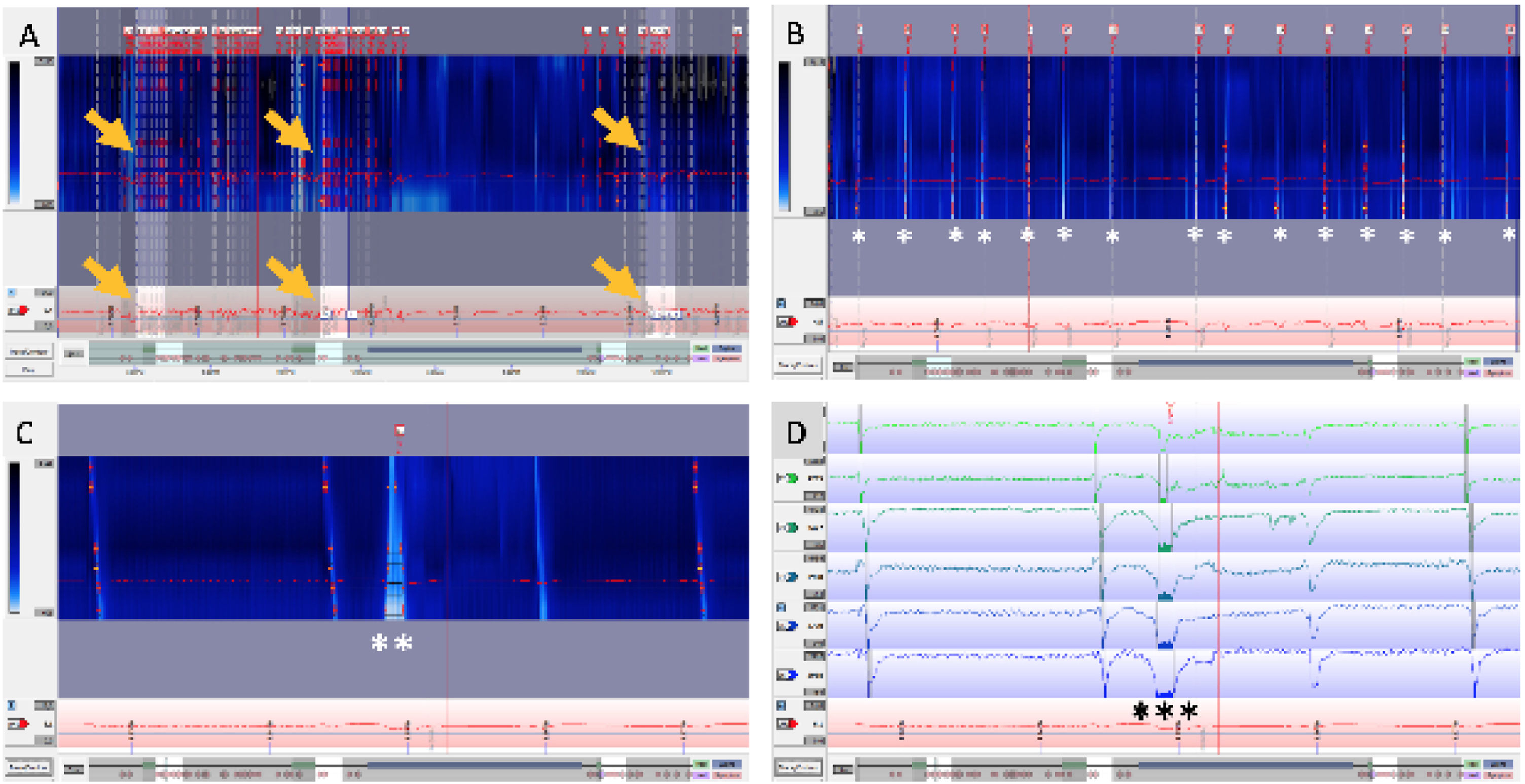
Trazado de pH-impedancia de 24 horas con protocolo de análisis posprandial en 3 comidas, de la misma paciente. A) Ventana de 24 horas: se observan 3 periodos posprandiales (flechas) analizados para obtener criterios propuestos por Nakagawa et al.31. B) Ventana de 60 minutos: periodo posprandial con 15 eventos de reflujos no ácidos (*). C) Ventana de 5 minutos en colorimetría con evento de reflujo no ácido (**). D) Trazado de impedancia, que muestra evento de reflujo no ácido aislado en detalle (***) para el mismo periodo analizado en C.
Hay pocos trastornos gastrointestinales que se presentan con una regurgitación posprandial frecuente y sin esfuerzo distintos del síndrome de rumiación:
Acalasia: Algunos pacientes con acalasia y alteración de la acomodación gástrica tienen regurgitación posprandial. Sin embargo, el síntoma predominante en los pacientes con acalasia es la disfagia35, que no es una característica clásica del síndrome de rumiación. La acalasia puede distinguirse del síndrome de rumiación por sus patrones característicos en la manometría esofágica de alta resolución, así como por la presencia de regurgitación o vómitos posprandiales tardíos.
Enfermedad por reflujo gastroesofágico: el síndrome de regurgitación en la rumiación carece de un sabor agrio, amargo o ácido, que sí es reportado por pacientes con enfermedad de reflujo gastroesofágico. A diferencia del reflujo patológico, los episodios de síndrome de rumiación no son nocturnos. Los medicamentos que suprimen la producción de ácido gástrico, como los inhibidores de la bomba de protones, no suelen mejorar los síntomas en los pacientes con síndrome de rumiación.
TratamientoLa estrategia terapéutica empieza con una adecuada explicación al paciente sobre la naturaleza de la dolencia; se le comenta que corresponde a un trastorno funcional benigno, además de los mecanismos subyacentes que lo producen, para lograr que asuma un rol activo en el manejo de esta condición. Es recomendable un enfoque multidisciplinario, en el que participen gastroenterólogos y equipos de salud mental, especialmente en pacientes con depresión subyacente, trastornos de ansiedad o síntomas refractarios.
Las terapias disponibles van enfocadas a aumentar la presión del esfínter esofágico inferior o a disminuir la presión gástrica generada por la contracción de la musculatura estriada de la pared abdominal. El pilar de la terapia para el síndrome de rumiación es la técnica de respiración diafragmática o respiración abdominal. La respiración diafragmática reduce la presión intragástrica posprandial, aumenta la presión de la zona de unión gastroesofágica y restaura el gradiente de presión a este nivel13. Respecto a los conceptos técnicos, se instruye a los pacientes para que coloquen una mano en el abdomen y otra en el tórax. Luego se les indica que inhalen lentamente por la nariz y que, durante la inhalación, solo la mano en el abdomen debe levantarse y la mano en el pecho debe moverse solo mínimamente. Los pacientes entonces exhalan lentamente por la boca. Cada inhalación o exhalación debe ser lenta y completa, con un objetivo de 6a 8respiraciones por minuto. La técnica se puede enseñar en decúbito supino y también en posición sentada (que es la manera en que los pacientes en general se alimentan)36. Algunos pacientes requieren varias sesiones para aprender la técnica. Suele instruirse a los pacientes para que ejecuten los ejercicios de respiración diafragmática inmediatamente después de una comida y los continúen de 10 a 15 min o más hasta que la sensación de regurgitación se resuelva. El objetivo es que con el tiempo ocurra la respiración diafragmática de manera inconsciente durante los episodios que precipitan la regurgitación. Se debe advertir a los pacientes de que la respiración diafragmática puede sentirse incómoda al comienzo de la terapia. Para disminuir esta sensación y evitar que se limite la adherencia, se les debe instruir en que se suelten los cinturones y eviten el uso de ropa ajustada. Los gastroenterólogos u otros clínicos familiarizados con la técnica pueden ofrecer una instrucción inicial durante la consulta médica36. También los fisioterapeutas con conocimiento de la técnica pueden ser parte del proceso de tratamiento.
Se ha descrito la enseñanza de esa técnica mediante biorretroalimentación, conocida en inglés como biofeedback, de la musculatura toracoabdominal a través de control electromiográfico. Un estudio clínico aleatorizado en 12 pacientes aplicó la biorretroalimentación guiada por electromiografía, consistente en 3 sesiones en 10 días, en las que, antes de una comida estandarizada, se les entrenaba para controlar la actividad de la musculatura abdominotorácica bajo visión electromiográfica conectada a un monitor y se les instruía a reducir la actividad de los músculos intercostales y abdominales anteriores y a aumentar la actividad del diafragma. Luego de comer, se les instruía en cómo prevenir los episodios de rumiación controlando esa musculatura. Después de la sesión, se les pedía a los participantes que realizaran los ejercicios en su casa diariamente 5 min antes y después de 3 comidas diarias (desayuno, almuerzo y cena). Se comparó con un grupo placebo de 11 pacientes, que recibieron simeticona. Dentro de los resultados, se observó que los pacientes que recibieron biorretroalimentación en comparación con el grupo placebo disminuyeron la actividad de los músculos intercostales y de la musculatura abdominal anterior. Además, la biorretroalimentación redujo en 74±6% los episodios de regurgitación vs. 1±14% en el grupo placebo, diferencia que fue estadísticamente significativa, sin reportarse efectos adversos29.
La respiración diafragmática asociada a terapia conductual y asistida por manometría esofágica con impedancia también fue bien tolerada por los pacientes, lo que permitió una disminución de la presión intragástrica, un aumento de la presión de la unión gastroesofágica y el restablecimiento de un gradiente de presión gastroesofágico negativo13. Esta última técnica diagnóstica supone un costo mayor y mayor dificultad en su ejecución, dado su escaso acceso.
En lo que concierne a la respiración diafragmática, se ha visto que incrementaría el tono vagal, pero este no es el mecanismo que explicaría la disminución de los episodios de rumiación19: es posible que afecte más específicamente el aumento de la contractilidad de los músculos de la pared abdominal; además, podría disminuir la ansiedad y aumentar la presión de la unión gastroesofágica19.
Respecto a los síntomas refractarios, se ha propuesto terapia farmacológica y, especialmente, se ha postulado el uso de baclofeno, agonista de ácido gamma-aminobutírico B (GABAB), que es capaz de disminuir las relajaciones transitorias del esfínter esofágico inferior y aumentar la presión sobre él en individuos sanos y en pacientes con enfermedad por reflujo gastroesofágico37,38. Solo 2ensayos han evaluado el impacto del baclofeno en la regurgitación del síndrome de rumiación. En un estudio doble ciego, con placebo y controlado cross-over, que evaluó la efectividad de baclofeno en pacientes con síndrome de rumiación, se observó una disminución de los episodios de regurgitación registrados por los pacientes y, mediante el estudio con manometría esofágica de alta resolución, en los usuarios del fármaco39. Otro estudio también mostró la efectividad del baclofeno en pacientes con episodios de rumiación, con una disminución de los episodios y un aumento de la presión del esfínter esofágico inferior. Sin embargo, faltan datos a largo plazo acerca de su eficacia y perfil de tolerancia40. El baclofeno cruza la barrera hematoencefálica y causa una variedad de efectos secundarios relacionados con el sistema nervioso central que incluyen principalmente confusión, mareos, vértigo, somnolencia, debilidad y temblores. Por lo general, se recomienda empezar con 5-10mg a la hora de acostarse, que pueden aumentarse lentamente hasta llegar a 10mg 3veces al día mientras se vigilan de forma estrecha los efectos secundarios.
Se han usado también en pacientes con síndrome de rumiación antidepresivos tricíclicos junto con técnicas de respiración diafragmática y audios de relajación por al menos 3 meses. Al seguimiento promedio de casi 9 meses, el 90% de los pacientes revelaron mejoría de los síntomas, con una mejoría promedio subjetiva cercana al 70%, con alza o estabilidad del peso en el 80% de los que reportaban baja de peso26. El antidepresivo tricíclico más usado en este estudio fue nortriptilina, que se inicia con 10mg en la noche y se aumenta semanalmente de 10mg la dosis diaria hasta alcanzar la mejoría de síntomas, minimizando los efectos adversos26. El tiempo promedio para observar una mejoría fue 6.3 semanas. El estudio no fue ciego y la mejoría se midió mediante un cuestionario que no está validado, lo que hace necesario crear y validar escalas que permitan comparar las estrategias de tratamiento.
En reportes de casos, el uso de goma de mascar se ha asociado con una reducción del número de episodios de rumiación, pero faltan ensayos aleatorizados para demostrar la efectividad de esta intervención41,42.
Por último, en cuanto a la cirugía, existe un reporte de 5 pacientes con diagnóstico de síndrome de rumiación: 4 de ellos, con presión del esfínter esofágico inferior disminuida, intervenidos mediante funduplicatura de Nissen, con lo cual se reportó alivio sintomático. Se describen eventos adversos como disfagia post-Nissen en 1 de los 5. Cabe destacar que no se reporta el uso de biofeedback previo a la cirugía ni el uso de fármacos, como baclofeno43.
Además, existe un caso reportado en la literatura de una paciente con historia de regurgitación de comida recientemente ingerida que pasó por muchos diagnósticos (patología biliar, gastroparesia, entre otros), que fue intervenida de colecistectomía, con tratamiento médico, piloroplastia, hasta que se alcanzó el diagnóstico de síndrome de rumiación por manometría antroduodenal. En el estudio histológico gástrico, se observaron fibras nerviosas y ganglios (plexo mientérico) normales en número y células de Cajal en adecuada cantidad dentro de la muscular propia. La paciente presentaba desnutrición importante y fue apoyada con nutrición enteral mediante yeyunostomía. A pesar del tratamiento con ejercicios respiratorios, se mantuvo con sintomatología de náuseas y vómitos, por lo que se le realizó una gastrectomía subtotal (80%) con reconstrucción en Y de Roux. La paciente fue seguida hasta 4 meses tras el procedimiento, con disminución de la sintomatología en más de un 70% y mejoría de su estado nutricional y de la calidad de vida44,45.
PronósticoExisten pocos estudios que hayan informado del seguimiento de resultados a largo plazo en pacientes con síndrome de rumiación, pero los limitados datos indican que los síntomas pueden volver a aparecer tras un tratamiento exitoso. En una encuesta de 47 adolescentes que habían completado un programa intensivo de hospitalización al menos un año antes por síntomas de síndrome de rumiación, la resolución ocurrió en el 20%, pero en el 73% de los encuestados la rumiación recurrió46. Este dato es muy importante y hace suponer que debe existir un seguimiento de los pacientes, ya que, como se ha descrito, la rumiación puede ir asociada a baja de peso significativa, con la consiguiente desnutrición.
ConclusiónEl síndrome de rumiación es una entidad clínica reconocida con criterios clínicos, que se incluyen dentro de los criterios de Roma IV, además de exámenes de apoyo diagnóstico bien establecidos. Es importante sospecharlo ante la historia de regurgitación posprandial, en pacientes catalogados con enfermedad por reflujo gastroesofágico refractario a inhibidores de la bomba de protones y en pacientes policonsultantes por «vómitos». Dentro del estudio complementario disponible en nuestro medio, iniciar el estudio de casos sospechosos con pH-impedancia de 24 h con protocolo de rumiación (3 comidas en 24 h y análisis adicional del periodo posprandial) podría tener un impacto favorable en el proceso diagnóstico de pacientes con larga historia de «reflujo gastroesofágico refractario», ya que permitiría seleccionar de mejor manera a quiénes derivar a procedimientos más costosos y menos disponibles, como manometría esofágica de alta resolución, idealmente con impedancia y protocolo de análisis posprandial. El tratamiento se basa en una explicación detallada y en el establecimiento de una sólida relación médico-paciente para promover la adherencia a ejercicios de respiración diafragmática, con biorretroalimentación o sin ella, en centros de derivación, y en el uso de baclofeno como terapia farmacológica de segunda línea.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.