La infección por Clostridium difficile (ICD) continúa siendo la principal causa de diarrea intrahospitalaria, y una de las principales causas de infección nosocomial. En las 2 décadas previas, la carga de infección por Clostridium difficile se ha incrementado en términos de incidencia, morbilidad, mortalidad y costos1. El espectro de manifestaciones de la infección por Clostridium difficile es muy amplio, abarca desde portadores asintomáticos a presentaciones fulminantes con megacolon tóxico2. Las estrategias de tratamiento deben ser basadas en la severidad de la enfermedad, historia previa de la ICD, y el riesgo individual del paciente a la recurrencia.
La vancomicina es el tratamiento de elección para la ICD severa o complicada. El metronidazol es apropiado para la enfermedad leve y la fidaxomicina es una opción terapéutica para pacientes con la ICD recurrente o con alto riesgo de recurrencia. El trasplante de microbiota fecal (TMF) se ha asociado con una resolución de los síntomas de ICD recurrente, pero su rol como tratamiento primario y en ICD severa no está establecido3. Existe un subgrupo de pacientes con ICD que desarrollan presentaciones fulminantes4, refractarias a los tratamientos convencionales. Presentamos el caso de un paciente con infección por VIH y colitis por Clostridium difficile, que fue tratado de forma exitosa con trasplante de microbiota fecal.
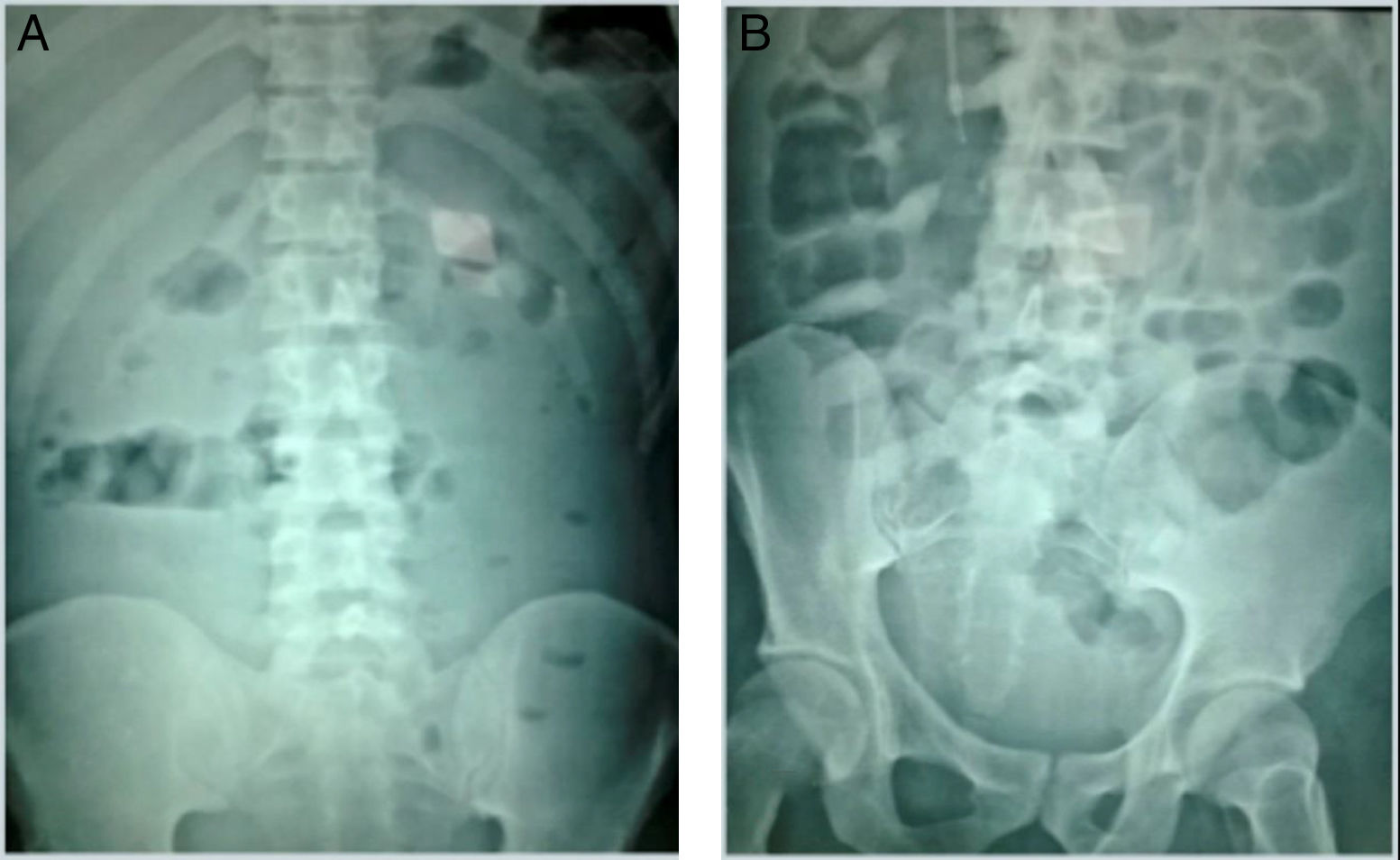
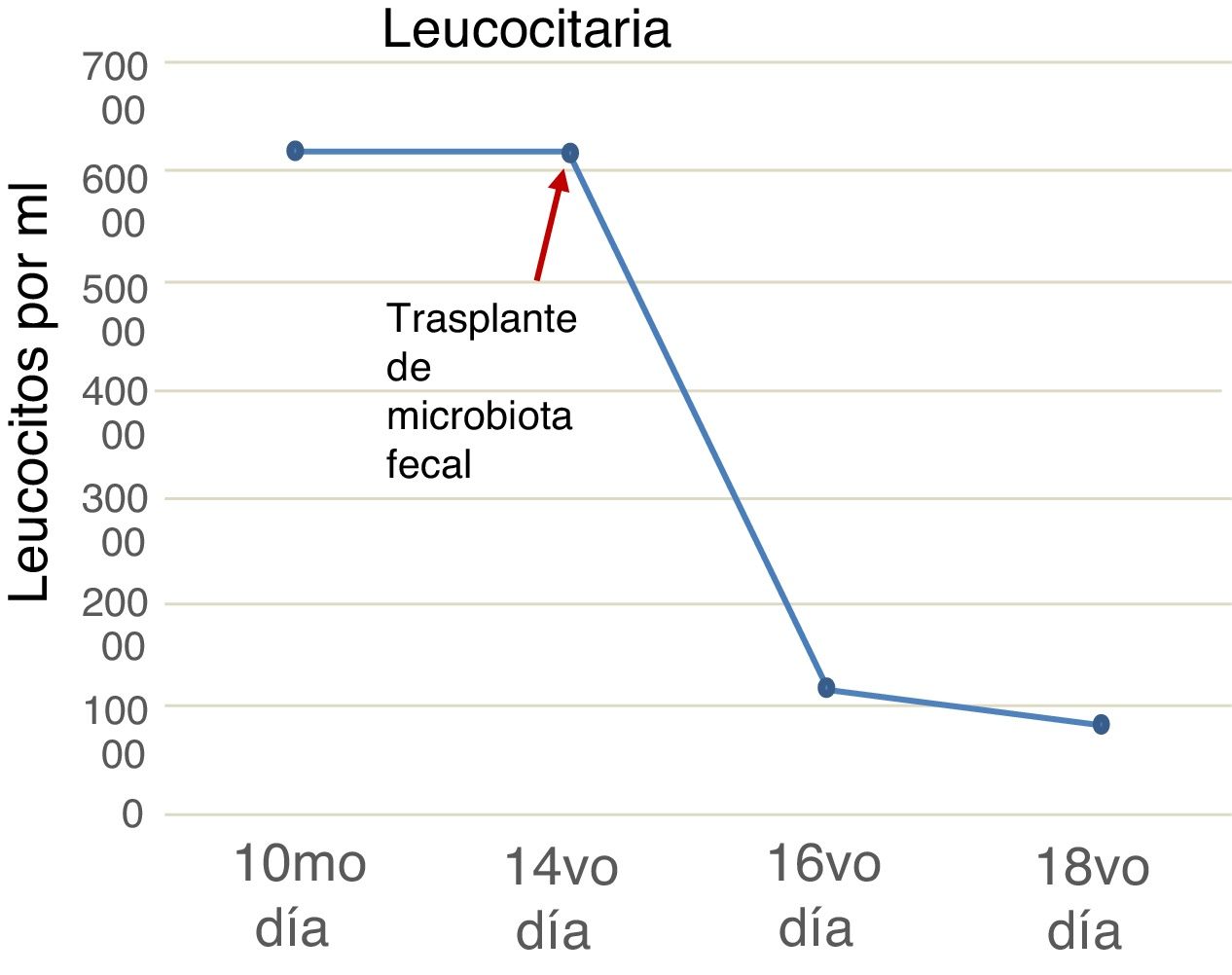
Se trata de un varón de 28 años con diagnóstico de infección por virus de la inmunodeficiencia humana/sida estadio C3 (cuenta de linfocitos TCD4 41 células/μl y carga viral de 127,305 copias/ml), con tratamiento para toxoplasmosis del sistema nervioso central y neumonía intrahospitalaria con pirimetamina, clindamicina, además de piperacilina con tazobactam. Al 10.° día del tratamiento desarrolló diarrea, distensión abdominal e hiperleucocitosis con 61,400 células/μl. Se realizó PCR para toxinas de Clostridium difficile que resultó positiva para la cepa hipervirulenta NAP01 ribotipo 27 (Xpert®C. difficile assay, Cepheid, EE.UU.). Se inició tratamiento con vancomicina 125mg/vo/6h y metronidazol 500mg/IV/8h. Debido a la falta de mejoría a las 48h, incrementamos la dosis de vancomicina a 500mg/vo/6h. Después de 12 días de tratamiento, hubo deterioro clínico manifestado por incremento del dolor abdominal y distensión (fig. 1). Por lo anterior iniciamos protocolo para trasplante de microbiota fecal. La madre sin historia de enfermedades crónicas y con un índice de masa corporal de 24 fue la donadora. Se realizó escrutinio para hepatitis viral A, B, C y VIH, y se realizaron coprocultivo, coproparasitoscópico, así como toxina para Clostridium difficile que resultaron negativos. Se obtuvieron 50g de heces de la donadora y se suspendieron en 100ml de solución salina al 0.9%. La muestra se homogeneizó por medio de un filtro, hasta la obtención de una solución líquida. Dos días previos al procedimiento se suspendieron todos los antibióticos incluyendo metronidazol y vancomicina. El receptor firmó consentimiento informado y posteriormente se infundieron 100ml de la muestra preparada a través de una sonda nasoyeyunal, debido a la ausencia de colonoscopías de urgencia en ese momento. Posterior a las 48h de la infusión, el paciente presentó una mejoría clínica dramática con la resolución del dolor, la distensión abdominal y el descenso de los leucocitos de 62,000 a 12,000 células/μl (fig. 2). El paciente se egresó y tras un año de seguimiento no ha presentado recurrencia de la enfermedad.
En una revisión sistemática que incluyó un total de 536 pacientes prevenientes de 36 estudios clínicos, la eficacia del TMF fue del 87% posterior al primer procedimiento. La resolución de la diarrea varió acorde al sitio de infusión: cuando el TMF fue infundido en el estómago, la eficacia fue del 81%; en el duodeno/yeyuno fue del 86%; en el ciego/colon ascendente fue del 93%: y en el colon distal fue del 84%5. Siguen en aumento el número de casos reportados que apoyan el uso del TMF en las fases agudas de los casos severos6. Sin embargo, existe preocupación respecto al mayor riesgo potencial de sepsis e infecciones posteriores al TMF. Un reciente estudio multicéntrico retrospectivo en 80 pacientes inmunocomprometidos con TMF sugiere que es una modalidad efectiva (78% de tasa de cura con un solo procedimiento), con pocos efectos adversos y sin complicaciones infecciosas relacionadas en estos pacientes de alto riesgo7. Existe además preocupación respecto a las potenciales complicaciones a largo plazo, secundarias al TMF. Se ha reportado un mayor riesgo de desarrollar obesidad, diabetes, cáncer de colon, aterosclerosis, síndrome de intestino irritable, hígado graso, asma y autismo8. Es fundamental el seguimiento clínico de los pacientes que recibieron TMF a través de los años para determinar la fuerza de asociación de los respectivos reportes.
Se han reportado muy pocos casos de pacientes con VIH que han recibido TMF como tratamiento para ICD, y en la mayoría de ellos en el contexto de recurrencia de la enfermedad7,9,10.
El TMF es una opción eficaz, simple y relativamente barata que debe considerarse en casos severos, particularmente en los que el tratamiento antibiótico de amplio espectro no puede ser retirado. Se deben realizar ensayos clínicos para demostrar la eficacia como tratamiento de primera línea en pacientes con enfermedad severa e inmunosupresión.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo/estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.