Clostridium difficile (C. difficile) es un bacilo grampositivo, causa común de diarrea en el medio hospitalario; siendo la incidencia documentada hasta un 10%. Hay distintos medios para su detección sin embargo en nuestro medio, una prueba muy utilizada es el inmunoanálisis de toxinas A y B.
Objetivos1) Estimar el valor predictivo positivo de la prueba de inmunoanálisis para detección de toxinas A y B de C. difficile; 2) establecer la incidencia de diarrea por C. difficile en el hospital, y 3) conocer los factores asociados más comunes.
MétodosEstudio de prueba diagnóstica. Se incluyó a los pacientes con cuadro indicativo de diarrea por C. difficile de enero del 2010 a agosto del 2013, en el Hospital Christus Muguerza Alta Especialidad y con prueba de inmunoanálisis positiva, y que se comprobó por biopsia de colon y cultivo de muestra fecal para determinación de C. difficile.
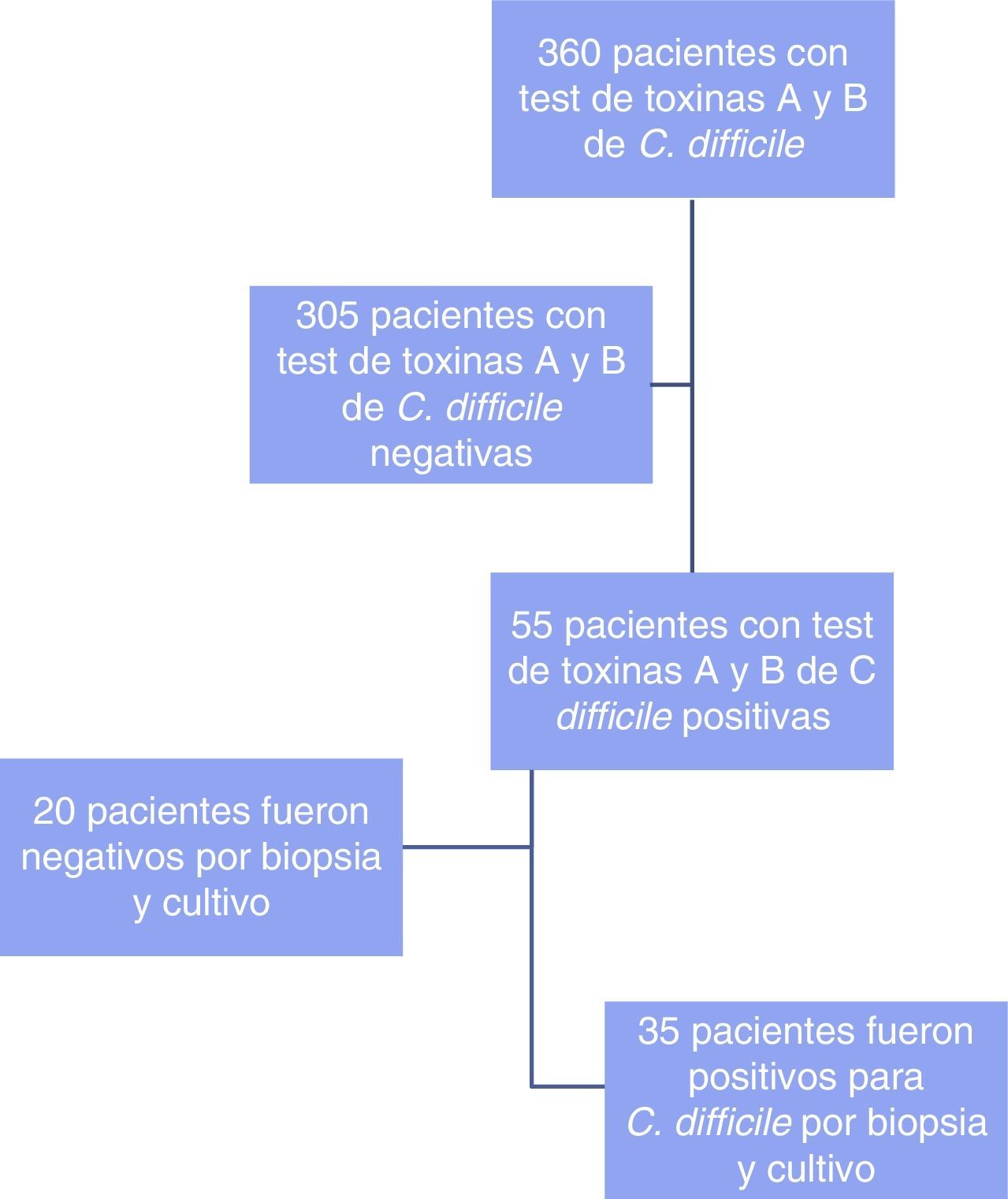
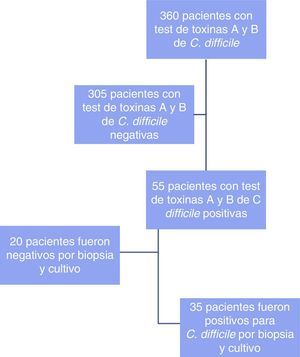
ResultadosSe analizó a 360 pacientes a los que se le solicitaron toxinas A y B, de los cuales 55 casos resultaron positivos; en 35 se demostró la presencia de C. difficile. La incidencia fue del 10.2% y el valor predictivo positivo (VPP) de la prueba de toxinas A y B de C. difficile fue de 0.64 (intervalo de confianza del 95%, 0.51-0.76). Se encontró que el uso de antibioticoterapia previa (n=29) y de inhibidores de bomba de protones (n=19) fue el factor asociado más común.
ConclusionesLa incidencia de C. difficile en nuestro medio es similar a la literatura revisada; sin embargo, el VPP de la prueba de detección de toxinas A y B fue bajo.
Clostridium difficile (C. difficile) is a Gram-positive bacillus that is a common cause of diarrhea in the hospital environment, with a documented incidence of up to 10%. There are different methods to detect it, but a widely used test in our environment is the immunoassay for toxins A and B.
AimsThe aim of our study was to 1) estimate the positive predictive value of the immunoassay for the detection of the C. difficile toxins A and B, 2) to establish the incidence of C. difficile-associated diarrhea in the hospital, and 3) to know the most common associated factors.
MethodsA diagnostic test accuracy study was conducted within the time frame of January 2010 to August 2013 at the Hospital Christus Muguerza® Alta Especialidad on patients with symptoms suggestive of C. difficile-associated diarrhea that had a positive immunoassay test and confirmation of C. difficile through colon biopsy and stool culture.
ResultsThe immunoassay for toxins A and B was performed in 360 patients. Fifty-five of the cases had positive results, 35 of which showed the presence of C. difficile. Incidence was 10.2% and the positive predictive value of the test for C. difficile toxins A and B was 0.64 (95% CI, 0.51-0.76). Previous antibiotic therapy (n=29) and proton pump inhibitor use (n=19) were the most common associated factors.
ConclusionsC. difficile incidence in our environment is similar to that found in the literature reviewed, but the positive predictive value of the test for toxin A and B detection was low.
La diarrea por Clostridium difficile (C. difficile) es la causa infecciosa más común en pacientes hospitalizados y está asociada a una mortalidad sustancial y a un elevado costo financiero1. En Estados Unidos, 1 de cada 100 pacientes hospitalizados desarrolla diarrea por C. difficile, mientras que la incidencia en la comunidad es de 1 por cada 100,0002.
C. difficile es un bacilo grampositivo anaerobio, formador de esporas toxigénicas, causante de una amplia gama de manifestaciones. El resultado de la colonización va desde portador asintomático hasta el desarrollo de una colitis seudomembranosa3.
La inoculación ocurre en el 5-15% de las personas sanas y la transmisión suele ser ocasionada por los mismos trabajadores de la salud al contaminarse con otros pacientes infectados. En Estados Unidos se reporta una incidencia del 1-2% en pacientes hospitalizados4. Entre las principales causas que predisponen a infección se encuentran: el uso de antibióticos, entre los cuales clindamicina, cefalosporinas, amoxicilina y fluoroquinolonas son los más relacionados; la edad mayor a 65 años; hospitalización prolongada, y el uso de inhibidores de la bomba de protones5-8. La mortalidad asociada a diarrea por C. difficile es alta, siendo hasta del 65% en personas ancianas sin tratamiento9,10.
El diagnóstico definitivo se obtiene con la demostración de la presencia de citotoxinas de C. difficile en las muestras de heces. El método de referencia es el test de citotoxicidad de la toxina B en cultivos celulares (gold standard), que es capaz de detectar una pequeña cantidad de toxina (10pg) en las heces, con una sensibilidad (94-100%) y una especificidad (99%) elevadas11. Los principales inconvenientes son la falta de cultivos celulares, no disponibles en todos los laboratorios, precisando un periodo de incubación de 48 -72 h. Por rapidez (2-6 h) y menor costo, el método más utilizado es el inmunoanálisis para la toxina A y B, que tiene una sensibilidad del 71-94% y una especificidad del 92-98%. El test de aglutinación de látex tiene una sensibilidad insuficiente, aproximadamente del 48 al 59%12,13. Otro método utilizado son las pruebas de amplificación de ácidos nucleicos, como la prueba de reacción en cadena de polimerasa (PCR), que tiene una sensibilidad del 100% y una especificidad del 96%; sin embargo, es una técnica compleja, con alto costo y detecta portadores asintomáticos11.
Este estudio tiene el objetivo de determinar el valor predictivo positivo de la prueba de inmunoanálisis de toxinas A y B de C. difficile utilizada en nuestro hospital para detección de los casos, establecer la incidencia de diarrea asociada C. difficile y conocer los factores asociados más comunes.
Material y métodosEs un estudio unicéntrico, observacional, descriptivo, retroelectivo, estudio de prueba diagnóstica. Se valoraron la incidencia de diarrea asociada a C. difficile dentro del hospital y el valor predictivo de la prueba de detección de toxinas A y B de C. difficile por inmunoanálisis comparado con el resultado anatomopatológico y el cultivo. Además, se documentaron los factores de riesgo asociados más comunes en los pacientes. La información se obtuvo de los registros de expedientes del departamento de Bioestadística.
Se incluyeron todos aquellos casos, mayores de 18 años de edad, que hubieran sido ingresados al Hospital Christus Muguerza Alta Especialidad, con cuadro clínico sospechoso de diarrea asociada a C. difficile durante su ingreso o curso intrahospitalario y que se les haya solicitado la prueba de toxinas A y B por inmunoanálisis. De los pacientes que tuvieron la prueba positiva se comprobó, en el expediente clínico, que se hubiera documentado la presencia de C. difficile por toma de biopsias de colon y cultivo por colonoscopia. En el periodo comprendido entre enero del 2010 y agosto del 2013.
Se excluyó a los pacientes menores de 18 años, aquellos que presentaron títulos positivos en la prueba de toxinas A y B de C. difficile en las 8 semanas previas o que la información en el expediente haya sido insuficiente.
Dentro de las especificaciones metodológicas, la prueba que se utiliza en el hospital Christus Muguerza Alta Especialidad es el inmunoanálisis enzimático cualitativo llamado Premier Toxins A&B para la detección de toxina A y B de C. difficile, utilizando como muestra la materia fecal, la cual consta de micropocillos que están recubiertos con anticuerpos monoclonales y policlonales específicos de la toxina, los cuales, si en la muestra se encuentran presentes, forman complejos de anticuerpos con antígeno convirtiendo el sustrato/cromógeno en un coloración y se compara con un control negativo y positivo con color amarillo bien definido. Se refiere que detecta niveles > 1.4ng/ml de toxina A y > 2.4ng/ml de toxina B.
Análisis estadísticoLas variables cuantitativas se expresan como media ± desviaciones estándar y las variables categóricas se expresan como recuento (porcentaje). Se calculó la incidencia de diarrea asociada a C. difficile; el valor predictivo positivo de la prueba con una tabla de 2×2 con sus intervalos de confianza (IC) del 95%, calculado por la fórmula de Wald. Se utilizó hoja de Excel de base de datos y el Software Medcalc para la recopilación de los resultados.
ResultadosSe analizó a 360 pacientes (fig. 1) a los que se les solicitaron la prueba de toxinas A y B de C. difficile por inmunoanálisis, de los cuales 55 casos resultaron positivas; se evaluaron las siguientes variables: edad, sexo, factores de riesgo asociados, días de estancia intrahospitalaria, estancia en unidad de cuidados intensivos (UCI), resultado anatomopatológico y tratamiento.
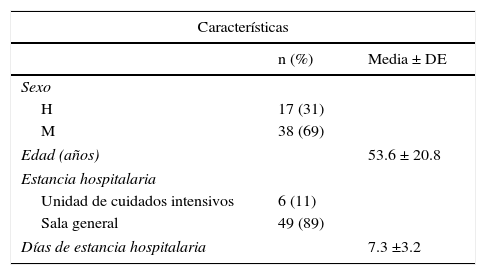
En lo que respecta a la edad, se encontró una media de 53.6±20.8 años (tabla 1), siendo el grupo de edad más frecuente el de 50 a 65 años. Al analizar el sexo de los pacientes, se encontró un total de 38 mujeres (69%) y 17 hombres (31%).
Características epidemiológicas de la población
| Características | ||
|---|---|---|
| n (%) | Media ± DE | |
| Sexo | ||
| H | 17 (31) | |
| M | 38 (69) | |
| Edad (años) | 53.6 ± 20.8 | |
| Estancia hospitalaria | ||
| Unidad de cuidados intensivos | 6 (11) | |
| Sala general | 49 (89) | |
| Días de estancia hospitalaria | 7.3 ±3.2 | |
DE: desviación estándar; H: hombres; M: mujeres; n: número de población.
Del total de la muestra, 6 pacientes (11%) estuvieron en la UCI, 49 pacientes en las salas generales (89%). De los pacientes que se encontraban en la UCI, uno de ellos falleció en ese internamiento.
Ahora bien, de aquellos pacientes con diagnóstico de diarrea por C. difficile se obtuvo una media de días de estancia intrahospitalaria de 7.3±3.2.
Se les realizó colonoscopia a los 55 pacientes, reportándose datos indicativos que se correlacionaron con C. difficile por biopsia y cultivo en 35 pacientes (64%), mientras que en 20 pacientes (36%) no se encontraron estos hallazgos.
De los 20 pacientes que resultaron negativos, en 10 solo se documentó inflamación aguda y crónica inespecífica, en 3 se encontró enfermedad de Crohn, en 3 se documentó CUCI, en 3 resultaron normales los estudios histopatológicos y en un paciente se encontró colitis infecciosa por Cryptosporidium.
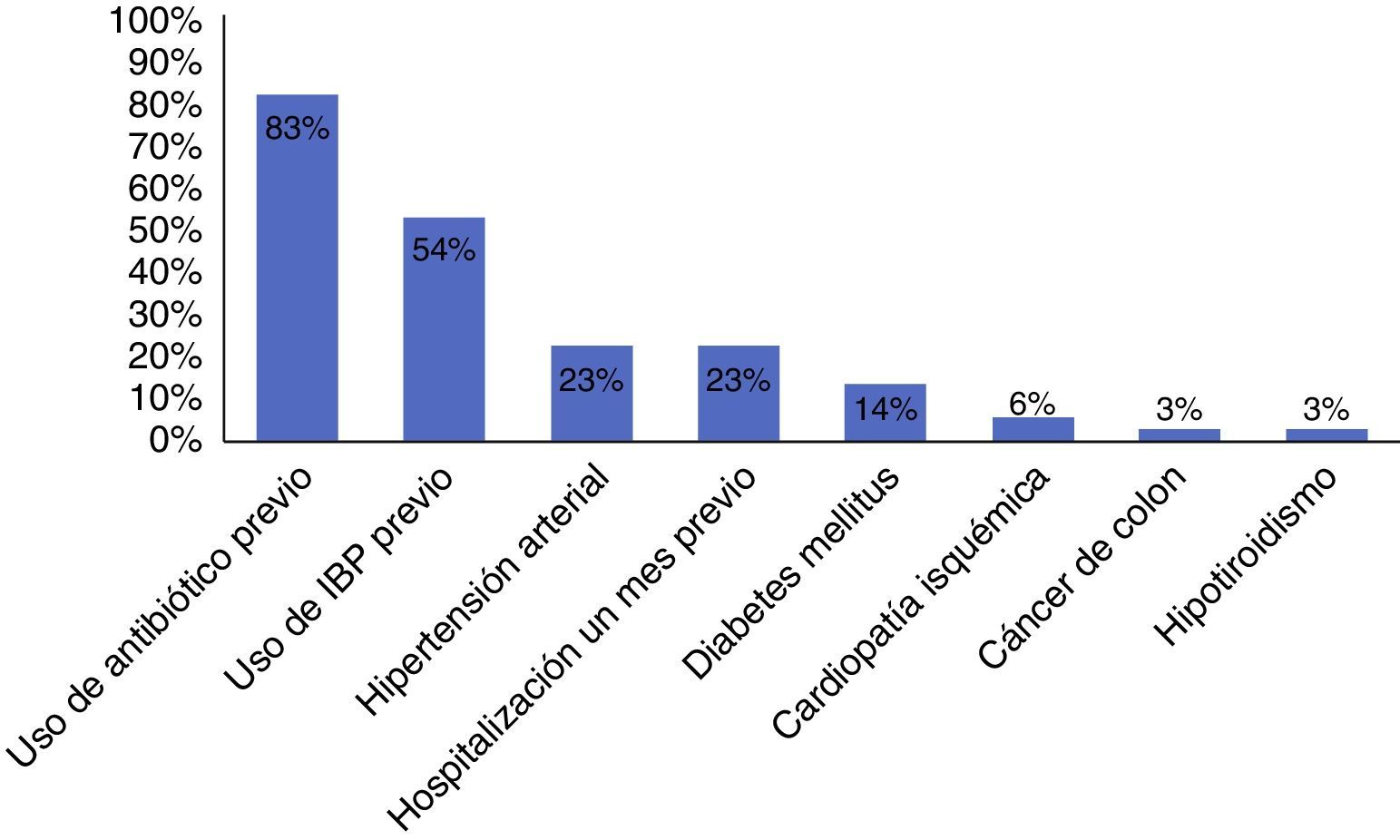
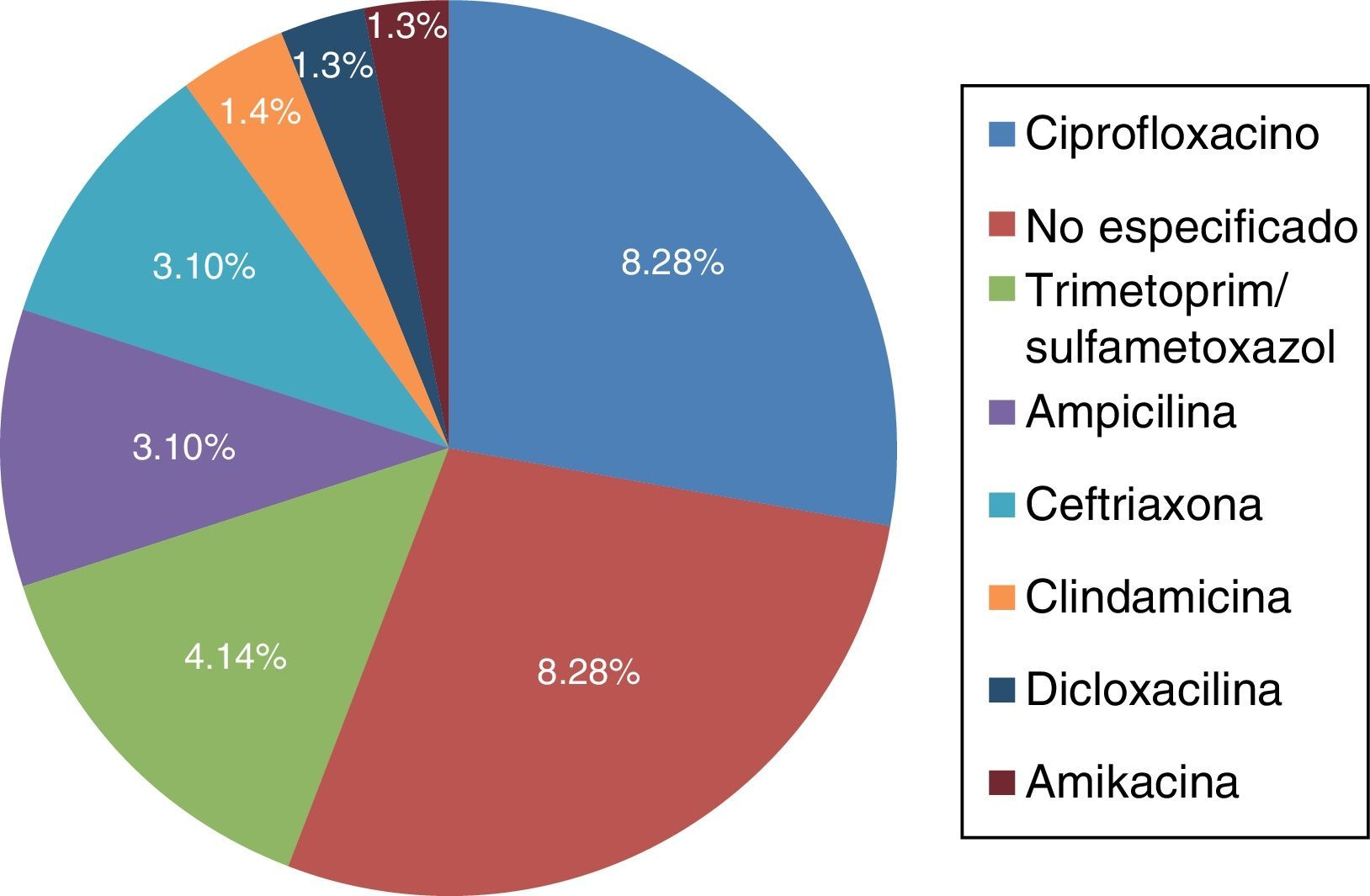
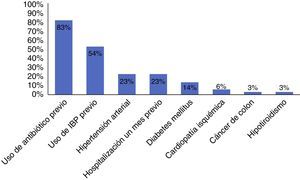
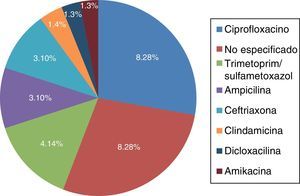
Los factores de riesgo asociados a infección por C. difficile (fig. 2) fueron el uso de inhibidores de bomba de protones y el antecedente de haber tomado antibiótico, dentro de los cuales (fig. 3) el ciprofloxacino fue el más relacionado.
Respecto al tratamiento de los 55 pacientes que resultaron con prueba positiva de toxinas A y B de C. difficile, 28 pacientes (51%) fueron tratados con metronidazol, 13 (24%) fueron tratados con vancomicina, y 14 (25%) necesitaron terapia combinada con metronidazol y vancomicina.
La incidencia de diarrea por C. difficile que se detecta en el Hospital Christus Muguerza Alta especialidad por inmunoanálisis de toxina A y B es del 10.2% en un periodo de 3 años, el valor predictivo positivo de la prueba inmunoenzimática de toxina A y B utilizada en relación con el diagnóstico anatomopatológico es de 0.64 (IC del 95%, 0.51-0.76).
DiscusiónDefinitivamente, la infección por C. difficile es un agente etiológico común de las diarreas intrahospitalarias en nuestro medio, siendo la incidencia similar a la reportada en la literatura1.
Por muchos años, la detección de toxinas A y B en heces por medio de citotoxicidad celular fue considerado el gold standard para el diagnóstico de infección por C. difficile. Recientemente, estudios han demostrado que el cultivo de toxinas tiene mayor potencial diagnóstico, por lo cual debe ser usado como el nuevo gold standard. Sin embargo, ambas pruebas son tardadas, laboriosas y requieren de personal entrenado. Esto nos lleva a que los ensayos inmunoenzimáticos de las toxinas son los más ampliamente utilizados para el diagnóstico de infección por C. difficile14.
Novak et al.15 compararon las diferentes pruebas utilizadas para el diagnóstico de C. difficile, encontrando un valor predictivo positivo para la prueba de toxinas A y B de 0.68, valor similar al encontrado en nuestro estudio (0.64). En otros estudios, como los realizados por Eastwood et al.16 y Planche et al.17, donde se analizaron la sensibilidad y la especificidad de las pruebas de detección de toxinas A y B de C. difficile en muestras fecales, se reportaron valores del 83 y el 95%, respectivamente, un valor predictivo positivo del 70% y un valor predictivo negativo del 96%.
Otras opciones potenciales para el diagnóstico que se han descrito en la literatura son la detección de glutamato deshidrogenasa, la PCR y la prueba de amplificación de ácidos nucleicos (NAAT)14.
La detección de glutamato deshidrogenasa puede ser utilizada como un estudio de tamizaje, debido a que presenta una sensibilidad cercana al 100%; sin embargo, tiene la desventaja de tener una especificidad baja18. La PCR y la NAAT tienen una gran sensibilidad y especificidad, cercanas al 90%, por lo que en algunos centros se ha tomado como método diagnóstico de elección; sin embargo, ambas tienen la desventaja de ser costosas, además de que no detectan la producción de toxinas, por lo que no pueden discriminar de pacientes portadores asintomáticos19,20.
Actualmente, las guías europeas y americanas han recomendado un algoritmo de 2 pasos para el diagnóstico por laboratorio de infección de C. difficile, el cual consiste en el uso de una prueba altamente sensible, como la detección de glutamato deshidrogenasa; seguida de una prueba con alta especificidad como la detección de toxinas A y B por inmunoanálisis18. Incluso hay quien propone un tercer paso para aquellos pacientes que resultan con toxinas negativas, pero de los que se tiene un fuerte cuadro clínico sospechoso, solicitando el cultivo de toxinas para estos pacientes21.
Dentro de los factores de riesgo asociados, el uso previo de antibióticos y el de inhibidores de bomba de protones fueron los principales documentados, como lo mencionan Camacho et al. en su estudio7. Dentro de los antibióticos, se analizó que el uso de quinolonas fue el principal antimicrobiano relacionado con infección, acorde con la literatura revisada5,10.
En cuanto al manejo terapéutico, se encontró que el uso de metronidazol fue la principal medida terapéutica, siendo además tratados con vancomicina o con la combinación de ambos. Estas medidas son las mismas que las reportadas en la literatura4,5. Debido a la emergencia de cepas hipervirulentas, la severidad, la esporulación y las resistencias antimicrobianas han aumentado, siendo las opciones terapéuticas limitadas para infección por C. difficile recurrente o refractaria al tratamiento. Se han utilizado rifaximina, fidaxomicina, nitazoxanida y tigeciclina como alternativa en estos casos; sin olvidar el trasplante de microbiota fecal como otra medida terapéutica para recurrencias22.
ConclusionesLa incidencia de C. difficile en nuestro medio es similar a la literatura revisada; sin embargo, el valor predictivo positivo de la prueba fue bajo. Los factores de riesgo más asociados fueron el uso de inhibidores de bomba de protones y el antecedente de antibioticoterapia previa.
En nuestro medio, debido al bajo costo y la rapidez, disponibilidad y facilidad de realizar la determinación de toxinas A y B de C. difficile; debe seguir siendo una prueba diagnóstica importante para la detección oportuna de infección asociada a C. difficile, sobre todo en aquellos centros donde no se cuenta con otros métodos para confirmar el cuadro clínico compatible con esta entidad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónNo se recibió patrocinio alguno para realizar este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.