La realización de una gastroenteroanastomosis (GEA) utilizando ultrasonido endoscópico (USE) y prótesis metálicas de aposición luminal (PMAL) es segura y efectiva para el tratamiento de obstrucción al tracto de salida gástrico de origen maligno, pero no en enfermedad benigna debido al impredecible cierre posterior al retiro de la PMAL, justificando la investigación en estos pacientes. Nuestro objetivo fue evaluar distintas técnicas endoscópicas para crear una GEA permanente en modelos porcinos.
Material y métodosSe trató de un estudio de investigación animal realizado en modelos porcinos en el bioterio de un hospital de tercer nivel de atención en México entre septiembre y noviembre de 2023. Se realizaron 5 técnicas: técnica directa (TD), cortes radiales (CR), cortes lineales (CL), escleroterapia con alcohol absoluto (EAA) y ablación con argón plasma (AAP). Se evaluó la eficacia técnica, la seguridad y la persistencia de la anastomosis a 4 semanas de la intervención y retiro de la PMAL.
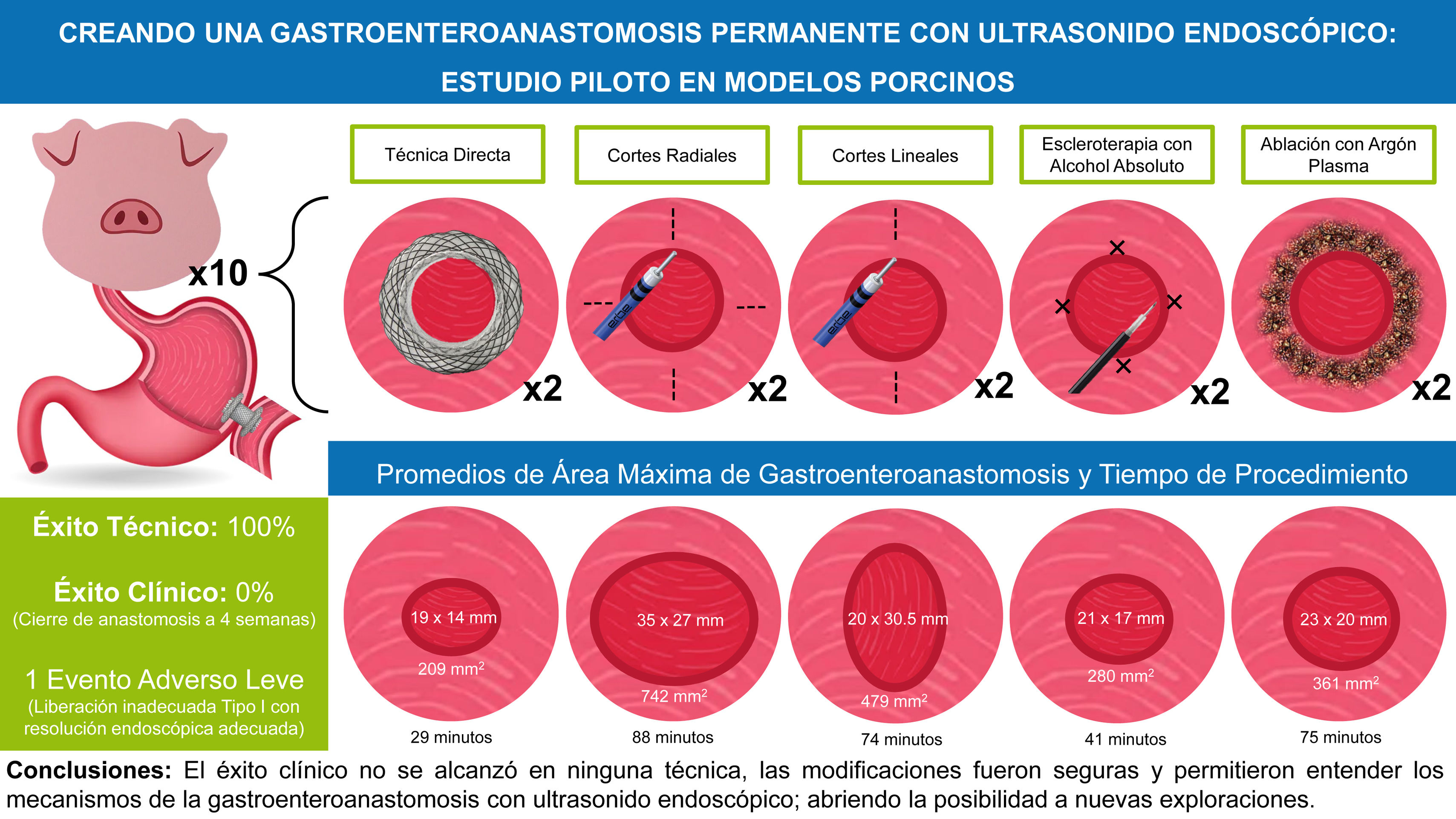
ResultadosSe incluyeron 10 modelos porcinos, 2 por grupo. El éxito técnico y clínico del 100 y 0%. Los tiempos de los procedimientos fueron: TD=29min; CR=88min; CL=74min; EAA=41min y AAP=75min; y la técnica CR presentó la mayor área de anastomosis (742mm2). Hubo un evento adverso (10%) el cual fue leve y no requirió intervención adicional.
ConclusionesAunque el éxito clínico no se alcanzó con ninguna técnica, las modificaciones fueron seguras y permitieron entender los mecanismos de creación de la GEA, abriendo la posibilidad para nuevas exploraciones.
The performance of gastroenteric anastomosis (GEA) utilizing endoscopic ultrasound (EUS) and lumen-apposing metal stents (LAMSs) is safe and effective for treating malignant gastric outlet obstruction, but not in benign disease, due to unpredictable GEA closure after LAMS removal. Our aim was to evaluate different endoscopic techniques for creating a durable GEA in porcine models.
Material and methodsAn animal study in porcine models was conducted at the vivarium of a tertiary care hospital in Mexico City, between September and November 2023. Five techniques were carried out: direct technique (DT), radial cut (RC) technique, linear cut (LC) technique, absolute ethanol sclerotherapy (AES), and argon plasma coagulation (APC). Technical efficacy, safety, and lasting patency of the anastomosis at 4 weeks after the intervention and LAMS removal were evaluated.
ResultsTen porcine models, 2 per group, were included. Technical success was 100% and clinical success 0%. Procedure times were 29min for the DT, 88min for the RC technique, 74min for the LC technique, 41min for AES, and 75min for APC. The RC technique had the largest anastomosis area (742mm2). There was one adverse event (10%); it was mild and did not require any additional intervention.
ConclusionsAlthough clinical success was not achieved with any of the techniques, the technical modifications were safe, providing a better understanding of the mechanisms involved in GEA and paving the way for new explorations.
Las gastroenteroanastomosis (GEA) guiadas por ultrasonido endoscópico (USE) con el uso de prótesis metálicas de aposición luminal (PMAL), han demostrado ser una técnica eficaz para el tratamiento de condiciones como la obstrucción al tracto de salida gástrica (OTSG) de origen maligno o en la creación de accesos para procedimientos intervencionistas como la colangiopancreatografía retrógrada endoscópica en los pacientes con anatomía modificada, con un éxito técnico del 93.5% (IC 95%: 89.7-96%) y eficacia clínica del 90.1% (IC 95%: 85.5-93.4%)1. Los eventos adversos son del 11.7% (IC 95%: 8.2-16.6%), la mayoría leves o moderados1.
Pérez Miranda et al. compararon la técnica de GEA con PMAL vs. la técnica laparoscópica para los pacientes con OTSM, no encontrando diferencias en éxito técnico (88 vs. 100%; p=0.11); clínico (84 vs. 90%; p=0.11); pero con eventos adversos y costo mayores para el grupo laparoscópico (12 vs. 41%; p=0.038 y $4515 vs. $14778; p<0.00001, respectivamente)2. Khashab et al. reportaron un éxito técnico mayor en el grupo quirúrgico (87 vs. 100%; p=0.009), eficacia clínica similar (87 vs. 90%; p=0.18) y similares eventos adversos (16 vs. 25%; p=0.3)3.
Son pocos los trabajos que incluyen la evaluación de PMAL para la creación de GEA en enfermedad benigna, incluyendo algunos reportes de casos y sin evaluaciones formales a largo plazo para enfermedades benignas, donde las causas incluyen: estenosis asociadas a úlceras pépticas, vólvulos gástricos, estenosis pilóricas refractarias, enfermedad de Crohn, estenosis posquirúrgicas y gastroparesia refractaria4–6. Además, la persistencia de la anastomosis una vez retirada la PMAL es impredecible. En este sentido, Krafft et al. evaluaron el cierre espontáneo o por segunda intención de las anastomosis creadas por PMAL de 20mm posterior a su retiro en los pacientes con bypass gástrico. Se observó que el 41% de las anastomosis persistieron durante el tiempo, de las cuales el 56% de los pacientes presentaron reganancia de peso significativa. Se observó una diferencia en la mediana de días de permanencia de la PMAL entre el grupo donde se mantuvo la persistencia y aquellos con cierre por segunda intención de la GEA posterior al retiro de la PMAL (77 días; RIQ: 42-124 vs. 35 días; RIQ: 26-45 días)7.
Durante la creación de una GEA quirúrgicamente, en la fase inicial existen varios factores proinflamatorios que incluyen: colagenasas y metaloproteinasas que debilitan la adhesión generando que su estabilidad sea directamente relacionada al mecanismo quirúrgico utilizado, previo a la formación de nuevo colágeno por fibroblastos y células de músculo liso de la muscular de la mucosa y muscular propia; de tal forma que existe una resistencia de la anastomosis a la presión intraluminal de solo el 50% en los primeros 2-3 días y del 100% a los 7 días posteriores a la GEA. La formación y permanencia de la GEA depende de factores locales (perfusión tisular, tensión anastomótica, adecuada aposición de bordes, ausencia de infección local, etc.) y sistémicos (desnutrición, hipovolemia, medicamentos, sepsis, inmunodeficiencias o diabetes mellitus)8. Sin embargo, el mecanismo de formación de la GEA guiada por USE es diferente, ya que aquí al utilizar una PMAL específicamente en el caso de la Hot Axios® (Boston Scientific, Marlborough, Massachusetts), se realiza una punción asistida por coagulación monopolar directa para traspasar ambas paredes a unir con una sonda de calibre 10.8Fr y posteriormente al liberar la prótesis, se expanden ambas paredes hasta alcanzar el diámetro designado, no generando ningún corte de espesor total como en la sutura mecánica o con engrapadoras quirúrgicas utilizados en cirugía convencional, donde se obtienen anastomosis circulares de 21 hasta 33mm o lineales de entre 30 y 60mm, reestructurando las paredes gástrica y enteral, favoreciendo una tensión baja entre los tejidos perianastomóticos9.
Es por ello que la creación de una GEA guiada por USE con uso de PMAL para los pacientes con enfermedad benigna dependería de la permanencia de la GEA una vez retirada la PMAL, por lo cual se hace necesario el estudio de modificaciones de la técnica original para este fin y es por ello que nuestro objetivo fue realizar un proyecto piloto, exploratorio con el objetivo de evaluar 4 modificaciones de la técnica original y un grupo control, en modelos biológicos de tipo porcino vivos, con el objetivo de buscar una GEA permanente.
Material y métodosSe trató de un ensayo clínico utilizando un modelo piloto experimental exploratorio, prospectivo, comparativo y longitudinal realizado en modelos animales porcinos in vivo, de acuerdo con las guías CONSORT para ensayos clínicos. Este estudio fue desarrollado en el bioterio de un hospital de tercer nivel de atención hospitalaria entre septiembre y noviembre del año 2023. Los procedimientos fueron realizados bajo los estatutos y las normas designadas por el instituto para el adecuado manejo de estos modelos animales.
Criterios de inclusiónSe incluyeron 10 modelos porcinos hembras, de la raza Landrace, con una edad de entre 6 y 10 semanas de edad y un peso entre 24 y 45kg. Todos los modelos incluidos fueron certificados como sanos por un médico veterinario de la comisión sanitaria mexicana.
Criterios de exclusiónSe excluyeron aquellos modelos que no pudieran completar la preparación correcta para la realización de la GEA, que presentaran complicaciones durante la inducción anestésica o no atribuibles al procedimiento, y aquellos que no pudieran completar el tiempo de seguimiento. En este caso, serían reemplazados por otros modelos, para no comprometer el tamaño de muestra contemplado.
Equipo utilizadoLos equipos utilizados fueron los siguientes: Ecoendoscopio lineal modelo EG-580UT (Fujifilm, Tokyo, Japón) multifrecuencia de 5/7.5/10/12MHz, con canal de trabajo de 3.8mm; un gastroscopio convencional modelo EG-530FP (Fujifilm, Tokyo, Japón), acoplado a un videoprocesador y fuente de luz modelo Eluxeo® 7000 (Fujifilm, Tokyo, Japón) y un procesador de USE SU-1 (Fujifilm, Tokyo, Japón). Se utilizó una unidad electroquirúrgica ERBE VIO® 300D (ERBE, Tübingen, Alemania) con el modo highcut monopolar con una potencia de corte de 120W en efecto 1. Los materiales para la creación de la GEA fueron: PMAL tipo Hot AxiosTM de 20mm de diámetro (Boston Scientific, Marlborough, Massachusetts), la cual es una prótesis tubular y con forma de «yoyo», hecha de nitinol y totalmente recubierta de silicon; cuchillo HybridKnife® tipo I (ERBE, Tübingen, Alemania); hemoclips tipo ResolutionTM (Boston Scientific, Marlborough, Massachusetts); aguja de inyección tipo InterjectTM de 23G o 25G (Boston Scientific, Marlborough, Massachusetts); un balón de expansión radial tipo CRETM 18-20mm (Boston Scientific, Marlborough, Massachusetts); una pinza tipo coagrasper (Olympus, Tokyo, Japón) en caso de hemorragia en modalidad soft a 20-30W efecto 2 y una unidad de argon plasma APC® 2 acoplada a una sonda tipo FiAPC® Axial (ERBE, Tübingen, Alemania) en modalidad forced APC a 50W.
Modelos in vivoLos 10 modelos porcinos vivos los cuales fueron adquiridos con un proveedor certificado (SCR), y previo a su inclusión en el estudio, el personal de veterinaria del hospital realizó una evaluación clínica de los modelos porcinos, de acuerdo a las normas previamente mencionadas, para asegurar el cumplimiento de los estándares de salud establecidos para la realización de este tipo de protocolos en el bioterio. Los modelos porcinos fueron tratados procurando el cuidado de los mismos, la seguridad de los investigadores y evitando el estrés del animal en todo momento. El manejo previo, transprocedimiento y posterior a la intervención; se realizó de acuerdo con la NOM-062-ZOO-1999.
Previo a la anestesia, todos los animales se sometieron a un periodo de ayuno de 24h, suficiente para vaciar el estómago, con el fin de prevenir la regurgitación o aspiración del contenido gástrico. Se inició premedicación con ketamina a 15mg/kg por vía intramuscular, para posteriormente ser limpiados con uso de jabón antiséptico y finalmente pasar a quirófano. Se realizó una canalización por vía auricular y se administró midazolam (5mg/kg en bolo y posteriormente 2mg cada 10 a 15min en dosis/respuesta para mantenimiento). Se realizó la intubación orotraqueal con cánulas de 5.5 a 6.5mm, y la anestesia transprocedimiento fue otorgada por médico veterinario en todo momento. Al finalizar el procedimiento, el modelo fue trasladado a un área especial que tiene una superficie de concreto de 28 m2, adecuadamente equipada para la correcta vigilancia postoperatoria. Los porcinos fueron mantenidos en ayuno y vigilancia posterior al procedimiento durante 4h, previo a su traslado final a un área de descanso y vigilancia posterior donde permanecieron durante todo el protocolo previo a su siguiente intervención.
A las 24h se inició una dieta convencional para este tipo de modelos la cual consistió en una mezcla del 16% de proteína cruda, del 6% de fibra cruda, del 3.5% de lípidos y el resto de hidratos de carbono por cada ración, con consumo de agua a libre demanda. En todos los casos se utilizaron analgésicos autorizados por el Servicio Nacional de Sanidad, Inocuidad y Calidad Agroalimentaria, ofreciendo cobertura analgésica por 3 días, la cual se extendió solo en caso de que el médico veterinario así lo determinara. Se programó una revisión clínica diaria durante toda su evolución y en caso de sospecha de algún evento adverso, el modelo se sometió directamente a una revisión endoscópica o quirúrgica, ya que no contamos con disponibilidad de estudios bioquímicos o de imagen. En caso de compromiso de la integridad del animal o presencia de secuelas incapacitantes se procedió a realizar eutanasia por parte del médico veterinario utilizando pentobarbital sódico a dosis de 200mg/kg por vía IV, conforme con la NOM-062-ZOO-1999.
Una vez finalizado el protocolo, se procedió a realizar la eutanasia correspondiente para valorar las características de las anastomosis creadas, la disposición, calibre y eventos adversos perianastomoticos. Los desechos, cadáveres y material orgánico se depositaron de acuerdo con la NOM-087-ECOL-SSA1-2002 así como a la Ley General del Equilibrio Ecológico.
ProcedimientosLa técnica convencional para realización de GEA se consideró como el grupo control y se analizaron 4 técnicas nuevas. Los procedimientos fueron fotodocumentados y grabados. Se evaluaron el éxito técnico, clínico y los eventos adversos. La evaluación final se realizó posterior a la eutanasia 1mes posterior a las técnicas evaluadas.
A. Técnica 1 «Gastroentero anastomosis convencional por técnica directa»Los modelos incluidos fueron el 1 (A) y el 2 (B).
Fundamento: Es una técnica comprobada, con una efectividad y eventos adversos aceptable para la paliación de la vía enteral1. La principal desventaja es que la permanencia de la anastomosis y el calibre son impredecibles4.
- •
A.1. Hot Axios® con técnica directa (TD) (día 1): Posterior al lavado y preparación del modelo animal, este se trasladó a sala. Se realizó la inducción anestésica y se administró profilaxis antibiótica con enrofloxacina al 10% (100mg/1ml) a dosis de 2.5mg/kg. Se realizó una ecoexploración gástrica y posteriormente se instiló agua inyectable a nivel pospilórico para la adecuada distensión de las asas. Se revisó el sitio y se realizó una punción directa con prótesis de 20mm de diámetro tipo Hot Axios™ con corriente monopolar de tipo AutoCut a 120W. Se liberó la prótesis, se confirmó su adecuada colocación y se realizó dilatación con balón de expansión radial tipo CRE a 18mm. El modelo porcino se egresó y pasó a vigilancia con esquema analgésico utilizando meglumina de flunixin 50mg/1ml a dosis de 2.2mg/kg por 3 días, se programó un ayuno total de 24h y posteriormente iniciarse la vía oral con la dieta previamente mencionada.
- •
A.2. Retiro de PMAL (30 días): Posterior al protocolo de ingreso a sala se realizó la revisión de la GEA por vía endoscópica para el posterior retiro de la PMAL con pinza de cuerpo extraño. Se evaluó la GEA anastomosis y se egresó manteniendo ayuno y observación de 4h, previo al inicio de la dieta.
- •
A.3. Revisión final (60 días): Posterior al protocolo de ingreso a sala se revisó el sitio de la GEA y se sacrificó al animal para realizar celiotomía e inspección de cavidad peritoneal y finalmente la extracción de la pieza gastroentérica involucrada, con la eutanasia correspondiente. El manejo de los restos biológico se realizó de acuerdo a la NOM-087-ECOL-SSA1-2002.
Los modelos incluidos fueron el 3 («C») y el 7 («G»).
Fundamento: En esta técnica modificada en la cual se realizaron cortes radiales (CR) de 1cm en disposición radial con el objetivo de crear un corte de espesor total de las capas gástrica y enteral, permitiendo una potencial remodelación perianastomótica de mejor calidad7,8.
- •
B.1. Hot Axios® (día 1): Al igual que en el modelo control se realizó la colocación de la GEA y se egresó el modelo a vigilancia.
- •
B.2. Realización de CR (15 días): Se decidió la realización de la maniobra a 15 días de colocación debido a que es el tiempo esperado para la formación de la GEA. Posterior el protocolo de ingreso a sala se realizó el retiro de la PMAL y se revisó el área de la GEA. Se identificaron los 4 puntos de circunferencia anastomótica a nivel gástrico y se procedió a realizar CR de 10mm de longitud sobre las paredes gástrica y enteral con el cuchillo tipo HybridKnife® tipo I con los parámetros: EndoCut I, efecto 1, duración de corte 3 e intervalo de corte 3. Se colocaron hemoclips tipo ResolutionTM con apertura de 11mm, en disposición paralela en el borde seleccionado, repitiendo el proceso en los 4 bordes de forma radial. Se colocó nuevamente la PMAL por vía endoscópica como protección de algún tipo de potencial perforación posterior, corroborando el adecuado posicionamiento y hemostasia, se revirtió la anestesia y se realizó el protocolo de egreso correspondiente.
- •
B.3. Retiro de PMAL (30 días): Posterior al protocolo de recepción. Se realizó el retiro de PMAL y se realizó una revisión de la nueva GEA, evaluando los diámetros alcanzados. Finalmente, se realizó el protocolo de egreso correspondiente.
- •
B.4. Revisión final (60 días): Se realizó al igual que en la TD el protocolo para celiotomía, exploración de cavidad peritoneal y extracción de la pieza gastroentérica involucrada con la eutanasia correspondiente.
Los modelos incluidos fueron el 4 («D») y modelo porcino 9 («I»).
Fundamento: Al igual que en CR el objetivo fue realizar 2 cortes lineales (CL) de espesor total con el objetivo de aumentar el diámetro de la anastomosis y mejorar la remodelación anastomótica7,8.
- •
C.1. Hot Axios® (día 1): Se realizó la colocación de la PMAL de forma convencional por TD y se egresó el modelo a vigilancia.
- •
C.2. Realización de CL (15 días): Posterior al protocolo de recepción, se retiró la PMAL y se evaluó la GEA para posteriormente realizar 2 CL transmurales con el cuchillo HybridKnife® tipo I y parámetros: EndoCut I efecto 1, duración de corte 3, intervalo de corte 3, al igual que en CR se colocaron un par de clips en disposición paralela en el borde seleccionado. Se colocó nuevamente la PMAL de protección y se realizó el protocolo de egreso.
- •
C.3. Retiro de PMAL (30 días): Se realizó el retiro de la PMAL, la revisión de la GEA con sus mediciones correspondientes y el protocolo de egreso.
- •
C.4. Revisión final (60 días): Se realizó el protocolo de celiotomía, exploración de cavidad peritoneal y extracción de la pieza gastroentérica involucrada con la eutanasia correspondiente.
Los modelos incluidos fueron el 8 («H») y el 10 («J»).
Fundamento: El objetivo en esta técnica fue la inyección de alcohol absoluto en el tejido adyacente a la circunferencia de la prótesis, el alcohol genera inflamación, destrucción tisular, fibrosis irreversible con disminución de la masa tisular por retracción9,10. El objetivo fue controlar la fibrosis alrededor de la PMAL la cual fungió como tutor manteniendo la aposición de los lúmenes mientras se reestructuró el tejido circundante.
- •
D.1. Hot Axios® y aplicación de EAA (día 1): Posterior a la colocación de la PMAL con TD, se identificaron 4 puntos de forma circunferencial a la prótesis y se procedió a la inyección de 1.5-2ml de etanol al 98% con aguja InterjectTM de 23G. Finalmente, se realizó dilatación del cuerpo de la prótesis hasta 18mm, se corroboró el adecuado posicionamiento y hemostasia previo al egreso.
- •
D.2. Retiro de PMAL (30 días): Se realizó el retiro de la PMAL y finalmente se evaluó la GEA con las mediciones correspondientes. Se egresó el modelo a vigilancia.
- •
D.3. Evaluación final (60 días): Se realizó el protocolo de celiotomía, exploración de cavidad peritoneal y extracción de la pieza gastroentérica involucrada con la eutanasia correspondiente.
Los modelos incluidos fueron el 5 («E») y modelo porcino 6 («F»).
Fundamento: En esta técnica el objetivo fue generar daño tisular y fibrosis de la GEA, con motivo de generar una remodelación controlada11.
- •
E.1. Hot Axios® (día 1): Posterior al protocolo de ingreso, se realizó la colocación de la PMAL con TD.
- •
E.2. Aplicación de argón plasma (15 días): Se realizó el retiro de la PMAL y se aplicó argón plasma con la unidad APC® 2 y sonda FiAPC® Axial en modo forzado a 50W y 1l/min, en la circunferencia de la GEA, con el objetivo de obtener un tono dorado del tejido circundante y con una extensión de hasta 5mm. Se colocó la PMAL nuevamente y se realizó el protocolo de egreso.
- •
E.3. Retiro de PMAL (30 días): Se realizó el retiro de la PMAL con la posterior revisión de la GEA y mediciones correspondientes, previo a su egreso.
- •
E.4. Revisión final (60 días): Se realizó el protocolo de celiotomía, exploración de cavidad peritoneal y extracción de la pieza gastroentérica involucrada con la eutanasia correspondiente.
El objetivo primario fue evaluar la potencial creación de una GEA permanente por medio de la utilización de 4 técnicas experimentales y un grupo control. El éxito clínico se definió como la persistencia de la anastomosis en la evaluación final del modelo (60 días). Secundariamente se evaluó la seguridad y éxito técnico de cada una de las técnicas empleadas.
Análisis estadísticoEl tamaño de muestra para nuestro estudio se realizó a conveniencia, basado en la probabilidad de permanencia de una GEA con alguna de las 4 maniobras evaluadas (25%), esto basado en estudios de permanencia previa de GEA en enfermedad benigna a corto y mediano plazo que varían de 20-41%4–7, y considerando una eficacia técnica de la GEA con PMAL, la cual se reporta del 93.5%1, nuestro tamaño de muestra fue de 10.4 (10 modelos). Se utilizó para este cálculo el programa estadístico validado (EpiInfo, EE. UU.). Se documentaron las características generales de los modelos y de las intervenciones incluyendo el éxito técnico, clínico y eventos adversos. Utilizamos una estadística descriptiva, donde las variables se expresaron en promedios para las cuantitativas y en porcentajes para las cualitativas.
ResultadosDurante el periodo comprendido entre septiembre y noviembre 2023 se realizaron un total de 32 intervenciones endoscópicas en los 10 modelos porcinos in vivo incluidos en el presente estudio. Todos los modelos fueron hembras; la edad promedio fue de 6.9 semanas y el peso de 23.8kg (tabla 1).
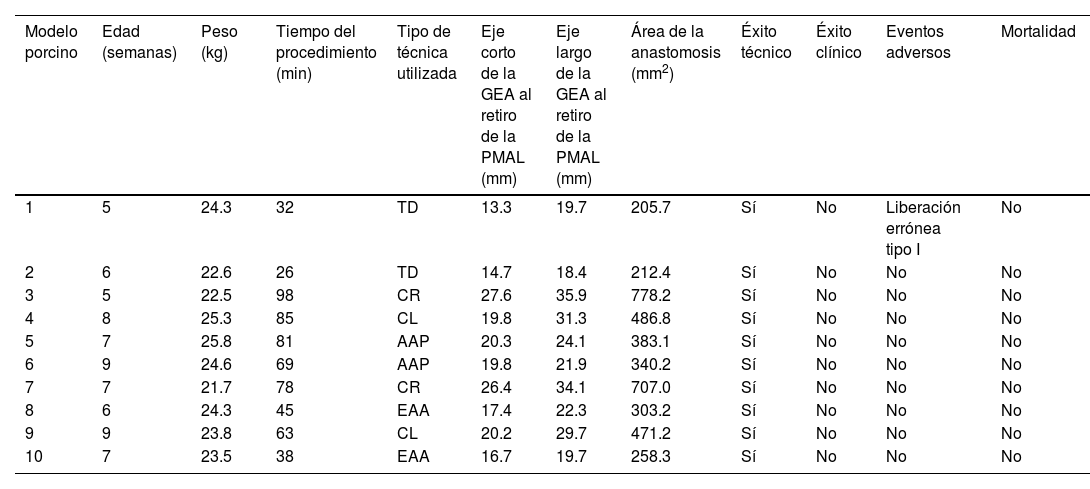
Características generales de los modelos, procedimientos y de las anastomosis creadas
| Modelo porcino | Edad (semanas) | Peso (kg) | Tiempo del procedimiento (min) | Tipo de técnica utilizada | Eje corto de la GEA al retiro de la PMAL (mm) | Eje largo de la GEA al retiro de la PMAL (mm) | Área de la anastomosis (mm2) | Éxito técnico | Éxito clínico | Eventos adversos | Mortalidad |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 5 | 24.3 | 32 | TD | 13.3 | 19.7 | 205.7 | Sí | No | Liberación errónea tipo I | No |
| 2 | 6 | 22.6 | 26 | TD | 14.7 | 18.4 | 212.4 | Sí | No | No | No |
| 3 | 5 | 22.5 | 98 | CR | 27.6 | 35.9 | 778.2 | Sí | No | No | No |
| 4 | 8 | 25.3 | 85 | CL | 19.8 | 31.3 | 486.8 | Sí | No | No | No |
| 5 | 7 | 25.8 | 81 | AAP | 20.3 | 24.1 | 383.1 | Sí | No | No | No |
| 6 | 9 | 24.6 | 69 | AAP | 19.8 | 21.9 | 340.2 | Sí | No | No | No |
| 7 | 7 | 21.7 | 78 | CR | 26.4 | 34.1 | 707.0 | Sí | No | No | No |
| 8 | 6 | 24.3 | 45 | EAA | 17.4 | 22.3 | 303.2 | Sí | No | No | No |
| 9 | 9 | 23.8 | 63 | CL | 20.2 | 29.7 | 471.2 | Sí | No | No | No |
| 10 | 7 | 23.5 | 38 | EAA | 16.7 | 19.7 | 258.3 | Sí | No | No | No |
AAP: ablación con argón plasma; CL: corte lineal; CR: corte radial; EAA: escleroterapia con alcohol absoluto; GEA: gastroenteroanastomosis; PMAL: prótesis metálica de aposición luminal; TD: técnica directa.
En cuanto a los procedimientos, los tiempos promedio registrados de acuerdo con la técnica implementada fueron los siguientes: TD=29min; CR=88min; CL=74min; EAA=41min y AAP=75min; de tal forma que la TD fue la más rápida y los modelos a quienes se realizaron CR fueron los que presentaron el tiempo más prolongado. Se alcanzó un éxito técnico en el 100% de los modelos; sin embargo, el éxito clínico fue del 0%, incluyendo a los pacientes del grupo control (TD). Sin embargo, se alcanzó una tolerancia a la vía oral en todos los casos a las 24h posteriores a cualquiera de las intervenciones (tabla 1).
En todos los casos se realizó la evaluación de la GEA a los 30 días (TD y EAA) y 15 días (CR, CL y AAP). Esto debido a que en TD y EAA no existió necesidad de realizar una GEA temporal inicial 15 días después de la colocación de la PMAL, a diferencia del resto de las técnicas donde primero se realizó la GEA temporal, tiempo en el cual se realizó la maniobra correspondiente (CR, CL y AAP), para posteriormente volver a dejar la PMAL como tutor y 15 días después retirarla definitivamente. En todos los casos, el retiro de la PMAL fue a los 30 días y se realizó la evaluación de la anastomosis obteniendo que la mayor distancia en eje corto fue para los pacientes con CR con un promedio de 27mm y la menor para la TD con 14mm; y en eje largo, la mayor distancia fue para CR con 35mm y la menor para TD con 19mm. Esto se vio reflejado en el promedio de área total de la anastomosis donde la técnica de CR fue la mayor con 742mm2 y la TD fue la que tuvo la menor área con 209mm2 (tabla 1 y fig. 1).
Con respecto a los eventos adversos presentados, solo hubo uno que fue un evento adverso menor el cual consistió en una liberación inadecuada de la PMAL (tipo I)12. Se obtuvo una adecuada resolución al extraer primero la prótesis y posteriormente realizar un cierre primario de la perforación gástrica con un clip tipo over-the-scope clip (OTSC, tipo a; Tübingen, Alemania), y finalmente una vez corroborado el cierre de la perforación gástrica, se realizó la colocación de la GEA con TD sin complicaciones inmediatas ni eventos adversos posteriores al procedimiento. No hubo necesidad de realizar una GEA adicional, ni tampoco hubo mortalidad en ninguno de los modelos de experimentación.
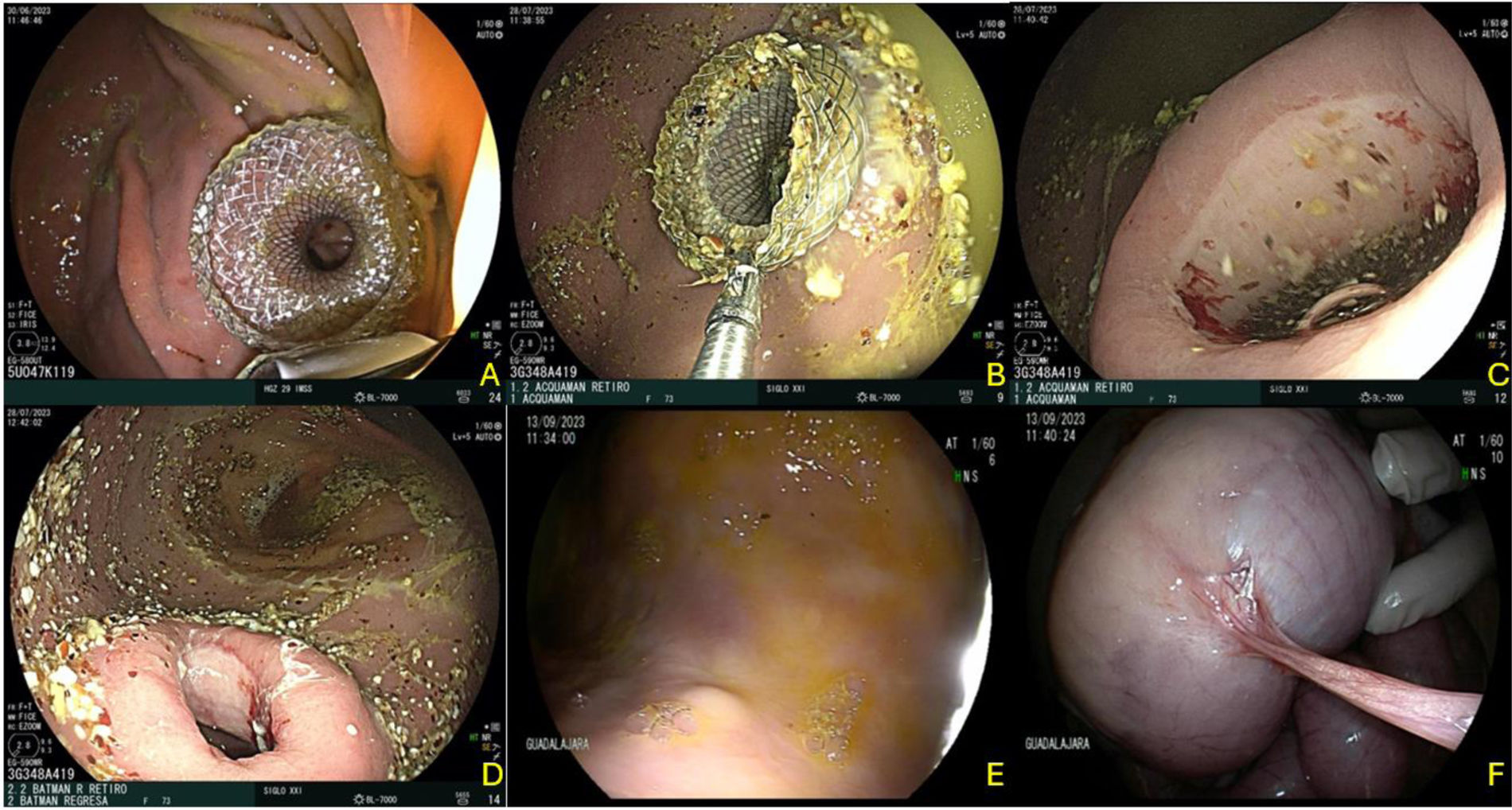
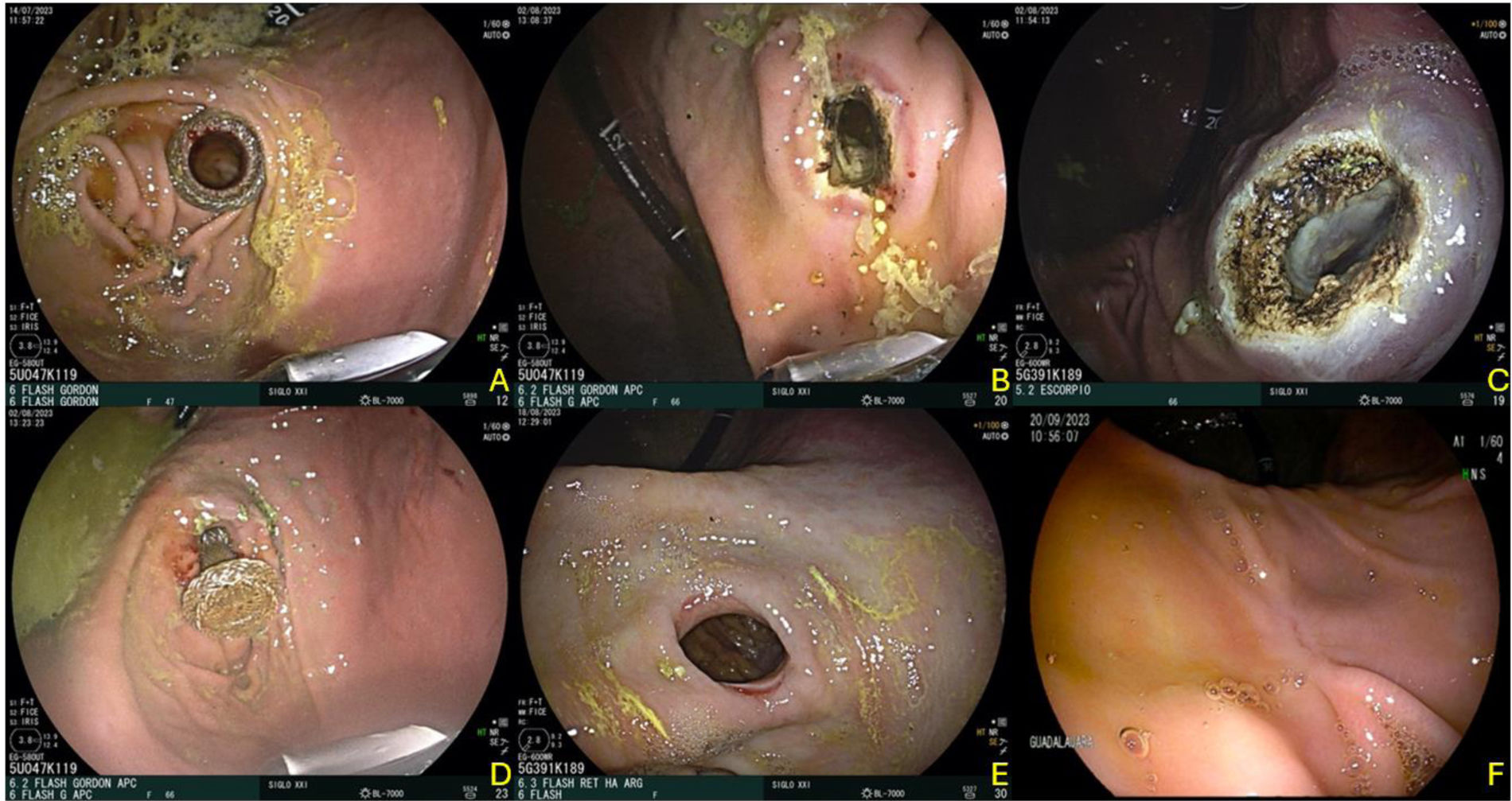
Evaluación por técnica realizadaCon respecto a la evaluación de estas técnicas, la TD fue la más rápida con 29min, pero la que obtuvo el menor diámetro con 209mm2, presentando uno de los modelos una mala colocación de la prótesis (inadecuada liberación tipo I) que fue resuelto endoscópicamente sin complicaciones y pudiéndose colocar nuevamente la GEA. En ambos modelos realizados durante la revisión final en la autopsia se observó un cierre total de la GEA y en ambos casos con adherencia de epiplón al sitio de la anastomosis (fig. 2).
Gastroenteroanastomosis por técnica directa. A) Colocación inicial de Hot Axios™. B) Retiro de la prótesis a 30 días. C y D) Estado de la anastomosis inmediatamente posterior al retiro. E y F) Evaluación final a 60 días observando el cierre total de la gastroenteroanastomosis por el lado mucoso gástrico, y la presencia de epiplón adherido al sitio de anastomosis.
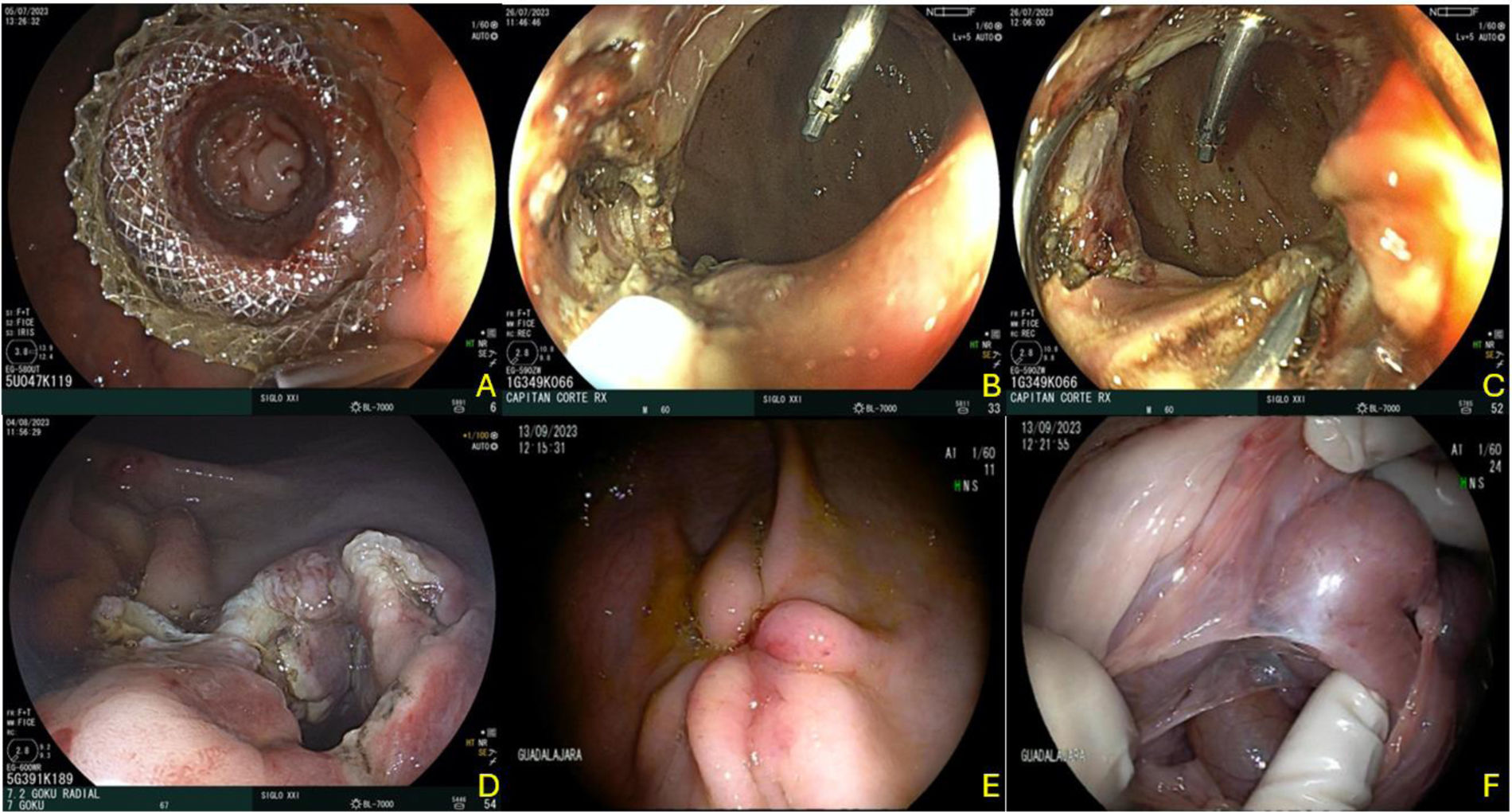
La técnica de CR fue la que obtuvo el mayor diámetro de todas con 742mm2, pero la de mayor duración con 88min. No se presentaron eventualidades durante la realización de los cortes en los 4 puntos cardinales y una vez colocadas las prótesis nuevamente como tutor, no existió ninguna migración. Se utilizaron 8 y 9 clips respectivamente por cada modelo y la tolerancia de la vía oral a las 24h fue adecuada en ambos casos, así como su evolución. Sin embargo, durante la evaluación final, se observó un cierre total de la GEA con presencia de adherencia de epiplón y del asa intestinal en esta región, pero sin permeabilidad de la GEA y en el otro caso solo presencia de epiplón en la cara extraluminal (fig. 3).
Gastroenteroanastomosis por técnica de cortes radiados. A) Colocación inicial de Hot Axios™. B y C) Realización de cortes radiados con colocación de clips de seguridad a 15 días. D) Retiro de prótesis a 30 días y estado de la gastroenteroanastomosis. E y F) Evaluación final a 60 días, observando una retracción cicatricial por el lado mucoso gástrico, y con adherencia de epiplón y parte del asa intestinal a nivel de la gastroenteroanastomosis.
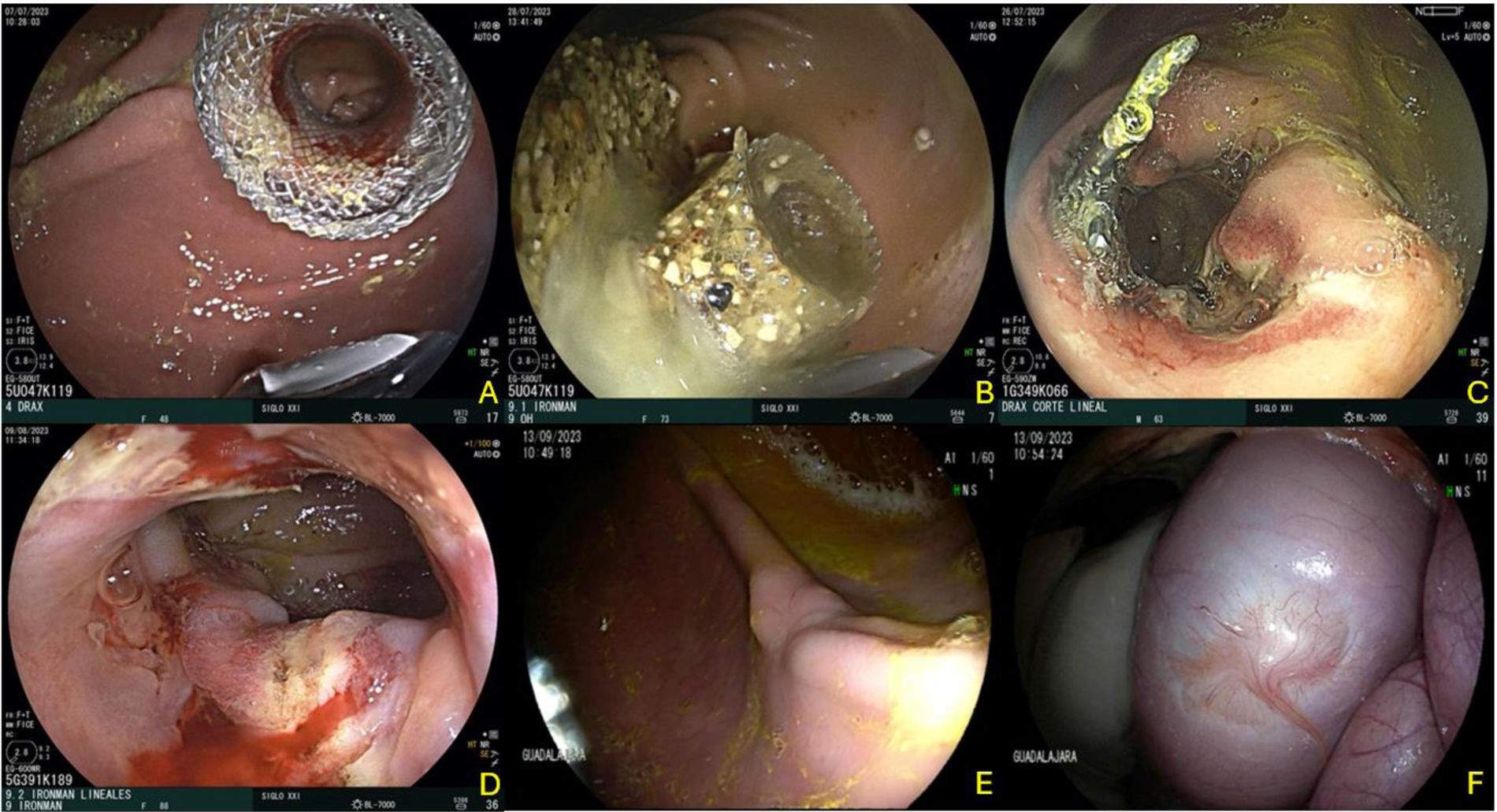
La realización de CL fue más rápida que CR con un tiempo de 74min, el diámetro de la anastomosis fue la segunda más grande después de la técnica de CR y no se presentaron complicaciones durante el procedimiento. Se utilizaron 3 y 4 clips por cada modelo y no existieron eventos adversos posteriores al mismo. Al igual que en el resto de las técnicas, se observó en la evaluación final una GEA cerrada con adherencia de epiplón en esta región para ambos modelos (fig. 4).
Gastroenteroanastomosis por técnica de cortes lineales. A) Colocación inicial de Hot Axios™. B y C) Revisión de la gastroenteroanastomosis a 15 días, y realización de cortes lineales con uso de clips en los bordes. D) Retiro de prótesis tutor a 30 días, y revisión del estado de la gastroenteroanastomosis. E y F) Evaluación final a 60 días, observando una cicatriz mucosa luminal, y por el lado extraluminal observando la cicatriz a nivel de la gastroenteroanastomosis y restos de epiplón.
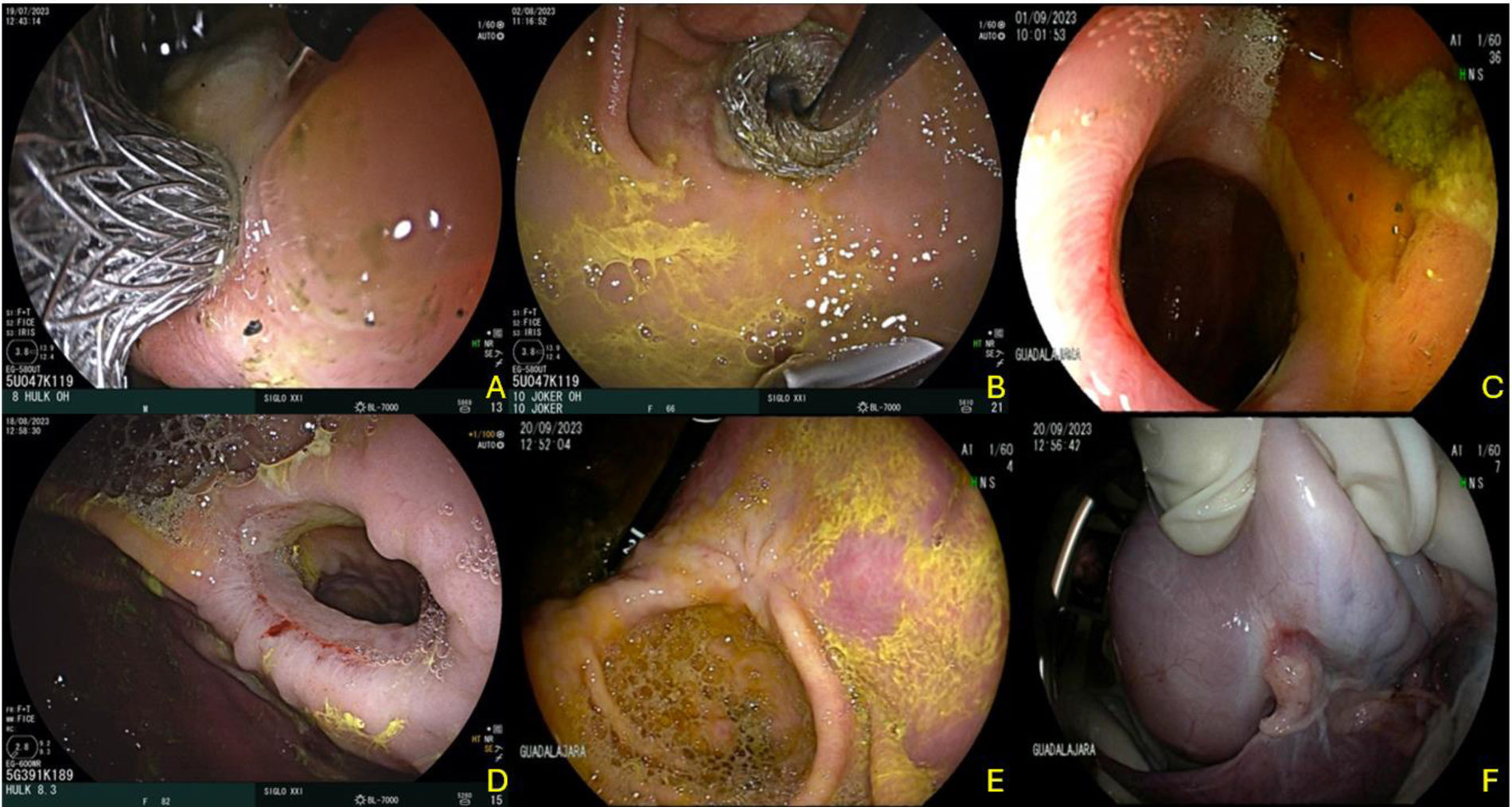
El alcohol absoluto representó una técnica que resultó promisoria, siendo la segunda más rápida después de la TD con 41min, esto debido a que se añade el tiempo de inyección una vez colocada la PMAL para la creación de la GEA. El promedio de alcohol inyectado fue de 2ml por cuadrante, abarcando tanto la pared gástrica como la enteral. No se observaron eventos secundarios posteriores a la aplicación y la prótesis sirvió como tutora durante los 30 días de permanencia para la formación de la GEA. Al retiro de la PMAL, los bordes de la anastomosis se observaron bien formados, pero con ulceración en ambos casos a nivel de la pared formada entre ambos órganos, sin evidencia de hemorragia digestiva. En la evaluación final, las GEA estaban cerradas y los modelos presentaron varias adherencias entre estómago, epiplón y pared intestinal y una retracción importante a nivel de la pared gástrica intraluminalmente (fig. 5).
Gastroenteroanastomosis por técnica de esclerosis con alcohol absoluto. A y B) Colocación inicial de Hot Axios™ con aplicación de alcohol absoluto alrededor y dentro de la prótesis. C y D) Visión endoscópica y estado de las gastroenteroanastomosis en ambos modelos a 30 días. E y F) Evaluación final a 60 días donde se observa una cicatriz luminal prepilorica en la región de la anastomosis, y en el lado extraluminal se observa la adherencia gástrica-epiplón-enteral.
La utilización del argón plasma para la creación de la GEA, demostró ser un procedimiento seguro y con adecuada eficacia técnica. Al igual que en las técnicas de CR y CL, la realización de la ablación de toda la circunferencia de la anastomosis generó una adición en el tiempo total del procedimiento con un promedio de 75min. Sin embargo, al retirar la PMAL se observó una adecuada creación de la GEA con bordes bien definidos y solo una discreta ulceración en ambos modelos. Sin embargo, en la evaluación final se observó una retracción cicatricial a nivel luminal, presencia de adherencias de epiplón en el lago extraluminal y cierre completo de la anastomosis (fig. 6).
Gastroenteroanastomosis por técnica de ablación con argón plasma. A) Colocación inicial de Hot Axios™. B y C) Aplicación de argón plasma en la gastroenteroanastomosis a los 15 días. D) Gastroenteroanastomosis y prótesis tutor a los 30 días. E) Estado de la gastroenteroanastomosis después del retiro de la prótesis Hot Axios™. F) Evaluación final a 60 días, observando un cierre total a nivel de sitio de gastroenteroanastomosis previa.
La OTSG es un padecimiento que genera una alta morbilidad-mortalidad y pérdida de la calidad de vida para los pacientes; donde los signos y síntomas están relacionados directamente con el tiempo y etiología de la obstrucción1,2. Para la obstrucción de origen maligno la gastroenterostomía quirúrgica ha sido clásicamente el estándar de tratamiento, pero asociada múltiples eventos adversos y a que no todos los pacientes son candidatos a este tipo de tratamiento3,8. La evolución endoscópica ha permitido ofrecer la alternativa paliativa por medio del uso de prótesis duodenales, las cuales presentan un buen éxito técnico y clínico a corto plazo, pero requiriendo múltiples procedimientos; y finalmente con el advenimiento la creación de una GEA por medio del USE, han generado buenos resultados hasta el momento, con un éxito técnico del 92% (IC 95%: 86-95%), clínico del 90% (IC 95%: 85-94%) y complicaciones de hasta el 12% (IC 95%: 6-16%)1,3,8. Sin embargo, a pesar de estas ventajas, su uso en enfermedad benigna ha sido limitado5,6,13,14, por el impredecible cierre de la GEA una vez retirada la PMAL. Es por ello, que este trabajo tuvo como objetivo primario, la evaluación de una potencial creación de GEA de tipo permanente, utilizando varias técnicas modificadas con respecto a la técnica original y donde pudimos confirmar la seguridad y eficacia de las 4 técnicas evaluadas, sin embargo, con un éxito clínico fallido en todos los modelos propuestos.
Para el presente trabajo utilizamos a 10 modelos porcinos hembras debido a que su anatomía es muy similar a la del ser humano. Para esto seguimos todos los protocolos de seguridad y ética correspondientes con el objetivo de evaluar la potencial creación de una GEA permanente. Pudimos confirmar que la TD, que fue la que definimos como técnica clásica o grupo control y que incluyó a 2 modelos porcinos, fue la más rápida con 29min y que, comparado con los trabajos de creación de GEA en humanos, es relativamente más rápida también utilizando esta TD con tiempos que tienen rangos desde los 42-65min1–3,7,14. Esto podría explicarse por 2 motivos: el primero, debido a que a diferencia de la creación de GEA en humanos, donde en la mayoría de los casos incluidos presentan algún tipo de enfermedad, ya sea benigna o maligna, lo cual modifica y dificulta de forma inicial la creación de esta GEA, y en segundo lugar, debido a que nosotros no utilizamos rayos X para crear la GEA sino solamente el USE, a diferencia de cuando se realizan en los pacientes, donde el uso de rayos X es imperativo para evaluar el sitio y la adecuada colocación de la PMAL posterior a su liberación1,2,14; lo cual, también confirma que la realización de una GEA sin uso de rayos X es no solo posible, sino seguro, ya que de los 10 modelos realizados, solo tuvimos una mala colocación (tipo I) y que pudo ser resuelta adecuadamente de forma endoscópica con cierre del defecto gástrico con clip OTSC tipo A, y en ese mismo tiempo, sin abortar el caso, pudimos colocar la GEA de forma adecuada, obteniendo una evolución del modelo similar a los otros 9 sin presencia de eventos adversos o procedimientos adicionales y ninguna mortalidad.
Decidimos utilizar 4 técnicas endoscópicas que consideramos reproducibles y se han utilizado con frecuencia en otras enfermedades de origen gastrointestinal, sin embargo, en este caso el objetivo fue buscar una remodelación «más estable» y potencialmente permanente de la GEA con respecto a la técnica original basado en la fisiopatología de las anastomosis gastroenterales8–11. De estas técnicas, 2 que fueron los CR y CL, son derivadas de la disección endoscópica submucosa y nuestros objetivos fueron 2: El primero mejorar el diámetro de la anastomosis, el cual fue alcanzado en ambos casos con un diámetro de 742mm2 para CR, y de 479mm2 para CL, lo cual representó un aumento de 3.5 y 2.2 veces mayor diámetro con respecto al grupo control (TD=209mm2). Este hallazgo es importante, debido a que a pesar de que el objetivo final no fue alcanzado, estas 2 técnicas generaron el mayor diámetro posible de una GEA por vía endoscópica, lo que podría tener implicaciones importantes en términos clínicos en un futuro en los pacientes con obstrucción al tracto, esto debido a la mejora de la tolerancia de la vía oral, evaluada por medio de un incremento en el puntaje de gastric outlet obstruction score (GOOS), la cual podría mejorar y mantenerse a mediano y largo plazo en estos pacientes en caso de lograrse una permanencia de la GEA. Diferencias clínicas que sí han sido confirmadas en los pacientes con OTSG, y donde el trabajo de Bejjani et al.15, así lo demostró, a través de un estudio multicéntrico realizado en 19 centros donde se incluyeron a 267 pacientes con OTSG, en quienes se comparó la eficacia clínica por medio de un incremento en el puntaje del GOOS al utilizar PMAL de 15 vs. 20mm y donde una mayor proporción de pacientes del grupo de 20mm presentó tolerancia a dieta blanda o sólida, comparado con el grupo de 15mm (91.2 vs. 81.2%, respectivamente; p=0.04). Confirmando así, que el diámetro de la GEA sí tiene una relación con el éxito clínico en los pacientes con OTSG, y que en este momento está limitado por el diámetro de la anastomosis y no por una GEA nativa de mayor diámetro como lo planteamos en el presente trabajo. En segundo lugar, nuestro objetivo fue la de generar un cuerpo extraño a nivel de la GEA con el uso de hemoclips, tanto para mejorar la seguridad en los cortes (en caso de una perforación potencial, que no se presentó en ningún modelo) y por otro lado para que la cicatrización y remodelación de las anastomosis fueran con este nuevo diámetro alcanzado, que como se esperaba fue mayor en el grupo CR al realizar una anastomosis que abarcó 4 puntos cardinales y no 2 como en CL, y aunque este objetivo no se alcanzó por la capacidad limitada de los clips, podría ser reevaluado en un futuro con el uso de mejores técnicas como la endosutura endoscópica que permitiría la presencia potencialmente permanente de un cuerpo extraño en la GEA creada. Con respecto al uso del alcohol y del argón plasma, decidimos implementar su uso en 2 técnicas, esto debido a su facilidad de utilización y seguridad, las cuales fueron confirmadas, sobre todo la del alcohol, quien mostró el segundo mejor tiempo con 41min con respecto a la TD, con solo 12min adicionales a esta; además, con la ventaja de realizarse en el mismo momento de la colocación de la PMAL, a diferencia de las otras 3 técnicas experimentales, donde la intervención se realizó al retiro temporal de la PMAL con una nueva recolocación de la misma, lo cual representó 2 intervenciones y no una como en este caso. En el caso del argón plasma, nuestro objetivo fue crear una remodelación más estable de la GEA entre la mucosa gástrica y la yeyunal, sin embargo; aunque la ulceración mostrada durante la evaluación de la GEA al retiro de a prótesis fue menor con respecto al resto de las técnicas, sugiriendo una mejor epitelización, lamentablemente, esto no tuvo traducción clínica durante la evaluación final, donde todas las GEA mostraron un cierre total.
Es importante considerar que aunque el éxito clínico no fue alcanzado, existen 4 factores que podrían haber influido en estos resultados: En primer lugar, que trabajamos en una estructura gastrointestinal sana, la cual no presenta la fisiopatología de una verdadera OTSG, que en comparación con el estudio de Krafft et al.4, en donde ellos describieron una persistencia de hasta el 41% de la anastomosis posterior al retiro de la PMAL en los pacientes sometidos a bypass gástrico previamente, esta anastomosis se realizó entre el pouch gástrico y el remanente, lo cual condiciona otras circunstancias físicas como el aumento de la presión intraluminal a nivel del pouch, lo cual a su vez impediría un cierre de la anastomosis creada y que es un efecto similar al evaluado en la OTSG de origen benigno o maligno y, por otro lado, la anastomosis de gastro-gástrica, lo cual al tratarse del mismo órgano, podría generar una anastomosis más estable y sin estructuras intermedias. En segundo lugar, la presencia de un cuerpo extraño consideramos que puede ser un factor importante, ya que en las anastomosis quirúrgicas que presentan un cuerpo extraño permanente como una sutura o sutura mecánica, esto interfiere con el cierre total de la anastomosis, lo cual es distinto a la técnica endoscópica, donde existe una aposición de bordes gástrico y enteral, que al retirarse la PMAL, se conservan los bordes bien irrigados y sin presencia de un cuerpo extraño que pudiera interferir en su cicatrización y cierre, y aunque en este estudio el uso de clips fungió como cuerpo extraño, esto no fue suficiente para su permanencia para este fin. En tercer lugar, el tiempo de permanencia de la PMAL in situ, ha sido un factor importante en estudios clínicos, para la evaluación de la permanencia de la anastomosis, no ha sido determinante o bien estudiado y que en nuestro caso fue de 15 días para CR, CL y AAP y de 30 días para TD y EAA, lo cual es poco, comparado con una media de 85 días en el estudio de Krafft et al.4, y donde el 41% presentó permanencia, pero que no necesariamente esta podría atribuirse al tiempo o a que se trató de gastro-gastro anastomosis y no GEA. Además, otro trabajo reciente por Abel et al.13, que evaluaron el uso de la PMAL para una GEA en los pacientes con enfermedad benigna, demostró una adecuada permeabilidad de las PMAL a largo plazo con una permanencia de hasta 286 días y 3 pacientes rebasando los 900 días (944, 1408 y 1444 días), lo cual si bien confirma que las PMAL pudieran permanecer in situ hasta por 4 años, esto no necesariamente podría estar relacionado con que exista una permanencia de la GEA aun al retiro de la PMAL a este tiempo. Y, en cuarto lugar, en la evaluación final de todos los modelos aquí estudiados, pudimos confirmar que, entre el tejido gástrico y enteral, se interpuso el epiplón el cual estaba incluido en todos los casos independientemente de la técnica utilizada. El epiplón u omento, es una fuente de múltiples factores de crecimiento, el cual contiene células madre pluripotenciales que se pueden diferenciar en diversos tipos de células y esto previene o limita la sepsis, promueve la angiogénesis y da soporte vascular, lo cual influye de forma tan eficiente en la reparación del tejido que sus propiedades han sido utilizadas en la práctica quirúrgica en múltiples procedimientos16. Si bien estas propiedades pueden prevenir de fugas anastomóticas y otras complicaciones, también podría tener un papel fundamental en el cierre de una anastomosis realizada por aposición como es nuestro caso, independientemente de la técnica utilizada, inclusive con el objetivo de generar cortes transmurales (CR, CL) o un daño tisular controlado (EAA, AAP).
Dentro de las limitaciones de nuestro trabajo se encuentra el seguimiento a corto plazo, considerando que potencialmente este factor podría ser considerado como importante para la creación de una anastomosis permanente; la ausencia de evaluación histológica, la cual podría habernos brindado información para poder intentar explorar el cierre prematuro de las anastomosis independientemente de la técnica empleada y finalmente el tamaño de muestra, que aunque calculado de acuerdo a conveniencia para este trabajo, podría considerarse como «limítrofe» en términos estadísticos, pero suficiente, como para ser tomado como base para la planeación de un proyecto futuro que busque el mismo tipo de objetivos, considerando variables como un seguimiento mayor y una modificación adicional a las técnicas aquí empleadas; sin embargo, aunque importantes consideraciones a tomar en cuenta, esto no invalida los resultados aquí obtenidos y que nos dejan entrever que existen múltiples factores que intervienen en la creación de una GEA permanente.
Finalmente, podemos concluir que, aunque el presente estudio no alcanzó el objetivo clínico de lograr crear una GEA permanente con ninguna de las técnicas implementadas; esto, debido a una compleja fisiopatología multifactorial, sí se pudieron realizar GEA no solo de mayor calibre con respecto a la técnica original, sino que sin gran compromiso en el tiempo y con un adecuado perfil de seguridad. Esto abre la posibilidad y necesidad de realizar nuevas exploraciones endoscópicas con el objetivo final de generar una alternativa terapéutica de mínima invasión segura, efectiva y permanente para el tratamiento de los pacientes con OTSG de origen benigno.
Responsabilidades éticasTodos los estudios procedimientos realizados en los modelos animales fueron realizados bajo las normas designadas por para la realización de estudios en modelos animales y de acuerdo con las normas oficiales mexicanas NOM-062-ZOO-1999, NOM-087-ECOL-SSA1-2002, así como a la Ley General del Equilibrio Ecológico y la Protección al Ambiente. Además de estar apegado a las directrices ARRIVE de acuerdo con la experimentación en modelos animales y apegado a las recomendaciones dadas por la directiva UE 2010/63/UE, para experimentación en modelos animales y también en apego a la guía de cuidado y utilización de los animales de laboratorio de la National Institutes of Health (NIH publications No 8023, revised 1978).
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses para la realización del presente trabajo.