La cirrosis hepática representa una causa importante de mortalidad a nivel mundial, con un aumento reciente en los casos secundarios a la enfermedad hepática esteatósica asociada a disfunción metabólica y el consumo de alcohol. Actualmente, el trasplante hepático es el único tratamiento definitivo, pero amerita el uso de inmunosupresión para prevenir el rechazo.
Los inhibidores de calcineurina son la piedra angular de la inmunosupresión en pacientes trasplantados. No obstante, su uso condiciona complicaciones metabólicas y renales, como el síndrome metabólico, la diabetes postrasplante y la enfermedad renal crónica. La minimización o suspensión de la inmunosupresión ha mostrado reducir estos efectos adversos en pacientes seleccionados, especialmente en aquellos con potencial inmunotolerancia. En estudios recientes se han identificado predictores de inmunotolerancia y complicaciones cardiovasculares en pacientes trasplantados. Por tanto, existe la necesidad de desarrollar estrategias individualizadas para equilibrar el riesgo metabólico con la prevención del rechazo.
.
Cirrhosis of the liver is a major cause of death worldwide, with a recent increase in cases secondary to metabolic dysfunction-associated steatotic liver disease and alcohol use. Liver transplantation is currently the only definitive treatment but requires immunosuppression for preventing graft rejection.
Calcineurin inhibitors are the cornerstone of immunosuppression in transplanted patients. However, their use conditions metabolic and renal complications, such as metabolic syndrome, post-transplant diabetes, and chronic kidney disease. Minimizing or discontinuing immunosuppression has been shown to reduce those adverse effects in selected patients, especially those with potential immunotolerance. Predictors of immunotolerance and cardiovascular complications in transplanted patients have been identified in recent studies. Thus, there is a need for developing individualized strategies for balancing metabolic risk and graft rejection prevention.
La cirrosis hepática (CH) constituye un problema de salud pública a nivel mundial, con una mortalidad que supera los dos millones de personas anualmente. En los últimos años la etiología de esta enfermedad ha evolucionado debido a la creciente pandemia de sobrepeso y obesidad. De tal manera, en la actualidad, en México, las principales causas de cirrosis son la enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD, por sus siglas en inglés), que predomina en personas mayores, junto con el consumo excesivo de alcohol en pacientes jóvenes. Por otro lado, la prevalencia del virus de la hepatitisC ha disminuido significativamente gracias a las altas tasas de curación y el acceso universal a los antivirales de acción directa (AAD)1-3.
El tratamiento curativo para la CH en etapa descompensada o ante casos seleccionados de carcinoma hepatocelular es el trasplante hepático (TH). No obstante, su acceso está limitado por la escasez de donantes2,4. Los avances en las técnicas quirúrgicas y los esquemas de inmunosupresión (IS) actuales han mejorado la supervivencia global de los pacientes trasplantados, alcanzando tasas del 93%, del 80.2% y del 64.3% a 1, 5 y 10años, respectivamente3. Estos resultados, sin embargo, dependen de factores como la etiología, la edad del receptor y la presencia de comorbilidades.
Dentro de los esquemas de IS, los inhibidores de la calcineurina (ICN) representan la piedra angular para prevenir el rechazo a corto y a largo plazo. El tacrolimus es el ICN más utilizado, y su uso está asociado a una mayor supervivencia del paciente y del injerto, además generando un impacto positivo en la calidad de vida5. Sin embargo, el uso prolongado de ICN conlleva importantes desafíos, particularmente en el desarrollo o empeoramiento del síndrome metabólico, entre otras complicaciones.
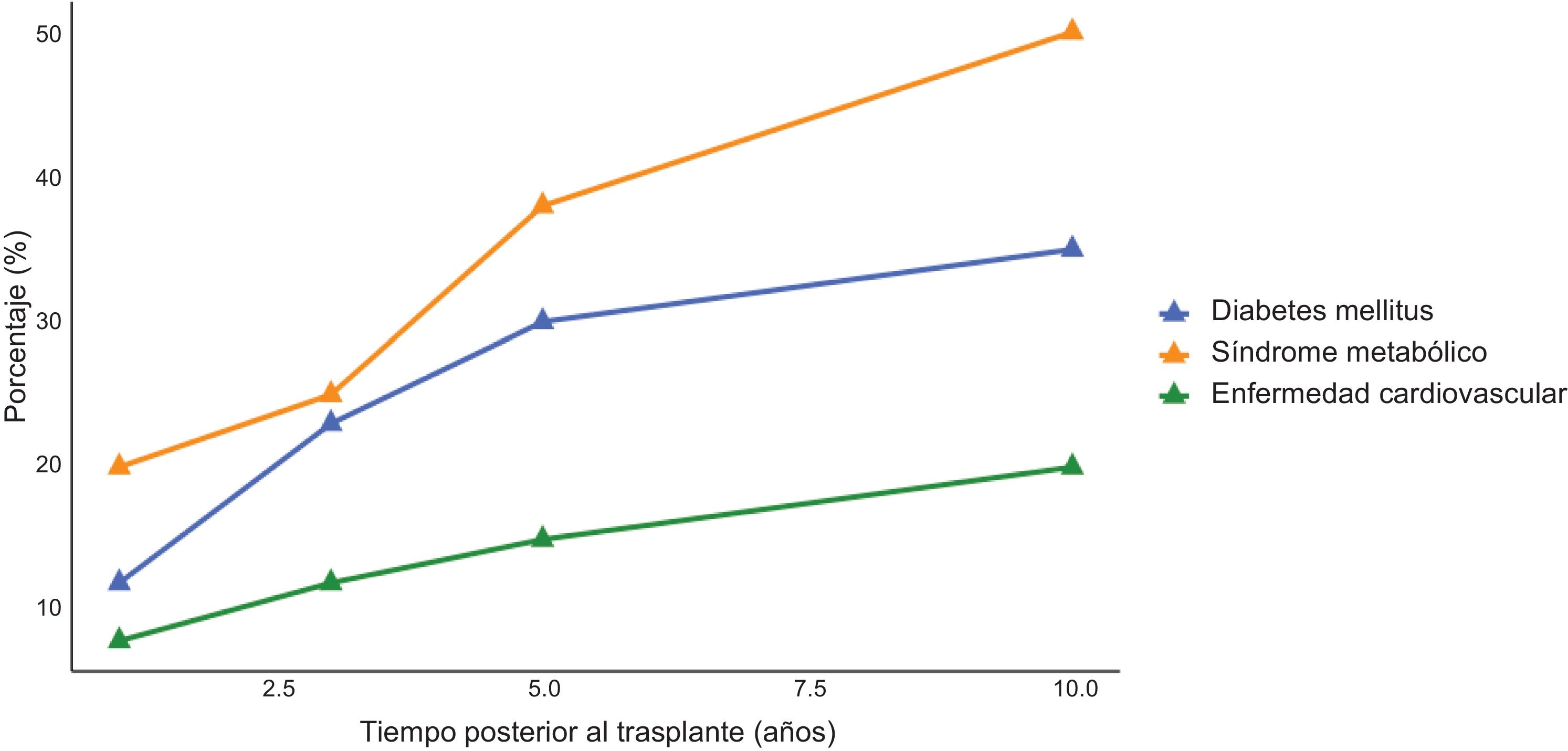
La MASLD se asocia estrechamente a otros trastornos metabólicos, como la diabetes mellitus, la hipertensión, la obesidad y la dislipidemia, y por ende se ve acompañada de un mayor riesgo de complicaciones cardiovasculares y renales, entre otras. Esto se ve agravado con el uso de IS. Entre las más preocupantes se encuentra el desarrollo de enfermedad renal crónica (ERC), definida como una tasa de filtrado glomerular <60ml/min durante más de 3meses, la cual afecta a más del 14% de los pacientes con TH después de 5años. En estos casos, los pacientes pueden llegar a requerir de diálisis o incluso un trasplante renal posterior al TH6. Adicionalmente, el síndrome metabólico ocurre en más del 20% de los pacientes tras el primer año de tratamiento, mientras que la diabetes de novo postrasplante (NODAT) afecta a más del 20% tras 2años de seguimiento. Estas alteraciones contribuyen a un aumento de la incidencia de enfermedad cardiovascular, que supera el 15% a los 3años postrasplante, siendo una de las principales causas de muerte en población trasplantada5 (fig. 1).
En estudios recientes se han identificado predictores no invasivos de complicaciones cardiovasculares en población TH. Por ejemplo, un parámetro de atenuación controlada (CAP) >270dB/m determinado durante una elastografía se asoció con un mayor riesgo de infarto de miocardio en pacientes con TH y que además presentaban diabetes7. Esto resalta la necesidad de ajustes individualizados en los esquemas de IS para equilibrar el riesgo metabólico y cardiovascular con la prevención del rechazo del injerto. Un estudio realizado por Angelico et al.8 demostró que la reducción de la dosis de ICN a menos del 25% de la dosis de mantenimiento, o su retiro total, disminuyó significativamente la prevalencia de síndrome metabólico en pacientes trasplantados: 8.3% en el grupo con reducción de dosis frente al 47.8% en el grupo sin cambios. Además, aquellos pacientes con alteraciones metabólicas previas experimentaron una mejoría en hasta el 50% tras la reducción de la IS. Es decir, en los pacientes en los que se logra la minimización o el retiro de la IS, se observa una reducción significativa en las complicaciones metabólicas asociadas.
Por tanto, últimamente se ha propuesto que se considere la implementación de un esquema de IS mínima o su suspensión completa en pacientes con mayor riesgo de complicaciones metabólicas, particularmente en pacientes en donde se sospeche que exista un grado de inmunotolerancia. En un ensayo clínico controlado y multicéntrico realizado en una población trasplantada altamente seleccionada se logró suspender la IS en el 41% de los participantes. Estos resultados sugieren que la combinación de parámetros clínicos podría ser útil para identificar a los candidatos adecuados para estas estrategias9. Por otro lado, en otro estudio multicéntrico se identificaron predictores asociados a la inmunotolerancia operacional. Los más relevantes de estos fueron una mayor edad y un tiempo prolongado desde el trasplante, mientras que los biomarcadores séricos no demostraron un papel tan significativo. Sin embargo, aunque existen múltiples estudios en esta área, se requieren estudios prospectivos con un tamaño de muestra más amplio10.
En conclusión, mientras que la IS sigue siendo la piedra angular del tratamiento posterior a un TH, su manejo debe adaptarse cuidadosamente en pacientes con un mayor riesgo de complicaciones metabólicas o cardiovasculares. Es crucial considerar estrategias de inmunosupresión mínima e inmunotolerancia en pacientes seleccionados para optimizar la calidad de vida y los resultados a largo plazo.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Consideraciones éticasEl presente artículo carece de información personal de pacientes o intervención alguna. Por tanto, se considera de bajo riesgo y no requirió revisión o aprobación por el comité de ética local. De la misma forma, los autores declaran que, al no contener información personal que permita identificar a los pacientes, este artículo no necesita de un consentimiento informado.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.