Colombia exhibe elevadas tasas de incidencia de cáncer gástrico que podrían explicarse por la variabilidad genética del H. pylori. Nuestro objetivo fue establecer la relación de los genotipos CagA y VacA de H. pylori con el cáncer y la displasia en una población de alto riesgo.
Material y métodosEstudio de casos y controles en 202 pacientes procedentes de una zona de alto riesgo de cáncer. Se incluyeron pacientes con cáncer gástrico y displasia, y pacientes con gastritis no atrófica (controles). El muestreo endoscópico y la clasificación histológica se realizaron de acuerdo al sistema de Sídney y la clasificación de Lauren. La información genética se obtuvo mediante reacción en cadena de la polimerasa sobre bloques de parafina. Se evaluaron las medidas de asociación de las variables de interés en modelos bivariados y multivariados. Un valor de p<0,05 se consideró significativo. Se empleó el programa SPSS® versión 25.
ResultadosLa edad mayor a 50 años (OR: 23,76; IC: 8,40-67,17; p=0,000) y el genotipo VacA s1m1 (OR: 6,18; IC: 1,25-30,51; p=0,025) se asociaron con mayor riesgo de desarrollar cáncer gástrico y displasia. El genotipo CagA+ no se mostró como un factor de riesgo para desarrollar estas enfermedades (OR: 1,02; IC: 0,39-2,62; p=0,965).
ConclusionesLos genotipos VacA de H. pylori son marcadores para el desarrollo de cáncer gástrico. Esta información se podría utilizar para crear un índice de riesgo en un modelo predictivo para optimizar la atención de los pacientes con mayor riesgo.
Colombia has high incidence levels of gastric cancer that can be explained by the genetic variability of Helicobacter pylori (H. pylori). Our aim was to establish the relation of the H. pylori CagA and VacA genotypes to dysplasia and gastric cancer, in a high-risk population.
Material and methodsA case-control study was conducted on 202 patients from a high-risk cancer zone. Patients with dysplasia and gastric cancer (cases) and patients with nonatrophic gastritis (controls) were included. Endoscopic sampling and histologic classification were carried out according to the Sydney system and the Lauren classification. Genetic information was obtained through polymerase chain reaction on paraffin blocks. The measures of association of the variables of interest were evaluated in bivariate and multivariate models. A P<0.05 was considered statistically significant and the SPSS version 25 program was employed.
ResultsAge above 50 years (OR: 23.76; CI: 8.40-67.17; P=0.000) and the VacA s1m1 genotype (OR: 6.18; CI: 1.25-30.51; P=0.025) were associated with higher risk for developing dysplasia and gastric cancer. The CagA+ genotype was not found to be a risk factor for developing those pathologies (OR: 1.02; CI: 0.39-2.62; P=0.965).
ConclusionsThe H. pylori VacA genotypes are markers for the development of gastric cancer. That information could be used to create a risk index in a predictive model to optimize the healthcare of higher-risk patients.
Las neoplasias gástricas representan una de las principales causas de muerte por cáncer a nivel mundial. Según datos de GLOBOCAN, para el año 2018 se presentaron 1.033.701 casos nuevos de cáncer de estómago con 782.685 muertes atribuibles a esta enfermedad1. Dos tercios de los cánceres de estómago ocurren en países en desarrollo, siendo Colombia uno de los países con más altas tasas de incidencia de la enfermedad2. Sin embargo, en el interior del país se presentan notables diferencias con relación a la incidencia y la mortalidad por la enfermedad. En este sentido, en las zonas costeras se presentan bajas tasas de incidencia, mientras que en la región Andina y el Suroccidente colombiano las tasas son notablemente altas. Estas diferencias obedecen a razones pobremente conocidas por lo cual han sido denominadas por algunos autores como el enigma colombiano3.
De acuerdo a la clasificación de Lauren, el cáncer gástrico se puede clasificar en tipo difuso e intestinal, exhibiendo importantes diferencias con relación a la epidemiología, asociación a lesiones premalignas e infección por H. pylori4,5.
En el histotipo intestinal, el factor de riesgo más importante es la infección por H. pylori, bacteria capaz de generar una respuesta mal adaptativa en la mucosa gástrica que induce atrofia, metaplasia, displasia y, finalmente, cáncer6. No obstante, solo algunos pacientes infectados por la bacteria desarrollan cáncer, por lo cual se ha planteado que la variabilidad genética de la bacteria modula el riesgo de carcinogénesis gástrica. Se ha demostrado por ejemplo que los genotipos CagA+ y VacA/s1m1 se asocian a un mayor riesgo cuando se compara con los genotipos CagA− y VacA/s2m27,8.
Aunque en la mayoría de estudios se ha planteado una asociación entre los genotipos CagA y VacA/s1m1 con el desarrollo de cáncer, esta hipótesis ha sido más difícil de probar en Colombia donde existen escasos estudios de asociación entre cáncer y los genotipos bacterianos9–11. En estas investigaciones, el enfoque ha sido predominantemente descriptivo donde se exponen frecuencias alélicas y genotípicas llegando a conclusiones contradictorias. Teniendo en cuenta las diferencias en la incidencia de cáncer en distintas regiones de Colombia, nos planteamos la hipótesis que la variabilidad genética de H. pylori, favorece la aparición de cáncer y displasia. Nuestro objetivo fue evaluar la asociación de los genotipos CagA y VacA de H. pylori con el cáncer gástrico y la displasia mediante un enfoque analítico donde se analiza la interacción de las variables en modelos bivariados y multivariados.
Material y métodosSe realizó un estudio analítico de casos y controles no pareado en pacientes con diagnóstico histopatológico en biopsias gástricas realizadas en el laboratorio «Compañía de Patólogos del Cauca» y el Departamento de Patología de la Universidad del Cauca ubicados al Suroccidente colombiano. De acuerdo a la información del Departamento Administrativo Nacional de Estadística de Colombia, el Departamento del Cauca muestra una de las tasas de mortalidad estandarizada por cáncer gástrico más altas del país, siendo de 14,7/100.000 habitantes/año.
La muestra se obtuvo por conveniencia incluyendo pacientes mayores de 18 años, con diagnóstico histopatológico de gastritis no atrófica (controles) los cuales se compararon con pacientes con diagnóstico microscópico de displasia y adenocarcinoma que asistieron a los centros de diagnóstico durante el año 2011. Como criterios de inclusión, los participantes del estudio debían tener infección por H. pylori determinada por estudio histopatológico y corroborada por pruebas de biología molecular. Se excluyeron participantes con cirugía gástrica previa, antecedentes de cáncer, tratamiento para H. pylori, inmunodeficiencias, y presencia de coinfección bacteriana determinada con las pruebas de reacción en cadena de la polimerasa.
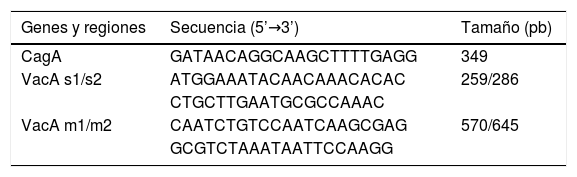
Las biopsias gástricas fueron obtenidas a través de gastroscopia por gastroenterólogos con amplia experiencia. Los pacientes asistieron con un periodo de ayuno de 8h. Se aplicó anestésico tópico y se tomaron 5 biopsias (una biopsia de antro curvatura mayor, una biopsia de antro curvatura menor, una biopsia de cuerpo curvatura mayor, una biopsia de cuerpo curvatura menor y una biopsia de incisura angularis). Las muestras se fijaron en formol al 10% y fueron teñidas con hematoxilina-eosina. Se empleó el sistema de Sídney para la clasificación de las biopsias12. Con el fin de controlar los sesgos en la información, los diagnósticos histopatológicos fueron corroborados por un segundo patólogo, y el diagnóstico histopatológico de infección por H. pylori se comprobó mediante reacción en cadena de polimerasa (PCR) sobre los bloques de parafina mediante la técnica de Chelex® (N.° C7901; Sigma, St. Louis, MO, EE. UU.). La amplificación de los genes CagA y VacA se efectuó por PCR de acuerdo a la descripción de Sugimoto et al.13. Las mezclas de PCR se prepararon con 50ng de DNA genómico, 100μmol dNTPs, 2,5μl de 10X PCR buffer, 1,0mM MgCl2, 1 U de Taq® ADN polimerasa (N.° M1665; Promega, Madison, WI, EE. UU.), y 30pmol de cada uno de los cebadores, como se indica en la tabla 1. La desnaturalización se inició a 95°C durante un minuto, seguido de 35 ciclos de desnaturalización a 94°C durante un minuto, hibridación a 52°C durante un minuto y extensión a 72°C durante un minuto, y un paso de extensión final a 72°C durante 10min. Los productos fueron analizados por electroforesis en geles de agarosa al 2% a 80 voltios durante 40min. El Instituto Nacional de Cancerología de Colombia facilitó cepas de H. pylori que sirvieron como controles. En la tabla 1 se muestran los cebadores empleados.
Como la variable edad tuvo una distribución normal, y se comprobó la hipótesis de homogeneidad de varianzas, se evaluaron las diferencias entre las medias de los grupos a través de la prueba t de Student. Las diferencias en las proporciones se evaluaron con la prueba de Chi-cuadrado. El OR con su valor de p fueron usados para evaluar el efecto de cada variable de interés sobre la variable respuesta (cáncer gástrico y displasia). Para evaluar posibles factores de interacción o confusión se realizó una prueba de regresión logística multivariada. Un valor de p<0,05 y un IC del 95% se consideraron estadísticamente significativos. Se empleó el programa SPSS® versión 25.
Consideraciones éticasLos participantes del estudio firmaron un consentimiento informado. El Comité de Investigaciones de la Universidad del Cauca brindó el aval ético.
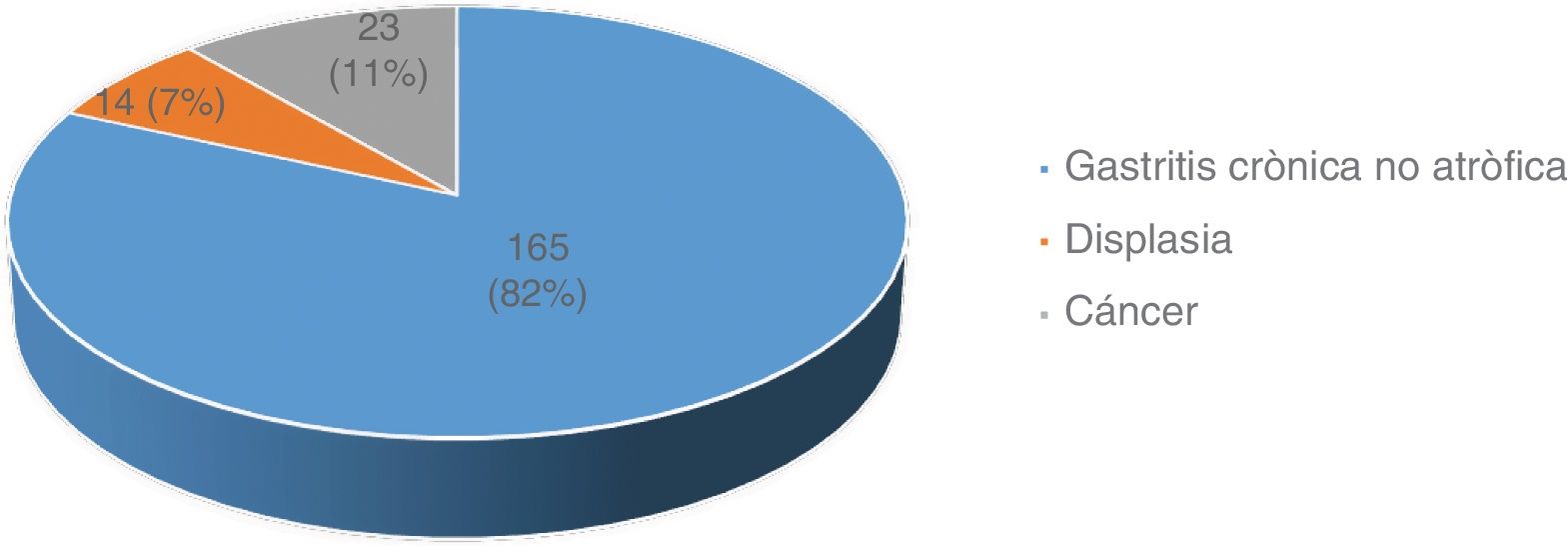
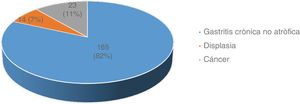
ResultadosDe un total de 654 pacientes que se diagnosticaron en los centros de referencia, se incluyeron en el estudio 202 participantes. La distribución de los pacientes de acuerdo al diagnóstico se muestra en la figura 1.
Debido a que el cáncer y la displasia son más frecuentes después de los 50 años de edad, los pacientes se categorizaron en 2 grupos (pacientes de 18 a 50 años y mayores de 50 años).
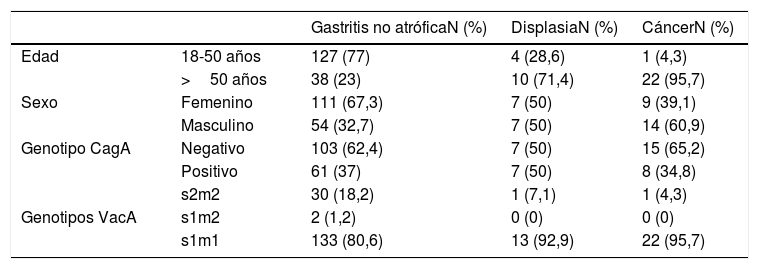
La distribución de los participantes en relación a la edad categorizada, el sexo y los genotipos bacterianos se muestra en la tabla 2.
Distribución de las variables de interés en los grupos de estudio
| Gastritis no atróficaN (%) | DisplasiaN (%) | CáncerN (%) | ||
|---|---|---|---|---|
| Edad | 18-50 años | 127 (77) | 4 (28,6) | 1 (4,3) |
| >50 años | 38 (23) | 10 (71,4) | 22 (95,7) | |
| Sexo | Femenino | 111 (67,3) | 7 (50) | 9 (39,1) |
| Masculino | 54 (32,7) | 7 (50) | 14 (60,9) | |
| Genotipo CagA | Negativo | 103 (62,4) | 7 (50) | 15 (65,2) |
| Positivo | 61 (37) | 7 (50) | 8 (34,8) | |
| s2m2 | 30 (18,2) | 1 (7,1) | 1 (4,3) | |
| Genotipos VacA | s1m2 | 2 (1,2) | 0 (0) | 0 (0) |
| s1m1 | 133 (80,6) | 13 (92,9) | 22 (95,7) |
Para evaluar las diferencias entre los grupos diagnósticos se realizó la prueba de Chi-cuadrado la cual mostró diferencias significativas entre el sexo y la edad categorizada p=0,000, pero no se encontraron diferencias significativas entre las frecuencias del genotipo CagA (p=0,175) ni de los genotipos VacA (p=0,364).
Por tratarse de un estudio no pareado, y con el fin de evaluar la distribución de los genotipos entre los grupos etarios; se compararon las proporciones de los genotipos en las edades categorizadas encontrando que la distribución de los genotipos no varía significativamente con la edad (prueba Chi-cuadrado para genotipos VacA p=0,835; prueba Chi-cuadrado para genotipos CagA p=0,610) (tabla 3).
Finalmente se agruparon los pacientes con displasia y cáncer, y se compararon con la categoría de referencia (gastritis no atrófica) obteniendo una relación de 4,4 controles por cada paciente con cáncer/displasia. Para evaluar la variable edad se realizaron test de normalidad para el grupo control (n=165) mediante el test de Kolmogorov-Smirnov (p=0,200). Por su parte, para el grupo de displasia y cáncer (n=37) se comprobó normalidad mediante el test de Shapiro-Wilk (p=0,700). Una vez establecida la distribución normal de los datos, se comprobó la hipótesis de homogeneidad de varianzas con la prueba de Levene basada en la media obteniendo un valor de p=0,745. Con esta información, se decidió continuar los análisis por la vía paramétrica.
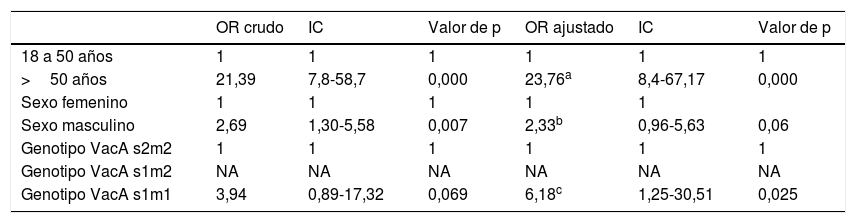
La prueba t de Student demostró diferencias estadísticamente significativas entre la media del grupo control (41 años) y la media de los participantes con cáncer y displasia (62 años) p=0,000. Para los análisis de asociación se tomaron como categorías de referencia la edad menor a 50 años, el sexo femenino, el genotipo CagA− y el genotipo VacA/s2m2. Como se muestra en la tabla 4, La edad categorizada y el sexo masculino se asociaron con un incremento en el riesgo de presentar cáncer y displasia tanto en el modelo bivariado como en el multivariado. Aunque los genotipos CagA y VacA no mostraron asociaciones significativas con el cáncer en el modelo bivariado, se introdujeron en un primer modelo de regresión logística dada la descripción en la literatura de su asociación con el cáncer. La variable CagA no mostró cambios en la significación en ninguno de los modelos, por lo cual se excluyó de la regresión final (OR crudo para CagA+: 4,68: IC: 0,28-77,74; p=0,282; OR ajustado: 1,02; IC: 0,39-2,62; p=0,965. La tabla 4 corresponde al modelo de regresión final y más parsimonioso.
Medidas de asociación para la edad, el sexo y los alelos
| OR crudo | IC | Valor de p | OR ajustado | IC | Valor de p | |
|---|---|---|---|---|---|---|
| 18 a 50 años | 1 | 1 | 1 | 1 | 1 | 1 |
| >50 años | 21,39 | 7,8-58,7 | 0,000 | 23,76a | 8,4-67,17 | 0,000 |
| Sexo femenino | 1 | 1 | 1 | 1 | 1 | |
| Sexo masculino | 2,69 | 1,30-5,58 | 0,007 | 2,33b | 0,96-5,63 | 0,06 |
| Genotipo VacA s2m2 | 1 | 1 | 1 | 1 | 1 | 1 |
| Genotipo VacA s1m2 | NA | NA | NA | NA | NA | NA |
| Genotipo VacA s1m1 | 3,94 | 0,89-17,32 | 0,069 | 6,18c | 1,25-30,51 | 0,025 |
IC: intervalo de confianza; NA: no aplica; OR: odds ratio.
En el presente estudio se observó un mayor riesgo de presentar cáncer gástrico y displasia en pacientes mayores a 50 años. Conclusiones similares han sido reportadas por otros autores14,15. Estos hallazgos son consistentes con la teoría de carcinogénesis en múltiples pasos ya que sugieren que la secuencia atrofia-metaplasia-displasia-cáncer se relaciona con el envejecimiento celular. Teniendo en cuenta que se incluyeron pacientes con displasia —una reconocida lesión premaligna—, los resultados de este estudio aportan información relevante para conocer los factores asociados a la carcinogénesis gástrica y sugieren que las variantes genéticas de H. pylori pudiesen emplearse como marcadores de riesgo en pacientes con lesiones premalignas como la displasia.
Del mismo modo estos hallazgos resaltan la importancia de priorizar el estudio endoscópico e histopatológico en pacientes mayores de 50 años donde las lesiones como el cáncer y la displasia son cada vez más prevalentes.
Con relación al sexo, encontramos diferencias significativas al comparar los grupos de estudio en la estimación cruda. La asociación del género masculino con el cáncer gástrico ha sido reportada por varios autores16,17 en concordancia con los resultados de esta investigación. Como explicaciones se ha planteado la mayor exposición de carcinógenos como el alcohol y el tabaco en el sexo masculino18,19, y el aparente efecto protector de los estrógenos en las mujeres20. No obstante, resulta llamativa la modificación en el efecto en el modelo multivariado con valores de «p» e intervalos de confianza muy cercanos a la hipótesis nula. Estos hallazgos sugieren que, en la población de estudio, la edad jugaría un papel más determinante que el sexo en el riesgo de desarrollar displasia o cáncer.
Si bien es cierto que la asociación entre los genotipos VacA con el cáncer se ha cuestionado por algunos autores21, en general la mayoría de las investigaciones han sugerido que los genotipos VacA/s1m1 y el genotipo CagA condicionan un riesgo mayor para el desarrollo de lesiones premalignas y cáncer22–24. En la presente investigación mostramos que en la población de estudio los genotipos s1m1 son prevalentes tanto en los pacientes con cáncer como en el grupo de referencia; sin embargo, la proporción de pacientes con genotipos s1m1 fue mayor en los pacientes con cáncer y displasia mientras que la proporción de los genotipos s2m2 fue mayor en el grupo de referencia. Resulta interesante la asociación demostrada del genotipo s1m1 con el cáncer gástrico en la regresión logística. Así, el análisis multivariado sugiere que el genotipo VacA/s1m1 incrementa el riesgo de desarrollar displasia y cáncer en pacientes mayores de 50 años (OR: 6,18; IC: 1,25-30,51; p=0,025). Esta información es congruente con el carácter multifactorial del cáncer gástrico y resalta la importancia de analizar las variables en modelos multivariados que permitan evaluar el efecto confusor o interactivo de los factores posiblemente involucrados en la carcinogénesis gástrica.
Por otra parte, nuestros resultados podrían ser útiles para intentar predecir el riesgo de progresión a cáncer. Se sabe por ejemplo que solamente el 0,8% de los pacientes con atrofia y el 3,9% de los pacientes con displasia finalmente desarrollan cáncer14,25; no obstante, tratar de predecir cuales pacientes forman parte de ese porcentaje resulta difícil. Con nuestros resultados podemos sugerir entonces que los pacientes con los genotipos s1m1 representan un grupo especial de riesgo donde estaría justificado un seguimiento endoscópico e histopatológico más periódico.
El potencial patogénico de los genotipos VacA/s1m1 se puede explicar por diversos mecanismos. Se ha mencionado por ejemplo la capacidad de inducir vacuolización celular, la activación de la MAP kinasas y la inhibición del sistema inmune26,27. Presumiblemente estos mecanismos facilitarían la transformación neoplásica en la mucosa gástrica28.
En Colombia existe un reducido número de publicaciones que abordan el tema de los genotipos bacterianos y cáncer. Yamaoka et al. compararon la distribución de los genotipos VacA/s1m1 en cuatro países. Aunque se demostró que el subtipo s1m1 predomina en Colombia, no se encontraron asociaciones estadísticamente significativas con el riesgo de cáncer29. Citelly et al. mostraron en cambio que el genotipo s1m1 estuvo presente en el 81% de los pacientes con cáncer y tan solo en cerca del 40% de los pacientes con gastritis siendo dicha diferencia significativa10. En la investigación publicada por Sicinschi et al. se contrastó la proporción de cepas VacA/s1m1 en 2 distintas áreas de alto y bajo riesgo del Departamento de Nariño (Colombia). El estudio concluyó que el genotipo citotóxico es más frecuente en la zona de alto riesgo p=0,04411. En relación al genotipo CagA, en la presente investigación no se demostró un riesgo mayor de desarrollar cáncer o displasia en pacientes con el genotipo CagA positivo. Estos resultados son similares a los reportados por Trujillo, pero difieren de las conclusiones reportadas por Citelly et al. y Sicinschi et al. Los estudios en mención muestran conclusiones contradictorias, no estiman magnitud de asociación y se enfocan en grupos poblacionales geográfica y culturalmente distintos al de nuestra población de estudio. Según el conocimiento de los autores, la presente investigación representa el primer estudio analítico que estima el riesgo de desarrollar adenocarcinoma y displasia evaluando las variantes genotípicas de H. pylori en una población del Cauca.
Es importante resaltar en nuestros resultados la presencia de intervalos de confianza relativamente amplios (especialmente para la variable edad). Lo anterior debido a que solo se documentaron cinco casos de displasia y cáncer en menores de 50 años y porque la aplicación estricta de los criterios de inclusión condicionó una reducción importante del número de participantes. No obstante, consideramos que los valores de p, los límites de los intervalos de confianza y las estimaciones obtenidas en el modelo multivariado permiten concluir que la edad y los genotipos VacA/s1m1 son variables que explican de manera parsimoniosa el riesgo de desarrollar displasia y cáncer. Para obtener estimaciones puntuales e intervalos de confianza más precisos, se recomienda en futuras investigaciones incluir un número mayor de pacientes con cáncer e incluir en el modelamiento multivariado otros factores de interés (por ejemplo, genotipos BabA, consumo de sal, hábitos alimentarios, entre otros).
En Colombia, a pesar de encontrarse zonas geográficas con prevalencias de infección por H. pylori similares, se han documentado tasas de incidencia de cáncer dispares. Este fenómeno ha sido llamado por algunos investigadores como el enigma colombiano3. Como una posible explicación del enigma se ha planteado la variabilidad genética del H. pylori y, aunque los hallazgos en nuestro estudio parecen brindar soporte a esta teoría, se deben considerar algunas limitaciones en nuestro estudio antes de llegar a esta conclusión. En este sentido, en la presente investigación la población se tomó de una misma región geográfica. Para precisar si la variabilidad genética del H. pylori influye en las diferencias geográficas de incidencia de cáncer, se sugiere realizar estudios comparativos de genotipificación en zonas de alto y bajo riesgo de cáncer. En el estudio de Trujillo et al.9 se planteó un diseño metodológico similar al sugerido, pero no se demostraron diferencias significativas entre los genotipos bacterianos en 2 zonas de Colombia con riesgo opuesto de cáncer. Por esta razón, se sugiere además que la selección de los pacientes en futuras investigaciones se complemente con análisis de ancestría genética toda vez que la población colombiana es bastante diversa desde el punto de vista genético. Los estudios de Kodaman et al. han mostrado la importancia de la composición ancestral de las poblaciones y las relaciones de co-evolución con la infección bacteriana30.
En conclusión, resulta plausible afirmar que los pacientes de sexo masculino, mayores a 50 años representan un grupo de mayor riesgo de cáncer gástrico. Dicho riesgo se puede potenciar con la presencia de variantes citotóxicas del VacA. Por esta razón, en pacientes con los genotipos VacA/s1m1 estaría justificado un seguimiento médico más estrecho. Esta información se propone para el desarrollo de una escala de riesgo de cáncer gástrico la cual permitiría lograr un diagnóstico oportuno de la enfermedad y optimizar el uso de recursos médicos sobre la población con mayor riesgo.
FinanciaciónEl presente trabajo ha sido financiado por el Programa de Salud de Colciencias de Colombia proyecto código 1103-519-29123.
Conflicto de interesesLos autores del presente artículo declaramos ningún conflicto de intereses.
Los autores expresan su agradecimiento al grupo de Genética Humana de la Universidad del Cauca por su apoyo en el desarrollo de esta investigación.