Los stents metálicos autoexpandibles (SEMS) son el tratamiento ideal de la obstrucción de salida gástrica maligna (OSGM) en pacientes con expectativa de vida corta, sin embargo, su disfunción es frecuente. El objetivo principal fue conocer los factores predictores de disfunción del SEMS en OSGM y los objetivos secundarios conocer el éxito técnico, éxito clínico y el impacto nutricional posterior al SEMS.
Material y métodosEstudio longitudinal, retrospectivo en el departamento de endoscopia gastrointestinal del Instituto Nacional de Cancerología de la Ciudad de México. Se incluyeron pacientes con diagnóstico de OSGM con colocación de SEMS de enero de 2015 a mayo de 2018. Utilizamos el sistema de puntuación de obstrucción de salida gástrica (GOOSS) para establecer éxito clínico y disfunción del SEMS.
ResultadosIncluimos 43 pacientes, el éxito técnico fue 97.7% (n=42) y el éxito clínico 88.3% (n=38). La disfunción del SEMS se presentó en el 30.2% (n=13), de estos pacientes en el 53.8% (n=7) la disfunción ocurrió en<6 meses posterior a su colocación. En el análisis univariado el subtipo histológico adenocarcinoma gástrico difuso (p=0.02) y uso de SEMS no cubiertos (p=0.02) fueron las variables asociadas a disfunción. La albúmina sérica y el índice de masa corporal (IMC) no aumentaron posterior al SEMS. El seguimiento medio fue 5.8 meses (1-24 meses).
ConclusionesLos SEMS tienen una adecuada eficacia técnica y clínica en el tratamiento de la OSGM. La disfunción del SEMS es frecuente y el tipo histológico cáncer gástrico difuso y el uso de SEMS no cubiertos parecen ser predictores de disfunción.
Self-expanding metallic stents (SEMS) are the ideal treatment for malignant gastric outlet obstruction (MGOO) in patients with a short life expectancy, but stent dysfunction is frequent. The primary aim of our study was to identify the predictive factors of SEMS dysfunction in MGOO and the secondary aim was to determine the technical success, clinical success, and nutritional impact after SEMS placement.
Material and methodsA retrospective, longitudinal study was conducted at the gastrointestinal endoscopy department of the Instituto Nacional de Cancerología in Mexico City. Patients diagnosed with MGOO that underwent SEMS placement within the time frame of January 2015 to May 2018 were included. We utilized the gastric outlet obstruction scoring system (GOOSS) to determine clinical success and SEMS dysfunction.
ResultsThe study included 43 patients, technical success was 97.7% (n=42), and clinical success was 88.3% (n=38). SEMS dysfunction presented in 30.2% (n=13) of the patients, occurring in<6 months after placement in 53.8% (n=7) of them. In the univariate analysis, the histologic subtype, diffuse gastric adenocarcinoma (p=0.02) and the use of uncovered SEMS (p=0.02) were the variables associated with dysfunction. Albumin levels and body mass index did not increase after SEMS placement. Medical follow-up was a mean 5.8 months (1-24 months).
ConclusionsSEMS demonstrated adequate technical and clinical efficacy in the treatment of MGOO. SEMS dysfunction was frequent and diffuse type gastric cancer and uncovered SEMS appeared to be dysfunction predictors.
La obstrucción de salida gástrica (OSG) es la obstrucción completa o incompleta del estómago distal, píloro o duodeno proximal, causada por una lesión obstructiva o compresión extrínseca. Las causas más frecuentes de OSG maligna (OSGM) son cáncer pancreático y gástrico con una incidencia del 15-25%1–4.
Anteriormente la gastro-yeyuno anastomosis (GYA) era el tratamiento estándar para la obstrucción de salida gástrica (OSG), sin embargo, la colocación endoscópica de SEMS permite reanudar la ingesta oral más rápido y una hospitalización más corta5,6, por lo que los SEMS se han convertido en el tratamiento ideal en pacientes con expectativa de vida corta, con múltiples estudios que confirman su eficacia y seguridad7–12, con éxito clínico del 77% al 94%12–25; sin embargo su disfunción se presenta hasta en el 26% de los pacientes26, causando frecuentes reintervenciones endoscópicas, aumentando costos y morbilidad, con pocos estudios que han reportado los factores que predicen la disfunción del SEMS en OSGM, como una puntuación de Karnofsky (PK) < 5026,27, carcinomatosis28, ascitis28,29 y expansión del SEMS<30%27, sin embargo no se han replicado dichos resultados en otros estudios similares.
El objetivo primario fue conocer los factores predictores de disfunción de los SEMS en pacientes con OSGM. Los objetivos secundarios fueron conocer el éxito técnico, el éxito clínico y el impacto nutricional posterior al SEMS.
Material y métodosSe realizó un estudio longitudinal, observacional, analítico, retrospectivo, durante el periodo de enero de 2015 a mayo de 2018 en el Departamento de Endoscopia Gastrointestinal del Instituto Nacional de Cancerología de la Ciudad de México.
PacientesSe incluyeron pacientes con diagnóstico de OSGM con enfermedad irresecable o en tratamiento paliativo en quienes se colocó un SEM.
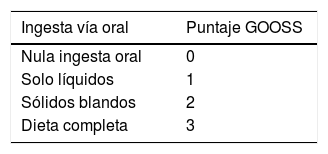
Los criterios de inclusión fueron pacientes mayores de 18 años, con obstrucción del estómago distal o duodeno evidenciado por endoscopia, causando dificultad para la ingesta oral con un GOOSS ≤ 2 (tabla 1), biopsias concluyentes de neoplasia maligna y que tuvieran tomografía axial computarizada, con la cual se evaluó la presencia de ascitis, carcinomatosis, metástasis a distancia y enfermedad irresecable. Los criterios de exclusión fueron pacientes embarazadas, perforación gastrointestinal, peritonitis, obstrucción distal a la OSGM, colocación de SEMS fuera del Instituto Nacional de Cancerología de la Ciudad de México, falta de expediente electrónico y seguimiento menor de 7 días.
TécnicaPara la colocación del SEMS se utilizó gastroscopio terapéutico Olympus GIF-1T140 y GIF-1TQ160. La localización y la longitud de la obstrucción se evaluaba endoscópicamente y fluoroscópicamente con medio de contraste, posteriormente se introducía una guía hidrofílica biliar a través de la estenosis y se introducía el SEMS a través de la guía, el cual se liberaba bajo visión endoscópica y fluoroscópica. La selección de la longitud del SEMS se realizó en función de la longitud de la estenosis, considerando mínimo 4 cm adicionales para asegurar 2 cm de stent previo y posterior a la estenosis. La selección del SEMS se realizó en función de la experiencia del endoscopista; fueron 4 endoscopistas con experiencia de más de 10 años en SEMS. Los 3 tipos de SEMS utilizados fueron WallFlex Duodenal (Boston Scientific), Wallstent duodenal (Boston Scientific) ambos SEMS no cubiertos (SEMS-NC) y Niti-S Pyloric/Duodenal (Taewoong Medical) SEMS parcialmente cubierto (SEMS-PC).
Medición y definición de las variablesUtilizamos sistema de puntaje de obstrucción de salida gástrica conocido como GOOSS por sus siglas en inglés (Gastric Outlet Obstruction Scoring System), el cual asigna puntos dependiendo del nivel de ingesta oral del paciente, permitiendo valorar de forma objetiva la habilidad de ingesta oral que presenta (tabla 1). El GOOSS fue creado en el año 2002 basándose en un sistema de puntaje que evalúa la ingesta oral en pacientes con disfagia maligna30, siendo actualmente la escala utilizada en múltiples estudios de OSGM26,27,29.
El éxito clínico se definió como un GOOSS≥2 después de 7 días de la colocación del SEMS. El éxito técnico se definió como un posicionamiento del SEMS preciso en el sitio de obstrucción. La disfunción del SEMS se definió como reaparición de síntomas de OSG con GOOSS<2 y SEMS con evidencia radiológica o endoscópica de crecimiento tumoral interno, colapsado, roto, migrado o alimento impactado. La duración de permeabilidad del SEMS se definió como el tiempo desde la colocación del SEMS hasta su disfunción, cuando no existió disfunción se consideró que la duración de la permeabilidad del SEMS fue igual a la sobrevida del paciente.
Se estudiaron las siguientes variables para predecir disfunción del SEMS: edad, sexo, órgano primario del cáncer, tipo histológico, localización de la obstrucción (antro, píloro, duodeno), longitud de la estenosis, tipo de obstrucción (intrínseca o extrínseca), PK, etapa clínica, ascitis, carcinomatosis, tipo de SEMS (marca comercial, SEMS-PC, SEMS-NC) y tratamiento adyuvante (quimioterapia y radioterapia posterior a la colocación de SEMS).
Se consideró estenosis intrínseca cuando se observó endoscópicamente tejido de aspecto tumoral que condicionara disminución de la luz gástrica o duodenal y estenosis extrínseca cuando endoscópicamente se observaba disminución de la luz gástrica o duodenal con mucosa normal.
Para evaluar el impacto nutricional de los SEMS en OSGM se consideró el IMC y la albúmina sérica previo y posterior al SEMS.
SeguimientoEl seguimiento se realizó a través del expediente electrónico hasta mayo de 2018, fallecimiento del paciente o pérdida del seguimiento.
Análisis estadísticoSe utilizó el programa SPSS versión 23; se realizó un análisis descriptivo con medidas de dispersión para las variables cuantitativas y se expresó mediante proporciones las variables cualitativas. Para el análisis inferencial utilizamos un modelo univariado mediante la prueba «t» de Student para las variables cuantitativas y la prueba Chi cuadrado para las variables cualitativas, teniendo como parámetro para alcanzar significación estadística un valor p<0.05 con intervalo de confianza del 95% (IC 95%).
Consideraciones éticasLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales. Se obtuvo consentimiento por escrito de todos los pacientes, preservándose en todo momento su anonimato. Este estudio fue aprobado por el Comité de Ética del Instituto Nacional de Cancerología de la Ciudad de México.
ResultadosSe evaluaron 45 pacientes y se excluyeron 2 pacientes, uno por seguimiento menor de 7 días y el segundo por falta de datos en el expediente electrónico. Se incluyeron 43 pacientes con diagnóstico de OSGM con colocación de SEMS.
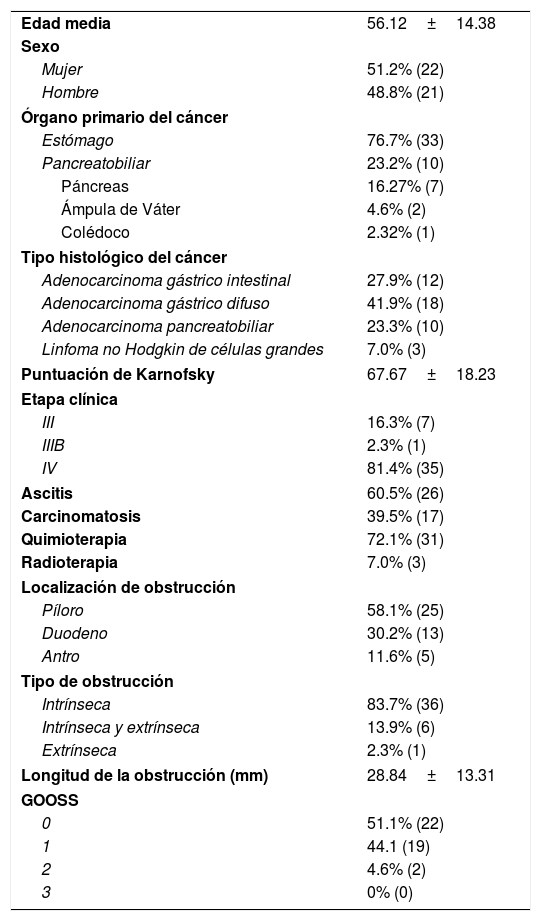
Características de los pacientesLas características demográficas y clínicas de los pacientes incluidos se muestran en la tabla 2. El 51.2% (n=22) fueron mujeres y el 48.8% (n=21) hombres; la edad media fue de 56.12±14.38 años. El órgano primario del cáncer fue el estómago en el 76.7% (n=33) y en 23.2% (n=10) fue pancreatobiliar (7 de páncreas, 2 ámpula de Váter y 1 de colédoco). El tipo histológico del cáncer fue adenocarcinoma gástrico difuso en el 41.9% (n=18), adenocarcinoma gástrico intestinal en el 27.9% (n=12), adenocarcinoma pancreatobiliar en el 23.3% (n=10) y linfoma no Hodgkin de células grandes 7.0% (n=3). La PK fue de 67.67±18.23. La etapa clínica fue III en el 16.3% (n=7), IIIB en el 2.3% (n=1) y IV en el 81.4% (n=35), el 60.5% (n=26) tenía ascitis y el 39.5% (n=17) carcinomatosis. La localización más frecuente de obstrucción fue el píloro en el 58.1% (n=25), seguida del duodeno en el 30.2% (n=13) y del antro en el 11.6% (n=5). El tipo de obstrucción fue intrínseca en el 83.7% (n=36), intrínseca y extrínseca en el 13.9% (n=6) y extrínseca en el 2.3% (n=1). La longitud de la obstrucción fue 28.84±13.31mm. Los SEMS que se utilizaron fueron: Wallflex 72.1%, Wallstent 14.0%, Niti-S 13.9%, de los cuales el 95.3% fueron SEMS-NC y 4.7% SEMS-PC. El 72.1% (n=31) recibió quimioterapia adyuvante y el 7.0% (n=3) radioterapia adyuvante. Siete pacientes tenían obstrucción biliar, requiriendo en 6 pacientes drenaje biliar endoscópico (por colangiopancreatografía retrógrada endoscópica o ultrasonido endoscópico) y un paciente drenaje biliar percutáneo.
Características demográficas y clínicas de los pacientes (n=43)
| Edad media | 56.12±14.38 |
| Sexo | |
| Mujer | 51.2% (22) |
| Hombre | 48.8% (21) |
| Órgano primario del cáncer | |
| Estómago | 76.7% (33) |
| Pancreatobiliar | 23.2% (10) |
| Páncreas | 16.27% (7) |
| Ámpula de Váter | 4.6% (2) |
| Colédoco | 2.32% (1) |
| Tipo histológico del cáncer | |
| Adenocarcinoma gástrico intestinal | 27.9% (12) |
| Adenocarcinoma gástrico difuso | 41.9% (18) |
| Adenocarcinoma pancreatobiliar | 23.3% (10) |
| Linfoma no Hodgkin de células grandes | 7.0% (3) |
| Puntuación de Karnofsky | 67.67±18.23 |
| Etapa clínica | |
| III | 16.3% (7) |
| IIIB | 2.3% (1) |
| IV | 81.4% (35) |
| Ascitis | 60.5% (26) |
| Carcinomatosis | 39.5% (17) |
| Quimioterapia | 72.1% (31) |
| Radioterapia | 7.0% (3) |
| Localización de obstrucción | |
| Píloro | 58.1% (25) |
| Duodeno | 30.2% (13) |
| Antro | 11.6% (5) |
| Tipo de obstrucción | |
| Intrínseca | 83.7% (36) |
| Intrínseca y extrínseca | 13.9% (6) |
| Extrínseca | 2.3% (1) |
| Longitud de la obstrucción (mm) | 28.84±13.31 |
| GOOSS | |
| 0 | 51.1% (22) |
| 1 | 44.1 (19) |
| 2 | 4.6% (2) |
| 3 | 0% (0) |
El éxito técnico de la colocación del SEMS fue 97.7% (n=42) y el éxito clínico 88.3% (n=38). En un paciente con obstrucción en el antro no se obtuvo éxito técnico inicialmente debido a que el SEMS fue liberado en el duodeno, sin embargo, en la misma endoscopia se colocó un segundo SEMS en el sitio de la obstrucción con éxito. El 95.3% (n=41) tenía un GOOSS de 0 o 1 previo al SEMS y posterior a la colocación del SEMS el 86% (n=37) tenía un GOOSS de 2 o 3 (tabla 3).
Disfunción de los stents metálicos autoexpandiblesLa disfunción del SEMS ocurrió en el 30.2% (n=13) de los pacientes, las características de estos pacientes fueron: 38.5% (n=5) hombres y 61.5% (n=8) mujeres, en la mayoría el órgano primario del cáncer fue estómago (92.3% [n=12]) y la histología más frecuente fue adenocarcinoma gástrico difuso (46.2% [n=6]), seguido de adenocarcinoma gástrico intestinal (23.1% [n=3]); la mayoría estaba en etapa clínica IV (92.3% [n=12]), el 76.9% (n=10) tenía ascitis y el 38.5% (n=5) tenía carcinomatosis. El sitio de obstrucción más frecuente fue el píloro (76.9% [n=10]), seguido del duodeno (15.4% [n=2]). El 92% tenía obstrucción intrínseca (n=12) y el 7.6% obstrucción extrínseca e intrínseca (n=1), el tipo de SEMS fue Wallflex en el 69.2% (n=9) y en el 84.6% (n=11) se utilizó SEMS-NC. La mayoría recibió quimioterapia adyuvante (84.6% [n=11]) y solo el 7.7% (n=1) recibió radioterapia adyuvante.
La causa de disfunción del SEMS (tabla 4) fue crecimiento tumoral en el 92.3% (n=12), alimento impactado en el 7.6% (n=1) y falta de expansión con angulación en el 7.6% (n=1); un paciente tuvo 2 causas de disfunción del SEMS (crecimiento tumoral con alimento impactado). La resolución de la disfunción del SEMS se logró en el 53.8% (n=7), y el método de resolución fue colocación de otro SEMS en 3 pacientes, electrocoagulación con argón plasma en 2 pacientes y dilatación con balón en 2 pacientes. En el grupo de pacientes que no hubo resolución de la disfunción del SEMS ocurrió lo siguiente: en 2 pacientes no se intentó la resolución endoscópica y en 3 pacientes se utilizó argón plasma, el cual fue fallido, y se colocó sonda nasoyeyunal.
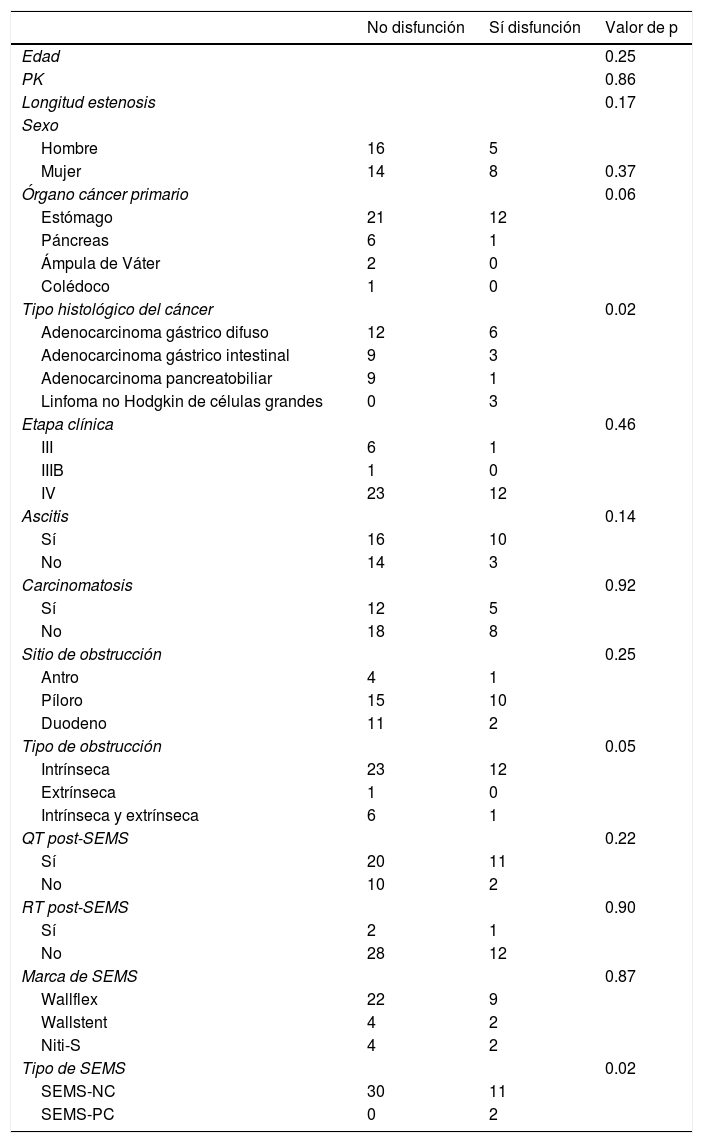
En el análisis univariado (tabla 5) el subtipo histológico adenocarcinoma gástrico difuso (p=0.02) y los SEMS-NC (p=0.02) fueron las variables con significación estadística asociadas a disfunción del SEMS. Además, mostraron una tendencia a ser predictores significativos para disfunción del SEMS, el estómago como órgano primario del cáncer (p=0.60) y tipo de obstrucción intrínseca (p=0.57).
Análisis univariado de factores asociados con disfunción del SEMS
| No disfunción | Sí disfunción | Valor de p | |
|---|---|---|---|
| Edad | 0.25 | ||
| PK | 0.86 | ||
| Longitud estenosis | 0.17 | ||
| Sexo | |||
| Hombre | 16 | 5 | |
| Mujer | 14 | 8 | 0.37 |
| Órgano cáncer primario | 0.06 | ||
| Estómago | 21 | 12 | |
| Páncreas | 6 | 1 | |
| Ámpula de Váter | 2 | 0 | |
| Colédoco | 1 | 0 | |
| Tipo histológico del cáncer | 0.02 | ||
| Adenocarcinoma gástrico difuso | 12 | 6 | |
| Adenocarcinoma gástrico intestinal | 9 | 3 | |
| Adenocarcinoma pancreatobiliar | 9 | 1 | |
| Linfoma no Hodgkin de células grandes | 0 | 3 | |
| Etapa clínica | 0.46 | ||
| III | 6 | 1 | |
| IIIB | 1 | 0 | |
| IV | 23 | 12 | |
| Ascitis | 0.14 | ||
| Sí | 16 | 10 | |
| No | 14 | 3 | |
| Carcinomatosis | 0.92 | ||
| Sí | 12 | 5 | |
| No | 18 | 8 | |
| Sitio de obstrucción | 0.25 | ||
| Antro | 4 | 1 | |
| Píloro | 15 | 10 | |
| Duodeno | 11 | 2 | |
| Tipo de obstrucción | 0.05 | ||
| Intrínseca | 23 | 12 | |
| Extrínseca | 1 | 0 | |
| Intrínseca y extrínseca | 6 | 1 | |
| QT post-SEMS | 0.22 | ||
| Sí | 20 | 11 | |
| No | 10 | 2 | |
| RT post-SEMS | 0.90 | ||
| Sí | 2 | 1 | |
| No | 28 | 12 | |
| Marca de SEMS | 0.87 | ||
| Wallflex | 22 | 9 | |
| Wallstent | 4 | 2 | |
| Niti-S | 4 | 2 | |
| Tipo de SEMS | 0.02 | ||
| SEMS-NC | 30 | 11 | |
| SEMS-PC | 0 | 2 | |
El tiempo de permeabilidad de los SEMS en el grupo de pacientes que disfuncionaron fue 5.4±3.5 meses y en 7 pacientes la disfunción ocurrió en<6 meses posterior a su colocación.
Impacto nutricionalEl IMC previo al SEMS fue 20.6±3.2kg/m2 y posterior al SEMS 20.7±3.3kg/m2. La albúmina sérica previo al SEMS fue 3.23±0.62g/dl y posterior al SEMS 3.05±0.64g/dl. Se realizó un subanálisis de los pacientes con sobrevida mayor de un mes posterior a la colocación del SEMS, incluyendo 28 pacientes en quienes el IMC previo al SEMS fue 19.7±2.8kg/m2 y posterior al SEMS 20.2±3.2kg/m2, la albúmina previo al SEMS fue 3.27±0.60g/dl y posterior al SEMS 3.09±0.59g/dl.
El seguimiento medio fue de 5.8 meses (1-24meses).
Discusión y conclusionesEn nuestro estudio reportamos un éxito técnico del 97.7% y éxito clínico del 88.3%, similar a lo reportado por otros estudios12–27; la disfunción del SEMS en nuestro estudio fue de 30.2%, una frecuencia mayor a la reportada por otros estudios, sin embargo solo en 7 pacientes (16.2%) el SEMS disfuncionó antes de 6 meses posterior a su colocación, es decir, antes de la vida media esperada del SEMS, lo que corresponde a una frecuencia similar a la reportada por Yamao et al.26 en su estudio retrospectivo de 278 pacientes con OSGM con una disfunción del SEMS del 16.6%. Un estudio de Tringali et al.12, con 108 pacientes con OSGM, reportó permeabilidad del SEMS a 14 días en el 94.6% de los pacientes, y la estimación de la permeabilidad del SEMS con Kaplan-Meier fue 92.9% a un mes, 86.2% a 2 meses, 81.9% a 3 meses y 63.4% a 6 meses, similar a nuestro estudio, en el cual a 6 meses el 69.8% de los pacientes permanecía con permeabilidad del SEMS.
En nuestro estudio el crecimiento tumoral fue la principal causa de disfunción de los SEMS (92.3%), similar a lo reportado por múltiples estudios25, y la resolución endoscópica de la disfunción del SEMS en nuestro estudio se logró en el 63.8%, lo que indica que a pesar de una alta frecuencia de disfunción, la reintervención endoscópica generalmente es factible y exitosa para restablecer la permeabilidad del SEMS.
Los factores que predicen la disfunción del SEMS en OSGM son poco comprendidos, con resultados contradictorios en los estudios publicados. Yamao et al.26, en 278 pacientes con OSGM, reportaron como predictores de disfunción del SEMS una PK<50 (p<0.01). Sato et al.28 reportaron la PK, la diseminación peritoneal y la ascitis como factores predictores de ineficacia clínica del SEMS. Sasaki et al.29, en un estudio retrospectivo de 97 pacientes con OSGM, reportaron la PK<50 y la ascitis como factores predictores de restricción de la ingesta oral de sólidos. Mendelsohn et al.14 concluyeron que la ascitis no debe ser una contraindicación para SEMS duodenal, ya que el éxito clínico del SEMS en pacientes con carcinomatosis fue del 81%. En nuestro estudio encontramos que el tipo histológico cáncer gástrico difuso y el uso de SEMS-NC son predictores para disfunción del SEMS en OSGM. Una explicación de nuestros resultados es que el cáncer gástrico difuso, al infiltrar la submucosa y muscular, condiciona menor distensibilidad gástrica y afección de la motilidad gástrica, favoreciendo un estómago retencionista. Respecto a los SEMS-NC como predictor de disfunción esto puede estar en relación con que el crecimiento tumoral interno fue la principal causa de disfunción de los SEMS.
Múltiples estudios han comparado SEMS-C y SEMS-NC para la paliación de OSGM. Hori et al.27, en un estudio retrospectivo de 126 pacientes con SEMS-NC y 126 pacientes con SEMS-C, mostraron crecimiento tumoral más frecuente en SEMS-NC (SEMS-NC 11.90% vs. SEMS-C 0.79%; p=0.002) y migración del SEMS más frecuente con SEMS-C (SEMS-C 8.73% vs. SEMS-NC 0.79%; p=0.005), la PK (p=0.04), ausencia de ascitis (p=0.02) y una expansión insuficiente del SEMS (<30%) (p=0.003) fueron significativamente asociados con crecimiento tumoral interno en SEMS-NC, mientras que un SEMS de longitud corta (p=0.05) y quimioterapia (p=0.03) fueron predictores de migración de SEMS-C, concluyendo que los SEMS-NC pueden ser una buena opción en pacientes recibiendo quimioterapia, y los SEMS-C largos pueden ser mejor en pacientes en buenas condiciones generales. Lim et al.31, en un estudio prospectivo aleatorizado en 120 pacientes con OSGM, compararon SEMS-C vs. SEMS-NC; el grupo de SEMS-NC tuvo mayor frecuencia de crecimiento tumoral interno (18.0% vs. 3.4%; p<0.02), mayor crecimiento tumoral externo (3.4% vs. 3.3%; p<0.99) y menor migración del SEMS (0% vs. 13.6%; p<0.01). Un estudio prospectivo aleatorizado en 80 pacientes con OSGM mostró que los SEMS-NC tuvieron mayor frecuencia de crecimiento tumoral (25.0% vs. 0%; p<0.01) y menor frecuencia de migración en 8 semanas (25.8% vs. 2.8%; p<0.01)32. Yamao et al.26 reportaron en un estudio de 278 pacientes que los SEMS-NC no predijeron crecimiento tumoral, pero los SEMS-C sí predijeron migración (p<0.01). En un metaanálisis que incluyó 849 pacientes con OSGM, reportaron no diferencias significativas en permeabilidad y tasa de reintervención entre el grupo SEMS-C y SEMS-NC, sin embargo los SEMS-C se asociaron con una mayor tasa de migración (RR: 3.48, IC 95%: 2.16-5.62, p<0.00001) y una tasa de obstrucción menor (RR: 0.42, IC 95%: 0.24-0.73, p=0.002)33. La discrepancia entre los estudios puede estar relacionada con los diferentes SEMS utilizados o la selección de pacientes, por lo que es necesario estudios de mayor calidad que comparen SEMS-C y SEMS-NC en OSGM. En nuestro estudio se utilizaron pocos SEMS-PC y ningún SEMS-C, por lo que no fue posible observar y evaluar la migración del SEMS como causa de disfunción.
Una de las principales metas en el paciente con OSGM irresecable o paliativo, es mantener una adecuada nutrición idealmente vía oral, ya que esto es un importante indicador de calidad de vida. La GYA proporciona una reducción efectiva de los síntomas obstructivos y permite la reanudación de la ingesta oral; sin embargo, la paliación quirúrgica conlleva riesgos significativos de morbilidad y mortalidad, con reportes de morbilidad de hasta el 15.7% y mortalidad hasta del 6.5%, siendo mayor cuando se combina con bypass biliar34. Los SEMS son menos invasivos, la ingesta oral mejora más rápido y se asocian a menos días de hospitalización35,36; sin embargo, la GYA puede ser mejor en pacientes con expectativa de vida mayor a 3 meses, en los que se identifiquen múltiples predictores de disfunción del SEMS.
En el aspecto nutricional, en nuestro estudio la albúmina sérica previo al SEMS fue 3.23±0.62g/dl y post SEMS 3.05±0.64g/dl, el IMC previo al SEMS fue 20.6±3.2kg/m2 y post SEMS 20.7±3.3kg/m2. Esto sugiere que los SEMS no tiene un impacto en la ganancia de peso o mejoría de albúmina sérica del paciente, sin embargo parece ser que los SEMS permiten mantener el peso y la albúmina inicial del paciente, lo cual se considera un punto relevante en la calidad de vida del paciente oncológico paliativo. Debemos considerar que la mayoría de los pacientes tenían ascitis, lo que puede aumentar progresivamente el peso del paciente sin poder discernir en qué pacientes la ganancia de peso es debido a una mejor ingesta oral o a un aumento de ascitis.
Las limitaciones de nuestro estudio son que no es un estudio aleatorizado, tiene un diseño retrospectivo y la inclusión de pocos pacientes, lo que disminuye su poder estadístico.
En conclusión, los SEMS son un tratamiento efectivo para la paliación de la OSGM, con adecuada eficacia técnica y clínica. La disfunción del SEMS es frecuente, sin embargo la resolución endoscópica se logra en la mayoría de los pacientes, el tipo histológico cáncer gástrico difuso y el uso de SEMS-NC parecen ser predictores de disfunción. Estos predictores pueden servir para realizar una mejor selección del paciente para SEMS, aunque faltan estudios grandes y de mayor calidad metodológica para establecer los factores predictores de disfunción del SEMS en OSGM.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.