La palabra amiloidosis hace referencia a un hallazgo patológico, que abarca un espectro heterogéneo de etiologías y presentaciones clínicas. La principal característica de la amiloidosis es el depósito de fragmentos de proteínas extracelulares insolubles dentro de varios órganos, doblados anormalmente de tal manera que los hace resistentes a la digestión1. Estos depósitos afectan tanto la estructura como la función de los órganos comprometidos.
Dentro del tracto gastrointestinal, el depósito de amiloide se produce en la muscularis mucosae, muy cerca de la vasculatura, los nervios y los plexos nerviosos2. Esta deposición aumenta la fragilidad de los vasos sanguíneos, dificulta la peristalsis intrínseca y disminuye la distensibilidad de la pared intestinal3. Esto explica los síntomas de la amiloidosis gastrointestinal que incluyen pérdida de peso, diarrea, dolor abdominal, malabsorción, reflujo esofágico y diversos grados de hemorragia digestiva superior e inferior4,5, siendo el sangrado severo una presentación muy infrecuente5. A continuación, se presenta el caso de un paciente con evidencia de amiloidosis gástrica, quien presenta sangrado gastrointestinal.
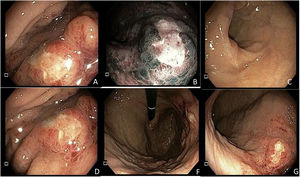
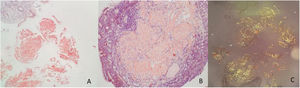
Se trata de un hombre de 59 años, sin antecedentes médicos de importancia, quien consulta en dos ocasiones al servicio de urgencias, por siete días de dolor epigástrico, melenas, diaforesis y disnea. En la valoración inicial evidencian anemia (hemoglobina: 9.7 g/dl), hemodinámicamente estable, por lo que se decide manejo ambulatorio con omeprazol oral. Reconsulta a las 48 horas por hematoquecia. Le realizan endoscopia de vías digestivas altas, en la que se identifica lesión elevada de 10 x 10 mm de aspecto neoplásico en cuerpo, hacia la curvatura mayor, con mucosa circundante de aspecto infiltrado (fig. 1). Se tomaron múltiples biopsias, con depósito de material extracelular e intersticial rosado pálido de aspecto hialino grueso y craquelado, el cual con la coloración de Rojo Congo se observa de color rosado salmón y con luz polarizada muestra birrefringencia verde manzana (fig. 2).
Endoscopia de vías digestivas altas con lesión de 10 mm x 10 mm de aspecto neoplásico en cuerpo hacia curvatura mayor. Figura 1A. Lesión en curvatura mayor bajo luz directa elevada con centro deprimido, de bordes irregulares, París 0-IIa + 0-IIc. Figura 1B. Lesión con superficie trabecular, con áreas ramificadas e irregulares, de color heterogéneo y patrón vascular con áreas que presentan vasos amputados bajo NBI (imagen de banda estrecha) en curvatura mayor del cuerpo gástrico. Figura 1C. Antro gástrico sin lesiones endoscópicamente evidentes. Figura 1D. Lesión visualizada desde la curvatura menor sin magnificación. Figura 1F. Retroflexión gástrica en la que se observa la lesión y fondo gástrico con mucosa normal. Figura 1G. Visión directa de todo el cuerpo gástrico.
Biopsia de lesión gástrica en curvatura mayor. Figuras 2 A y 2 B. Material proteináceo extracelular, craquelado o fisurado, color salmón, acelular. Tinción Rojo Congo positiva que corresponde a material amiloide. Figura 2C. Luz polarizada, birrefringencia verde manzana.
En conjunto con el servicio de hematología se evaluó la posibilidad de amiloidosis secundaria, sin evidenciarse un pico monoclonal. Llamó la atención un discreto aumento de las cadenas Kappa respecto a Lambda en valores no compatibles con amiloidosis AL (amiloide derivado de la cadena ligera de inmunoglobulina), por lo que se concluye que tiene un amiloidoma gástrico único. En junta multidisciplinaria se decide manejo conservador con inhibidor de bomba de protones (IBP) y seguimiento endoscópico. A las ocho semanas se realiza seguimiento endoscópico con mejoría de la lesión inicial, biopsias de control nuevamente compatibles con amiloidoma sin cambios respecto a las previas. Se realiza ultrasonografía endoscópica en la que no hay evidencia de compromiso de capas profundas, presencia de adenopatías perilesionales, ni masas subepiteliales. A los siete meses de seguimiento la evolución del paciente es favorable, sin nuevos episodios de sangrado gastrointestinal y con última endoscopia de hace cuatro semanas sin cambios en la lesión descrita previamente.
La presentación de esta entidad en el tracto gastrointestinal suele ser sistémica. La amiloidosis gastrointestinal localizada sin evidencia de compromiso de otros órganos o una discrasia de células plasmáticas asociada es rara y no suele provocar la muerte6. El caso reportado entra dentro de las estadísticas publicadas de otros países, en lo que se diagnosticó un amiloidoma circunscrito al sistema gastrointestinal. En una revisión retrospectiva de 2,334 pacientes con amiloidosis que fueron evaluados en un único centro de referencia durante un período de 13 años, el 3.3% de los casos tenían una afectación del tracto gastrointestinal comprobada por biopsia7. De estos, solo el 21% tenía amiloidosis restringida al tracto gastrointestinal.
La terapia varía significativamente dependiendo de la causa y el tipo de proteína amiloide depositada en los tejidos. Las complicaciones gastrointestinales se tratan con control sintomático. La amiloidosis localizada se caracteriza por el depósito de amiloide AL restringido al tracto gastrointestinal. Para aquellos pacientes asintomáticos, no se requiere de ninguna intervención y la observación es fundamental. Sin embargo, los pacientes con síntomas recurrentes o severos pueden requerir cirugía para escisión localizada del tejido comprometido8. El reto es decidir qué pacientes son aptos para seguimiento y cuales se benefician de una intervención quirúrgica temprana. En el caso que presentamos se realizó un análisis con diferentes especialistas y se definió que se beneficiaba de manejo conservador expectante. Lo anterior, debido a que el compromiso gástrico del paciente era muy extenso y de ser llevado a cirugía requeriría una gastrectomía subtotal, que es un procedimiento mayor, con una tasa importante de complicaciones. Se tomó en consideración la evolución favorable con el manejo sintomático con IBP, la no recurrencia de sangrado y su estado asintomático actual. Los resultados del seguimiento hasta ahora han sido favorables.
Consideraciones éticasPara la elaboración del presente documento se firmó consentimiento informado por parte del paciente. No fue requerida la aprobación del Comité de Bioética de la Pontificia Universidad Javeriana y de acuerdo con la Declaración de Helsinki y en la Resolución 008430 de octubre 4 de 1993, la publicación presentada se considera como investigación sin riesgo.
FinanciaciónPara la elaboración del presente artículo no se recibió patrocinio de ninguna de las instituciones participantes
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.