Introducción
En la actualidad se encuentran disponibles mejores estrategias para el manejo de los pacientes con actividad grave y refractaria de la colitis ulcerosa crónica idiopática (CUCI) que consisten en nuevos fármacos inmunomoduladores, además de la terapia biológica dirigida al bloqueo de vías infl amatorias, en particular contra el factor de necrosis tumoral alfa.
El objetivo del presente trabajo es dar a conocer la experiencia con ciclosporina oral en microemulsión como tratamiento inicial en dos pacientes con CUCI grave refractaria a esteroides intravenosos, según la escala de Truelove-Witts.
Casos clínicos
Caso 1
Hombre de 40 años con historia de tabaquismo desde los 22 años. CUCI con afectación distal de seis años de evolución. De manera intermitente tuvo cuadros de actividad moderada a grave, que al principio recibieron tratamiento ambulatorio con 4.5 g/día de mesalacina y prednisona con dosis mayores de 20 mg/día. Se agregó azatioprina a dosis de 100 mg/día, equivalente a 1.5 mg/kg/día. Presentó dos brotes que requirieron hospitalización, y en los mismos se recurrió a los esteroides intravenosos con mejoría.
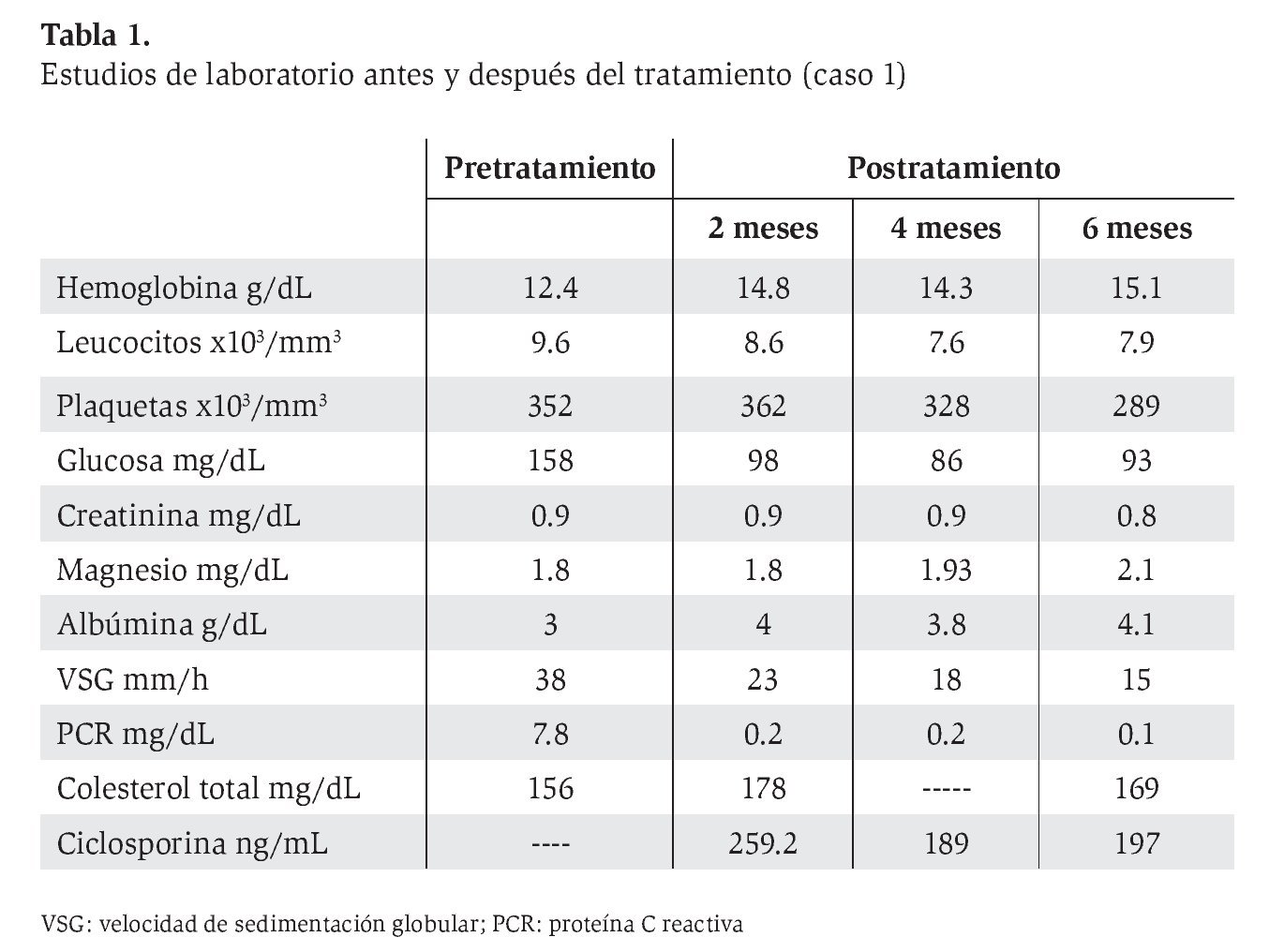
Acudió por cuadro grave con dolor abdominal sin irritación peritoneal, anemia, fiebre de 39 ºC y diarrea con rectorragia y 8 a 10 evacuaciones al día. La placa simple de abdomen en dos posiciones, exámenes de laboratorio, hemocultivo, urocultivo y coprocultivo arrojaron resultados negativos. Se realizó rectosigmoidoscopía flexible, durante la cual se observó actividad grave grado III de la Clínica Mayo19 y se tomaron muestras para biopsia, que mostró CUCI con actividad grave y descartó presencia de citomegalovirus (CMV). La toxina A de Clostridium difficiley la ameba en fresco resultaron negativas. Se inició tratamiento con 100 mg IV cada ocho horas de hidrocortisona, 4.5 g/día de mesalacina y la azatioprina se incrementó a 150 mg/día. Los valores basales de proteína C reactiva (PCR) fueron de 7.83 mg/dL, los de magnesio de 1.8 mg/dL y el colesterol total de 156 mg/dL. Tras cinco días de tratamiento con esteroides intravenosos, continuó con 6 a 8 evacuaciones y rectorragia. Se decidió iniciar microemulsión de ciclosporina oral con 1.7 mL cada 12 horas. Después de 24 horas de tratamiento disminuyeron las evacuaciones, mejoró el dolor abdominal y se egresó con tratamiento a base de 40 mg/día de prednisona, 150 mg/día de azatioprina, 4.5 g/día de mesalacina y 1.7 mL cada 12 horas de ciclosporina (3 mg/kg). Se siguió por consulta externa cada mes. Al segundo mes desarrolló diabetes mellitus secundaria a esteroides que se manejó con la combinación de sulfonilurea y biguanida. La PCR, la velocidad de sedimentación globular y la concentración de hemoglobina mejoraron en forma significativa (Tabla 1). La glucemia se controló tras la disminución gradual de esteroides. Al sexto mes se encontró asintomático, se retiraron la prednisona y la ciclosporina, pero se lo mantuvo en vigilancia en la consulta externa con remisión completa de la CUCI.
Caso 2
Hombre de 43 años, con historia de tabaquismo desde los 14 años, ingesta de alcohol ocasional. Bajo tratamiento médico antihipertensivo con captopril, a dosis de 25 mg tres veces al día desde 2006 con buen control.
Se estableció el diagnóstico de CUCI de 7 años de evolución con pancolitis y tratamiento con mesalacina y 30 mg/día vía oral de prednisona en dosis descendente por espacio de tres meses hasta suspender. Se mantuvo en remisión de 2003 a 2005, en que presentó un nuevo brote de actividad moderada. Requirió azatioprina adyuvante y se logró la mejoría de los síntomas. Suspendió el tratamiento con azatioprina tres meses antes del nuevo brote. Se ingresó con ligero dolor abdominal y evacuaciones con rectorragia 10 a 12 veces al día. Inició tratamiento con 100 mg de hidrocortisona intravenosa cada ocho horas, 4.5 g/día de mesalazina e incremento de azatioprina a 100 mg/día (equivalente a 1.5 mg/kg/día). Se realizó rectosigmoidoscopia flexible y se encontró actividad grave grado III de la clínica Mayo;19 también se tomaron muestras para biopsia. La ameba en fresco y la toxina A de Clostridium difficile resultaron negativas. La biopsia reportó CUCI con actividad grave, sin inclusiones de CMV. Después de cinco días de tratamiento continuó con una rectorragia de 6 a 8 evacuaciones e incremento del dolor abdominal. Se obtuvieron valores basales de PCR, magnesio y colesterol total. Se inició microemulsión de ciclosporina a dosis de 1.5 ml cada 12 horas. Tras 36 horas de tratamiento disminuyó la rectorragia hasta desaparecer. Egresó con tratamiento de 40 mg/d de prednisona, 125 mg/d de azatioprina, 2 g/d de mesalacina y 1.9 mL cada 12 horas de ciclosporina (3 mg/kg). Se siguió con frecuencia mensual en consulta externa y a los 6 meses de tratamiento con ciclosporina mostró mejoría clínica y de laboratorio. Se suspendió la prednisona y la ciclosporina.
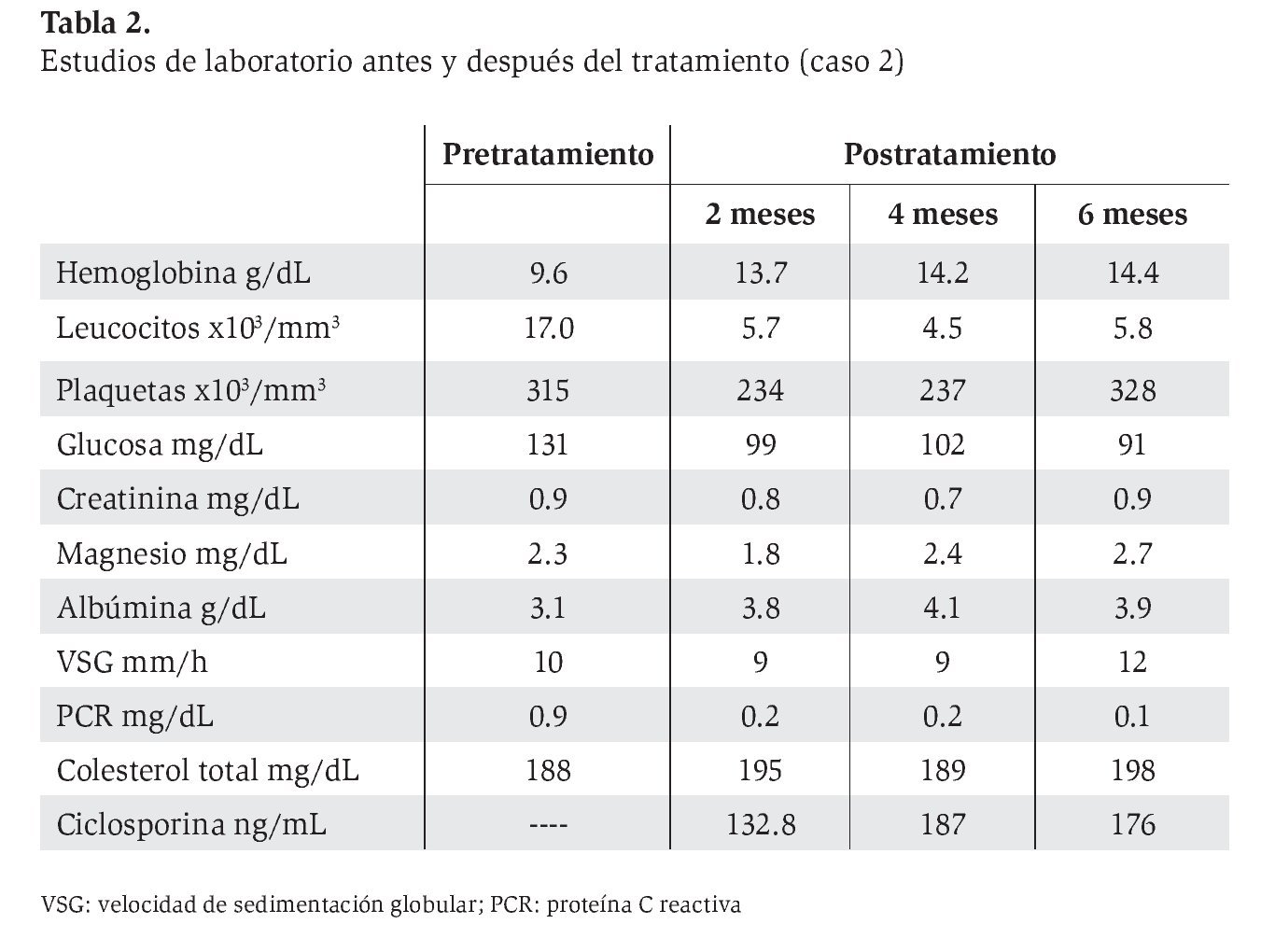
En la actualidad, la enfermedad sigue en remisión. En la Tabla 2 se muestran los parámetros de laboratorio previos y posteriores al tratamiento.
Discusión
Alrededor de 15% de los pacientes con CUCI tiene algún ataque grave que requiere hospitalización para tratamiento con esteroides intravenosos.1 Por falta de respuesta al tratamiento médico, 25% a 35% requieren proctocolectomía. Por tradición, los esteroides intravenosos (hidrocortisona, 200-400 mg/día, o metilprednisolona, 40-60 mg/día) se han utilizado como terapia de primera línea en casos graves o en casos de falta de respuesta a la terapia con esteroides orales a dosis máxima.2 De no obtener mejoría entre el tercer y quinto día de terapia con esteroides intravenosos y antes de la realización de proctocolectomía, se debe considerar el uso de ciclosporina a dosis de 2 a 4 mg/kg/ día o infliximab, 5 mg/kg.3-5 En pacientes sin respuesta a los esteroides intravenosos, la tasa de requerimiento de proctocolectomía puede llegar a ser hasta de 23%.6,7 El uso de ciclosporina intravenosa por 7 a 10 días puede reducir la necesidad de protocolectomía hasta en 80% de los casos, en especial cuando se utiliza ciclosporina oral y análogos de la purina como terapia de mantenimiento, pero pese a ello, la tasa de proctocolectomía es de 20% a 35% al año y 40% a los 4 años.8-11 La ciclosporina en microemulsión para administración oral puede ser tan efectiva como la terapia estándar de ciclosporina para administración intravenosa en pacientes con cuadros graves y refractarios a los esteroides.12,13 Los eventos adversos más comunes son hipertensión arterial, convulsiones, parestesias, temblor, cefalea, hiperplasia gingival, hipertricosis, trastornos electrolíticos, infecciones oportunistas, anafilaxis y nefrotoxicidad. Se recomienda la vigilancia estrecha con biometría hemática, electrólitos séricos, pruebas de función renal y hepática así como determinar los niveles séricos de ciclosporina.14,15 El nivel sérico de ciclosporina debe mantenerse entre 100 ng/mL y 200 ng/mL, dosis que parecen ser igual de efectivas en la fase de mantenimiento. La dosis recomendada es de 4 a 8 mg/kg/día y puede modificarse a 0.5 mg/kg a 1 mg/kg para conseguir los niveles requeridos.16 La ciclosporina oral se ha utilizado como puente para el uso posterior de inmunomoduladores y como terapia de mantenimiento por 3 a 6 meses en los pacientes respondedores.
La experiencia reportada en estos dos casos y lo publicado en la literatura permiten concluir que la terapia con ciclosporina oral puede ser una opción terapéutica para inducir la remisión de cuadros de CUCI grave refractarios a tratamiento con esteroides IV a dosis convencionales, y evitar la colectomía en pacientes con cuadros graves refractarios a la terapia convencional.
Correspondencia: Dr. Enrique Coss Adame,
Departamento de Gastroenterología, Instituto Nacional de Ciencias Médicas y Nutrición Salvador
Zubirán, Vasco de Quiroga 15, Colonia Sección XVI, Delegación Tlalpan, C.P. 14000, México, D. F.;
Tel: (+5255) 5573 3418. Fax: (+5255)5655 0942-
Correo electrónico: ecossmex@hotmail.com