La hepatitis viral aparece más frecuentemente al nacer o durante la infancia y es una enfermedad cuyas vías de transmisión incluyen lágrimas, bilis, fluidos sexuales, sudor, leche, orina, heces y saliva. El objetivo del presente estudio fue analizar la especificidad de la inmunocromatografía y la prueba ELISA para el antígeno de superficie de hepatitis B y compararlas con la prueba PCR.
Materiales y métodosLa muestra estuvo compuesta por 140 hombres y 60 mujeres referidos al hospital de la Escuela de Medicina de la Universidad de Urmia para diagnóstico de VHB por medio de prueba PCR. La prueba ELISA fue realizada con el kit de la Pioneer Medicine Company (Teherán, Irán).
ResultadosLos resultados de la prueba rápida HBsAg y de la prueba ELISA fueron comparados con la prueba de PCR. La prueba rápida de HBsAg tuvo una sensibilidad del 97% y especificidad del 91%, mientras que la prueba ELISA tuvo una sensibilidad del 78% y especificidad del 76%.
Discusión y conclusiónDe acuerdo con nuestros resultados, la prueba de inmunocromatografía fue precisa para diagnosticar HBsAg en sangre y la prueba ELISA tuvo sensibilidad y especificidad aceptables en comparación con la prueba de PCR.
Viral hepatitis, which appears most frequently at birth or during childhood, is a disease whose transmission routes include tears, bile, sexual fluids, sweat, milk, urine, feces, and saliva. The aim of the present study was to analyze the specificity of the immunochromatographic and ELISA diagnostic tests for hepatitis B surface antigen and compare them with PCR testing.
Materials and methodsThe study sample was made up of 140 men and 60 women referred to the Urmia Medical University hospital to undergo PCR testing for HBV diagnosis. The ELISA test was performed using the Pioneer Medicine Company kit (Tehran, Iran).
ResultsThe results of the HBs-Ag rapid test and the ELISA test were compared with the PCR test. The HBs-Ag rapid test had 97% sensitivity and 91% specificity, whereas the ELISA test had 78% sensitivity and 76% specificity.
Discussion and conclusionAccording to our results, the immunochromatographic test was accurate for diagnosing HBs-Ag in blood and the ELISA test had acceptable sensitivity and specificity, compared with PCR testing.
La presencia de antígeno de superficie de hepatitis B (HBsAg), y el DNA del virus de la hepatitis B (VHB) implican enfermedad infecciosa por el VHB. Los niveles altos de VHB y ADN y niveles bajos de aminotransferasas indican una respuesta débil del sistema inmunitario al virus. Los niveles altos en plasma o suero del tipo IgM de antivirus de hepatitis C y HBsAg indican una hepatitis aguda o la reactivación de una infección crónica por VHB, mientras que los niveles bajos indican infecciones inmunitarias previas1–3. Los niveles séricos de enzimas hepáticas son los factores bioquímicos más importantes para diagnosticar la infección crónica por VHB4 y el ensayo inmunoabsorbente ligado a enzimas (ELISA, por sus siglas en inglés), durante el cual sucede la reacción, con base en una interacción primaria antígeno-anticuerpo, es el método serológico más ampliamente utilizado para identificar antígenos y anticuerpos de VHB en los países desarrollados. Los avances en métodos diagnósticos proporcionan nuevas oportunidades para mejorar tamizaje, referencias y tratamiento. Estudios previos sobre infección por VHB se han concentrado en respuestas inmunitarias, vigilancia de cirrosis y tratamiento. Un gran número de métodos categorizados como procedimiento de inmunoanálisis enzimático (EIA, por sus siglas en inglés) se benefician de anticuerpos que pueden funcionar como factores de identificación5. Las desventajas de la prueba ELISA son la extensa duración temporal que conlleva, que requiere equipo sofisticado y técnicos capacitados, y suministro constante de electricidad. Además, las mutaciones de moléculas de anticuerpos y antígenos reducen la sensibilidad diagnóstica del método6. Los pacientes negativos para HBsAg son portadores de mutaciones en la región del gen S, lo que incapacita la habilidad de producir HBsAg. Debido a su alta sensibilidad y especificidad, los métodos EIA cuantitativos son los de uso más frecuente en hospitales de referencia y centros de transfusión sanguínea. La prueba de inmunocromatografía es una prueba cualitativa para detectar presencia de HBsAg en suero, plasma y sangre, y se utiliza cuando no existe la posibilidad de realizar un EIA7,8. Los métodos de reacción en cadena de la polimerasa (PCR, por sus siglas en inglés) se aplican como el estándar de oro en la mayoría de los centros médicos de investigación y diagnóstico avanzados. El proceso de replicación de ADN es utilizado cuantitativamente para evaluar la presencia de VHB por medio del aislamiento del ADN viral y replicándolo con cebadores oligonucleótidos9,10. Es muy importante comprender el concepto de índices de evaluación de pruebas diagnósticas en consideración de la amplia utilización de pruebas diagnósticas en procedimientos médicos. El objetivo del presente estudio fue comparar la cromatografía, la PCR y la ELISA, para determinar cuál método de prueba resultaba superior en la práctica médica.
Materiales y métodoSe utilizó el suero de 200 pacientes (140 hombres y 60 mujeres) que fueron atendidos en el hospital de la Escuela de Medicina de la Universidad de Urmia entre noviembre 2013 y diciembre de 2014. El suero se conservó a -70°C en el Departamento de Bioquímica Clínica y los experimentos fueron realizados en enero del 2015. El ADN de ácido nucleico viral fue purificado del ADN de las muestras de suero de los pacientes utilizando el kit de Magcore Cat. No. MVN 400-03, con un dispositivo magnético. La extracción y preparación del AND de virus de la hepatitis para las pruebas de PCR en tiempo real fue realizada utilizando un equipo genético nuevo (VHB RQ Ref. #HBV0913A-V3.2) y una máquina genética de Rotor (dispositivo PCR, Australia). Se midió fluoresceína-amidita por medio del progreso de las curvas sigmoides en las muestras de pacientes positivos, de acuerdo con el volumen en la cantidad y número de virus por unidad/ml. Todas las muestras que contenían entre 10,000 IU/ml y 100,000 IU/ml fueron consideradas positivas, y los resultados de los casos PCR negativos fueron considerados como muestras negativas. Los casos PCR positivos y negativos fueron divididos en dos grupos y se realizaron pruebas para HBsAg en las muestras de suero con inmunocromatografía y ELISA.
El procedimiento ELISASe utilizó el kit de la Pioneer Medicine Company (Terán, Irán), con número de registro 93002. Las pruebas ELISA fueron realizadas después del proceso de incubación y los casos positivo-negativo controles. Utilizamos un ELISA Reader Awareness Device (EE. UU.) para leer las pruebas y registrar la densidad óptica de los pocillos, a una longitud de onda de 450-nm versus la referencia de 630-nm, para lograr resultados más precisos. Las densidades ópticas (DO) por debajo de 0.15 para casos negativos y por arriba de 0.8 para casos positivos fueron consideradas el valor de punto de corte para la absorción de DO.
El método rápido: inmunocromatografíaUtilizamos el Ab Core Cassette de la Rojan Azma Company, con información de referencia REF: Ab-3101. Las muestras de suero (0.075ml) fueron colocadas en el sitio designado del cassette y los resultados fueron observados cualitativamente. La aparición de dos líneas rojas indicó un resultado positivo y la aparición de una línea roja indicó un resultado negativo (fig. 1).
La capacidad de una prueba para distinguir a sujetos sanos de pacientes es evaluada por sensibilidad, especificidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN). Comprender estos valores es relativamente sencillo.
Los autores intentaron presentar dichos conceptos utilizando los resultados actuales para facilitar la comprensión.
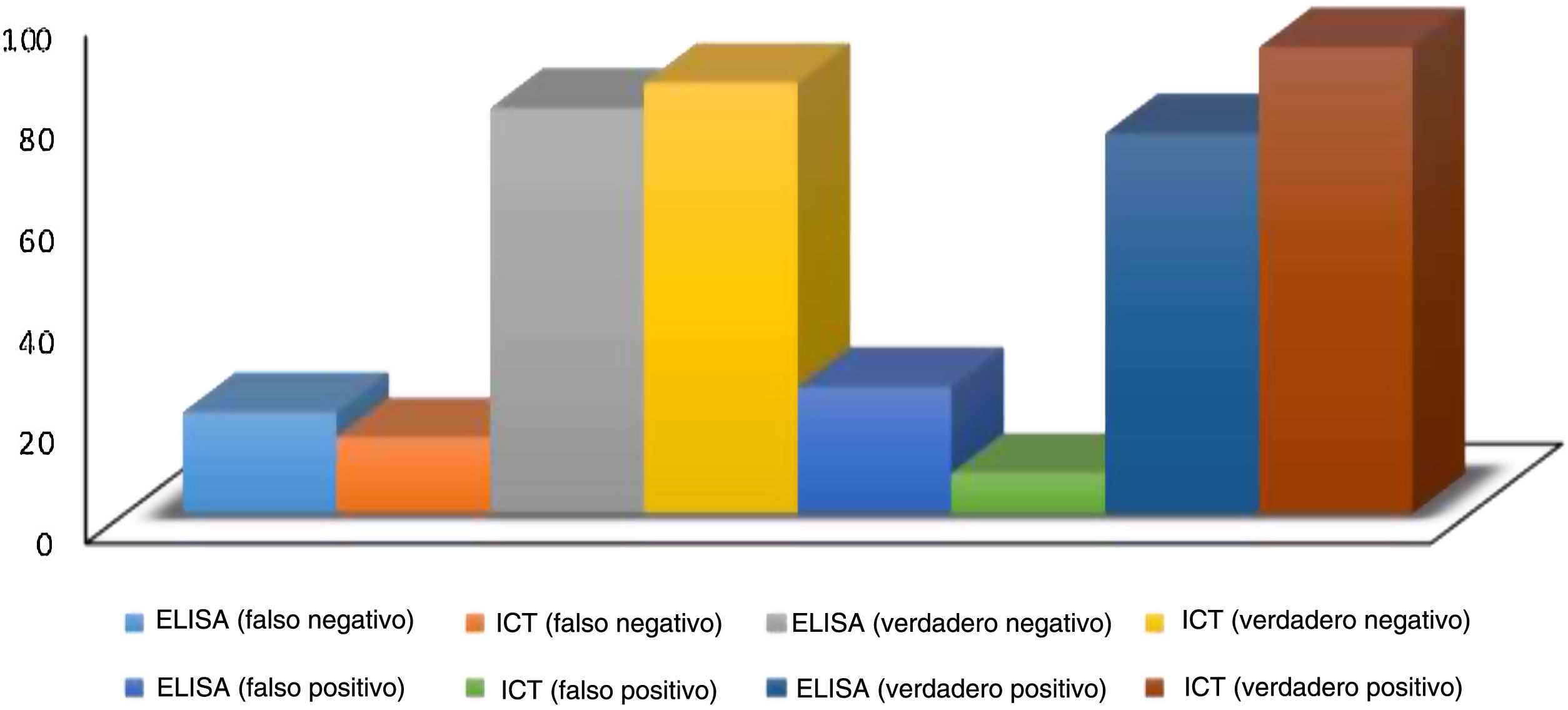
ResultadosEn el presente estudio analizamos la sensibilidad y la especificidad para diagnosticar HBsAg de las pruebas de inmunocromatografía y ELISA. Los resultados de dichos métodos fueron comparados con los resultados del procedimiento de PCR para VHB. El método inmunocromatográfico logró una sensibilidad del 97% y una especificidad del 91%, con un VPP de 0.92 y un VPN de 0.85, en comparación con los resultados PCR. Los datos de PCR e inmunocromatografía presentaron altas sensibilidades, con lo que se identificó a la inmunocromatografía como un método aceptable para diagnosticar hepatitis B. El método ELISA logró una sensibilidad del 78%, especificidad del 76%, VPP de 0.75 y VPN de 0.80, en comparación con los resultados PCR. Estos resultados también mostraron que el método ELISA fue aceptable respecto a eficiencia, alta sensibilidad y especificidad (tablas 1 y 2; fig. 2).
El virus de la hepatitis B es altamente infeccioso a nivel mundial y lleva a una insidiosa infección de largo plazo. Las infecciones por hepatitis B son más prevalentes en regiones endémicas (más del 75%), específicamente en el sureste asiático y África, con un riesgo de infección de por vida de entre el 60 y el 80%. Europa del Este, el Medio Oriente y la India han mostrado un riesgo de infección intermedio que va del 20 al 60%. En los Estados Unidos, casi 1.25 millones de personas tienen infección crónica por VHB, y se estima que anualmente ocurren 78,000 casos nuevos de VHB, principalmente entre adultos jóvenes sexualmente activos, negros y latinos, y usuarios de drogas intravenosas11,12. Es una infección de transmisión sanguínea importante, con implicaciones graves para receptores de sangre, si la sangre infectada no es identificada durante el tamizaje. Es también el principal agente etiológico de hepatitis crónica, cirrosis hepática y carcinoma hepatocelular, en países en vías de desarrollo13,14. La pandemia global de hepatitis B, especialmente en el contexto de coinfección con VIH y hepatitis C, es crítica. A pesar de que todos los métodos de laboratorio utilizados para diagnosticar hepatitis B tienen sus ventajas y desventajas, no existen investigaciones a la fecha que estudien las causas de las posibles diferencias de resultados15,16. Los presentes resultados y su aplicación práctica son significativos porque la prueba inmunocromatográfica es precisa para diagnosticar HBsAg en sangre y la prueba ELISA tiene una sensibilidad y especificidad aceptables, en comparación con el procedimiento de PCR, el cual es considerado el estándar de oro. La detección y diagnóstico de infecciones por VHB está basada principalmente en ensayos inmunitarios, entre los cuales los más comunes son la prueba ELISA y la inmunocromatografía. Sin embargo, las pruebas de diagnóstico rápidas son más fáciles de realizar y representan el mínimo de incomodidad para el paciente, ya que se requiere un volumen de muestra muy pequeño. El presente estudio comparó dos métodos comúnmente utilizados para diagnosticar VHB. La presencia de HBsAg en el suero de los pacientes fue medido utilizando el método ELISA y la inmunocromatografía, y la especificidad y sensibilidad de dichos procedimientos fueron comparadas con la especificidad y sensibilidad del método PCR. La inmunocromatografía tuvo sensibilidad considerablemente mayor que la ELISA, con tasas de 91% y 75% respectivamente, lo cual fue reflejado en mejores valores VPP y VPN de la inmunocromatografía. Nuestros resultados están acorde con los de estudios previos que reportan las ventajas de la inmunocromatografía sobre la ELISA por su bajo costo, facilidad de uso, eficiencia y estatus de prueba rápida (Nazir, Yousuf et al., 2019; Asaduzzaman, Milon et al., 2018). Se ha reportado que la inmunocromatografía para HBsAg tiene buena sensibilidad y excelente especificidad en comparación con los inmunoensayos de laboratorio7. Lau et al. declararon que las pruebas EIA son el método estándar para detectar HBsAg y HBeAg mientras que la inmunocromatografía tiene varias ventajas17. La prueba PCR es conocida como el estándar de oro para detectar secuencias de ADN y cuantificar el VHB, pero si se utilizan métodos serológicos y moleculares en conjunto, la precisión diagnóstica para infección por VHB aumenta18. La sensibilidad y especificidad de la prueba de inmunocromatografía fue del 100% en suero recolectado en un estudio coreano que evaluó el desempeño de un dispositivo de diagnóstico19, al igual que en nuestro ensayo. En otro estudio se reportó que de 660 sujetos 38 dieron positivo para HBsAg utilizando la inmunocromatografía, mientras que utilizando ELISA fueron 71 los positivos20. En el presente estudio, la inmunocromatografía fue un método aceptable para diagnosticar hepatitis B, con un buen nivel de sensibilidad y especificidad. El presente estudio reveló un mayor VPP con la inmunocromatografía, además de una mejor eficiencia (92%), que ELISA, en la mayoría de los casos de VHB. La inmunocromatografía «rápida» de un paso, legible visualmente, de ensayo de captura de antígeno para tamizaje rápido de HBsAg fue evaluada y mostró una sensibilidad del 97% y especificidad del 91%, lo cual coincide con los hallazgos actuales. Otros estudios también han indicado valores de seroprevalencia de 0.82% y 0.91% para inmunocromatografía y ELISA respectivamente21. Amini et al. observaron que las inmunocromatografías para detectar HBsAg realizadas en suero/plasma y especímenes de sangre capilar completa tuvieron buena sensibilidad y especificidad importante.
ConclusiónLa inmunocromatografía fue un método aceptable para diagnosticar hepatitis B, con buenos niveles de sensibilidad y especificidad, en comparación con el método PCR, el cual es considerado el estándar de oro. Por lo tanto, lo consideramos un método satisfactorio para diagnosticar hepatitis B.
Responsabilidades éticasEste artículo no contiene información personal que pueda identificar a los pacientes. Las muestras fueron archivadas por el Departamento de Bioquímica Clínica del Hospital de la Escuela de Medicina de la Universidad de Urmia.
FinanciaciónLa presente investigación, realizada en la Universidad Azad de Urmia, fue financiada por los autores. No se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.