El infliximab (IFX) es un anticuerpo monoclonal quimérico que funciona en contra del factor de necrosis tumoral alfa (TNF-α) y se utiliza para tratar enfermedades autoinmunes como la artritis reumatoide, la psoriasis y la enfermedad inflamatoria intestinal (EII)1. El IFX ha sido asociado a efectos secundarios poco frecuentes que incluyen infecciones, reacciones cutáneas, autoinmunidad (vasculitis cutánea, síndrome tipo lupus, lupus eritematoso sistémico, enfermedad pulmonar intersticial), complicaciones neurológicas, insuficiencia cardiaca y malignidad1-5.
Las manifestaciones cutáneas relacionadas con el IFX son reacción a infusión, vasculitis, infecciones cutáneas, psoriasis, eccema y cáncer de piel3. En el presente artículo describimos el caso de un paciente pediátrico con enfermedad de Crohn fistulizante que desarrolló púrpura de Henoch-Schönlein relacionada con IFX.
El caso de una niña de 15 años diagnosticada con enfermedad de Crohn fistulizante fue llevado en el Departamento de Gastroenterología Pediátrica. Aunque había estado tomando un agente 5-ASA, azatioprina y esteroides intermitentes durante 2años, no experimentó recurrencia de actividad de la enfermedad o fístulas. Comenzó con IFX (Remicade) (5mg/kg/dosis, semanas 0-2-6-8), pero fue ingresada en el hospital con lesiones purpúricas en las piernas 10días después de la quinta dosis de IFX.
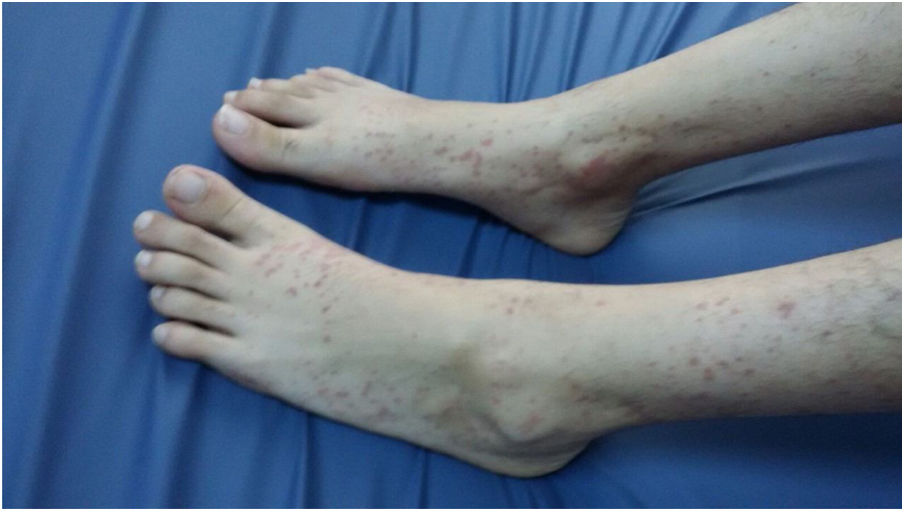
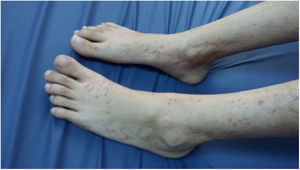
La paciente no había tomado ningún otro medicamento ni productos herbales. Tras el examen físico se determinó su peso en 50kg (percentil 10-25), su altura en 160cm (percentil 25-50), y su temperatura corporal fue de 36°C. Presentaba lesiones purpúricas en las piernas (fig. 1), el abdomen era blando y no doloroso, sin distensión, y el examen del sistema cardiovascular y respiratorio no presentó anormalidades.
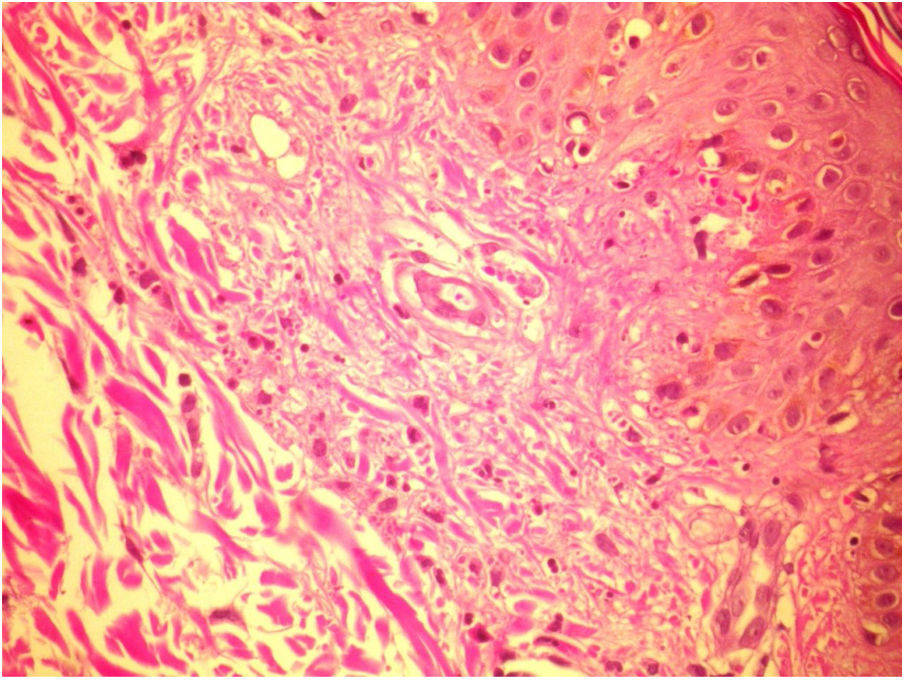
Los exámenes de laboratorio no revelaron trombocitopenia o trastorno de coagulación. Las pruebas serológicas para hepatitis°CA, B y C, VEB, parvovirus, VHS y CMV fueron negativas. Los niveles de electroforesis de proteína, crioglobulina, AELO, factor reumatoide, suero amiloide tipoA y C3 y C4 estuvieron dentro de los límites normales. El anticuerpo anticitoplasma de neutrófilos fue levemente positivo. El examen histopatológico de los especímenes de la biopsia cutánea reveló vasculitis leucocitoclástica (figs. 2 y 3). Dado que la vasculitis fue considerada un efecto secundario del IFX, el tratamiento fue suspendido. Las lesiones cutáneas se resolvieron completamente 3días después de la suspensión del tratamiento con IFX. No se llevó a cabo la reinstauración con terapia anti-TNF-α debido a que la paciente fue perdida para seguimiento.
Los agentes anti-TNF (IFX, etanercept y adalimumab) han sido asociados cada vez con más casos de enfermedades autoinmunes1-6. A pesar de que la evidencia respalda un perfil de buena seguridad y tolerancia para dichos agentes, los reportes de reacciones adversas, que incluyen infecciones, reacciones cutáneas, autoinmunidad (vasculitis cutáneas, síndrome tipo lupus, lupus eritematoso sistémico, enfermedad intersticial pulmonar) y malignidad, están en aumento1-5.
En su reciente estudio prospectivo, Mälkönen et al.7 reportaron que el 48% de los niños con EII presentaron lesiones cutáneas relacionadas con IFX, las cuales eran frecuentemente manifestaciones cutáneas tipo psoriasis. En un estudio con pacientes adultos con EII, Hellström et al.8 encontraron que la terapia anti-TNF estaba frecuentemente asociada con un nuevo inicio de reacciones cutáneas (especialmente eccema escamoso), de manera más común en pacientes con enfermedad de Crohn.
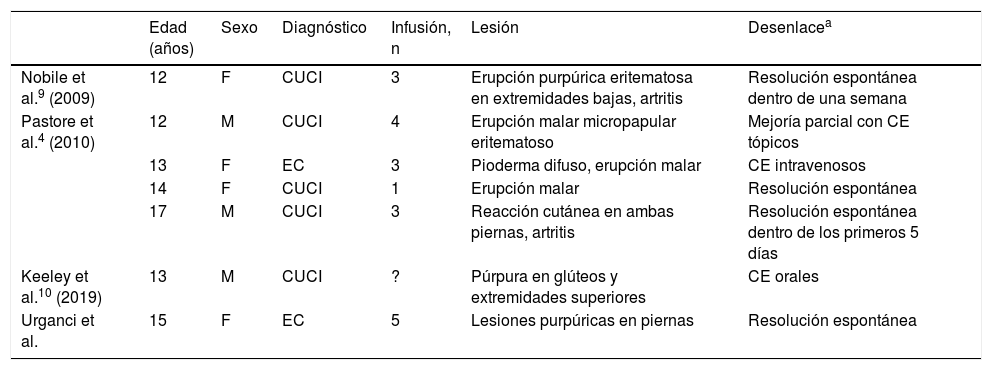
En reportes sobre pacientes adultos, la vasculitis leucocitoclástica es descrita como el tipo más común de vasculitis, y la púrpura como la lesión más frecuente asociada al uso de inhibidores de TNF1,2,5. Se ha reportado un total de 125 casos de vasculitis relacionada con inhibidores de TNF en adultos. Sokumbi et al.1 describieron 8 pacientes con vasculitis (5 tratados con IFX, 2 con etanercept y 1 con adalimumab), Fujikawa et al.2 describieron 3 pacientes (2 con IFX, 1 con etanercept), Song et al.3 describieron un paciente tratado con IFX, y Ramos-Casals et al.5 describieron 113 pacientes (etanercept: 59, IFX: 47, adalimumab: 5, otros agentes: 2). Las características clínicas de los pacientes pediátricos4,9,10 con púrpura de Henoch-Schönlein relacionada con IFX se muestran en la tabla 1.
Características clínicas de casos pediátricos reportados con púrpura de Henoch-Schönlein relacionados con infliximab
| Edad (años) | Sexo | Diagnóstico | Infusión, n | Lesión | Desenlacea | |
|---|---|---|---|---|---|---|
| Nobile et al.9 (2009) | 12 | F | CUCI | 3 | Erupción purpúrica eritematosa en extremidades bajas, artritis | Resolución espontánea dentro de una semana |
| Pastore et al.4 (2010) | 12 | M | CUCI | 4 | Erupción malar micropapular eritematoso | Mejoría parcial con CE tópicos |
| 13 | F | EC | 3 | Pioderma difuso, erupción malar | CE intravenosos | |
| 14 | F | CUCI | 1 | Erupción malar | Resolución espontánea | |
| 17 | M | CUCI | 3 | Reacción cutánea en ambas piernas, artritis | Resolución espontánea dentro de los primeros 5 días | |
| Keeley et al.10 (2019) | 13 | M | CUCI | ? | Púrpura en glúteos y extremidades superiores | CE orales |
| Urganci et al. | 15 | F | EC | 5 | Lesiones purpúricas en piernas | Resolución espontánea |
EC: enfermedad de Crohn; CE: corticoesteroides; CUCI: colitis ulcerosa crónica inespecífica.
Ramos-Casals et al.5 reportaron que una cuarta parte de los pacientes con vasculitis relacionada con agente anti-TNF presentaban afectación extracutánea, como enfermedad intersticial pulmonar. Sokumbi et al.1 encontraron que la neuropatía renal y la vasculitis renal eran los casos más frecuentes de afectación extracutánea. Nobile et al.9 y Pastore et al.4 describieron casos pediátricos con artritis. En nuestro caso no detectamos afectación sistémica.
Las reacciones vasculares ocurren en promedio dentro de las primeras 18 semanas de tratamiento (rango de 6-38 semanas)1,4. En nuestro paciente, la púrpura de Henoch-Schönlein se desarrolló 10 días después de la quinta dosis de terapia IFX.
Aunque la patogénesis de la vasculitis asociada a agentes anti-TNF es aún desconocida, se han propuesto varios posibles mecanismos, como el desarrollo de anticuerpos antagonistas a los agentes anti-TNF que llevan a una hipersensibilidad inmunológica tipoIII mediada por complejos1,2,11 y a un cambio de respuesta a citocina Th1 predominante a respuesta Th2 asociada con un mecanismo inmunológico mediado por anticuerpos11.
Pastore et al.6 examinaron la incidencia de eventos adversos graves en pacientes en un centro de referencia pediátrico en relación con trastornos inflamatorios crónicos reumatológicos y gastroenterológicos. Concluyeron que la terapia anti-TNF-α era bien tolerada generalmente, y que los eventos graves adversos frecuentemente asociados con IFX eran raros y no fatales11. En pacientes con reacciones leves, como lesiones cutáneas aisladas o alteraciones inmunológicas, la suspensión de la terapia anti-TNF podría ser suficiente. También podría considerarse una terapia con esteroides breve. En nuestro paciente, las lesiones cutáneas se resolvieron completamente tras suspender la terapia con IFX, tal como ocurrió en los casos reportados por Nobile et al.9 y Pastore et al.4 El tratamiento con esteroides intravenosos o tópicos no fue necesario.
En conclusión, más allá de los beneficios clínicos del IFX, los clínicos deben tener en mente los efectos secundarios de la sustancia. La evaluación clínica e inmunológica de línea de base previa a comenzar la terapia anti-TNF debería ser llevada a cabo en los pacientes, al igual que un seguimiento cercano.
Consideraciones éticasSe solicitó el consentimiento informado del paciente para recibir el tratamiento y participar en la investigación descrita anteriormente.
El presente trabajo cumple con las regulaciones de investigación bioética actuales, y dada la naturaleza retrospectiva de un reporte de caso único, no se requirió la autorización del comité de ética institucional.
En el caso de que el paciente pudiera ser identificado o reconocido por medio de las imágenes o los datos presentados en el artículo, el autor declara que el consentimiento informado del paciente fue obtenido para la publicación de sus imágenes y datos.
FinanciaciónNo se recibió financiamiento alguno en relación con este artículo.
Conflicto de interesesLos autores declaran que no existe conflicto de intereses.


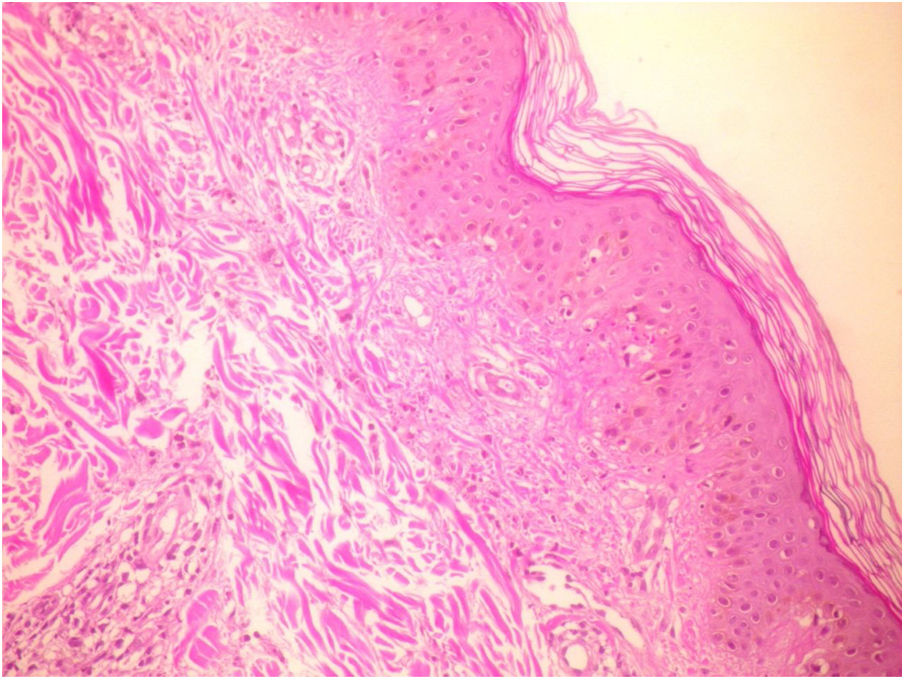
![Biopsia de lesiones cutáneas presentando vasculitis leucocitoclástica (tinción hematoxilina-eosina [H&E], ×20). Biopsia de lesiones cutáneas presentando vasculitis leucocitoclástica (tinción hematoxilina-eosina [H&E], ×20).](https://static.elsevier.es/multimedia/03750906/0000008700000001/v2_202202040701/S0375090621000720/v2_202202040701/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w97o/wdEXW47bqlyT1CqG6R0=)
![Biopsia de lesiones cutáneas presentando vasculitis leucocitoclástica (tinción hematoxilina-eosina [H&E], ×40). Biopsia de lesiones cutáneas presentando vasculitis leucocitoclástica (tinción hematoxilina-eosina [H&E], ×40).](https://static.elsevier.es/multimedia/03750906/0000008700000001/v2_202202040701/S0375090621000720/v2_202202040701/es/main.assets/thumbnail/gr3.jpeg?xkr=ue/ImdikoIMrsJoerZ+w97o/wdEXW47bqlyT1CqG6R0=)


