La resonancia magnética con gadolinio para la evaluación de lesiones hepáticas es un método cada vez más utilizado en la práctica clínica, particularmente para pacientes con lesiones focales sospechosas, ya sean benignas o malignas. En el caso del carcinoma hepatocelular, el rendimiento diagnóstico de la resonancia magnética a través de protocolos «convencionales» y mediante la tomografía computarizada multidetector, que consiste en la evaluación de múltiples fases con contraste intravenoso, depende en gran medida del tamaño de la lesión, considerándose más certero en lesiones>2cm. Sin embargo, para aquellas lesiones de 1-2cm, el establecimiento de un diagnóstico definitivo es un verdadero reto, con valores de sensibilidad del 45-65%, aunque por lo general con una excelente especificidad (>95%). Además, si la lesión tiene un diámetro<1cm, el diagnóstico es generalmente poco fiable. En estos 2 últimos escenarios, el uso complementario de medios de contraste hepatoespecíficos puede ser útil. El objetivo de este artículo es revisar la evidencia actual de la utilidad de este nuevo método de diagnóstico no invasivo en las lesiones hepáticas.
Gadolinium-enhanced magnetic resonance for the evaluation of hepatic lesions is increasingly being used in clinical practice, especially in patients with suspicious focal lesions, whether benign or malignant. In regard to hepatocellular carcinoma, the diagnostic performance of magnetic resonance through the «conventional» protocols and multi-detector computerized tomography consisting of multiphase evaluation with intravenous contrast, largely depends on the size of the lesion. They are more reliable in lesions>2cm. However, in lesions measuring 1-2cm, establishing the definitive diagnosis is a real challenge, with sensitivity values of 45-65%, but generally with excellent specificity (>95%). Furthermore, if the lesion has a diameter<1cm, diagnosis is usually unreliable. In these last 2 settings, the complementary use of liver-specific contrast agents can be advantageous. The aim of our article was to review the current evidence on the usefulness of this new non-invasive diagnostic method in hepatic lesions.
La resonancia magnética (RM) con gadolinio para la evaluación de lesiones hepáticas es un método cada vez más empleado en la práctica clínica, en particular para aquellos pacientes con sospecha de lesiones focales tanto benignas como malignas.
En el caso del carcinoma hepatocelular (CHC), tumor epitelial cuya incidencia va en incremento y que en la actualidad ocupa el 5.o lugar en frecuencia, el desempeño diagnóstico de los protocolos de RM y tomografía computarizada multidetector (TCMD) denominados «convencionales» —consistentes en evaluaciones multifásicas con contraste intravenoso— depende en gran medida del tamaño de la lesión, siendo consideradas como confiables con valores de sensibilidad del 100% para ambas modalidades si estas son mayores de 2cm1–4.
Sin embargo, establecer un diagnóstico de certeza para aquellas lesiones entre 1-2cm es un verdadero reto, particularmente en pacientes con cirrosis, grupo en el que se presentan el 80% de los CHC y en quienes la incidencia anual de este tipo de lesiones es del 2-8%5–7, con valores de sensibilidad del 44-47% para lesiones de 1-2cm1–4 y del 29-43% si miden menos de 1cm2–4. En tumores con un diámetro menor a 1cm, el diagnóstico en general no es confiable. Este escenario es cada vez más frecuente debido al empleo del ultrasonido como método de escrutinio como modalidad primaria inicial recomendada por la mayoría de las guías6,8–10. En estos 2 últimos escenarios y en el caso de lesiones consideradas como indeterminadas tras el análisis con estrategias convencionales, el uso complementario de medios de contraste hepatoespecíficos (HE) en RM podría ser de utilidad.
El objetivo del presente manuscrito es realizar una revisión sobre la evidencia actual del papel emergente de los contrastes HE en la evaluación de lesiones focales, particularmente del CHC, y los cuales de acuerdo a la literatura parecen ser el método más sensible para su detección al incrementar estos valores entre un 6% y un 15% más11–13, así como de sus principales diagnósticos diferenciales.
Contrastes hepatoespecíficos: tipos y propiedadesUna forma sencilla de clasificar los medios de contraste empleados en RM divide a los agentes en 2 grandes grupos: 1) no HE y 2) HE. El primer grupo congrega a los medios «tradicionales», basados en agentes quelantes de gadolinio, cuyo comportamiento típico es intravascular y extracelular. Por otra parte, los medios de contraste específicos para el hígado se subdividen en aquellos captados por las células de Kupffer, que consisten en moléculas superparamagnéticas de ferumóxidos de Fe, y en aquellos que son captados por hepatocitos funcionales. Este último agrupa a compuestos basados también en gadolinio denominados gadobenato de dimeglumina (Gd-BOPTA) y al ácido gadoxético (Gd-EOB-DTPA), los cuales son considerados contrastes intravasculares, extracelulares e intrahepáticos, y motivo del presente trabajo.
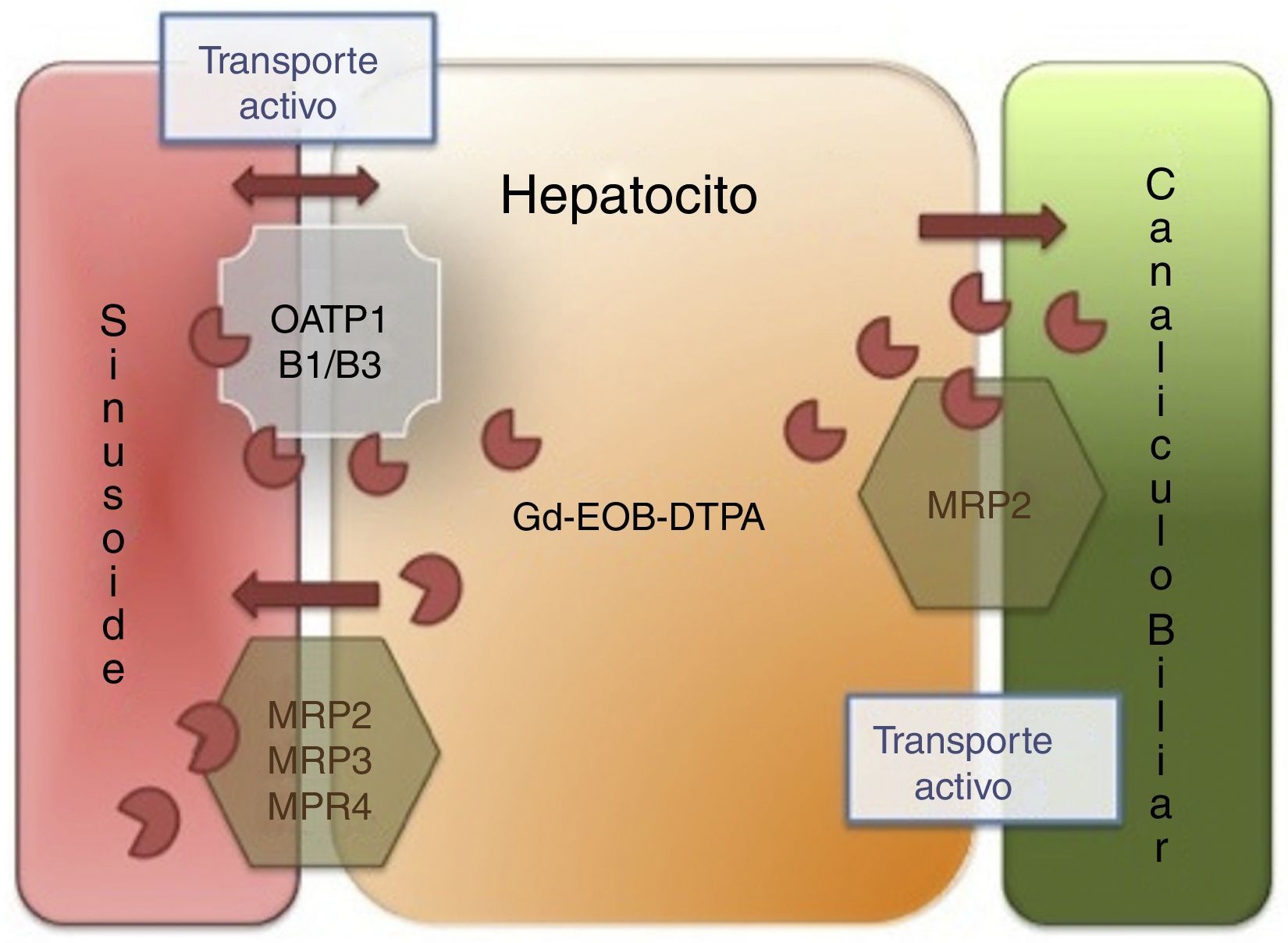
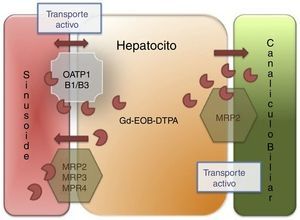
El Gd-BOPTA tiene una menor entrada al hepatocito (3-5%) que el ácido gadoxético (50%), y ambos se eliminan sin cambios hacia la vía biliar14. En caso de obstrucción de la vía biliar existe un incremento en su eliminación renal. El paso intracelular depende de la expresión de receptores de membrana denominados MRP3/4 y OATP8, también conocido como 1B1/B3 (por sus siglas en inglés de proteína multifármaco-resistente y polipéptido transportador de aniones orgánicos respectivamente) localizados en la membrana sinusoidal basolateral que colinda con el sinusoide y espacio de Disse, mientras que el transportador MRP2, localizado en la membrana canalicular, es el encargado de excretar el contraste hacia el canalículo biliar14 (fig. 1).
Mecanismo de acción de los contrastes hepatoespecíficos. El agente hepatoespecífico se introduce al hepatocito a través del polipéptido transportador del anión orgánico (OATP1, B1/B3), sale a través de las proteínas dependientes de ATP multifármaco-resistentes (MRP2, MRP3, MRP4) localizadas en la membrana sinusoidal. El MRP2 es regulado por recuperación de la membrana (disminución del flujo de salida de bilis) o introducción (aumento del flujo de salida), finalmente el agente hepatoespecífico no es metabolizado por el hepatocito y es excretado sin cambios en la bilis.
Este tipo de agentes HE tienen un comportamiento similar a los contrastes «tradicionales» durante las fases arterial, portal y venosa, es decir permiten evaluar la perfusión de la lesión, la cual es un elemento por imagen indispensable para establecer el diagnóstico diferencial. Sin embargo, el verdadero efecto diagnóstico adicional que ofrecen estos contrastes requiere de imágenes en una fase más tardía (15-25min) denominada hepatobiliar, tiempo necesario para que el hepatocito funcional concentre en su interior el medicamento15–18. Es decir, un protocolo clásico de RM para evaluación de lesión focal incluiría las secuencias convencionales en T1 doble eco (dentro y fuera de fase), T2 con y sin saturación de grasa, colangio 3D, T1 contrastado multifásico (simple, arterial, portal, venoso y tardío de 2-3min), difusión y de manera adicional un T1 en fase hepatobiliar15, protocolo de aproximadamente 50min de duración.
Utilidad del ácido gadoxético en la evaluación de nódulos displásicos de alto grado y carcinoma hepatocelularEl uso de este tipo de medios de contraste permite distinguir entre lesiones que contienen hepatocitos y aquellas que no los contienen. Por ende, lesiones malignas compuestas por hepatocitos no funcionales (nódulos displásicos de alto grado y CHC) o ausentes de hepatocitos (metástasis), no muestra captación de este tipo de contraste en fase hepatobiliar (fig. 2). Asimismo, estos agentes también han sido utilizados para distinguir la hiperplasia nodular focal del carcinoma fibrolamelar, así como del adenoma hepático, 2 lesiones benignas con diferentes estrategias de seguimiento y tratamiento19.
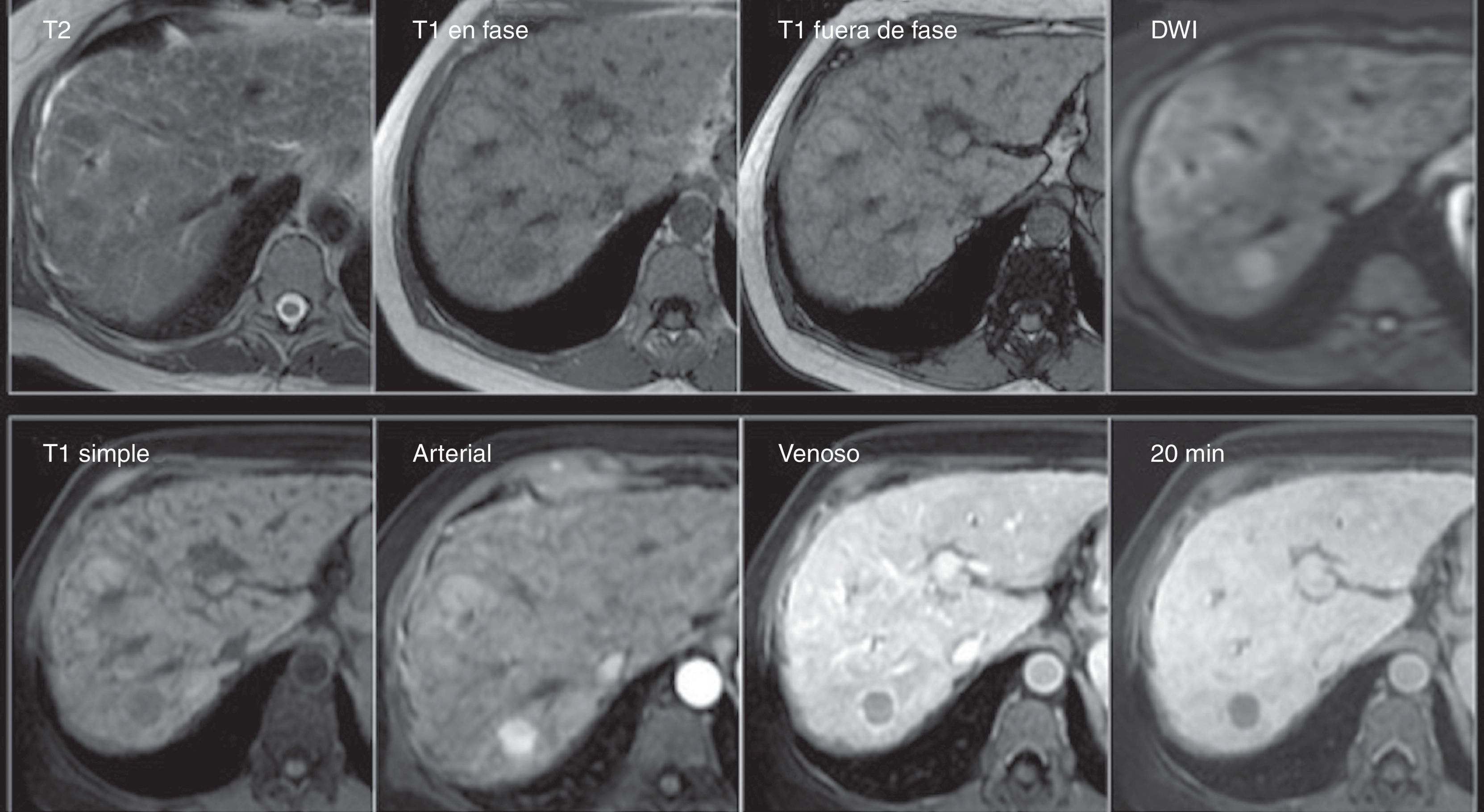
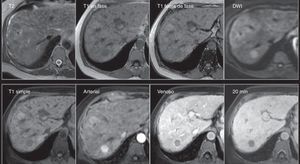
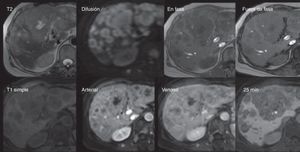
Carcinoma hepatocelular de pequeño tamaño. Mujer de 60 años con hígado con cambios por cirrosis con importante lobulación y nodularidad de sus contornos, así como intensidad de señal heterogénea del parénquima, y con lesión indeterminada por TCMD (no mostrada). Fila superior: Nótese la lesión redondeada del segmento 7, isointensa en T2 e hipointensa en T1 tanto dentro como fuera de fase, y con restricción a la difusión (DWI). Fila inferior: En las fases dinámicas en secuencias LAVA, existe importante reforzamiento en la fase arterial con lavado rápido en fase venoportal —observe el realce del resto del parénquima— y la hipointensidad de la lesión en la fase hepatobiliar de 20min, hallazgos característicos de carcinoma hepatocelular.
El empleo de estos medios de contraste podría ser especialmente útil en aquellos pacientes con lesiones hepáticas que no cumplen con el comportamiento vascular «clásico» del CHC. Las características típicas que definen a un CHC en un estudio de RM dinámico o multifásico posterior al contraste intravenoso de acuerdo a las guías de la American Association for the Study of Liver Diseases (AASLD) son: 1) una lesión hipervascular durante la fase arterial, y 2) durante la fase venosa lavado del mismo o aparición de cápsula en caso de no existir lavado, esta última no considerada en las guías aunque de gran especificidad diagnóstica (fig. 2)19–21. Este comportamiento es altamente indicativo de corresponder a un CHC con valores de especificidad superiores al 95%, aunque con una sensibilidad del 45-65% en lesiones de 1-2cm de diámetro8,22. Sin embargo, la ausencia de características vasculares «clásicas» ocurre de manera relativamente frecuente debido a que durante el proceso de hepatocarcinogénesis —proceso complejo y gradual de alteraciones epigenéticas y genéticas de transformación de células hepáticas malignas a CHC—, se reconoce que el aporte vascular de la lesión oscila en un espectro donde inicialmente existe predominio de flujo vascular portal debido al mayor número de tríadas portales y un menor grado de flujo arterial «normal» como es el caso de los nódulos de regeneración, hasta un aporte 100% arterial a partir de vasos «anormales» debido a la nula o menor densidad de tríadas portales y mayor de sinusoides con capilarización y de arterias no pareadas, es decir de aquellas arterias no asociadas a tríadas portales, como ocurre en los CHC pobremente diferenciados, que muestran un realce típicamente arterial y un lavado portal y venoso20,23. Además, en el inter de este espectro existen lesiones con escaso flujo portal, así como una mezcla de aporte arterial normal y anormal, y es aquí en donde se encuentran algunas lesiones consideradas nódulos displásicos de alto grado y CHC en etapa temprana (microinvasores) o también denominados in situ, en su mayoría menores de 2cm de diámetro, ambas de difícil detección con los métodos convencionales20,23. Por lo tanto, tanto los nódulos displásicos de alto grado como los CHC en etapa temprana pueden mostrarse atípicos, siendo hipervasculares en la fase arterial aunque sin lavado en las fases portal o venosa, o con ausencia de vascularidad arterial y presencia de la misma en fases más tardías. Por este motivo, la sensibilidad general de la RM con el uso de contrastes convencionales es de tan solo el 62%19. En el caso de este tipo de lesiones, si se emplearan contrastes HE y si la lesión fuera hipointensa en la fase de 20min, la conducta a seguir sería un seguimiento estrecho de la lesión o la realización de una biopsia ante la alta sospecha de CHC. Es decir, en la fase hepatobiliar, estas lesiones no concentran el medio de contraste ya que carecen de hepatocitos funcionantes, lo que las diferencia del hígado perilesional de mayor intensidad de señal por la presencia intracelular del contraste HE.
La razón de emplear contrastes HE en el diagnóstico de nódulos displásicos de alto grado y de CHC tempranos es que existe evidencia reciente que sugiere que la expresión de los transportadores encargados de introducir a la célula estos medios de contraste disminuye durante el proceso de hepatocarcinogénesis antes de que ocurran los cambios secuenciales típicos de la vascularidad tumoral mencionada con anterioridad. La reducción en la expresión del transportador OATP8 puede en parte atribuirse a la expresión del factor nuclear 3beta del hepatocito, un factor de transcripción que se sobreexpresa en los CHC y que reprime la transcripción del OATP815.
Por lo tanto, las potenciales indicaciones del empleo de contrastes HE serían aquellos pacientes con lesiones mayores de 2cm consideradas indeterminadas tras el análisis convencional por vía tomográfica o de RM con contrastes no HE, y de manera inicial en aquellas menores de 2cm, que frecuentemente resultan indeterminadas después de seguir dichas estrategias.
Evidencia de la utilidad del ácido gadoxético en valoración de lesiones focales y carcinoma hepatocelularDe acuerdo a series iniciales, el desempeño diagnóstico de la RM con contrastes HE para establecer el diagnóstico de nódulos displásicos de alto grado o CHC bien diferenciado en lesiones consideradas previamente indeterminadas mejora de forma significativa cuando se compara con las estrategias convencionales, con valores de sensibilidad y especificidad del 82-99% y del 70-95% respectivamente19,24–26. El comportamiento hipointenso de una lesión en la fase hepatobiliar es considerado como un signo que, en conjunto con el resto de las características que se evalúan de forma convencional, mejora el desempeño global de la prueba. De acuerdo a Kim et al. en un estudio de 96 pacientes con 116 nódulos de 1-2cm de diámetro, en el cual se comparó la RM con contraste HE vs. un estándar de referencia patológico y/o de seguimiento durante 18 meses, la sensibilidad de los signos radiológicos considerados como diagnósticos de acuerdo a las guías de la AASLD fue del 67% (IC: 51-79%), y esta mejoró hasta el 84% (IC: 70-92%) cuando a estos signos radiológicos se sumaron la hipointensidad en T1 en la fase hepatobiliar y/o la hiperintensidad de la lesión en secuencias T219. En otro estudio de 62 pacientes con 83 CHC y en el cual se comparó el desempeño diagnóstico de la TCMD multifásica, con la RM con contraste HE vs. enfermedad (resección quirúrgica), no se observó una diferencia significativa entre los métodos de imagen de manera global24. Sin embargo, en el subgrupo de lesiones menores de 1cm, se vio una diferencia significativa en la sensibilidad (70 vs. 30-50%, p<0.05).
En un estudio de 34 pacientes explantados con 102 nódulos hepáticos, ninguno de los 32 nódulos displásicos de bajo grado mostró un comportamiento de hipointensidad en la fase hepatocelular, contrario a los CHC en donde solo uno de 40 tumores no mostró el comportamiento típico de hipointensidad en dicha fase27. Este estudio coincide con los resultados observados en varios estudios durante el seguimiento de nódulos no hipervasculares en la fase arterial y con hipointensidad en la fase hepatocelular, en donde la tasa acumulativa de desarrollo de CHC típico osciló del 15 al 35% a un año y hasta el 46% en 2 años, principalmente en lesiones mayores de 1cm28–30. Estos resultados han motivado que algunas asociaciones médicas hayan incorporado el uso de contrastes HE en sus algoritmos diagnósticos como prueba a seguir, una vez detectada alguna anormalidad en los estudios iniciales (ultrasonido o elevación del marcador tumoral)31,32.
Sin embargo, debe tenerse en cuenta que el 5-12% de los CHC y hasta cerca del 30% de los nódulos displásicos de alto grado no son hipointensos en las fases hepáticas del contraste HE, e incluso pueden presentar mayor acúmulo del contraste en la fase hepatobiliar14,16,24,30. Este hallazgo posiblemente se debe a la sobreexpresión paradójica de los genes OATP8 y a la ausencia de conductos biliares funcionales o del transportador de membrana de salida en algunos tumores, en donde se especula un origen celular diferente o alteraciones genéticas durante la hepatocarcinogénesis14,33. La mayoría de estos tumores son histológicamente moderadamente o bien diferenciados34,35. En este escenario, se recomienda buscar otros signos que apoyen el diagnóstico de CHC como son: ausencia de cicatriz central, imagen de nódulo en nódulo, presencia de anillo hipointenso, hiperintensidad en las secuencias de difusión por restricción de la misma y/o caída de señal (hipointensidad) en las secuencias fuera de fase debido a la presencia de grasa intralesional36.
Además debe de considerarse que la presencia de algunos factores puede limitar la eficacia de la fase hepatobiliar en la detección y caracterización de las lesiones. Aquellos pacientes con importante disfunción hepática o colestasis pueden mostrar una limitada concentración de los agentes hepatobiliares37. Estudios recientes reportan que el desempeño diagnóstico de los contrastes HE disminuye al agravarse la cirrosis al reducir el realce en la fase hepatocelular38.
Diagnóstico diferencialLa principal utilidad de los estudios con contrastes HE es la mejor caracterización de lesiones focales, en particular la distinción entre tumores benignos y malignos. Sin embargo, no se recomienda que un protocolo de estudio de lesión focal hepática solo incluya la fase hepatobiliar, ya que todas las lesiones que no estén compuestas por hepatocitos se comportarán como hipointensas. Por este motivo, es importante conocer algunas lesiones cuyo comportamiento con este tipo de medios de contraste pueda ser el de hipointensidad en la fase hepatobiliar debido a la carencia histológica de hepatocitos funcionantes, con el fin de evitar diagnósticos erróneos. La distinción entre ellas dependerá del análisis en conjunto de todas las secuencias, comportamiento en T1, T2, saturación grasa, doble eco, difusión y características de la perfusión, es decir si presenta realce arterial o venoso, presencia o no de lavado, tipo de realce (central o periférico), y presencia o no de cápsula. Las características por RM de las diferentes lesiones focales se resumen en la tabla 1 y en las figuras 3–6.
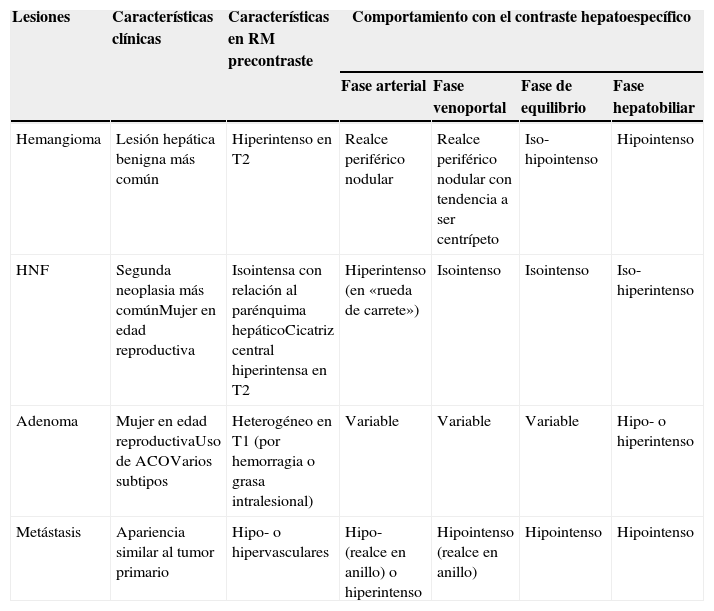
Características importantes para diferenciar las lesiones hepáticas más frecuentes con el uso de contrastes hepatoespecíficos
| Lesiones | Características clínicas | Características en RM precontraste | Comportamiento con el contraste hepatoespecífico | |||
|---|---|---|---|---|---|---|
| Fase arterial | Fase venoportal | Fase de equilibrio | Fase hepatobiliar | |||
| Hemangioma | Lesión hepática benigna más común | Hiperintenso en T2 | Realce periférico nodular | Realce periférico nodular con tendencia a ser centrípeto | Iso-hipointenso | Hipointenso |
| HNF | Segunda neoplasia más comúnMujer en edad reproductiva | Isointensa con relación al parénquima hepáticoCicatriz central hiperintensa en T2 | Hiperintenso (en «rueda de carrete») | Isointenso | Isointenso | Iso-hiperintenso |
| Adenoma | Mujer en edad reproductivaUso de ACOVarios subtipos | Heterogéneo en T1 (por hemorragia o grasa intralesional) | Variable | Variable | Variable | Hipo- o hiperintenso |
| Metástasis | Apariencia similar al tumor primario | Hipo- o hipervasculares | Hipo- (realce en anillo) o hiperintenso | Hipointenso (realce en anillo) | Hipointenso | Hipointenso |
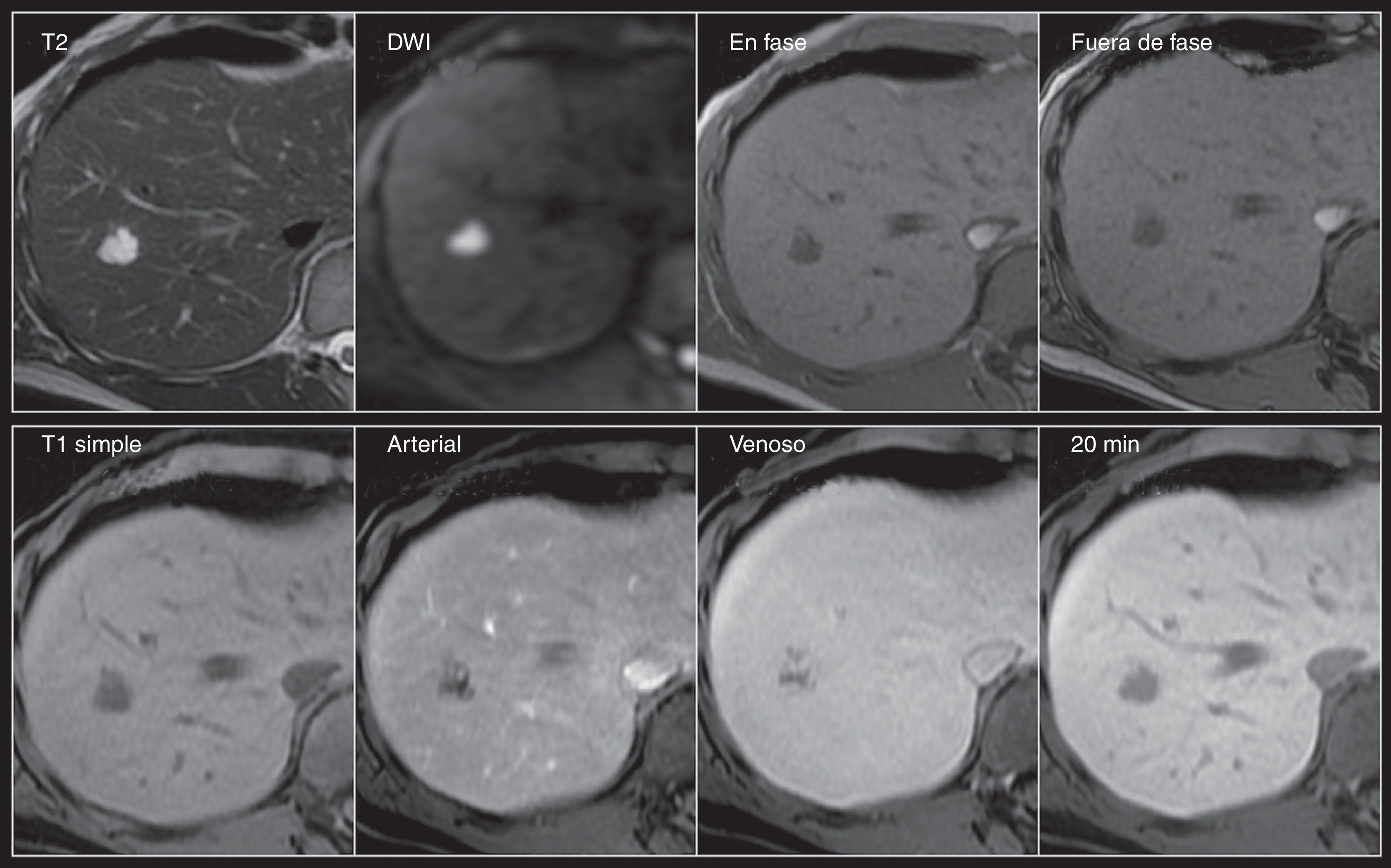
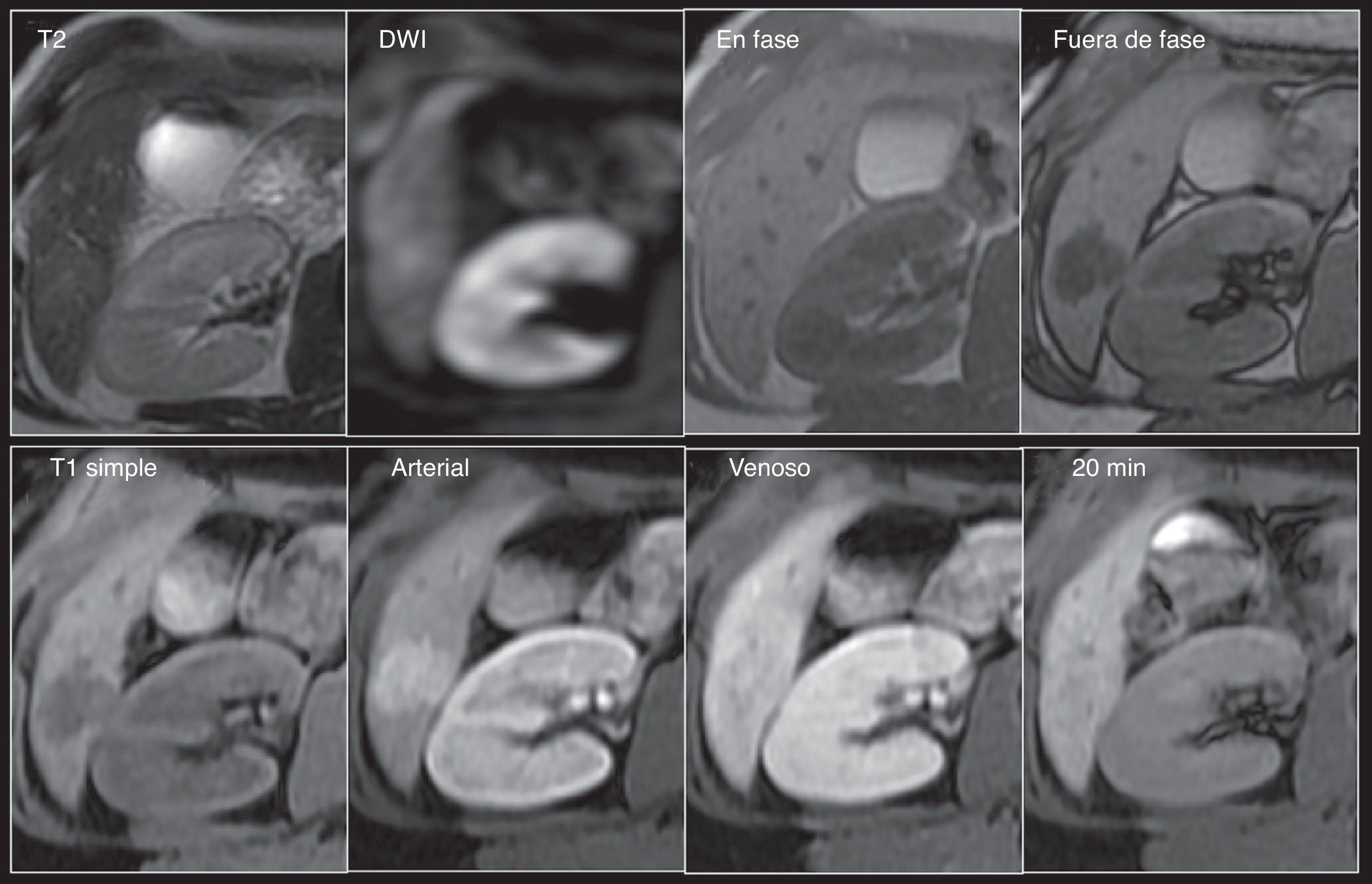
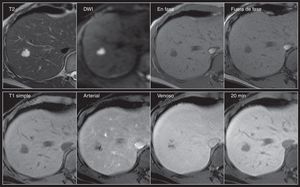
Hemangioma. Mujer de 56 años con hallazgo ultrasonográfico de lesión focal hepática en el segmento 8. Fila superior: Lesión nodular de contornos lobulados, hiperintensa en T2 y con importante restricción de la difusión, e hipointensa en T1 tanto en las imágenes dentro como fuera de fase. Fila inferior: Nótese el típico reforzamiento nodular periférico desde la fase arterial con llenado centrípeto progresivo en la fase venoso —intensidad de señal similar al resto del parénquima— e hipointensidad en la fase tardía de 20min, característicos del hemangioma cavernoso.
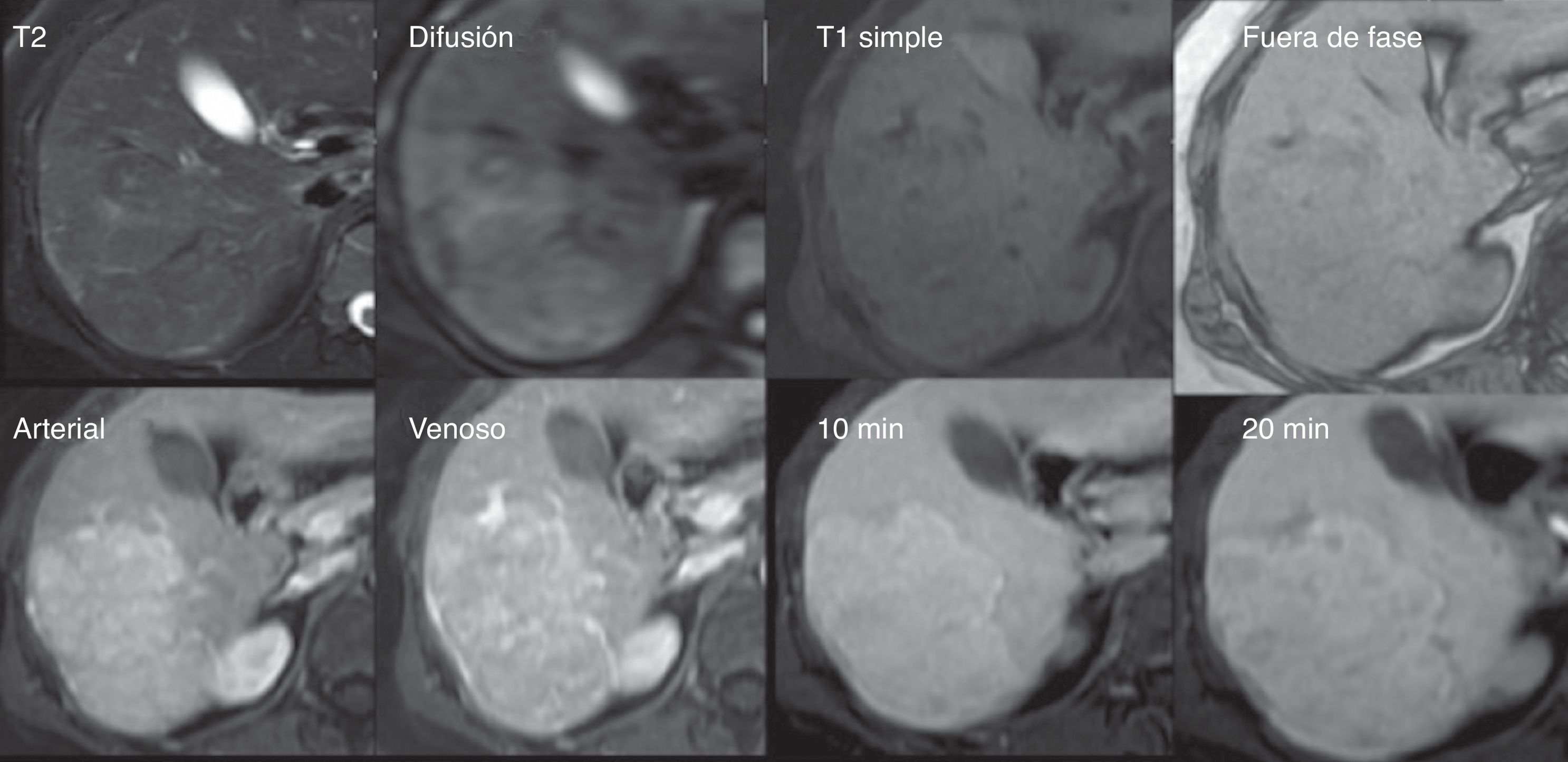
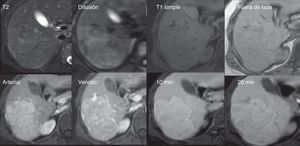
Hiperplasia nodular focal. Mujer de 42 años con lesiones focales en los segmentos 6 y 7 con ultrasonido y tomografía computarizada indeterminados. La distinción entre adenoma vs. hiperplasia nodular focal es relevante debido a su distinto manejo. Fila superior: Lesión nodular isointensa en T2, con cicatriz central hiperintensa en la difusión (DWI) e isointensa al resto del parénquima en T1 sin decaimiento de la señal en la secuencia fuera de fase. Fila inferior: En las secuencias dinámicas con ácido gadoxético, la lesión presenta realce desde la fase arterial. En las fases de equilibrio y hepatobiliar de 20min muestra un comportamiento similar al resto del parénquima, llamando la atención la presencia de una cicatriz central hipointensa —carente de hepatocitos—; estos datos son típicos de la hiperplasia nodular focal.
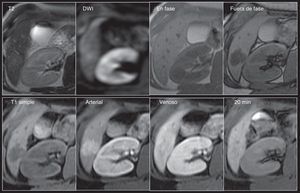
Adenoma. Mujer de 40 años con lesión focal en el segmento 6 observada por ultrasonido. Por TCMD no fue posible distinguir entre adenoma o hiperplasia nodular focal sin cicatriz central. Fila superior: Lesión hiperintensa al resto del parénquima en T2 con discreta restricción a la difusión (DWI), isointensa en las imágenes T1 dentro de fase y marcadamente hipointensa en la secuencia fuera de fase. Fila inferior: La lesión muestra reforzamiento importante en la fase arterial y es isointensa en las fases venosa y hepatobiliar. Es importante recordar que el comportamiento con el contraste HE dependerá del subtipo de adenoma. En este caso, la distinción con la hiperplasia nodular focal se pudo establecer debido a la importante caída de señal observada en las imágenes fuera de fase, característica de la presencia de grasa intralesional en los adenomas.
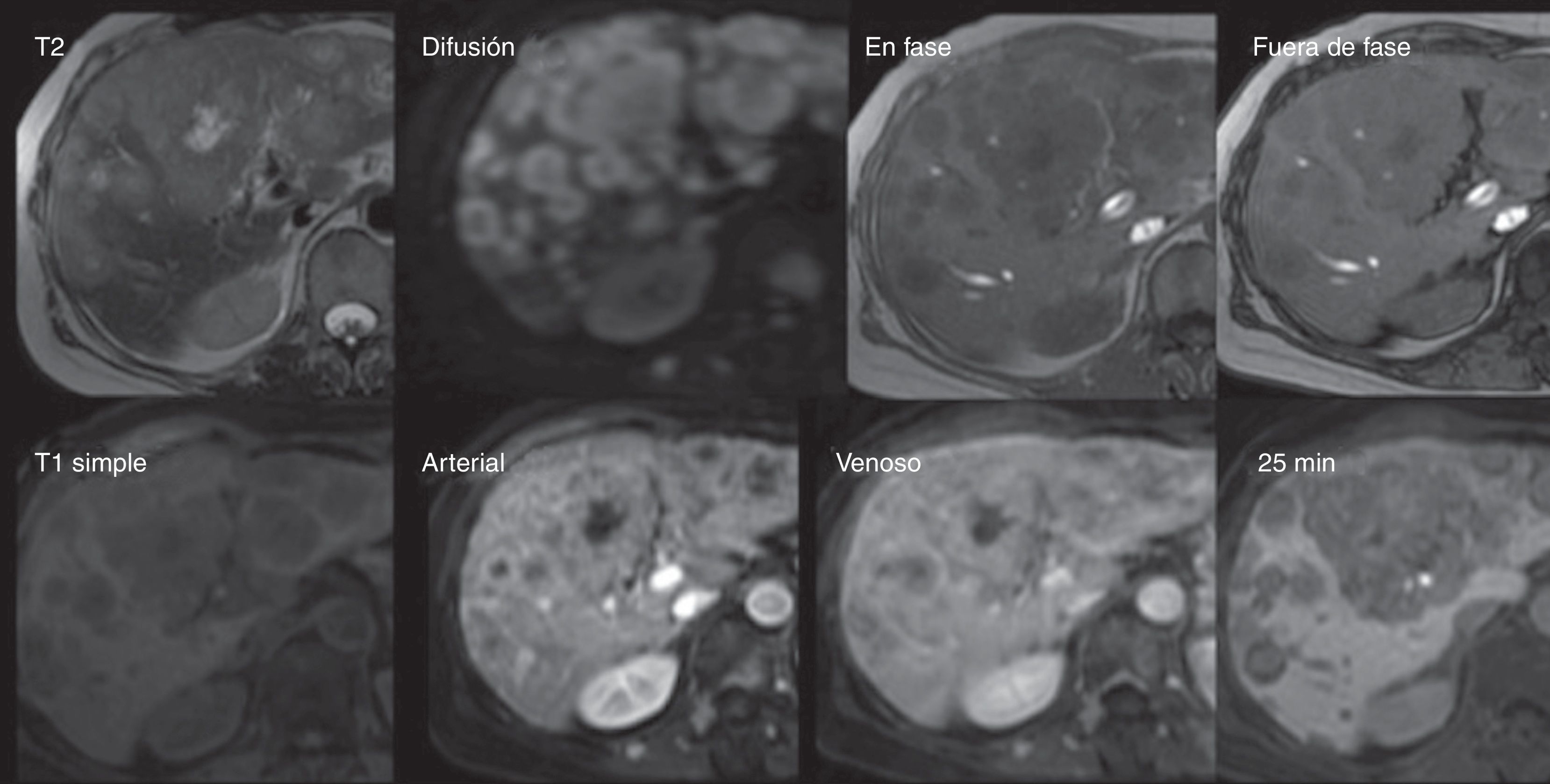
Metástasis. Mujer de 61 años con antecedente de cáncer de mama izquierdo. En ultrasonido de seguimiento se identifican múltiples lesiones focales dispersas en el parénquima hepático. Se realiza RM para mejor caracterización. Fila superior: Presencia de múltiples imágenes redondeadas, de distribución difusa, hipointensas en T1 e hiperintensas en T2 y difusión (DWI), sin decaimiento de la señal en la secuencia fuera de fase. Fila inferior: En las secuencias dinámicas con ácido gadoxético, dichas lesiones presentan reforzamiento en anillo en la fase arterial y centrípeto en las fases más tardías; en fase hepatobiliar se observan hipointensas por ausencia de hepatocitos—De manera adicional se identifican otras lesiones de similares características y reforzamiento en los cuerpos vertebrales y músculos paravertebrales. Datos en relación con metástasis.
Sin embargo, existen aún un grupo de pacientes en quienes el empleo de este tipo de contrastes es limitado. En particular, pacientes con disfunción hepática (hiperbilirrubinemia>3mg/dL), aquellos pacientes con lesiones focales en quienes interesa además evaluar la permeabilidad vascular sobre todo la portal debido al bajo volumen de contraste empleado, en el seguimiento postablación de CHC, y como se mencionó con anterioridad, aquellos individuos con CHC bien diferenciados que pueden acumular el medio de contraste en las fases tardías hepatobiliares y en pacientes con hemangiomas de llenado rápido7. Un análisis global y conjunto de las características por RM de la lesión en las secuencias de difusión y su comportamiento en T2 puede ser útil para establecer la distinción entre estas entidades.
Artificios respiratorios. Se ha demostrado que la adquisición triple de la fase arterial con una sola apnea proporciona imágenes adecuadas en la mayoría de los pacientes que experimentan artificios de movimiento respiratorio en la fase arterial con el uso del agente hepatoespecífico39.
Otros puntos a considerar son el costo (hasta 3 veces superior), el impacto en el tiempo de exploración (20min más en la duración del estudio) y el potencial menor realce en la fase arterial con el empleo de dosis aprobadas (0.025mmol/kg)3.
ConclusionesLa reciente introducción de contrastes HE en la evaluación de lesiones focales hepáticas es un complemento adicional potencialmente útil en aquellas lesiones consideradas como indeterminadas, ya sea en tumores>2cm sin un comportamiento característico en los estudios multifásicos con gadolinio convencional o por tomografía computarizada, o en aquellas lesiones<2cm en pacientes con hepatopatía de base, en quienes la detección temprana y precisa de CHC es fundamental.
Por este motivo, si bien el papel de este tipo de medios de contraste aún se encuentra por definir a través de ensayos clínicos con mayor número de pacientes, sobre todo en pacientes con cirrosis avanzada, su uso puede ayudar a mejorar la sensibilidad y especificidad diagnósticas cuando se compara con el desempeño de las estrategias convencionales en estos grupos de pacientes.
FinanciamientoNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener conflictos de intereses.