¿ I. Síndrome de intestino irritable
El síndrome de intestino irritable (SII) es un trastorno heterogéneo que puede afectar entre 10% y 20% de la población.1 Debido a su alta prevalencia, a la cronicidad de sus síntomas y al impacto en la calidad de vida, los costos implicados son enormes.2,3 Por ejemplo, múltiples estudios han mostrado que los pacientes con SII utilizan más los servicios de salud (en términos de consultas, exámenes de laboratorio, medicamentos, e incluso cirugías), que aquellos con enfermedades orgánicas sin SII.4,5 Otro hecho relevante es que la mayoría de quienes padecen este trastorno, se encuentran entre la tercera y quinta décadas de la vida, y ven considerablemente afectada su productividad.6
Asimismo, una vez que se diagnostica este problema, el 75% de los sujetos permanece sintomático durante cinco años en promedio.7 Todos estos factores contribuyen a que el costo del diagnóstico y tratamiento de estos pacientes sea elevado; por ejemplo, los costos directos e indirectos en Estados Unidos por el manejo del SII son cercanos a los 30 mil millones de dólares por año.8,9
¿ Definición
Actualmente, el diagnóstico de SII se considera "positivo" y no de exclusión, lo que significa que se basa en la presencia de síntomas característicos.
Dado que no existen biomarcadores en el SII, se han diseñado a través de los años criterios clínicos basados en estas manifestaciones. Actualmente los más utilizados son los criterios de Roma II, aunque desde 2006 están disponibles los criterios de Roma III10 (Tablas 1 y 2), los cuales han mostrado tener una sensibilidad de 70.7%, una especificidad de 87.8%, y un valor predictivo positivo cercano al 100%. Estos últimos criterios se encuentran en proceso de traducción y validación en nuestra población.11
La nueva propuesta de Roma III radica sustancialmente en subclasificar a los pacientes de acuerdo a las formas de las evacuaciones utilizando la escala de Bristol, aunque la relación de estos subtipos con los mecanismos fisiopatológicos asociados al SII se desconoce. Simren y colaboradores12 evaluaron prospectivamente en 129 pacientes la relación entre mecanismos fisiopatológicos (tránsito colónico, motilidad antroduodenal e hipersensibilidad rectal) y los subtipos de SII de acuerdo a Roma III, y demostraron que los pacientes con SII asociado a estreñimiento (SII-E) tienen un tránsito colonico más lento (1.8 ± 2.9 días) y los que tienen SII asociado a diarrea (SII-D) un tránsito más acelerado (1 ± 1.4 días). También documentaron que los pacientes con SIID tuvieron mayor frecuencia de contracciones antroduodenales durante el ayuno, mayor duración de la fase III del complejo motor migratorio y mayor velocidad de propagación del mismo comparados con los otros grupos (p < 0.05). Como hallazgo interesante, la sensibilidad, el tono y la distensibilidad rectales fueron similares entre los diversos subtipos de SII. Así pues, se demuestra que los nuevos criterios de Roma III sí se asocian a alteraciones motoras, mas no con fenómenos de hipersensibilidad visceral.
Uno de los problemas surgidos con el uso de Roma III es que aparentemente existen poblaciones donde el subtipo más común es el SII mixto (SII-M), a diferencia de lo reportado con los criterios de Roma II. Utilizando un análisis denominado "evaluación momentánea ecológica", el grupo de Drossman13 demuestra que los sujetos con SII-M tienen síntomas muy relacionados y similares a los de los pacientes con SII-E, por lo que sugieren que en estos casos el abordaje terapéutico debe ser similar al utilizado en el SII-E.
¿ Epidemiología
En nuestro país la prevalencia es similar a la reportada en la literatura mundial y se han realizado al menos tres trabajos: Uno con vo luntarios universitarios en el Distrito Federal en el que, utilizando un cuestionario con los criterios de Roma II, se encontró una prevalencia de 35.5% (IC 95% 30.4-41.0);14 otro en el que se utilizó el mismo cuestionario y se realizó en población abier ta del Estado de Tlaxcala, que mostró una prevalencia de SII de 16.0% (IC 95% 12.9-19.5),1 y el tercero, en población abierta de la ciudad de Veracruz, que reportó una prevalencia de 16.7%.15 Los subtipos más comunes encontrados son el SII-E y en segundo lugar el SII-M. Al igual que en otros países la prevalencia de esta enfermedad es mayor en mujeres y más común entre los 30 y 50 años.
¿ Fisiopatología
Aunque no se conoce cuál es la causa del SII, actualmente se cree que su etiología es multifactorial con interacción de varios agentes que conducen a alteraciones sensitivas y motoras dentro del sistema nervioso entérico. Las infecciones, los trastornos emocionales y la dieta son algunos de los factores implicados con mayor frecuencia en estas alteraciones.
Los agentes infecciosos han cobrado relevancia en los últimos años; este nuevo paradigma resulta muy interesante pero controversial. Con respecto a la dieta, muchos pacientes refieren que sus síntomas tienen relación directa con la ingesta de alimentos; mientras en algunos las molestias desaparecen con la suspensión de ciertos alimentos, otros describen una franca exacerbación de su sintomatología.
La probabilidad de que la flora entérica o microbiótica juegue un papel en la patogénesis del SII, ha comenzado a atraer la atención científica a pesar de que desde hace algún tiempo existen pruebas que sugieren un vínculo y hay varios puntos muy controversiales.
El término de SII postinfeccioso es cada día más familiar y se ha utilizado para los sujetos que desarrollan síntomas de SII luego de una infección gastrointestinal (viral, bacteriana e incluso parasitaria). El estudio de Walkerton en Ontario16 es conocido por ser uno de los más representativos del SII postinfeccioso. En éste se evalúo a una cohorte de 4 561 sujetos que en Mayo de 2000 estuvieron expuestos a aguas contaminadas por E. coli 0157:H7 y Campylobacter sp y se analizó la prevalencia de SII a 12 meses, demostrando que cerca 40% de los sujetos que tuvieron infección desarrollaron SII. Ocho años después del brote infeccioso, el mismo grupo de investigadores17 demuestra que aunque a lo largo del tiempo los síntomas tienden a disminuir, la prevalencia del SII sigue siendo significativamente mayor que en la población general. De forma interesante los autores reportan la prevalencia de dispepsia postinfecciosa en esta misma cohorte de pacientes demostrando que la prevalencia de dispepsia es significativamente mayor en los sujetos expuestos que en los controles (49.3% vs 30%, RM 2.27, IC 95% 1.74-2.95).18
Mucho se ha dicho que probablemente algunos parásitos sean responsables de síntomas atribuibles a SII siendo también controvertido el papel de las parasitosis en estos casos. Un estudio que resulta muy interesante es el presentado por Wensaas y colaboradores19 y realizado en Noruega donde tras un brote de giardiasis (n = 1 250) se reporta que a tres años (n = 818), 45.3% de los pacientes desarrollaron SII (RR 3.31, IC 95% 2.80-3.92), 19.3% dispepsia funcional (RR 3.37, IC 95% 2.55-4.45) y 46.2% manifestaron síntomas atribuibles a síndrome de fatiga crónica (RR 3.80, IC 95% 3.18-4.532). Esto resulta interesante ya que existe una alta prevalencia de SII asociada a otros trastornos funcionales, además de llamar la atención por la alta prevalencia de giardiasis en un país como Noruega.
El interés en el rol de las bacterias como agentes responsables del SII se ha reavivado a raíz de la hipótesis que plantea un sobrecrecimiento bacteriano hasta en el 80% de quienes sufren de SII.20,21 Este nuevo paradigma, aún muy controversial, sugiere que el excesivo crecimiento de bacterias puede estar asociado con alteraciones en la función motora del intestino delgado y ser la causa de los síntomas (especialmente distensión e inflamación abdominal), más aún cuando la erradicación de esta sobrepoblación bacteriana utilizando antibióticos se ha acompañado de una mejoría sintomática superior al 80%.20,21 Estos sorprendentes resultados han recibido múltiples críticas porque se ha cuestionado la reproducibilidad de los datos, se ha utilizado un estándar de oro imperfecto para el diagnóstico de sobrepoblación (pruebas de aliento con lactulosa), y la mejoría sintomática se ha analizado a corto plazo con instrumentos que evalúan múltiples síntomas.
En una revisión sistemática y metanálisis acerca de la prevalencia de sobrepoblación bacteriana (SPB), Moayyedi y colaboradores22 encontraron que de 2 452 estudios, sólo 16 fueron elegibles y evaluados, y únicamente 11 cumplieron la metodología necesaria; es más, sólo seis contaron con controles sanos. Considerando a la prueba de aliento con lactulosa como el estándar de oro, se estimó una prevalencia de SPB del 61%, con la prueba de aliento con glucosa ésta fue del 28%, mientras que con aspirado y cultivo duodenal fue de 4%. En el análisis global, independientemente de la prueba se estimó que la razón de momios para SPB en SII es de 3.6 (IC 95% 1-12.4), concluyendo que existe una gran heterogeneidad en los estudios y que la asociación entre SII y SPB es cuestionable.
Sin embargo, la asociación es interesante y prometedora para explicar síntomas en un subgrupo de pacientes como son aquellos con SII-D y distensión abdominal.
¿ Tratamiento
Actualmente se considera que el paciente con SII debe recibir un tratamiento "integral" con un perfil de seguridad adecuado y dirigido a la mejoría global de sus síntomas y de su calidad de vida . El tratamiento puede basarse en el síntoma más molesto para el paciente (dolor abdominal o distensión), en el hábito intestinal predominante (diarrea o estreñimiento) o en la fisiopatología de la enfermedad (comorbilidad psiquiátrica, hipersensibilidad visceral, etc.).
En general, entre los fármacos utilizados para el manejo tradicional del SII se incluyen antiespasmódicos, laxantes, antidiarreicos, analgésicos viscerales, y antiflatulentos. Además, se ha demostrado que el uso de antibióticos, probióticos y agentes que actúan sobre receptores de la serotonina y canales de cloro pueden ser útiles para el manejo del SII.
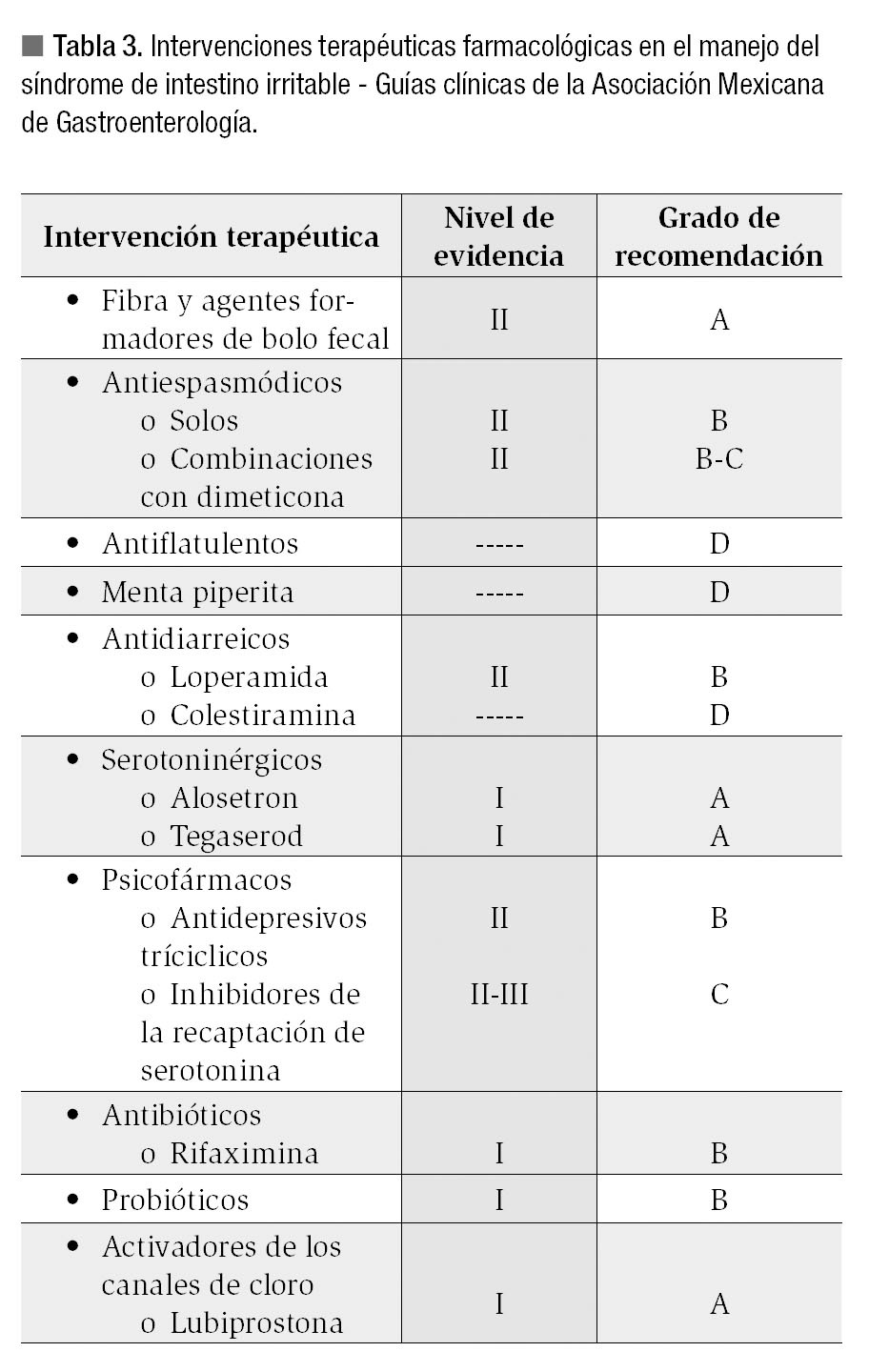
La Asociación Mexicana de Gastroenterología23 publicó recientemente las guías clínicas de diagnóstico y tratamiento del SII, así como una revisión técnica sobre el tema24 con recomendaciones específicas respecto al uso de cada una de las intervenciones terapéuticas en el manejo de los pacientes con SII (Tabla 3).
¿ II. Estreñimiento
El estreñimiento es un síntoma gastrointestinal común que se presenta entre el 2% y el 20% de la población general;25,26 en Estados Unidos afecta al menos al 10% de la población y anualmente es responsable de más de 2.5 millones de visitas médicas y de 92 000 hospitalizaciones.27 Si consideramos que al 85% de estos pacientes en algún momento se le prescribe algún laxante, los costos relacionados con este problema son extremadamente altos; por ejemplo, en 1994 ascendieron a 840 millones de dólares.28,29 El estreñimiento es un problema cuya prevalencia es mayor en mujeres que en hombres, en niños que en adultos, en pacientes de edad avanzada que en jóvenes y en personas no anglosajonas.30 Aunque en la mayoría de los casos es de naturaleza leve e intermitente, sin una causa orgánica identificable y se resuelve exitosamente con modificaciones higiénico-dietéticas (por ejemplo, ejercicio e ingesta de fibra), existe un pequeño grupo de pacientes con síntomas crónicos que resultan muy difíciles de tratar. Estos pacientes son los que detrás su evaluación y manejo inicial son referidos al gastroenterólogo.31
¿ Definición
El término "estreñimiento" puede tener diferentes significados para los individuos, ya que depende principalmente de cómo percibe cada sujeto su hábito intestinal. Sin embargo, la mayoría de los pacientes con estreñimiento refiere uno o más de los siguientes síntomas: Evacuaciones duras, infrecuentes, acompañadas de esfuerzo excesivo y sensación de evacuación incompleta.32 La frecuencia de las deposiciones es uno de las manifestaciones que pueden medirse de una forma más objetiva y en base a esto ha sido podido establecer cuál es la frecuencia normal en la población general. Por ejemplo, un estudio epidemiológico realizado en el Reino Unido demostró que el 98% de los adultos presenta tres o más evacuaciones por semana.33 Así, el tener menos de dos evacuaciones por semana se considera anormal. La definición más aceptada para estreñimiento crónico, es la recomendada por el consenso internacional de Roma III. Aunque tradicionalmente, se ha utilizado el término de estreñimiento para describir la baja frecuencia de evacuaciones, la mayoría de los pacientes con estreñimiento refiere uno o más de los siguientes síntomas: Evacuaciones duras, esfuerzo excesivo, sensación de evacuación incompleta, sensación de "obstrucción" del canal anal y ocasionalmente necesidad de realizar maniobras digitales para favorecer la defecación. Por ejemplo, en un estudio realizado por nuestro grupo (n = 1 041) demostramos que si bien la mayoría de la población (n = 907, 87%) presenta al menos una evacuación cada 48 horas, siendo ésta tipo 3-4 en la escala de Bristol la mayor parte de las veces (67%), hasta una tercera parte (n = 356, 34%) de los sujetos considera que sufre de estreñimiento.34
¿ Etiología y mecanismos fisiopatológicos
Aunque la mayoría de las veces el estreñimiento es consecuencia de alteraciones funcionales primarias del colon y el ano o el recto, también puede estar relacionado con el uso de medicamentos, lesiones anatómicas, y enfermedades metabólicas o neurológicas (estreñimiento secundario). En ausencia de causas secundarias, se considera que el estreñimiento es primario o idiopático. Éste debe considerarse esencialmente un trastorno de la motilidad colorrectal y en la actualidad puede clasificarse en tres subgrupos: 1) Estreñimiento con tránsito colónico lento (inercia colónica), 2) disfunción del piso pélvico (disinergia del piso pélvico), y 3) estreñimiento con tránsito colónico normal (estreñimiento funcional).35,36 Además, puede existir una sobreposición entre estos subgrupos, y así por ejemplo en un estudio donde se evaluó a más de 1 000 pacientes con estreñimiento idiopático, la forma más prevalente fue el estreñimiento funcional (59%) seguido por la disinergia del piso pélvico (25%), la inercia colónica (13%) y una combinación de disinergia e inercia colónica (3%).37
1. Estreñimiento con tránsito colónico lento. Este tipo de estreñimiento se presenta con mayor frecuencia en mujeres jóvenes y se caracteriza por la presencia de evacuaciones con una frecuencia menor de tres veces por semana (usualmente una o menos) y puede asociarse a inflamación o dolor abdominal y urgencia para defecar, sin ser éstos los síntomas predominantes (incluso pueden estar ausentes).38 El problema suele iniciarse desde la pubertad y en algunos casos los factores dietéticos y culturales juegan un papel en su génesis. Sin embargo, se cree que la inercia colónica tiene alteraciones fisiopatológicas reales, y se han postulado al menos dos mecanismos: 1) Disminución en el número de contracciones colónicas propagadas de alta amplitud, y 2) aumento no coordinado de la actividad motora del colon distal, lo que produce una barrera funcional o resistencia al tránsito colónico normal.39,40 Algunos de los hallazgos histopatológicos descritos incluyen alteraciones en el número de neuronas en los plexos mientéricos que expresan la sustancia P (un neurotransmisor excitatorio),41 menor producción de neurotransmisores inhibitorios como óxido nítrico y péptido intestinal vasoactivo,42 y disminución en el número de células intersticiales de Cajal.43
2. Disfunción del piso pélvico. La disfunción o disinergia del piso pélvico ocasiona un tipo de estreñimiento que algunos autores han designado como obstructivo y que es resultado de alteraciones en los mecanismos de la defecación. Se caracteriza por la incapacidad para evacuar adecuadamente la materia fecal almacenada en el recto, aún cuando el tránsito colónico sea normal. Otros términos utilizados para referirse a este problema son: Anismo, disquezia, contracción paradójica del piso pélvico, retención rectal funcional, obstrucción rectosigmoidea y síndrome espástico del piso pélvico.44 La falla para evacuar efectivamente el recto se debe a la incapacidad para coordinar de forma adecuada los músculos abdominales y del piso pélvico durante la defecación. Otros factores que contribuyen a este trastorno son la presencia de dolor secundario a fisuras en la región perianal, intususcepción, rectocele y descenso excesivo del piso pélvico.6 Algunos pacientes tienen historia de abuso físico o sexual, así como de trastornos de la alimentación.45
3. Estreñimiento funcional. El subgrupo de estreñimiento más comúnmente visto es el que se presenta en individuos con tránsito colónico normal en quienes no existen alteraciones en los mecanismos de la defecación; a éste se le denomina estreñimiento funcional. Aunque no presentan alteraciones motoras a nivel colorrectal, estos pacientes creen estar estreñidos, ya que perciben dificultad para evacuar y aumento en la consistencia de las heces. Si el síntoma principal es la inflamación o el dolor abdominal asociado a alteraciones en la frecuencia y consistencia de las evacuaciones, debe considerase que se trata de un SII con predominancia de estreñimiento.46 Los pacientes que no experimentan dolor o inflamación pero sí esta percepción alterada de la frecuencia y consistencia en las evacuaciones, son los que realmente deben clasificarse como casos de estreñimiento funcional.
¿ Abordaje diagnóstico
El primer paso en la evaluación del estreñimiento es excluir enfermedades metabólicas y alteraciones estructurales del colon. Se recomienda realizar citología hemática completa, perfil bioquímico (glucosa, urea y creatinina), determinación de calcio y pruebas de función tiroidea si el contexto clínico del paciente lo amerita. Cuando existen datos de alarma (estreñimiento de reciente aparición, fiebre, anorexia, pérdida de peso, historia familiar de neoplasias gastrointestinales) o el paciente es mayor de 50 años se requiere una evaluación completa del colon para descartar organicidad, específicamente neoplasias colorrectales. En estos casos se considera que la colonoscopia debe ser el estudio de primera elección; de no ser factible este procedimiento se sugiere realizar un colon por enema con doble contraste y rectosigmoidoscopia flexible.
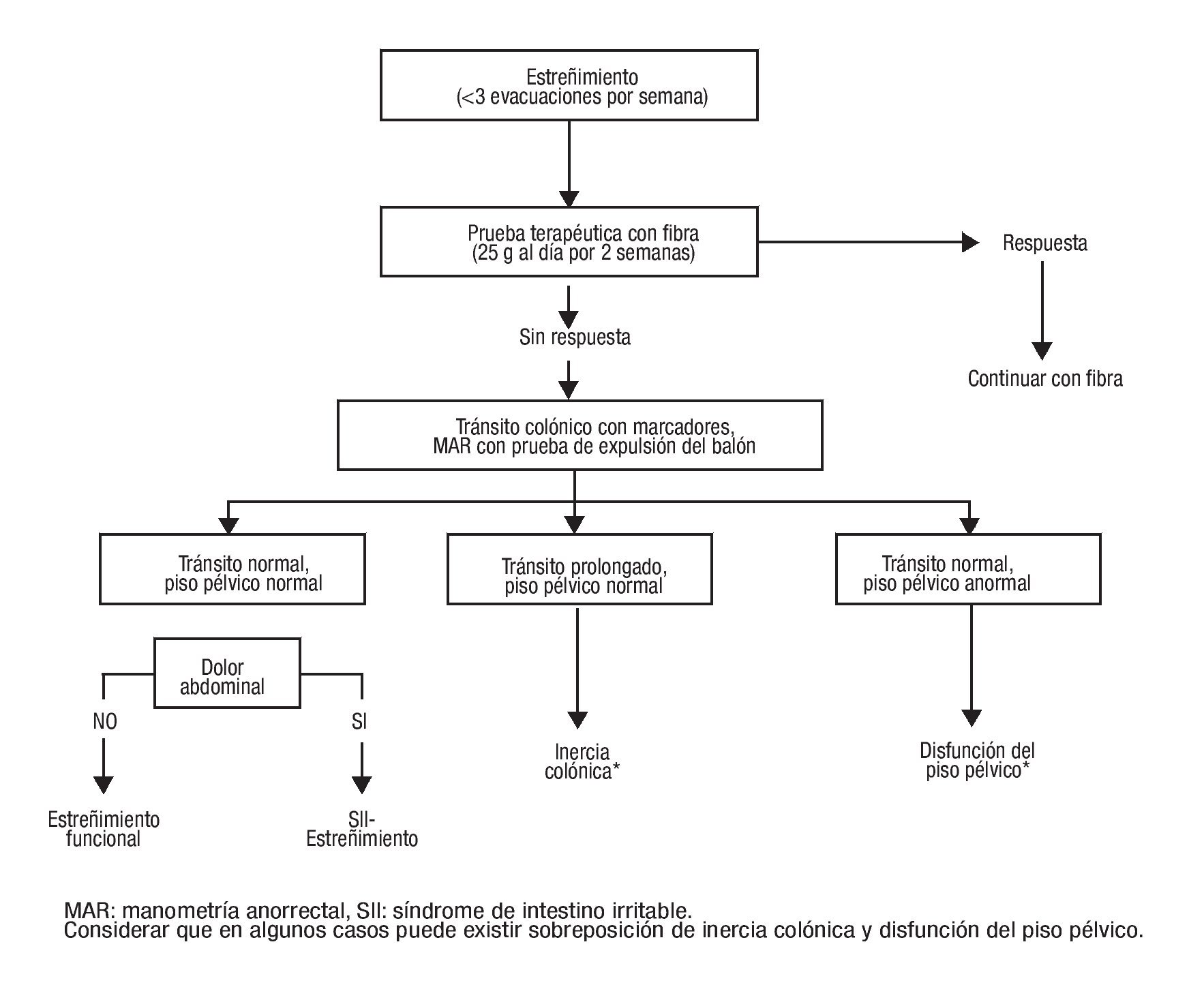
Antes de iniciar el abordaje diagnóstico es recomendable que el paciente complete al menos dos semanas de tratamiento con una dieta rica en fibra (25 g divididos en dos tomas diarias). Si el paciente no tolera esta cantidad de fibra, se recomienda reducir 50% la dosis en la primera semana y posteriormente incrementarla gradualmente hasta alcanzar la dosis sugerida. Sólo aquellos pacientes que continúen con menos de tres evacuaciones por semana después de esta prueba terapéutica deben ser sometidos a estudios fisiológicos colorrectales más avanzados para tratar de establecer la causa del estreñimiento. Se recomienda practicar inicialmente en todos los casos una evaluación del tránsito colónico. En la Figura 1 se propone un algoritmo para el abordaje diagnóstico del estreñimiento crónico.
¿ Figura 1.Algoritmo diagnóstico para la evaluación del estreñimiento.
¿ Tratamiento
Dentro de las medidas generales, todos los pacientes deben recibir información adecuada respecto al consumo de fibra, la ingesta suficiente de líquidos y la práctica de ejercicio. A los obsesionados con el hecho de que deben evacuar diariamente, se les ha de explicar que el patrón normal de evacuaciones puede ser de incluso una deposición cada tercer día. En cuanto a la dieta, se debe recomendar la necesidad de incluir al menos 20 a 30 g de fibra al día, proveniente de ser posible de fibra natural e ingerir al menos entre seis y ocho vasos de agua al día.47 Debido a que el inicio de la defecación es un reflejo condicionado aprendido, se debe enfatizar que el sujeto establezca un patrón regular de evacuaciones, habitualmente en las primeras dos horas después de levantarse y después del desayuno.
Estreñimiento con tránsito colónico lento. Los laxantes son la piedra angular en el tratamiento de este subgrupo de pacientes. Inicialmente, todos los sujetos deben realizar una prueba con laxantes formadores de bolo (psyllium, ispagula o metilcelulosa) como medicamentos de primera línea.47,48 Si el problema persiste o la cantidad de fibra es poco tolerada, se ha de recurrir a los agentes hiperosmóticos como el hidróxido de magnesio, la lactulosa y el polietilenglicol.24 En una revisión sistemática reciente, este último resultó ser el tratamiento más eficaz y con menos efectos adversos dentro de este grupo de medicamentos de segunda línea.49 La dosis recomendada es variable, pero habitualmente es de 10 a 20 gramos al día en dosis divididas. El uso de laxantes de tercera línea, como los emolientes (docusato de sodio o docusato de calcio) y los estimulantes (cáscara sagrada y sen) debe ser limitado y por corto tiempo debido a sus efectos adversos. Los procinéticos como cisaprida y en especial tegaserod (6 mg dos veces al día) han mostrado ser suficientemente eficaces para el manejo de estos pacientes.50
Estreñimiento obstructivo. La terapia de biorretroalimentación es el tratamiento de elección para este tipo de estreñimiento y consiste en reeducar los músculos del piso pélvico y el esfínter anal a través de estímulos visuales y auditivos.51
El objetivo es enseñar a los pacientes a relajar los músculos del piso pélvico durante el pujo y coordinar esta relajación con maniobras abdominales que favorezcan la defecación. Esta terapia se puede realizar con manometría anorrectal o electromiografía. Los beneficios parecen mantenerse a largo y plazo y el porcentaje de éxito es cercano al 70%.48
Cirugía. En los pacientes que a pesar del tratamiento médico persiste el estreñimiento y en los que hay evidencia de que no tienen disfunción del piso pélvico, se puede considerar como última medida el tratamiento quirúrgico. En general éste se indica en pacientes que después de un mínimo de tres meses de tratamiento médico intensivo no tienen mejoría. Antes de decidir la cirugía es importante verificar que el problema está confinado al colon y que no existe una disfunción neuromuscular intestinal generalizada. Para este propósito, se recomienda realizar estudios de vaciamiento gástrico, manometría esofágica y manometría antroduodenal.52 Las opciones quirúrgicas incluyen colectomía con ileostomía o con anastomosis ileorrectal. El porcentaje de satisfacción posterior a la colectomía varía entre 39 y 100% y las complicaciones más comunes son obstrucción intestinal, diarrea e incontinencia.53 Finalmente, los pacientes que tienen rectocele con repercusión clínica deben ser sometidos a corrección quirúrgica.