La prevalencia del síndrome de intestino irritable (SII) es muy elevada, lo que comporta una gran repercusión sanitaria, social y económica. El número de consultas médicas, de pruebas diagnósticas (en este caso no diagnósticas) y de prescripciones terapéuticas es muy grande, con el consiguiente gasto de recursos. El SII supone, además, una de las primeras causas de absentismo laboral. Por otra parte, si bien el SII no pone en riesgo la vida del paciente sí condiciona de forma considerable la calidad de ésta.
Se han publicado diversos estudios epidemiológicos sobre la prevalencia del SII y se ha hallado que ésta oscila entre 5% y 20%, dependiendo de la población estudiada y de los criterios diagnósticos empleados.1 En cualquier caso, el SII está presente en todos los países y constituye una causa importante de frecuentación médica. Desde hace mucho tiempo se ha dicho que sólo la tercera parte de los sujetos con SII buscaban atención médica. Aunque estos datos procedían de investigaciones en Estados Unidos de América (EUA),2 los obtenidos en la población española demuestran que más de las dos terceras partes de personas con SII acuden al médico.3 Los motivos por los que unas personas buscan asistencia sanitaria y otras no lo hacen no están del todo claros. Algunos estudios parecen indicar que la razón fundamental es la intensidad de las molestias, mientras que según otros los factores psicosociales son los determinantes. Otro de los factores que sin duda influye en la decisión de consultar al médico es la facilidad de acceso y gratuidad del sistema sanitario en el que se encuentra el paciente. Así, en España el 58% de los sujetos con SII con estreñimiento y el 67% de SII con diarrea buscan atención sanitaria.4
Teniendo en cuenta los datos anteriores es obvio que la repercusión económica del SII es muy grande. Para su cálculo han de tenerse en cuenta tanto los costes directos (visitas médicas, procedimientos diagnósticos, precio del tratamiento, consultas de urgencia o ingresos hospitalarios) como los costes indirectos (absentismo laboral, disminución en la productividad o cirugía innecesaria). Durante el año 2000 en EUA los costes directos del SII fueron de 1 353 millones de dólares y los indirectos de 205 millones de dólares.5 A este enorme monto habría que sumarle todas aquellas medicaciones que no precisan prescripción médica y también los gastos paramédicos que corren a cargo del enfermo.
Además, los estudios que han comparado la repercusión de la enfermedad en la calidad de vida han constatado que el deterioro es similar en los pacientes con SII y enfermedad inflamatoria intestinal (EII).6 ¿Puede alguien seguir pensando que el SII es una enfermedad de segunda? ¿Es poco importante porque el intestino de los pacientes que lo padecen no está (visiblemente) inflamado? ¿Es éste sólo el hermano pobre - y aún no adoptado - de la EII?
¿ Diagnóstico clínico del síndrome de intestino irritable
Con el objetivo de buscar un diagnóstico positivo del SII, y que no se trate solamente de un diagnóstico de exclusión, se han descrito diversos criterios que agrupan diferentes síntomas considerados como fundamentales. Esta aproximación al diagnóstico no es nueva de la patología digestiva ya que ha sido utilizada con mucha frecuencia tanto para enfermedades reumatológicas como para trastornos psiquiátricos. En el caso del SII gran parte del mérito se debe a Manning y colaboradores quienes en 1978 publicaron los primeros criterios.7 Posteriormente, en 1992, se establecieron unos más precisos, los llamados "criterios de Roma",8 que inicialmente incluían síntomas de posible estreñimiento, y no sólo de diarrea como ocurría con los de Manning. Estos criterios de Roma fueron modificados y se añadió la duración mínima de los síntomas de tres meses.9 Con el tiempo, en 1999, un grupo de expertos consideró que era preciso acotar más la temporalidad del síndrome para establecer el diagnóstico y decidieron que los síntomas debían haber estado presentes al menos durante 12 semanas (no necesariamente consecutivas) durante los últimos 12 meses; nacieron así los "criterios de Roma II".10 En la actualidad, desde 2006, el diagnóstico clínico del SII debe seguir los "criterios de Roma III" en los que tan sólo se necesita tener molestias tres días al mes en los últimos tres meses, aunque con inicio de los síntomas cuando menos seis meses antes.11
Probablemente los criterios de Roma son importantes (e inexcusables) a la hora de incluir pacientes en estudios de investigación. No obstante, muchos enfermos con síntomas presentes no los cumplen; también ellos deberían beneficiarse de los avances fisiopatológicos y terapéuticos dirigidos a aquellos en quienes se cumplen todos los criterios y se establece el diagnóstico.12 Otro posible defecto de los actuales criterios diagnósticos es que no tienen en cuenta aspectos que con enorme frecuencia acompañan al síndrome como son las manifestaciones extradigestivas y los trastornos psicológicos. Si verdaderamente consideramos al SII en la esfera biopsicosocial parecería lógico incluir alguno de estos aspectos en la valoración diagnóstica.
¿ Posibles conexiones entre el síndrome de intestino irritable y la enfermedad inflamatoria intestinal
Las enfermedades se conocen inicialmente por sus manifestaciones clínicas. Después, el estudio de sus mecanismos fisiopatológicos y sus respectivas respuestas terapéuticas hacen que sean clasificadas de una u otra manera. De tal forma, si un paciente padece dolor abdominal y diarrea su cuadro puede corresponder tanto a un SII como a una EII. Naturalmente, al realizar las exploraciones complementarias se demostrará si existen o no lesiones morfológicas evidentes y si el diagnóstico definitivo es de SII o de EII. Pero, ¿y si la causa de ambos fuese común?, ¿y si fuesen los extremos opuestos del espectro de la inflamación intestinal, la micro y la macroinflamación?, ¿y si la EII es la expresión inflamatoria de una causa común y los pacientes con SII no logran desarrollar esos mecanismos inflamatorios? Evidentemente, no se trata más que de especulaciones aunque algunos datos indican que esta hipótesis no es totalmente descabellada. La posible conexión entre SII y EII se podría sustentar en cinco puntos: En primer lugar, ambas patologías presentan síntomas semejantes; en segundo lugar, con frecuencia los síntomas se solapan en un mismo paciente; en tercer lugar, tienen una agregación familiar común; en cuarto lugar, participan de ciertos factores predisponentes comunes, tales como el antecedente de una gastroenteritis aguda (GEA); y en quinto lugar, y fundamental, la demostración de signos microinflamatorios en el intestino de enfermos con SII.
El solapamiento entre SII y EII se ha analizado en diferentes estudios, en todos los cuales se ha puesto de manifiesto que la prevalencia de SII en pacientes con colitis ulcerosa o enfermedad de Crohn en fase de quiescencia es dos a tres veces superior a la de la población general.13-15 Estos datos apoyan la hipótesis de que los brotes inflamatorios podrían tener un papel fisiopatológico en el desarrollo del SII. Por otra parte, se ha podido comprobar que es muy frecuente que los pacientes con EII presenten síntomas compatibles con SII durante años antes del diagnóstico de la enfermedad inflamatoria. De hecho, la presencia de un cuadro compatible con trastornos funcionales digestivos (TFD) puede comportar un retraso en el diagnóstico de la EII.16
En los pacientes que presentan solapamiento de las dos entidades, es fundamental establecer un diagnóstico preciso del origen de los síntomas en cada momento de la evolución para así evitar tratamientos innecesarios (con esteroides o inmunomoduladores, por ejemplo) o para no retrasar la introducción de los mismos cuando verdaderamente sean necesarios. Este aspecto supone un reto importante para el médico y, en muchas ocasiones, se precisa la realización de pruebas molestas e invasivas como la endoscopia para establecer el diagnóstico diferencial. En el intento de prescindir de la endoscopia se están desarrollando y validando en la actualidad pruebas basadas en marcadores de inflamación en sangre y heces con capacidad para discriminar entre SII y EII activa.17
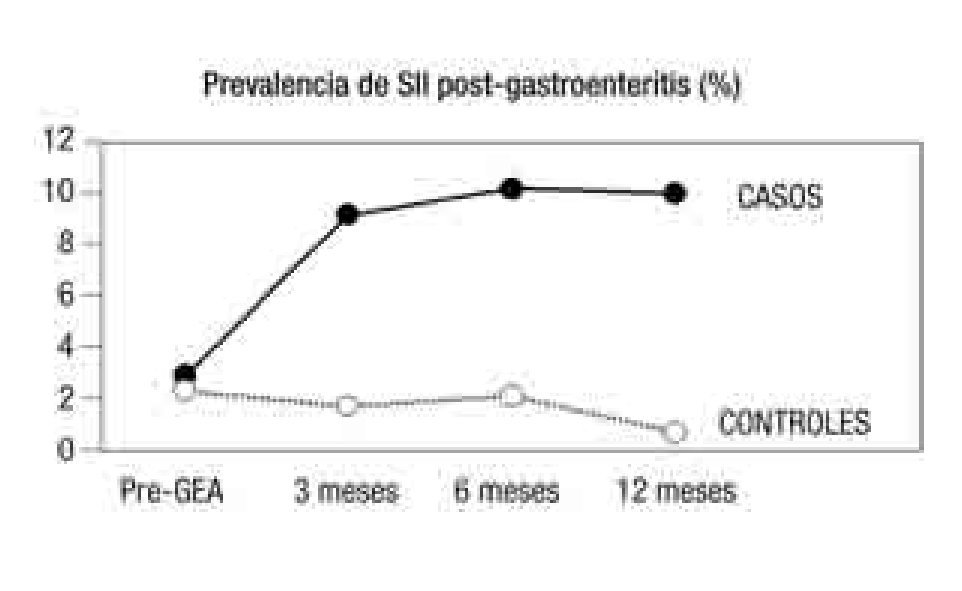
Por otra parte, se ha comprobado que los familiares de primer grado de enfermos con EII padecen dos veces más TFD que un grupo control de similares características.18 Además, tanto en el SII como en la EII el antecedente de una GEA es un factor de riesgo para padecer la enfermedad19,20 (Figura 1).
¿ Figura 1. La prevalencia del síndrome del intestino irritable (SII) aumentó de forma muy considerable a lo largo del primer año de evolución en los pacientes que sufrieron una gastroenteritis aguda por Salmonella, mientras que se mantuvo estable en los sujetos controles que no sufrieron la infección.19
Además, desde hace muchos años se especula con la posibilidad de que en el SII existan cambios inflamatorios mínimos, de difícil demostración, que serían los causantes del síndrome. Esta posibilidad convertiría a este TFD en una "forma menor" de EII.
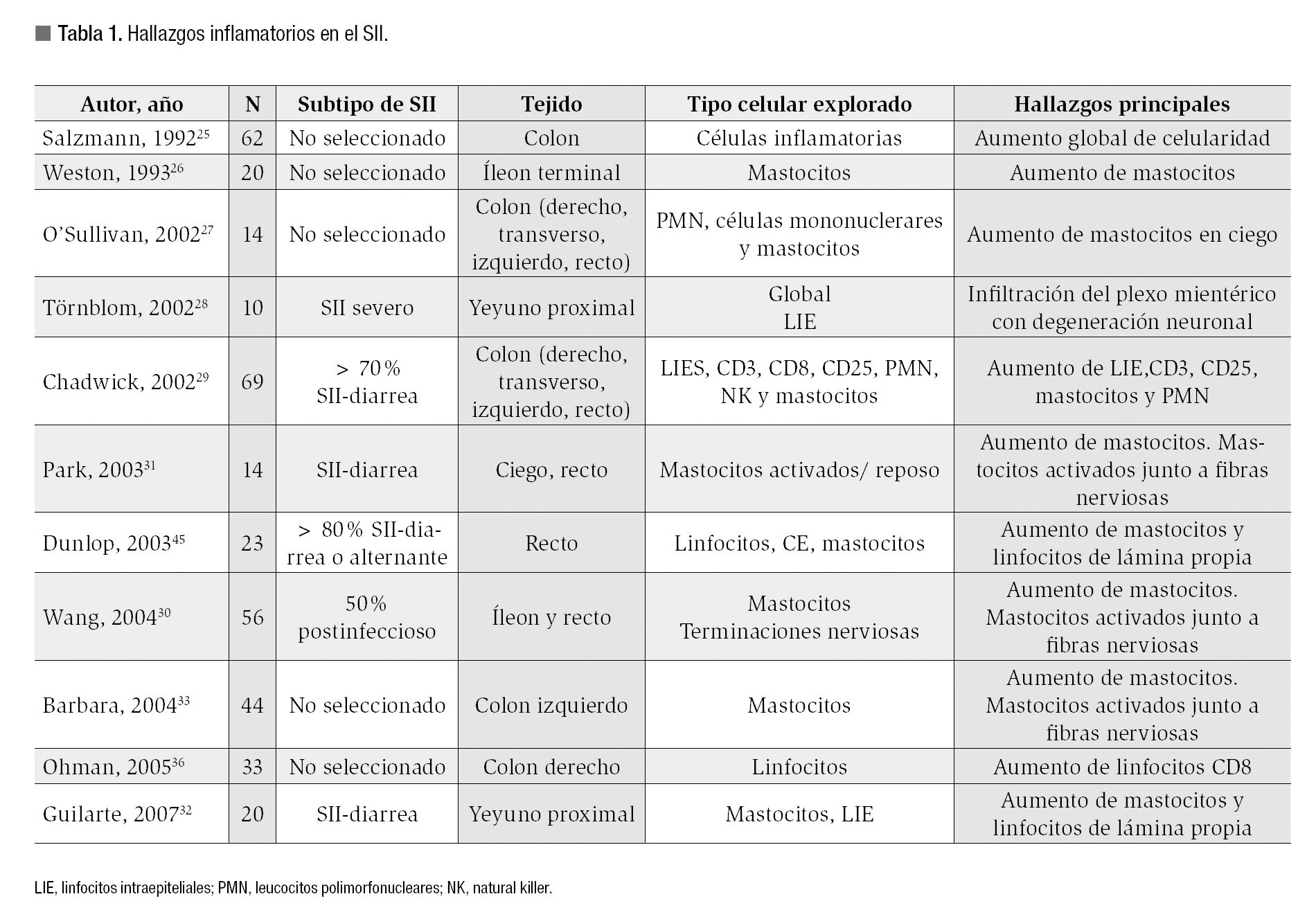
¿ Hallazgos inflamatorios presentes en el síndrome de intestino irritable
Los signos macroscópicos de inflamación, como el edema y eritema de la mucosa o la presencia de aftas o úlceras, y los signos microscópicos compatibles con colitis linfocítica o colágena obligan a descartar el diagnóstico de SII. Por lo tanto, durante años se consideró que en la mucosa intestinal de pacientes con SII no existen hallazgos inflamatorios y que su presencia descarta por completo el diagnóstico. A su vez, la investigación de la fisiopatología del SII se ha centrado en el estudio de las alteraciones de la motilidad y de la sensibilidad visceral. Así, se ha comprobado que la mayor percepción de los estímulos generados en la pared gastrointestinal o hipersensibilidad visceral es un mecanismo fisiopatológico fundamental en el SII. Sin embargo, en los últimos años, la constatación de que la presencia o la actividad de las células inmunitarias en la mucosa de pacientes con SII pueden ser diferentes a las de los individuos sanos ha llevado a postular que la inflamación o activación inmunitaria de bajo grado tienen un papel patogénico en el SII (Tabla 1). Se especula que los cambios microinflamatorios podrían ser el origen de la hipersensibilización de las terminales nerviosas a nivel del tejido intestinal contribuyendo a establecer o perpetuar la hipersensibilidad visceral.21 Esta hipótesis se ve reforzada por los estudios realizados en animales de experimentación en los que se ha podido comprobar que incluso una inflamación leve o anatómicamente distante puede provocar cambios persistentes en los nervios entéricos y en la función muscular digestiva, siendo el mecanismo responsable de la sensibilización de las terminaciones aferentes de la pared intestinal.22-24
El primer trabajo acerca de los fenómenos inflamatorios en el SII fue el publicado en 1989 por Salzmann y colaboradores,25 quienes cuantificaron la celularidad global de la lámina propia en sujetos con SII. De forma global, los 62 pacientes con SII presentaban un aumento significativo de la celularidad en la mucosa en comparación con sujetos sanos, siendo este incremento más marcado en aquellos casos de SII con predominio de diarrea. Sin embargo, en este estudio no se determinaron los tipos celulares implicados. Posteriormente dos grupos investigadores independientes coincidieron en el hallazgo del aumento en el número de mastocitos en la mucosa ileal26 y en el ciego27 en pacientes con SII no seleccionados de acuerdo a su hábito deposicional.
Un enfoque más temerario y controvertido fue el estudio de las biopsias transmurales del yeyuno proximal obtenidas mediante laparoscopia en diez pacientes con SII muy grave. El hallazgo más relevante consistió en que en todas las biopsias se observó algún grado de degeneración ganglionar del plexo mientérico asociada a infiltración linfocitaria de bajo grado. Estos resultados no son fácilmente reproducibles y, por otra parte, son discutibles debido a que el tejido control se obtuvo a partir de autopsias y a que no se conoce bien si los dos grupos fueron comparables en cuanto a la edad, la manipulación del tejido u otras circunstancias que podrían haber influido en las conclusiones.28
Chadwick y colaboradores29 realizaron el análisis microscópico sistemático de la mucosa colónica en el SII en biopsias mucosas de las cuatro regiones del colon (colon ascendente, transverso, descendente y recto) utilizando un marcaje inmunohistoquímico para la cuantificación de las diferentes células del sistema inmune (neutrófilos, mastocitos, linfocitos CD3, CD8, CD25 y NK1). En el estudio histológico de rutina de los 69 casos de SII no seleccionados (de los cuales hasta un 70% correspondieron a los subgrupos de diarrea o hábito deposicional alternante), se observaron dos patrones: 1. Normalidad histológica, y 2. Aumento inespecífico de la celularidad en la lámina propia. En ambos grupos la cuantificación de las células inflamatorias mostró diferencias significativas con la población control. Así, se observó que los linfocitos intraepiteliales y los linfocitos CD3 de la lámina propia casi duplicaban a los de la población control y el incremento de los linfocitos CD25 excedió 6.5 veces a los controles. A su vez, sólo en el grupo con un patrón de aumento inespecífico de la celularidad de la lámina propia el recuento de leucocitos polimorfonucleares y de mastocitos fue superior al conteo en las biopsias de sujetos sanos.
La constatación de un aumento de mastocitos en la mucosa de pacientes con SII llama poderosamente la atención ya que estas células, además de participar en fenómenos inflamatorios, secretan potentes sustancias neuromoduladoras con efectos sobre las terminaciones nerviosas aferentes como la histamina y la triptasa y, por tanto, podrían tener un papel relevante en la respuesta a los estímulos mecánicos y químicos.
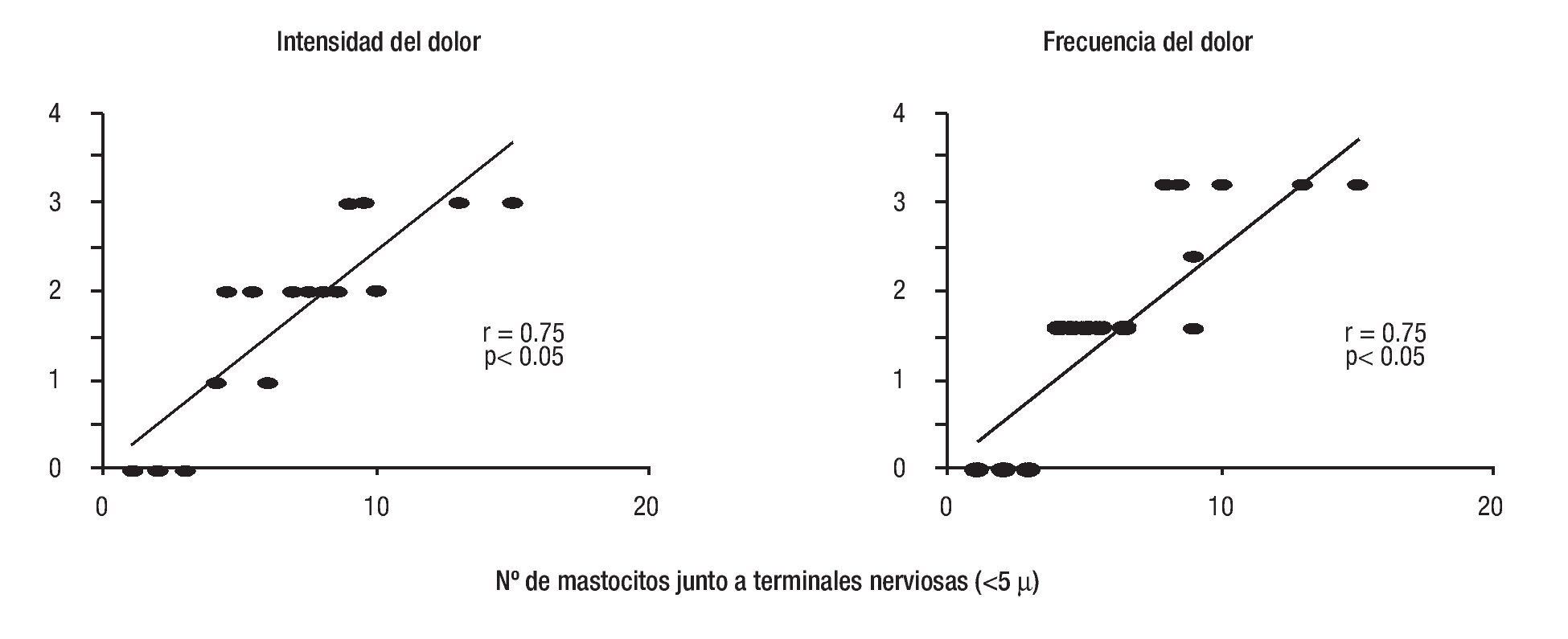
Esta hipótesis se ha comprobado en tres trabajos en los que se observa que, en la mucosa de ciego, colon izquierdo, recto e incluso de yeyuno de pacientes con SII,30-32 el número de mastocitos activados es superior al de biopsias de personas sanas. Además, se ha podido constatar un hecho fundamental, como es el que estas células mastocitarias activadas se encuentran junto a las terminales nerviosas de la mucosa, hecho que no ocurre en los controles sanos.31-33 El estudio de Barbara y colaboradores33 ha aportado además un dato clave: Existe una correlación positiva entre la intensidad de estas alteraciones mastocitarias y la intensidad y frecuencia del dolor abdominal que presentan los pacientes con SII (Figura 2). Además, un estudio más reciente ha demostrado una correlación entre la intensidad del infiltrado de mastocitos en la mucosa del colon con la presencia de depresión y de fatiga, sugiriendo también la relación entre factores psicológicos alterados y la microinflamación.34
¿ Figura 2.Correlación entre la intensidad/frecuencia del dolor abdominal y el número de terminaciones nerviosas a una distancia menor o igual a 5 micras en la mucosa del colon de pacientes con SII.33
El hallazgo del aumento de otro tipo celular, los linfocitos CD25, ha suscitado igualmente interés ya que estas células tienen una acción reguladora que se considera importante para la prevención de la autoinmunidad y para el control de la respuesta inflamatoria del intestino. Ello conduce a la hipótesis de que en los pacientes con SII podría existir una exposición antigénica (autógena o exógena) y que las células CD25 evitarían la progresión a una forma más florida de inflamación.29,35
En otro estudio, además de cuantificar específicamente los diferentes tipos de células inmunes, se comprobó que la expresión de la molécula de adhesión intestinal, integrina beta7, o su ligando es superior en los linfocitos T de los pacientes con SII que en los controles, esta circunstancia que es similar a lo que ocurre en la colitis ulcerosa.36
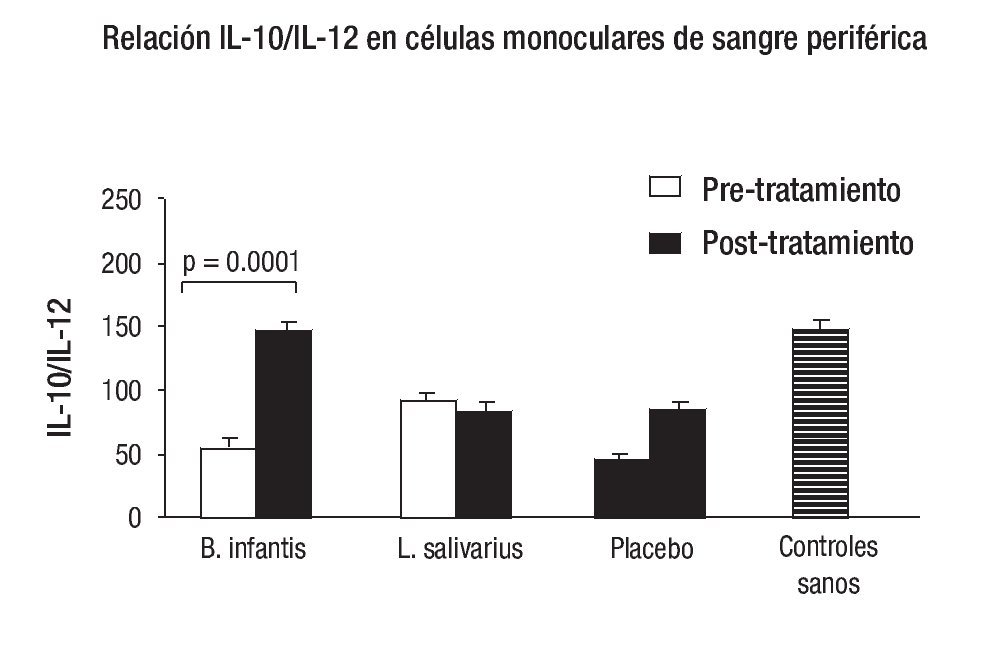
Por otra parte, dicho proceso inflamatorio es modulado por la presencia de las citoquinas proy antiinflamatorias. La producción de citoquinas por las células mononucleares de sangre periférica es un parámetro que se puede obtener de forma sencilla y poco invasiva. Se ha observado que la producción de citoquinas in vitro es mayor en pacientes con SII que en controles sanos, lo que se ha constatado en los diferentes subtipos de SII (con diarrea, estreñimiento y alternante).37-41 Por otra parte, se ha demostrado que la producción de la citoquina antiinflamatoria IL-10 está disminuida respecto a la pro-inflamatoria IL-12, de forma que el cociente IL-10/IL-12 muestra una reducción mayor del 50% con respecto a los controles sanos.40 Los mismos autores ponen de manifiesto que una cepa de organismos probióticos que consiguen la normalización de dicho perfil pro-inflamatorio también produce una mejoría clínica significativa; con el resto de cepas investigadas no se observó mejoría clínica ni normalización del perfil de las citoquinas (Figura 3).40
¿ Figura 3.Normalización del perfil de la expresión de citoquinas IL-10/ IL-12 en células mononucleares de sangre periférica de pacientes con SII tratados con el probiótico B. infantis.40
Para analizar la presencia en la mucosa intestinal de otros marcadores de inflamación se ha recurrido también a algunas técnicas sencillas y no invasivas. Kristjansson y colaboradores41 utilizaron un material de celulosa en un parche (patch) que en contacto con la mucosa rectal tiene capacidad para adsorber y permitir analizar diferentes moléculas de interés. Estos investigadores observaron que en pacientes con SII la mieloperoxidasa y la lipocalina, marcadores de actividad de los polimorfonucleares, estaban aumentadas entre cuatro y siete veces por encima de los niveles en los controles sanos y a un nivel similar al de pacientes con colitis linfocítica, enfermedad celíaca o colitis ulcerosa inactiva; debe tenerse en cuenta que el incremento en los casos de colitis ulcerosa activa superó entre 100 y 200 veces los valores normales. La presencia de marcadores de la inflamación en el SII también se ha evaluado en las heces. En este caso los valores de proteína eosinofílica X, mieloperoxidasa, triptasa, interleuquina 1-ß, TNF-α no difirieron de los obtenidos en los controles, mientras que en la colitis linfocítica sí se encontraron aumentadas la proteína eosinofílica X, la mieloperoxidasa y la triptasa.42 De la misma forma, la calprotectina no se encuentra elevada en heces de pacientes con SII, y por ello su determinación se ha propuesto como una técnica sencilla y no invasiva para el diagnóstico diferencial entre la EII y las patologías funcionales intestinales.43
¿ Síndrome del intestino irritable postinfeccioso: un posible modelo de inflamación
Aunque los signos microinflamatorios se han observado en la población no seleccionada de pacientes con SII, los estudios presentan una limitación importante ya que se trata de poblaciones heterogéneas, en cuanto a las manifestaciones clínicas y el tiempo de evolución. En cambio, cuando el cuadro de SII se desarrolla tras la curación de una infección aguda bacteriana (SII postinfeccioso), podemos disponer y analizar los datos referentes a las circunstancias iniciales. El subgrupo de pacientes con SII postinfeccioso constituye un modelo muy interesante para estudiar la patogenia del SII por ser más homogéneo que la población global con esta condición. De hecho, esta situación constituye un "experimento natural" que se inicia periódicamente al azar en la población sana y permite aproximarnos a la historia natural del desarrollo y persistencia de los fenómenos inflamatorios en este subgrupo de SII postinfeccioso (Tabla 2).
En este campo Spiller y colaboradores44 han realizado aportaciones relevantes. El grupo ha descrito como hallazgo más significativo en la mucosa del colon de pacientes con SII postinfeccioso el incremento de células enterocromafines y de linfocitos intraepiteliales que se sitúa aproximadamente en un nivel seis veces superior a la cuantificación en los controles sanos. Estas alteraciones son cuantitativa y cualitativamente similares a los hallazgos inmunohistológicos en biopsias mucosas obtenidas luego de dos semanas de una infección aguda por Campylobacter.
En otro estudio los mismos autores comprobaron que cuatro meses después de la infección aguda sólo se observaba la hiperplasia de células enterocromafines en los casos con SII postinfeccioso y no en pacientes que tras la infección quedaron asintomáticos.45 Asimismo, quienes luego de la gastroenteritis infecciosa desarrollaron SII presentaron tres meses después una expresión de interleuquina pro-inflamatoria 1-ß superior a la de los controles sanos y los controles que no desarrollaron SII postinfeccioso tras la gastroenteritis.46
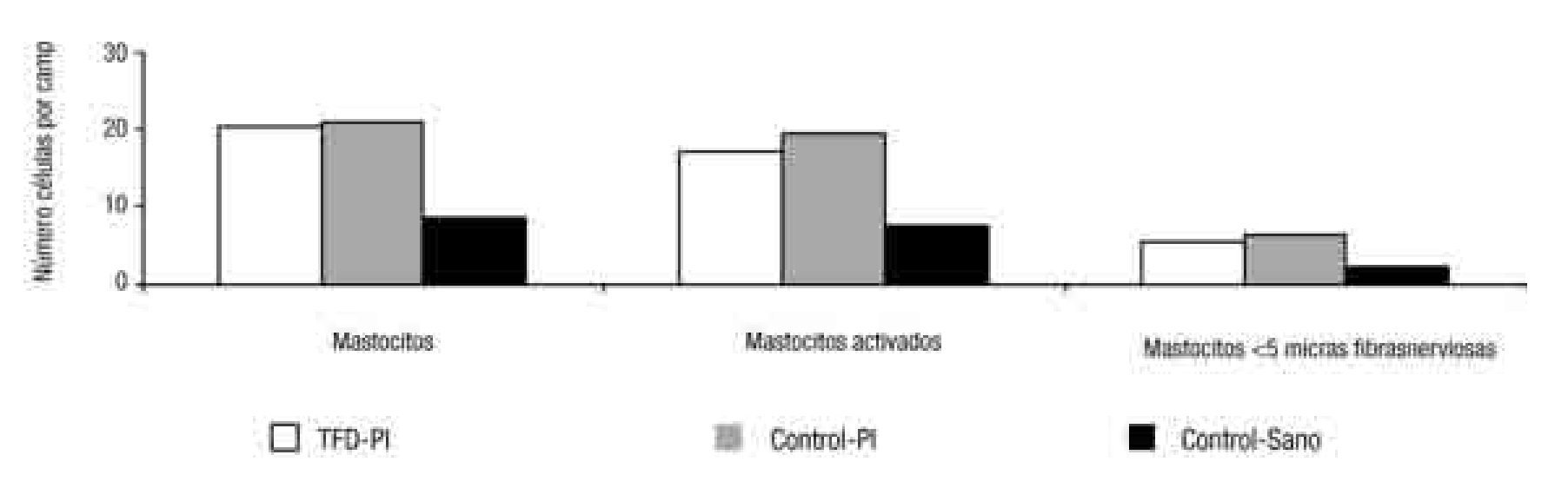
Con el paso del tiempo los fenómenos inflamatorios postinfecciosos podrían atenuarse a pesar de la permanencia del SII y de la hipersensibilidad visceral. Esta circunstancia se ha observado en un estudio prospectivo realizado por nuestro grupo, en el que tres años después de un brote de GEA por Salmonella la mucosa de pacientes que habían desarrollado SII o dispepsia funcional, mostraba un número similar de células inmunes y una producción de citoquinas equiparable a los controles47 (Figura 4).
¿ Figura 4.Los pacientes que sufrieron con anterioridad una gastroenteritis, tanto los que desarrollaron un trastorno funcional digestivo (TFD-PI), como los que se mantuvieron asintomáticos (Control-PI), tuvieron mayor número de mastocitos, de mastocitos activados y de mastocitos en las proximidades de las terminaciones nerviosas que los controles sanos. Sin embargo, no hubo diferencias entre el grupo TFD-PI y el grupo Control-PI.47
No se conocen con exactitud los mecanismos que provocan la persistencia de estas alteraciones inmunológicas y el desarrollo de SII post-infeccioso sólo en algunos sujetos de una población previamente sana. Se han identificado varios factores, unos dependientes del patógeno o de la enfermedad aguda y otros atribuibles al huésped. La duración prolongada de la gastroenteritis, el sexo femenino y la edad menor de 60 años son factores que aumentan el riesgo de padecer un trastorno funcional intestinal. Pero son dos mecanismos dependientes del huésped los que tienen más implicaciones en la fisiopatología del SII: El polimorfismo de los genes que codifican las citoquinas pro o antiinflamatorias y los estresores psicológicos temporalmente cercanos a la infección aguda.48
La persistencia de actividad inflamatoria o cambios neuroinmunes podría estar determinada genéticamente. Los escasos estudios ponen de manifiesto que los genotipos relacionados con la alta producción de la citoquina pro-inflamatoria TNF-α y con la baja producción de la interleuquina reguladora IL-10 son más frecuentes en pacientes con SII que en la población general pudiendo contribuir al perfil proinflamatorio que se ha observado en la expresión de citoquinas en los pacientes con SII.49,50
Por otra parte, los estresores psicológicos temporalmente cercanos a la infección aguda son factores asociados al desarrollo de SII postinfeccioso. Quienes experimentan SII tienen niveles superiores de ansiedad, depresión, somatización y neuroticismo en el momento de la infección aguda que quienes no desarrollan el síndrome; 45,51 también el nivel de eventos estresantes es un factor predictivo de la aparición de SII postinfeccioso.52
La posibilidad de una relación causal entre los estresores psicológicos y los fenómenos inflamatorios es una hipótesis atractiva que merece investigación exhaustiva. El eje hipotálamo-hipofisario-adrenal y el sistema autonómico simpático son los efectores de la respuesta al estrés y podrían ser los mediadores de tal relación. Por el momento podemos decir que, como grupo, los pacientes con SII tienen una respuesta exagerada a la infusión de hormona liberadora de corticotropina con un incremento superior a lo esperado de la ACTH y el cortisol, y que estos fenómenos se correlacionan positivamente con el nivel también aumentado de la IL-6.37 Ésta y otras interacciones entre las respuestas neuroendocrinas e inmunológicas podrían ser un camino para intentar desvelar los interrogantes actuales acerca de la fisiopatología del SII.