La hepatitis alcohólica es una condición frecuente en la población mexicana, se caracteriza por insuficiencia hepática aguda sobre crónica, importante reacción inflamatoria sistémica y fallo multiorgánico, que en la variante grave de la enfermedad implica una elevada mortalidad. Por lo anterior, la Asociación Mexicana de Gastroenterología y la Asociación Mexicana de Hepatología conjuntaron un equipo multidisciplinario de profesionales de la salud para elaborar el primer consenso mexicano de hepatitis alcohólica. El consenso fue elaborado con la metodología Delphi, emitiendo 37 recomendaciones. La enfermedad hepática relacionada con el consumo de alcohol comprende un amplio espectro, que incluye esteatosis, esteatohepatitis, fibrosis en diferentes grados, cirrosis y sus complicaciones. La hepatitis alcohólica grave se define por una función modificada de Maddrey ≥ 32 o por un puntaje de MELD (Model for End-Stage Liver Disease) igual o mayor a 21. Actualmente no existe un biomarcador específico para el diagnóstico. La presencia de leucocitosis con neutrofilia, hiperbilirrubinemia (> 3 mg/dL), AST > 50 U/L (< 400 U/L), relación AST/ALT > 1.5-2 pueden orientar al diagnóstico. La piedra angular del tratamiento es la abstiencia junto con el soporte nutricional. Los esteroides estan indicados en la forma grave, en donde han resultado efectivos para reducir la mortalidad a 28 días. El trasplante hepático es en la actualidad la única opción con que se cuenta para salvar la vida de pacientes que no responden a los esteroides. Ciertos fármacos, como la N-acetilcisteína, el factor estimulante de colonias de granulocitos y la metadoxina, pueden ser una terapia adyuvante que puede mejorar la supervivencia de los pacientes.
Alcoholic hepatitis is a frequent condition in the Mexican population. It is characterized by acute-on-chronic liver failure, important systemic inflammatory response, and multiple organ failure. The severe variant of the disease implies elevated mortality. Therefore, the Asociación Mexicana de Gastroenterología and the Asociación Mexicana de Hepatología brought together a multidisciplinary team of health professionals to formulate the first Mexican consensus on alcoholic hepatitis, carried out utilizing the Delphi method and resulting in 37 recommendations. Alcohol-related liver disease covers a broad spectrum of pathologies that includes steatosis, steatohepatitis, different grades of fibrosis, and cirrhosis and its complications. Severe alcoholic hepatitis is defined by a modified Maddrey's discriminant function score ≥ 32 or by a Model for End-Stage Liver Disease (MELD) score equal to or above 21. There is currently no specific biomarker for its diagnosis. Leukocytosis with neutrophilia, hyperbilirubinemia (> 3 mg/dL), AST > 50 U/l (< 400 U/l), and an AST/ALT ratio > 1.5-2 can guide the diagnosis. Abstinence from alcohol, together with nutritional support, is the cornerstone of treatment. Steroids are indicated for severe disease and have been effective in reducing the 28-day mortality rate. At present, liver transplantation is the only life-saving option for patients that are nonresponders to steroids. Certain drugs, such as N-acetylcysteine, granulocyte-colony stimulating factor, and metadoxine, can be adjuvant therapies with a positive impact on patient survival.
A escala mundial, la mitad de las muertes debidas a cirrosis hepáticas se relacionan con el consumo de alcohol. En nuestro país, la cirrosis hepática por alcohol también representa aproximadamente el 50% de las causas. Esto genera en México un problema de salud pública que impacta directamente en mortalidad elevada y, como consecuencia, altos costos para el sistema de salud. La hepatitis alcohólica (HA) es una condición frecuente en la población mexicana, que suele caracterizarse por insuficiencia hepática aguda sobre crónica (acute-on-chronic liver failure [ACLF]), importante reacción inflamatoria sistémica y fallo multiorgánico; que en la variante grave de la enfermedad implica una elevada mortalidad. Por lo anterior, la Asociación Mexicana de Gastroenterología (AMG) y la Asociación Mexicana de Hepatología (AMH) conjuntaron un equipo multidisciplinario de profesionales de la salud conformado por gastroenterólogos, hepatólogos e investigadores clínicos en este ámbito, para la elaboración de primer consenso mexicano de hepatitis alcohólica, para que se estableciera un documento con recomendaciones que puedan ayudar a toda la comunidad médica que brinda atención clínica a pacientes con esta enfermedad.
El objetivo primario de este consenso fue elaborar un documento que reuniera características de análisis de la evidencia actual sobre conceptos básicos, epidemiología, diagnóstico y tratamiento de la HA, enfocado a la aplicación en la práctica clínica diaria en México.
MetodologíaEn noviembre de 2018 la AMH y la AMG realizaron el convenio de colaboración para redactar el primer consenso mexicano de HA. Se utilizó el proceso metodológico Delphi para el desarrollo del consenso1. Se designaron 2 coordinadores uno por parte de la AMH (JAVRV) y otro por parte de la AMG (MFHT) y se invitaron 23 expertos de las especialidades de Gastroenterología y Hepatología. En enero de 2019, los coordinadores (JAVRV y MFHT), en conjunto con otros tres expertos (RCO, JMAL, ESGJ) realizaron una búsqueda exhaustiva en las siguientes bases de datos: CENTRAL (The Cochrane Central Register of Controlled Trials), MEDLINE (PubMed), EMBASE (Ovid), LILACS, CINAHL, BioMed Central y World Health Organization International Clinical Trials Registry Platform (ICTRP). La búsqueda comprendió el período del 1 de enero de 1990 a febrero de 2019. En casos particulares para el segmento de conceptos básicos y tratamiento el periodo se extendió desde el año 1971. Se incluyeron todas las publicaciones en inglés y español. Se dio preferencia a los consensos, guías, revisiones sistemáticas y metaanálisis, También se realizaron búsquedas complementarias, electrónicas y manuals, en los archivos de la Revista de Gastroenterología de México y en todas las publicaciones que los coordinadores consideraron relevantes hasta febrero de 2019. Los criterios de búsqueda incluyeron los siguientes términos: «alcoholic hepatitis» combinado con los siguientes términos: «epidemiology», «incidence», «prevalence», «Mexico», «pathophysiology», «mortality», «diagnosis», «differential diagnosis», «treatment», «antibiotics», «infection», «therapy», «management», «steroids», «nutrition», «review», «guidelines», «transplant», «meta-analysis» y sus equivalentes en español. Toda la bibliografía se puso a disposición de los miembros del consenso mediante una biblioteca virtual.
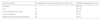
Posteriormente, los coordinadores elaboraron 36 enunciados, los cuales se sometieron a una primera votación anónima vía electrónica (21 al 27 de febrero de 2019) cuya finalidad fue evaluar la redacción y el contenido de los enunciados. Los participantes del consenso emitieron su voto considerando las siguientes respuestas: a) totalmente de acuerdo, b) parcialmente de acuerdo, c) incierto, d) parcialmente en desacuerdo y e) totalmente en desacuerdo. Terminada la primera votación, los coordinadores realizaron las modificaciones correspondientes. Los enunciados que alcanzaron un acuerdo total(> 75%) se mantuvieron y, los que tuvieron un desacuerdo total(> 75%) se eliminaron. Los enunciados que tuvieron ≤ 75% de acuerdo total y ≤ 75% desacuerdo total se revisaron y reestructuraron. Los enunciados revisados se sometieron a una segunda votación anónima por vía electrónica (3 al 8 de marzo de 2019). De acuerdo con los comentarios de la segunda votación los enunciados revisados se sometieron a una tercera votación (9 de 15 de marzo de 2019) donde, además de la redacción, a cada uno de los enunciados se les estableció un grado de recomendación y se evalúo la calidad de la evidencia para sustentar dicha recomendación empleando el sistema Grading of Recommendations Assessment, Development, and Evaluation (GRADE)2. En el sistema GRADE la calidad de la evidencia no se califica únicamente con base en el diseño o la metodología de la investigación, sino que se juzga en función de una pregunta claramente planteada con relación a una variable de desenlace también claramente formulada3. Sobre estas bases, la evidencia puede ser alta, moderada, baja o muy baja. El sistema GRADE también establece la fuerza de las recomendaciones en fuerte o débil, a favor o en contra de la intervención o del enunciado. Como se muestra en la tabla 1, el sistema GRADE se expresa empleando un código que usa letras mayúsculas para hablar de la calidad de la evidencia, seguidas de un índice numérico para indicar la fuerza de la recomendación a favor o en contra de la intervención o enunciado.
Código del sistema GRADE. Sistema GRADE: Clasificación de la calidad de la evidencia de la fuerza de las recomendaciones
| Calidad de la evidencia | Códigos |
|---|---|
| Alta | A |
| Moderada | B |
| Baja | C |
| Muy baja | D |
| Fuerza de la recomendación | Códigos |
|---|---|
| Fuerte a favor de la intervención | 1 |
| Débil a favor de la intervención | 2 |
| Débil en contra de la intervención | 2 |
| Fuerte en contra de la intervención | 1 |
Los resultados de la tercera votación se presentaron los días 15 y 16 de marzo de 2019 en una reunión presencial realizada en la ciudad de Ensenada, Baja California. En esta reunión, los enunciados que obtuvieron un acuerdo > 75% fueron ratificados. Aquellos enunciados que no alcanzaron un 75% de acuerdo en las votaciones previas se discutieron con la finalidad de tratar de llegar a un consenso o, en caso contrario, eliminarlos; y se volvieron a votar.
Una vez establecidos todos los enunciados del consenso, los coordinadores elaboraron el presente manuscrito, el cual fue revisado y aprobado por todos los miembros del consenso.
Consideraciones éticasLos autores de este trabajo declaramos que para esta investigación no se han realizado experimentos en seres humanos ni en animales. No existen conflictos sobre confidencialidad ya que en este artículo no aparecen datos de pacientes. Además, debido a que no se utilizaron datos de personas ni pacientes, no se requirió de consentimientos informados.
ResultadosDe forma inicial, los coordinadores propusieron 36 enunciados. En la primera votación un enunciado fue eliminado por no alcanzar consenso. La segunda votación se realizó sobre 35 enunciados y, de acuerdo con los resultados de la segunda votación, se propusieron dos enunciados nuevos; así, se logró obtener un total de 37 enunciados para la tercera votación. En la reunión presencial se presentaron un total de 37 enunciados, 31 (84%) para ratificarse y 6 (16%) para volver a ser votados. Al final de esta reunión presencial se decidió dejar un total de 37 enunciados una vez revisados, eliminados y fusionado varios enunciados. Dichos enunciados se clasificaron en 6 segmentos:
- •
Conceptos básicos sobre enfermedad hepática relacionada con el consumo de alcohol.
- •
Pruebas diagnósticas para la detección de la enfermedad hepática relacionada con el consumo de alcohol.
- •
Diagnóstico de la hepatitis alcohólica.
- •
Evaluación y pronóstico de los pacientes con hepatitis alcohólica.
- •
Tratamiento de la fibrosis por enfermedad hepática relacionada con el consumo de alcohol.
- •
Tratamiento de la hepatitis alcohólica.
A continuación, se presentan los enunciados finales a manera de recomendaciones y los resultados de la votación.
- A.
CONCEPTOS BÁSICOS SOBRE ENFERMEDAD HEPÁTICA RELACIONADA CON EL CONSUMO DE ALCOHOL
- 1.
El trastorno por consumo de alcohol se define como el consumo riesgoso de alcohol con compromiso en diferentes ámbitos como el social, familiar y laboral; que provoca malestar o deterioro clínicamente significativo, con varios grados de gravedad dependiendo del número de criterios cumplidos. Se debe evitar el término alcoholismo ya que, aparte de no ser útil clínicamente, puede ser perjudicial por la estigmatización social que implica.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
De acuerdo con la Organización Mundial de la Salud (OMS), a escala mundial el 50% de las muertes por cirrosis se relacionan con el consumo de alcohol4. En 2013, más de 23,000 personas murieron por cirrosis en México, casi tres cuartas partes de las cuales eran del sexo masculino. En nuestro país, la cirrosis hepática es la cuarta causa de pérdida de salud y acumula el 4.1% de la carga de enfermedad de acuerdo al indicador de años de vida saludable perdidos (AVISA); se ubica en el quinto lugar de la mortalidad general y en el cuarto respecto a causas de muerte prematura. En la población mexicana predomina el alcohol como causa de la cirrosis en hombres, mientras que en mujeres es más común la hepatitis C. A escala nacional 46% de la carga de enfermedad por cirrosis se asocia con el consumo de alcohol y 35% con la hepatitis C5.
El Manual Diagnóstico y Estadístico de Trastornos Mentales (DSM), versión IV, describía dos diferentes trastornos relacionados con el consumo de alcohol: el abuso de alcohol y la dependencia al alcohol, cada uno de ellos con criterios específicos6. El DSM-5 integra estos dos trastornos en uno solo que en la actualidad se denomina trastorno por consumo de alcohol que se clasifica, a su vez, en leve, moderado o grave. De acuerdo con el DSM-5, se diagnostica trastorno por consumo de alcohol cuando son positivos dos o más de los 11 criterios expuestos en ese manual (ver tabla 2). La gravedad del trastorno por consumo de alcohol se determina con base en el número de criterios positivos: leve 2-3 criterios, moderado 4-5 criterios y grave, 6 o más criterios positivos7.
Criterios del DSM-5 para definir al trastorno por consumo de alcohol
| 1 | ¿Ha tenido momentos en que terminó bebiendo mayor cantidad o por más tiempo de lo que pretendía? |
| 2 | ¿Más de una ocasión ha querido disminuir o suspender el consumo de alcohol, o ha tratado pero sin lograrlo? |
| 3 | ¿Ocupa mucho tiempo en beber o en conseguir alcohol, o pasa mucho tiempo enfermo por causa de la bebida o recuperándose de los efectos secundarios del consumo de alcohol? |
| 4 | ¿Ha deseado una bebida alcohólica con tanta desesperación que no puede pensar en otra cosa? |
| 5 | ¿Ha notado que beber, o estar enfermo por haber bebido, a menudo interfiere con el cuidado de su hogar o su familia?, ¿O causó problemas de trabajo? ¿O problemas escolares? |
| 6 | ¿Continuó bebiendo a pesar de que estaba causando problemas con su familia o amigos? |
| 7 | ¿Ha renunciado o dejado de hacer actividades que fueron importantes o interesantes para usted, o que le dieron placer, para beber? |
| 8 | ¿Más de una vez se ha metido en situaciones mientras o después de beber que aumentaron sus posibilidades de lesionarse (como conducir, nadar, usar maquinaria, caminar en un área peligrosa o tener relaciones sexuales sin protección)? |
| 9 | ¿Continua bebiendo aún a pesar de que esto le hace sentir deprimido o ansioso o a pesar de haberle llevado a padecer algún otro problema de salud?, ¿o ha tenido un olvido, o pérdida de memoria o «laguna mental»? |
| 10 | ¿Ha tenido que beber mucho más de lo que una vez llegó a tomar para obtener o alcanzar el efecto deseado? ¿O encontró que su cantidad habitual de bebidas tuvo mucho menos efecto que antes? |
| 11 | ¿Ha notado que cuando los efectos del alcohol se van agotando, tiene síntomas de abstinencia, como dificultad para dormir, temblores, inquietud, náuseas, sudor, taquicardia o convulsiones? ¿O ha sentido cosas que no estaban allí? |
Todos los criterios se deben interrogar tomando en consideración los últimos 12 meses.
Los términos alcoholismo, alcohólico y abuso de alcohol se han eliminado y ya no se consideran apropiados pues estigmatizan al paciente. También se han eliminado, de los criterios para definir al trastorno por consumo de alcohol, el hecho de haber tenido problemas de índole legal o judicial relacionados con el consumo de bebidas alcohólicas8.
De acuerdo con la Clasificación Estadística Internacional de Enfermedades y Problemas Relacionados con la Salud, en su décima revisión (CIE-10), se considera consumo nocivo de alcohol al que provoca daño físico o mental a la salud9.
- 2.
La enfermedad hepática relacionada con el consumo de alcohol comprende un amplio espectro que incluye esteatosis, esteatohepatitis, fibrosis en diferentes grados, y cirrosis y sus complicaciones.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Aunque no necesariamente son etapas progresivas de la enfermedad, y todas ellas pueden coexistir en un mismo paciente, la enfermedad hepática relacionada al consumo de alcohol (EHA) comprende diversos grados de lesión que van desde la esteatosis simple hasta la cirrosis10. La esteatosis simple, inicialmente macrovesicular y posteriormente mixta (macro y microvesicular), es el cambio más temprano y está presente en 90% de los individuos que consumen alcohol en forma riesgosa11,12 o en el consumo por atracón13 (ver definición de términos más adelante); sin embargo, esta lesión frecuentemente es reversible tras mantener abstinencia14. Aunque la prevalencia de cada lesión histológica en la EHA no se conoce con exactitud15, se estima que un 25% de los pacientes con EHA desarrollan esteatohepatitis y que cerca de 15% progresan a cirrosis16-18. El riesgo acumulado a 5 años, de desarrollar hepatocarcinoma en pacientes con cirrosis por alcohol, se estima en 1%19. La lesión hepática (esteatosis, esteatohepatitis y fibrosis) en la EHA comienza afectando a los hepatocitos perivenulares, posteriormente progresa a los hepatocitos medio lobulillares y finalmente afecta a los hepatocitos periportales13.
- 3.
Los pacientes con enfermedad hepática relacionada con el alcohol requieren de una evaluación psiquiátrica integral y manejo concomitante por personal capacitado en adicciones.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La abstinencia de alcohol es crucial en todo paciente con EHA, la intervención psicosocial por personal capacitado es una herramienta fundamental para lograr la abstinencia y evitar la recaída en el consumo de alcohol20.
Diversas intervenciones psicosociales han demostrado efectividad para favorecer la abstinencia de alcohol; dentro de ellas, la terapia de facilitación de doce pasos (TSF)21, la terapia de mejora motivacional (MET)22 y la terapia de habilidades de afrontamiento cognitivo-conductuales23; las tres intervenciones han demostrado mejoría igualmente significativa y sostenida para lograr la abstinencia y evitar la recaída hasta en un seguimiento a un año24.
Una revisión sistemática realizada por Khan A. et al., que incluyó 13 estudios (cinco fueron ensayos clínicos aleatorizados y el resto observacionales) donde participaron 1,945 pacientes, evaluó el efecto de la terapia de mejora motivacional, terapia cognitivo-conductual (TCC), entrevista motivacional, terapia de apoyo, y psicoeducación. Se encontró que la psicoterapia integrada con TCC, la terapia de mejora motivacional y la atención médica integral incrementaron la abstinencia de alcohol; sin embargo, ninguna intervención psicosocial logró mantener la abstinencia, pero una terapia integrada con TCC y atención médica parece reducir la recidiva25.
En México, el Programa de Acción Específico para la Prevención y Atención Integral de las Adicciones 2013-2018 considera preponderante la identificación de grupos de riesgo a fin de derivarlos para que reciban intervenciones acordes a sus necesidades y condiciones de riesgo, y para quienes presentan uso o abuso de tabaco, alcohol u otras drogas, es prioritario ofrecer intervenciones breves, tratamiento especializado, rehabilitación y apoyo para su reinserción social26.
- 4.
La cuantificación de la ingesta de alcohol por gramos/día puede estimarse mediante la fórmula: gramos/día de alcohol = (cantidad ingerida en mililitros) (graduación alcohólica de la bebida ingerida) (0.8)/100. Como alternativa para estandarizar la medición del consumo de alcohol se propone que una bebida estándar equivale en promedio a 10-14 gramos de alcohol.
Acuerdo alcanzado: totalmente de acuerdo el 96%, parcialmente de acuerdo el 4%.
La OMS, en su guía sobre la intervención breve para evitar el consumo riesgoso de alcohol, define una bebida estándar como 10 g de etanol puro y recomienda, tanto para hombres como para mujeres, no exceder dos bebidas estándar por día27. Cabe mencionar que este parámetro sugerido por la OMS parece ser el más apropiado por ser el más simple y sencillo de replicar en la práctica clínica y para estandarizar estudios clínicos28. Sin embargo, la cantidad de alcohol que contiene una bebida estándar es variable de acuerdo con cada región continental, e incluso difiere en cada país del mundo, encontrando en la literatura que la cantidad de alcohol en una bebida estándar puede ir desde 8 (Islandia) hasta 20 (Austria) gramos de etanol puro29. Para el caso particular de México, la Norma Oficial Mexicana (NOM), NOM-142-SSA1/SCFI-2014, sobre «Bebidas alcohólicas. Especificaciones sanitarias. Etiquetado sanitario y comercial», publicada en el Diario Oficial de la Federación (DOF) en marzo de 2015, específicamente indica que el contenido aproximado de alcohol en una «bebida estándar» es de 13 g considerando que su gravedad especifica es de 0.785 g/mL30. En la tabla 3 se muestran los diferentes tipos de bebidas alcohólicas estándar y su composición según lo establecido en la NOM-142-SSA1/SCFI-2014.
- 5.
Respecto a los patrones de consumo se define como: a) «consumo riesgoso de alcohol», al consumo de más de tres bebidas estándar por día en hombres (> 30 g/día) y más de dos bebidas estándar por día en mujeres (> 20 g/día); b) «episodio de consumo excesivo», al consumo de seis o más bebidas estándar (≥ 60 g de alcohol en una ocasión); y c) «consumo por atracón», al consumo en menos de dos horas de cuatro o más bebidas estándar en mujeres (> 40 g de alcohol) y de cinco o más bebidas estándar en hombres (> 50 g de alcohol).
Tipos de bebidas alcohólicas estándar de acuerdo con la NOM-142-SSA1/SCFI-2014, sobre «Bebidas alcohólicas. Especificaciones sanitarias. Etiquetado sanitario y comercial»
| Tipo de bebida | Porcentaje de volumen alcohólico (% Alc. Vol.) | Cantidad expresada en mL |
|---|---|---|
| Cerveza | 5 | 330 mL |
| Vino | 12 | 140 mL |
| Vino fortificado (ej: jerez) | 18 | 90 mL |
| Licor o aperitivo | 25 | 70 mL |
| Bebidas espirituosas (destilados) | 40 | 40 mL |
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La cantidad consumida de alcohol, independientemente del patrón de consumo, es el factor de riesgo más importante para desarrollar EHA31. Estudios epidemiológicos han demostrado una fuerte correlación entre la cantidad y la duración del consumo del alcohol y la presencia de cirrosis32. En una cohorte que incluyó a 6,970 adultos de la población general, la frecuencia de cirrosis fue significativamente mayor entre quienes consumían ≥ 30 g/día de alcohol en comparación con quienes eran abstinentes o quienes consumían < 30 g/día (2.2% vs. 0.08%). Los sujetos que registraron un consumo alcohólico > 120 g/día tuvieron el mayor riesgo de padecer cirrosis (13.5%)33.
Las mujeres son más susceptibles al daño hepático por alcohol que los hombres34,35. Algunos estudios incluso han reportado que la mujer tiene mayor riesgo de padecer EHA consumiendo la mitad de la dosis de alcohol considerada riesgosa en el hombre; así mismo, la mujer tiene mayor riesgo de progresión acelerada de la enfermedad y riesgo de desarrollo de cirrosis vs. el hombre. Un estudio demostró que las mujeres que consumían > 100 g/día de alcohol desarrollaban cirrosis en un tiempo medio de 13.5 años, en comparación, los hombres que la desarrollaron en un tiempo medio de 20 años34. Las mujeres con trastorno por consumo de alcohol que ingieren > 20 g /día de alcohol tienen mayor riesgo de desarrollar EHA36.
El patrón de consumo de alcohol, especialmente el «consumo episódico excesivo» y el «consumo por atracón» (del inglés binge drinking), es otro factor que se ha propuesto en modelos experimentales como posible factor de riesgo para el desarrollo de EHA; sin embargo, hasta el momento, en humanos no se ha demostrado con claridad que un determinado patrón de consumo se relacione con mayor riesgo de EHA37. Tampoco se ha demostrado en humanos la relación en cuanto al tipo de bebida alcohólica consumida o la calidad del alcohol consumido en el desarrollo de formas graves como la hepatitis alcohólica (HA)38.
En pacientes con comorbilidades tales como síndrome metabólico o hepatitis virales crónicas por virus B o virus C, el consumo de alcohol, incluso en cantidad menor a lo que se considera «consumo riesgoso», puede favorecer y acelerar la progresión del daño hepático39,40. Estos pacientes deben evitar el consumo de alcohol.
El tabaquismo frecuentemente es una condición asociada con el consumo de alcohol. Se sabe que fumar uno o más paquetes por día aumenta tres veces el riesgo de desarrollar cirrosis por alcohol en comparación con los no fumadores41.
- 6.
La «hepatitis alcohólica» representa una condición grave que frecuentemente se comporta como «falla hepática aguda sobre crónica». Se caracteriza por presencia de inflamación sistémica y predisposición al desarrollo de infecciones, falla renal, encefalopatía y disfunción multiorgánica, con mortalidad elevada de 20-50% en los siguientes tres meses, aunque puede ser mayor en población mexicana.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La hepatitis o esteatohepatitis por alcohol tiene un amplio espectro clínico que va desde el estado asintomático, con mínimos síntomas o signos clínicos de enfermedad en su forma leve, hasta un cuadro caracterizado por falla hepática aguda sobre crónica en su forma grave42-44. La HA grave se define por una función modificada de Maddrey ≥ 32 o por un puntaje de MELD (Model for End-Stage Liver Disease) igual o mayor a 2142. Su mortalidad a tres meses es elevada, pero variable en función de la población estudiada. Sidhu SS et al. estiman la mortalidad a tres meses, en HA, de 30-70%45. En algunas poblaciones, particularmente las europeas, la mortalidad general por HA es baja. En el estudio STeroids Or Pentoxifylline for Alcoholic Hepatitis (STOPAH) la mortalidad a 28 días osciló entre 13.5% y 19.4%46.
Una reciente revisión sistemática, que incluyó 77 estudios publicados entre 1971 y 2016, analizando un total de 8,184 pacientes, encontró que la mortalidad general por HA a 28 días fue de 26%, a 90 días de 29% y a 180 días de 44%. Al comparar la frecuencia de mortalidad entre las diferentes décadas no se observaron cambios significativos a lo largo del tiempo ni a 28 ni a 90 días (correlación de Pearson r -0.216, p = 0.098; y r 0.121, p = 0.503, respectivamente). Sí se observó un pequeño pero significativo incremento en cuanto a la mortalidad a los 180 días (r 0.461, p = 0.036)47.
En México, un estudio multicéntrico que incluyó 175 pacientes de cuatro diferentes hospitales, encontró que 121 (69%) pacientes tenían cirrosis subyacente, 125 (71%) pacientes desarrollaron al menos una complicación durante la hospitalización: Insuficiencia renal aguda (IRA) 43%, infecciones 48%, encefalopatía hepática (EH) 49% y hemorragia gastrointestinal 17%. La mortalidad global intrahospitalaria y a 90 días fue de 36% y 51%, respectivamente. Las principales causas de mortalidad a 90 días fueron: sepsis 20%, falla hepática 24% y falla multiorgánica 46%. En este mismo estudio se demostró que la cantidad consumida de alcohol tiene impacto negativo en la supervivencia de los pacientes; así, los pacientes con un consumo de alcohol > 120 g/día fallecieron en un 76% vs. 46% de los pacientes que consumieron menores cantidades de alcohol (p < 0.0001). La mortalidad en pacientes mexicanos clasificados como ABIC (Age-Bilirubin-INR-Creatinine) B y C fue tan alta como 50% y 81%, respectivamente48.
Otro factor de mal pronóstico relacionado a mayor mortalidad en pacientes mexicanos es la malnutrición. Un estudio que incluyó 76 pacientes con HA, de los cuales tenían cirrosis subyacente el 76.3%, y en quienes se evaluó el estado nutricional mediante la Valoración Global Subjetiva (VGS), se encontró que 38 (50%) presentaban malnutrición severa, 22 (28.9%) se encontraban en riesgo de malnutrición y solo 16 (21.1%) estaban bien nutridos. La mortalidad global a 30 días fue de 60.5% y en el análisis multivariado mediante regresión logística se evidenció que la presencia de malnutrición severa se asocia con mortalidad temprana (30 días): razón de momios (RM) = 6.4; (IC 95%: 1.9-22.1); p = 0.00349.
- 7.
La hepatitis alcohólica se clasifica como: a) «definitiva» cuando existe confirmación histológica; b) «probable» cuando el diagnóstico clínico es basado en el consumo riesgoso de alcohol, consumo activo hasta ocho semanas previas, desarrollo de ictericia, relación AST/ALT > 1.5, elevación de aminotransferasas, que usualmente es < 400 UI/L, y ausencia de otras causas de daño hepático; así como c) «posible» cuando el diagnóstico clínico es incierto.
Acuerdo alcanzado: totalmente de acuerdo el 95%, parcialmente de acuerdo el 5%.
La HA se clasifica como «probable» cuando clínicamente se cumplen los siguientes criterios diagnósticos: bilirrubina sérica total (BT) > 3 mg/dL, elevación de aspartato aminotransferasa (AST) y alanino aminotransferasa (ALT) > 50 UI/L, pero < 400 UI/L, relación AST/ALT > 1.5. Todos ellos deben estar presentes en el contexto clínico y de historia de consumo riesgoso de alcohol mencionados con anterioridad42,50. Adicionalmente, no deben de existir factores confusores; es decir, el perfil autoinmunitario debe ser negativo (anticuerpos antinucleares [ANA] < 1:160 o anticuerpos antimúsculo liso [ASMA] < 1:80); no deben haber enfermedades hepáticas metabólicas, sepsis, choque, uso de cocaína ni de fármacos o herbolaria (en los últimos 30 días42) con potencial hepatotóxico conocido.
La HA se considera «definitiva» cuando el diagnóstico clínico ha sido confirmado por hallazgos típicos en la biopsia: esteatosis macrovesicular, inflamación lobular con infiltración de células mononucleares, predominantemente neutrófilos, satelitosis, lesión hepatocelular evidenciada por presencia de cuerpos de Mallory-Denk o por degeneración balonoide de los hepatocitos, necrosis, bilirrubinostasis canalicular o ductular y fibrosis que típicamente se describe como pericelular y perisinusoidal51. Un cambio característico del daño hepático por alcohol son las lesiones fibroobliterativas venosas y la esclerosis hialina, que no se observan en el daño hepático no alcohólico32.
La HA se clasifica como «posible» cuando se sospecha clínicamente pero están también presentes factores confusores como posibilidad de hepatitis isquémica ante la presencia de hemorragia gastrointestinal severa, hipotensión, uso de cocaína reciente; posibilidad de daño idiosincrático por fármacos o herbolaria; incertidumbre respecto al consumo riesgoso de alcohol (p. ej., cuando el paciente niega el consumo de alcohol); hallazgos atípicos en los estudios paraclínicos (p. ej., AST < 50 UI/L o > 400 UI/L, relación AST/ALT < 1.5), ANA > 1:160 o ASMA > 1:80). En estos casos es recomendable realizar biopsia hepática para confirmar el diagnóstico de HA42.
- B.
PRUEBAS DIAGNÓSTICAS PARA DETECCIÓN DE ENFERMEDAD HEPÁTICA RELACIONADA CON EL ALCOHOL
- 8.
La biopsia hepática se puede realizar para establecer el diagnóstico definitivo de enfermedad hepática relacionada al consumo de alcohol, para valorar el estadio exacto y pronóstico de la hepatopatía y para excluir causas adicionales o alternativas de daño hepático. Sin embargo, al ser un procedimiento invasivo no se recomienda en todos los casos y deberá evaluarse individualmente el riesgo contra el beneficio.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95%, parcialmente de acuerdo el 5%.
La biopsia hepática no se recomienda en forma rutinaria para establecer el diagnóstico de EHA52-54. La esteatosis por alcohol es evidente mediante estudios de no invasivos de imagen como el ultrasonido, la tomografía o la resonancia magnética, siendo el primero el más costo-efectivo54 y la última la más exacta para detección e incluso cuantificación de la esteatosis, aunque con el inconveniente de ser costosa y no estar ampliamente disponible55. Bioquímicamente, la elevación de AST y de la gama-glutamiltransferasa (GGT) son indicadores de consumo excesivo de alcohol y se encuentran ampliamente disponibles en la práctica clínica. En el otro extremo, tampoco se considera necesaria la biopsia hepática para establecer el diagnóstico de cirrosis por alcohol, ya que el antecedente de consumo riesgoso de alcohol, las alteraciones bioquímicas con elevación de AST, GGT, una relación AST/ALT > 1.5-2.0 y el volumen corpuscular medio (VCM) elevado, generalmente en el contexto de una anemia macrocítica hipercrómica o megaloblástica, aundado a la exclusión de enfermedades virales crónicas como hepatitis B o C, o enfermedades de tipo autoinmunitario, suelen ser suficientes para llegar al diagnóstico de cirrosis por EHA52,53.
En el contexto de una HA «probable» los criterios clínicos se consideran suficientes para establecer el diagnóstico en la práctica clínica, reservando la biopsia hepática, generalmente por vía transyugular, al paciente con HA «posible», como se ha detallado anteriormente42,56.
Los hallazgos de la biopsia en la EHA son prácticamente indistinguibles de los hallazgos en la enfermedad por hígado graso no alcohólico (EHGNA) y, por tanto, no se recomienda realización de estudio histopatológico con el fin de diferenciar entre estas dos enfermedades13,57.
- 9.
La medición de la rigidez hepática por elastografía puede ser útil para evaluar la fibrosis hepática en enfermedad hepática relacionada con el alcohol.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95%, parcialmente de acuerdo el 5%.
Sin embargo, no debe utilizarse en pacientes con hepatitis alcohólica, ya que sobreestima el grado de fibrosis.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 85%, parcialmente de acuerdo el 10%.
Los métodos no invasivos para evaluar la fibrosis hepática se encuentran menos validados en EHA, en comparación con a otras etiologías; p. ej., hepatitis virales crónicas o esteatohepatitis no alcohólica (EHNA)32.
Entre los métodos radiológicos disponibles para evaluar la fibrosis, la elastografía es el que tiene mayor validación para detección de fibrosis avanzada, y mejor desempeño para descartar la presencia cirrosis en comparación con su desempeño para confirmar la presencia de cirrosis58. No existe consenso en cuanto a los valores de corte para definir cirrosis en el contexto de la EHA y está descrito que existe el riesgo de resultados falsos positivos en pacientes con consumo activo de alcohol32. Una reciente revisión sistemática con metaanálisis que evaluó la exactitud diagnóstica de la elastografía transitoria, para establecer el grado de fibrosis en pacientes con EHA, sugiere utilizar un valor de corte < 9.5 kPa para descartar fibrosis avanzada (F3) un valor de corte < 12.5 kPa para descartar la presencia de cirrosis (F4); sin embargo, también recomiendan precaución ya que los datos obtenidos en esta revisión provienen en su mayoría de estudios retrospectivos y el riesgo global de sesgos fue alto para la mayoría de los estudios evaluados; además se requieren estudios prospectivos que evalúen la exactitud de estos puntos de corte propuestos59.
La elastografía no se recomienda para estimar el grado de fibrosis hepática en los pacientes con HA, ya que la presencia de inflamación tanto hepática como sistémica, la colestasis y la hiperbilirrubinemia, la esteatosis, la congestión venosa hepática, entre otros, sobreestiman el grado de fibrosis60.
- 10.
El ultrasonido, tomografía y resonancia magnética pueden cuantificar esteatosis y ayudan a excluir otras causas de daño hepático crónico, pueden reconocer etapas avanzadas de la enfermedad (cirrosis) y sus complicaciones; sin embargo, no pueden discriminar si el daño es secundario a alcohol versus otras etiologías.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95%, parcialmente de acuerdo el 5%.
El ultrasonido, la tomografía y la resonancia magnética son útiles para detectar esteatosis61; sin embargo, el ultrasonido es de todos estos métodos de imagen el que tiene menor sensibilidad y menor especificidad, en especial cuando la esteatosis afecta a menos de 20-30% del parénquima hepático. El parámetro de atenuación controlada (CAP) ha demostrado ser útil para cuantificar la esteatosis hepática, pero no es específico de EHA y, por lo tanto, no distingue la esteatosis alcohólica de la esteatosis secundaria a cualquier otra etiología. Cuando, además de un consumo riesgoso de alcohol, el paciente padece otras enfermedades (p. ej.: hepatitis B o C, síndrome metabólico, obesidad, etc.), el resultado debe interpretarse de acuerdo con el contexto clínico apropiado y de forma individualizada62,63. La resonancia magnética es capaz de detectar esteatosis desde que un 5-10% del parénquima se encuentra afectado. La elastografía por resonancia magnética es más costosa y en general está menos disponible, pero es más exacta para estimar el grado de esteatosis y de fibrosis en comparación con otros tipos de elastografía64.
Los estudios de imagen no discriminan entre EHA y otras etiologías como causa de la hepatopatía, pero sí son de utilidad para evaluar anatómicamente el hígado y las vías biliares, descartar procesos de tipo obstructivo primarios y secundarios y, en el contexto del paciente cirrótico, independientemente de la etiología, son útiles para evaluar la presencia y magnitud de complicaciones derivadas de la hipertensión portal: ascitis, vasos colaterales, lesiones focales61.
- 11.
En pacientes con sospecha de hepatitis alcohólica e ictericia, el ultrasonido se recomienda como herramienta de tamizaje para diferenciar de procesos obstructivos de la vía biliar.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
El ultrasonido es la técnica de imagen no invasiva de primera línea que permite diferenciar la colestasis intrahepática de la extrahepática. El ultrasonido tiene una elevada exactitud para evidenciar el sitio y la causa en un proceso obstructivo biliar65. Es también una técnica costo-efectiva para discriminar entre un proceso obstructivo y diferenciarlo de la ictericia no obstructiva66.
- 12.
Cuando existe duda o no es factible precisar si el paciente tiene o no historia de consumo riesgoso de alcohol, el índice de enfermedad hepática alcohólica/enfermedad hepática grasa no alcohólica (ANI) mayor de 0 orienta a enfermedad hepática alcohólica.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
El índice de enfermedad hepática alcohólica/enfermedad hepática grasa no alcohólica (ANI) es una herramienta con elevada exactitud para diferenciar entre la EHA de EHGNA. Su aplicación es recomendable en casos en donde se tiene duda respecto del consumo riesgoso de alcohol como desencadenante de lesión hepática en presencia de esteatohepatitis. La abstinencia alcohólica a corto plazo no afecta el resultado del ANI. Otras enfermedades hepáticas (p.ej: virales o autoinmunitarias) deben ser excluidas previamente a aplicar el ANI. Este índice es más exacto cuando el MELD es menor a 20. El ANI se puede calcular gratuitamente en la página web de la Clínica Mayo67.
Las variables más relevantes identificadas mediante análisis de regression logística con capacidad para discriminar entre EHA y EHGNA son el VCM, la relación AST/ALT, el índice de masa corporal (IMC) y el sexo. Un valor de ANI mayor a cero favorece la etiología por alcohol, un valor de ANI menor a cero favorece el diagnóstico de EHGNA. El ANI obtuvo una c-estadística de 0.989 en la muestra de derivación, y de 0.974, 0.989, 0.767 en las tres muestras de validación del modelo. El ANI ha resultado ser superior para diferencias entre EHA y EHGNA en comparación con otros biomarcadores como son la proteína tirosina fosfatasa 1b, la relación AST/ALT, la GGT y la transferrina carbohidrato deficiente68.
- C.
DIAGNÓSTICO DE HEPATITIS ALCOHÓLICA
- 13.
La hepatitis alcohólica es una entidad clínica caracterizada por la aparición súbita de ictericia y elevación de aminotransferasas (particularmente AST), que ocurre en pacientes con consumo continuo y en rango riesgoso de alcohol. En la forma grave se pueden encontrar también otros signos de descompensación hepática como infección bacteriana, ascitis, hemorragia variceal y/o encefalopatía.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La HA grave es una entidad clínica caracterizada por el establecimiento súbito de ictericia y elevación de aminotransferasas, particularmente de la AST, que ocurre tras el antecedente de consumo riesgoso de alcohol por más de seis meses, con menos de 60 días (ocho semanas) de abstinencia antes del establecimiento de la ictérica50. El punto de corte respecto a la duración y cantidad de alcohol relacionados con el desarrollo de HA no están completamente establecidos; pero en general se considera que un promedio de consumo de alcohol de ≥ 40 g/día en mujeres y ≥ 50-60 g/día en hombres, es un parámetro razonable para el diagnóstico de HA. Respecto a la duración, generalmente los pacientes con HA tienen antecedente de consumo intenso de alcohol por más de cinco años, pudiendo haber periodos intermitentes de abstinencia42. La ictericia frecuentemente se acompaña de fatiga, hepatomegalia, descompensación (ascitis, EH, infección bacteriana, hemorragia variceal). La biopsia hepática revela esteatohepatitis con cuerpos hialinos de Mallory-Denk, degeneración balonoide de hepatocitos, bilirrubinostasis y fibrosis avanzada/cirrosis43.
- 14.
La elaboración de una historia clínica detallada permite la identificación del alcohol como agresor hepático. Puede apoyarse de escalas como AUDIT, AUDIT-C y CAGE.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Diferentes cuestionarios se encuentran disponibles para detectar el trastorno por consumo de alcohol y, en general, han demostrado mayor sensibilidad que cualquier prueba bioquímica disponible69,70.
Dentro de los cuestionarios más ampliamente utilizados se encuentra el cuestionario CAGE (acrónimo del inglés: Cut down, Annoyed, Guilty, Eye-opener), el cual consta de cuatro sencillas preguntas; responder «sí» a dos o más correlaciona positivamente con la presencia de dependencia severa al alcohol (término considerado en el DSM-IV). El cuestionario CAGE ha sido ampliamente validado, reportándose una sensibilidad entre 91% y 95%, especificidad entre 76% y 77% para identificar pacientes con consumo excesivo de alcohol y dependencia alcohólica o alcoholismo respectivamente (DSM-IV); sin embargo, su sensibilidad es mucho menor cuando se ha comparado con el Alcohol Use Disorders Identification Test (AUDIT): 40% vs. 93%, respectivamente71.
El AUDIT es el cuestionario que se considera el procedimiento de elección para identificar el consumo riesgoso de alcohol71. Fue diseñado por la OMS y ha sido ampliamente validado para la detección del trastorno por consumo de alcohol, incluso leve. El formato es simple y consta de 10 preguntas de opción múltiple que otorgan, según la respuesta elegida, entre 0 y 4 puntos. Un resultado ≥ 8 indica trastorno por consumo de alcohol (sensibilidad 92% y especificidad 94%); un resultado ≥ 20 indica trastorno severo por consumo de alcohol72.
El AUDIT-C es una versión simplificada del AUDIT. Con una sensibilidad y especificidad semejantes al AUDIT, el AUDIT-C consta de cuatro preguntas de opción múltiple e incluso existen calculadoras en línea, muy prácticas para el consultorio. Como en el AUDIT, cada opción otorga un puntaje que va de 0 a 4. Un resultado ≥ 3 en mujeres y ≥ 4 en hombres indica trastorno por consumo de alcohol73.
- 15.
No existe un biomarcador específico para el diagnóstico de hepatitis alcohólica. Las alteraciones que orientan al diagnóstico de hepatitis alcohólica son: leucocitosis con neutrofilia, hiperbilirrubinemia (generalmente > 3 mg/dL), AST > 50 U/L (usualmente < 400 U/L), relación AST/ALT > 1.5-2.0.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Para establecer el diagnóstico clínico de HA (HA «posible») es imprescindible una BT > 3 mg/dL, elevación de AST y ALT > 50 UI/L pero < 400 UI/L, relación AST/ALT > 1.5, (anteriormente se consideraba una relación AST/ALT > 2)42,50,56. Apoya el diagnóstico de HA la presencia de leucocitosis a expensas de neutrofilia, coagulopatía y trombocitopenia43.
- 16.
La biopsia hepática se utiliza para confirmar el diagnóstico, sin embargo, no es imprescindible y debe reservarse para casos de incertidumbre diagnóstica.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
En la práctica clínica, la biopsia hepática se puede realizar vía percutánea, guiada por ultrasonido, o por vía transyugular debido a la frecuente trombocitopenia y coagulopatía en los pacientes con HA, el abordaje transyugular suele ser la vía de elección54,56. Sin embargo, en pacientes con HA «probable» no es indispensable realizar una biopsia hepática pues la posibilidad de encontrar en la histopatología un diagnóstico diferente a la HA es menor al 10%. Por otro lado, en pacientes con HA «posible» sí es recomendable la realización de biopsia hepática para confirmar o descartar el diagnóstico de HA42.
- 17.
Los hallazgos histopatológicos como esteatosis macrovesicular, esteatohepatitis, degeneración balonoide de los hepatocitos, infiltración por neutrófilos polimorfonucleares y cuerpos hialinos de Mallory-Denk pueden ayudar al diagnóstico, pero no son patognomónicos.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La biopsia hepática establece el diagnóstico definitivo de HA42,48,49. La biopsia hepática también es de utilidad para estimar el pronóstico de la HA a corto plazo50 y de la falla hepática aguda sobre crónica relacionada con el alcohol51. El grado de fibrosis (en puente, avanzada o presencia de cirrosis), el grado severo de infiltración neutrofílica, el tipo de bilirrubinostasis hepatocelular, aunada a la presencia de bilirrubinostasis ductular o canalicular y la presencia de megamitocondrias, son factores histológicos independientemente asociados con la mortalidad a 90 días. Además, el tipo de bilirrubinostasis con afección hepatoceular más afección ductular o canalicular también es factor predictivo del desarrollo de infecciones bacterianas52. Estos hallazgos no son patognomónicos, la EHNA puede histológicamente presentarse con hallazgos semejantes por tanto el criterio clínico es fundamental para establecer el diagnóstico de HA51,57.
- D.
EVALUACIÓN Y PRONÓSTICO DE PACIENTES CON HEPATITIS ALCOHÓLICA
- 18.
En todos los pacientes con hepatitis alcohólica se deben realizar evaluaciones nutricional, psicológica, psiquiátrica y por trabajo social completas.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Desde hace varios años se ha reportado que los pacientes con HA y desnutrición tienen mayor morbilidad y mortalidad74. Esto se ha corroborado en la población mexicana ya que se reportó, como un factor de riesgo independiente, que la desnutrición aumenta la mortalidad en pacientes mexicanos con esta enfermedad. Higuera de la Tijera et al. describieron que la desnutrición severa se asoció con mayor mortalidad a 30 días (RM = 6.4; IC 95%: 1.9-22.1; p = 0.003)49.
La ESPEN (European Society for Clinical Nutrition and Metabolism) recomienda ofrecer terapia nutricional a todo paciente con HA grave que no cumpla requeremientos calóricos por consumo espontáneo de dieta, para así mejorar la supervivencia, disminuir tasas de infecciones, mejorar la función hepática y resolver EH, en su caso. Sin embargo, en distintos metaanálisis no se ha demostrado mejoría en la supervivencia75.
Se recomienda una ingesta calórica diaria de 35-40 kcal/kg y una ingesta proteínica diaria de 1.2-1.5g/kg. A pesar de esto, en la práctica clínica estos objetivos son difíciles de lograr, por lo que en pacientes que no cumplan estos requerimientos se recomienda otorgar soporte nutricional enteral a través de sonda nasoenteral75.
En el estudio multicéntrico más reciente que combinó esteroides y dieta enteral no se demostró mejoría en de la supervivencia al combinarlos, pero sí se observó (de manera significativa) mayor mortalidad en aquellos que tuvieron dieta hipocalórica (21.5 kcal/kg-1/d-1)76.
Así mismo, se recomienda suplementar micronutrientes por la ESPEN como complejo B, en especial tiamina, vitamina D y zinc74.
Por lo anterior, este consenso recomienda en todo paciente con HA una evaluación nutricional adecuada y un consumo energético diario de 35-40 kcal/kg, la ingesta diaria de proteínas de 1.2-1.5 g/kg, así como suplementar micronutrientes.
La vía oral debe ser la primera opción, de tener algún impedimento, como EH, reflejo tusígeno o deglutorio alterados, la dieta podrá administrarse vía nasoenteral. La vía parenteral debe reservarse como última opción, solo en aquellos que tengan una contraindicación para la vía enteral.
Los pacientes con trastorno por consumo de alcohol tienen una alta prevalencia de comorbilidad psiquiátrica, especialmente trastornos de ansiedad, trastornos afectivos, psicosis, trastornos de estrés postraumático y esquizofrenia77. Así mismo, pueden tener antecedentes de abuso sexual, abuso físico o aislamiento social50. Lo anterior puede ser un factor que aumentará el riesgo de recaída en el consumo del alcohol. Es por esto que este consenso recomienda una valoración psicológica y psiquiátrica, quienes se deben de encargar del manejo de abuso de sustancias, incluido el alcohol.
Además, tienen un alto riesgo de desarrollar otras adicciones, opiodes, benzodiazepinas y la nicotina. La sinergia de alcohol y consumo de tabaco está establecida como riesgo importante para enfermedades cardiovasculares y cáncer, incluyendo el hepatocarcinoma. Debido a que los pacientes con trastorno de abuso de alcohol son fumadores intensos se recomienda la valoración psicológica y psiquiátrica, así como la referencia a clínicas de adicciones28,78.
Además, se recomienda una valoración por el equipo de trabajo social ya que cualquier adicción, incluida al alcohol, afecta adversamente al sistema familiar y a todos sus individuos, incluyendo niños, contribuyendo así a la separación familiar ya sea por afectación a la carga financiera o emocional, lo que lleva al sufrimiento individual de los miembros de la familia. Los niños de padres con adicciones están en riesgo aumentado de bajo rendimiento escolar, trastornos del comportamiento, trastornos psiquiátricos y de abuso de sustancias también79.
- 19.
La evaluación integral del paciente con hepatitis alcohólica confirmada debe incluir:
- a)
Búsqueda de focos infecciosos.
- b)
Descartar hemorragia de tubo digestivo.
- c)
Descartar encefalopatía.
- d)
Descartar lesión renal aguda.
- e)
Búsqueda de complicaciones crónicas de hepatopatía.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Es de suma importancia buscar sitios primarios de infección, ya que estos pueden ser un factor que lleve a un mal pronóstico. Las infecciones, al no detectarse y tratarse, pueden llevar al desarrollo de lesión renal agudo (LRA) y falla orgánica múltiple, elevando la mortalidad. Se ha reportado por Louvet et al. una tasa de infección al ingreso, en pacientes con HA grave, de un 25%, los pacientes infectados elevan su mortalidad en un 30% a dos meses80. Incluso en el estudio STOPAH las infecciones estuvieron en el 24% de las muertes81.
Se requiere un alto índice de sospecha para identificar infecciones bacterianas o fúngicas, ya que pueden estar ausentes signos cardinales como fiebre. Y otros signos, como taquicardia y leucocitosis, pueden no ser muy específicos de infección en estos pacientes. El síndrome de respuesta inflamatoria sistémica (SRIS), que puede estar presente en presencia o ausencia de infección al ingreso, es un factor de riesgo para desarrollar falla orgánica múltiple. La procalcitonina sérica es un marcador útil para detectar infecciones bacterianas82. Como las guías europeas, recomendamos en este consenso realizar radiografía de tórax, exámen general de orina, paracentesis diagnóstica (en quien tenga ascitis) y descartar infecciones de tejidos blandos. Además, se recomienda firmemente pancultivar a todos los pacientes28.
Además, se recomienda descartar la presencia de LRA, ya que se ha reportado como uno de los predictores más importantes de mortalidad a 90 días. La presencia de SRIS, elevación de bilirrubinas y coagulopatía al ingreso, son predictores útiles de desarrollar LRA83.
En un estudio observacional de 71 pacientes, en población mexicana, Higuera de la Tijera et al. demostraron que la cantidad de consumo de alcohol está relacionada con la presencia de LRA, reportando consumos de 219 g/día vs. 101 g/día; p = 0.001. También se reportó que la presencia de LRA fue un factor aislado asociado con mayor riesgo de muerte (RR = 6.7, p = 0.02). Llama la atención que la presencia de otras complicaciones que debemos monitorizar como hemorragia de tubo digestivo alto (HTDA) o EH, por sí solas, no aumentaron la mortalidad; sin embargo, al presentarse combinadas entre sí o con LRA la mortalidad sí aumentó. Se comportaron como factores predictores de muerte: la presencia de LRA y EH (RR = 8.9, p = 0.001), la presencia de EH y HTDA (RR = 6.7, p = 0.01) y la presencia de LRA, HTDA y EH mostró el riesgo más elevado (RR = 10.0, p = 0.001)84.
- 20.
Se debe establecer la gravedad de la hepatitis alcohólica, esto define el tipo de tratamiento a administrar.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
- 21.
La aplicación de las diferentes escalas (Maddrey, MELD, Glasgow, ABIC) es útil para establecer la gravedad, predecir la mortalidad y la indicación del tratamiento con corticosteroides.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Es fundamental establecer la severidad de la enfermedad en pacientes con HA, ya que esto norma la conducta a seguir, como la indicación para hospitalizarse o manejarse de manera ambulatoria; así como el tratamiento a otorgar y el pronóstico de supervivencia.
Existen diferentes escalas para establecer la gravedad de la enfermedad; la función discriminatoria de Madrey (FdM) fue la primera escala que diferenció individuos con una mayor mortalidad a corto plazo; continúa siendo una de las más utilizadas85. Se utiliza un puntaje corte de ≥ 32 para identificar pacientes con HA grave con mortalidad alta a corto plazo (20-50%). Los pacientes con HA leve (FdM < 85-87) tienen menos de 10% de mortalidad a 30 días28,50,81,85,86,87.
Se han desorrallado otras escalas de evaluación de gravedad como:
- •
MELD
- •
ABIC
- •
Glasgow
La escala de MELD está ya bien validada como puntaje pronóstico en enfermedad hepática avanzada; sin embargo, también ha desmostrado su utilidad para valorar mortalidad en HA, sugiriendose que un puntaje MELD > 20 eleva la mortalidad a 30 y 90 días28,50,86.
La escala de ABIC es un acrónimo de A: edad (Age), B: Bilirrubinas séricas, I: INR y C: Creatinina sérica. Esta escala da valores de 6.71 (riesgo bajo), 6.71-9 (riesgo intermedio) y ≥ 9 riesgo alto de mortalidad a 90 días, con supervivencia reportada de 100, 70 y 25%28,50,86,87.
La escala de Glasgow es más reciente y utiliza las siguientes variables: edad, bilirrubinas séricas del día uno, urea del día uno, bilirrubina de los días 6-9, tiempo de protrombina y conteo periférico de leucocitos. El puntaje va de 5-12, el punto de corte para definir gravedad es ≥ 9 con una mortalidad a 90 días del 52%28,50,87.
Recientemente Forrest et al. realizaron un estudio, en los pacientes del STOPAH, en el que compararon la efectivadad para predecir mortalidad a 28 y 90 días de las distintas escalas (FdM, MELD, ABIC, Glasgow). Reportaron que la FdM tiene un peor rendimiento y concluyen que MELD, ABIC y Glasgow son superiores para predecir mortalidad (AUROC: 0.670, 0.704, 0.726 y 0.713, respectivamente)88.
En México, Altamirano et al. reportaron que, en población mexicana, la escala de ABIC y MELD son las que mejor rendimiento y exactitud pronóstica tuvieron para predecir gravedad y mortalidad, con AUROC de 82 y 83, respectivamente48.
Este consenso recomienda establer la gravedad y pronóstico de la HA al utilizar cualquiera de las escalas comentadas anteriormente, para definir el inicio de manejo con esteroide.
- 22.
La escala de Lille es útil para evaluar la respuesta al tratamiento y se calcula a los siete días de iniciada la terapia con corticosteroides. Si es > 0.45 el paciente se considera como no respondedor.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La escasez de terapias efectivas para HA grave, y la necesidad de identificar de manera temprana los pacientes que no responden a esteroides, llevaron al desarrollo de la escala de Lille89. Esta escala incluye seis variables: edad, creatinina, albúmina, tiempo de protrombina, BT y evolución de la BT al día siete. Los pacientes que tengan un puntaje de Lille ≥ 0,45 tienen una supervivencia a seis meses del 25%, comparado con el 85% del resto, por lo que se sugiere que son «no respondedores» y se debe suspender el tratamiento con esteroide. La principal ventaja de la escala de Lille es su componente dinámico de la evolución de la BT, la cual es la variable con más precisión y exactitud para predecir mortalidad a los seis meses87.
En un metaanáilisis por Mathurin et al. se evaluó de nuevo la escala de Lille y se identificaron tres grupos de pacientes de acuerdo con la respuesta al esteroide: 1) respondendores completos (puntuación de Lille ≤ 0.16); 2) respondendores parciales (puntuación de Lille 0.16-0.56) y 3) respondedores nulos (puntuación de Lille ≥ 0.56), abriendo la ventana para suspender esteroides en aquellos que son respondedores nulos90.
Además, recientemente se ha demostrado que aplicar la escala de Lille al día cuatro de iniciar el esteroide es similar en la exactitud de predecir mortalidad que aplicarlo al día siete; sin embargo, se necesita validar este hallazgo91. Por otro lado, Louvet et al. demostraron la utilidad de combinar las distintas escalas y reportaron que la mejor combinación fue la escala de Lille + MELD para predecir con más exactitud la mortalidad en pacientes con HA grave92.
- 23.
La abstinencia del consumo de alcohol es el factor pronóstico más importante para la supervivencia a largo plazo en pacientes con hepatitis alcohólica. A corto plazo, la mortalidad está determinada por causas relacionadas con la respuesta inflamatoria, al daño hepático (hemorragia variceal, hipertensión portal), infecciones y falla orgánica.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La supervivenica a largo plazo, despues de un episodio de HA grave, está fuertemente relacionada con el éxito en la abstinencia en el consumo del alcohol. Louvet et al. realizaron un estudio donde describen los factores para predecir supervivencia a corto y largo plazo, reportando que el consumo de alcohol definido como ≥ 30 g/día, no estuvo asociado con mortalidad a corto plazo (p = 0.24); sin embargo, tuvo una fuerte asociación con la mortalidad a largo plazo (> 6 meses), reportando un hazard ratio (HR) = 3.9; p < 0.001. De manera adicional reportaron la relación entre la cantidad de alcohol consumida y la mortalidad a largo plazo: HR = 2.36 (p = 0.052) para ingesta de 1-29 g/día, HR = 3.2 (p = 0.003) para ingesta de 30-49 g/día, HR = 3.51 (p = 0.0001) para ingesta 50-99 g/día y HR = 5.61 (p = 0.0001) para ingestas > 100 g/día93,94. Lo que condiciona que la piedra angular para mejorar la supervivencia es el manejo efectivo del trastorno de abuso de alcohol28.
La supervivencia a corto plazo está determinada con la presencia de SRIS, independientemente de presencia de infección, y disminuye si se presenta junto con hemorragia variceal, LRA o EH28,82.
Ya ha sido demostrado en población mexicana, por Higuera de la Tijera et al., el aumento de la mortalidad a corto plazo en pacientes con HA grave con LRA (RR 6.7, p = 0.02), así como la combinación de LRA + HTDA + EH que eleva el riesgo de mortalidad a RR 10, p = 0.00184.
- E.
TRATAMIENTO DE LA FIBROSIS POR ENFERMEDAD HEPÁTICA RELACIONADA CON EL ALCOHOL
- 24.
En pacientes con hepatitis alcoholica no se conoce con exactitud el momento en el que la fibrosis ya no es reversible, sin embargo, la evidencia demuestra que la eliminación del consumo de alcohol puede revertir o frenar la fibrosis.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Algunas de las complicaciones observadas en la EHA no se deben a la toxicidad inherente de la sustancia, sino que se presentan debido a la fibrosis hepática en sus diferentes estadios. A pesar de que la prevención y detención de la progresión de la fibrosis se establece como un objetivo adecuado en este contexto, no se conoce con precisión el momento en el que se inicia, los fenómenos individuales determinantes del patrón de progresión, ni el punto de no retorno de la fibrosis. La cantidad, duración y patrón del consumo de alcohol, hepatitis virales, interacciones con el ambiente del huésped, el género y los factores genéticos y nutricionales son los factores principales para el desarrollo y progresión de la EHA95. Por razones desconocidas la mayoría de los consumidores de alcohol no desarrollarán enfermedad hepática grave con fibrosis; aunque la mayoría desarrollan hígado graso alcohólico, solo 10-35% desarrollan esteatohepatitis alcohólica y 8-20% desarollan cirrosis hepática con consumos incluso de 12-24 g/día de alcohol96.
De cualquier manera, el consumo sostenido de alcohol está relacionado con episodios de HA, lo que conlleva a presentaciones más descompensadas de EHA y, por lo tanto, a mayores morbilidad y mortalidad, siendo el principal factor de riesgo para el daño hepático y sus complicaciones95. Además, el consumo de alcohol sostenido, coexistente con otras comorbilidades hepáticas (EHGNA, hepatitis C crónica, hepatitis B crónica, enfermedad hepática metabólica o autoinmunitaria, etc.) aumenta el riesgo de fibrosis96,97. Por ello la abstinencia total y sostenida del consumo de alcohol es la piedra angular para frenar e incluso revertir la fibrosis hepática relacionada con su consumo, siempre y cuando no se haya cruzado el umbral de daño irreversible28,50,98.
- 25.
No existe evidencia de que algun medicamento (ácidos ursodesoxicólico, quenodesoxicólico, obeticólico u otros) tenga beneficio en la regresión de la fibrosis por enfermedad hepática relacionada con el consumo de alcohol, en especial con hepatitis alcohólica.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95.5%, totalmente en desacuerdo el 4.5%.
A pesar de que existe evidencia y fundamentos fisiopatológicos que demuestran que los ácidos ursodesoxicólico, quenodesoxicólico y obeticólico son útiles para frenar la progresión de la fibrosis en modelos experimentales de enfermedades hepáticas colestásicas y EHGNA; a la fecha no existen ensayos clínicos que demuestren seguridad y efectividad en cuanto a la mejoría histológica del proceso inflamatorio, ni regresión de la fibrosis en la EHA en cualquiera de sus diferentes etapas o estadios de daño, incluyendo la HA98,99-101.
Cabe señalar que actualmente existe un estudio, en fase II, que investiga los cambios en la puntuación de MELD tras seis semanas de administración de ácido obeticólico, con resultados pendientes101.
- 26.
No existe evidencia de que los antioxidantes (silimarina, vitamina E) reduzcan el daño inflamatorio hepático ni conduzcan a la regresión de la fibrosis en pacientes con hepatitis alcohólica.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95.5%, totalmente en desacuerdo el 4.5%.
A pesar de ser productos popularmente percibidos como aparentemente inocuos y de gran éxito comercial, no existe evidencia de que la silimarina tenga utilidad alguna en la HA102. De acuerdo con dos revisiones de la literatura médica, un metaanálisis y un reporte de evidencia, no existen beneficios contundentes que apoyen la prescripción de este antioxidante, con estudios incluidos con gran heterogeneidad y con discordancia en sus resultados103-105. Respecto a los suplementos de vitaminas, incluida la vitamina E, no existe sustento científico que apoye su uso como monoterapia ni combinado con el tratamiento tradicional para la HA106.
- F.
TRATAMIENTO DE LA HEPATITIS ALCOHOLICA
- 27.
La estrategia terapéutica que permanece como piedra angular en el tratamiento de la hepatitis alcohólica aguda es la abstinencia de alcohol.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Dado que la HA, por definición, requiere del consumo de alcohol de forma significativa, sostenida y reciente, aunado a riesgos individuales y ambientales, la suspensión de su consumo se recomienda como medida imperativa a quien la padece. La manutención de la abstinencia es especialmente importante tras 90 días de iniciado el cuadro, umbral tras el cual se espera un proceso de recuperación del funcionamiento hepático107. Se sabe que los pacientes que retoman el consumo tienen, en general, peor pronóstico. En el estudio STOPAH se observó que la abstinencia en el consumo de alcohol de forma sostenida era el único factor asociado con la supervivencia a un año, beneficio que se perdía con consumos tan bajos como una a dos bebidas alcohólicas por día, lo que aumentaba la mortalidad81,108. En el grupo de este consenso creemos firmemente que para lograr este objetivo es necesario entablar un manejo multidisciplinario para el tratamiento del trastorno por abuso de alcohol, por lo que debe involucrarse una valoración por parte de trabajo social, psicología y psiquiatría, así como garantizar una adecuada red de apoyo.
- 28.
El apoyo nutricional es fundamental en el tratamiento de la hepatitis alcohólica. La ingesta calórica recomendada es de 35-40 cal/kg/día con ingesta de proteínas de 1.2-1.5 g/kg/día. Adicionalmente, es importante tratar las deficiencias de otros nutrimentos como vitaminas y minerales.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
A pesar de que existen controversias, el soporte nutricional ha adquirido gran importancia en el contexto de HA debido a que ha mostrado beneficios en la tasa de mortalidad, desarrollo de EH e infecciones109. El beneficio no ha sido mayor con dieta suplementada que con dieta solamente, por lo que la prioridad es enfocarse en el contenido calórico que ha mostrado tener impacto en la mortalidad cuando es menor de 21.5 kcal/kg/día. Particularmente en la HA grave, la recomendación actual de ingesta proteica es de 1.2-1.5 g/kg, con ingesta calórica de 35-40 kcal/kg50,28. Incluso se ha comparado la nutrición enteral como monoterapia contra prednisolona, observando similaridades estadísticas en los desenlaces clínicos110. La valoración por personal de nutrición debe implementarse al momento del diagnóstico, ya que se ha demostrado que los efectos de la desnutrición y el catabolismo pueden influir en la respuesta al tratamiento farmacológico con esteroides, aumentan el riesgo de infecciones, la morbilidad y la mortalidad111.
- 29.
El tratamiento con corticoesteroides en hepatitis alcohólica está indicado en casos de hepatitis alcohólica aguda grave (indice de Maddrey mayor a 32 o indice de MELD mayor a 20).
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
El tratamiento farmacológico con corticoesteroides en HA solamente se justifica en casos graves definidos por una FdM ≥ 32 o MELD > 20, esto siempre y cuando no exista alguna contraindicación para su administración. El fármaco de elección es la prednisolona, que en estudios mexicanos ha sido sustituida por prednisona, por ser el corticosteroide disponible en México112. El beneficio de la administración de prednisolona en dosis de 40 mg por día es limitado, ya que en el estudio STOPAH solo ha demostrado mejorar la supervivencia a corto plazo; es decir, 28 días, en comparación contra la monoterapia con pentoxifilina o placebo y contra uso concomitante de pentoxifilina-prednisolona. Desafortunadamente, el uso de corticosteroides no tiene efecto alguno sobre mortalidad más allá de los 28 días. Dos metaanálisis, que ya incluyen los resultados del estudio STOPAH, confirmaron este beneficio en la mortalidad a 28 días, sin extensión a los seis meses, lo que sugiere la necesidad de establecer nuevos objetivos clínicos y nuevas estrategias terapéuticas113,114. Existe riesgo de descompensar algunas condiciones tras el inicio de la terapia con corticosteroides, por lo que es necesario tener en cuenta las contraindicaciones para su administración (tabla 4). Dentro de ellas las infecciones, que son una causa frecuente de mortalidad en HA, adquieren gran trascendencia. Clásicamente se ha sugerido el control de la infección previo al inicio del esteroide; sin embargo, existe evidencia de resultados similares en cuanto a mortalidad, en aquellos pacientes con HA más infección activa que iniciaron concomitantemente antibiótico con esteroide vs. aquellos sin infección28,115.
- 30.
La N-acetilcisteína en infusión intravenosa ha demostrado aumentar la supevivencia a corto plazo, pero no a largo plazo (tres a seis meses) solo cuando se utiliza junto con prednisolona. No se recomienda su utilización de forma rutinaria.
Contraindicaciones para el uso de corticoesteroides en pacientes con hepatitis alcohólica aguda28,115,116
| Absolutas |
| • Infección por virus de hepatitis B activa |
| • Tuberculosis activa |
| Relativas |
| • Infección activa o sepsis |
| • Diabetes mellitus descontrolada |
| • Hemorragia gastrointestinal no controlada |
| • Lesión renal aguda (creatinine > 2.5 mg/dL) |
| • Pancreatitis aguda |
| • Infección por VIH, hepatitis C |
| • Hepatocarcinoma |
| • Lesión hepática idiosincrática por fármacos |
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La N-acetilcisteína se ha sugerido como una opción terapeútica debido a que su mecanismo de acción consiste en aumentar las reservas de glutatión para reducir el estrés oxidativo, que es un factor fisiopatológico cardinal en pacientes con HA. En un ensayo clínico controlado se comparó la administración de prednisolona contra su administración concomitante con N-acetilcisteína intravenosa en el manejo de HA grave. Para la N-acetilcisteína se utilizaron varias posologías y velocidades de infusión en el primer día de administración y se continuó a dosis e 100 mg por kg de peso corporal del día dos al cinco. Se observó disminución significativa en la mortalidad a un mes en el grupo de prednisolona + N-acetilcisteína (8%) contra prednisolona sola (24%); sin embargo, no hubo diferencias en cuanto a la mortalidad a tres o seis meses. En un subanálisis se encontró también disminución de la mortalidad específica por síndrome hepatorrenal a seis meses y en la frecuencia de infecciones116,117. A pesar de estos resultados se requiere de mayor evidencia para recomendar su uso rutinario, ya que sigue sin mejorar el umbral de mortalidad general después de un mes. En México no se dispone de prednisolona, por lo que la replicación de estos resultados con formulaciones disponibles (prednisona) podría ser viable.
- 31.
En la actualidad no se tiene evidencia cientifica de que la pentoxifilina sea útil, sin embargo, esta ha demostró beneficio para disminuir riesgo de lesión renal, sindrome hepatorenal y muerte en algunos estudios.
Calidad de la evidencia: C1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La pentoxifilina es un inhibidor de la fosfodiesterasa, inhibe las acciones del factor de necrosis tumoral alfa (TNF alfa), una de las citocinas clave en la fisiopatología de la HA118. Uno de los primeros estudios prometedores fue realizado por Akriviadis et al. Los resultados de este estudio aleatorizado, doble ciego, controlado, con pacientes con HA grave (índice de Maddrey > 32) reportaron que el tratamiento con pentoxifilina mejoró la supervivencia a corto plazo y que el beneficio parecía estar relacionado con una disminución significativa en el riesgo de desarrollar síndrome hepatorrenal119. Sin embargo, estudios realizados posteriormente no han demostrado ningun beneficio sobre este efecto en la mortalidad. Una revisión sistemática de Cochrane, donde se analizaron cinco estudios clínicos, concluyó que no se puede apoyar ni rechazar el uso de pentoxifilina para el tratamiento de la HA grave de acuerdo con la evidencia disponible120. Mediante estudios posteriores se exploró la posiblidad de valorar si la pentoxifilina proporcionaba un efecto aditivo al uso de esteroides en HA. Sin embargo, un estudio multicentrico, aleatorizado, doble ciego, de 23 hospitales en Francia, no logró demostrar que la combinación de prednisolona (40 mg al dia) con pentoxifilina (400 mg tres veces al día durante cuatro semanas) mejorara la supervivencia a seis meses121. Los resultados de una revision sistématica y metaanálisis, donde incluyeron 2,639 pacientes de 25 estudios, confirmaron que la pentoxifilina como monoterapia no ejerce ningun efecto sobre la reducción de la mortalidad122.
- 32.
El tratamiento oportuno de las infecciones en hepatitis alcohólica es primordial.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
En pacientes con HA la frecuencia de infecciones se reporta hasta en 25% de los casos, aumentando la tasa de fallas orgánicas y de muerte123. En el estudio STOPAH, 24% de las muertes ocurridas se consideraron secundarias a eventos infecciosos, independientemente del tratamiento referido81. La mortalidad en pacientes con infecciones y HA grave se incrementa incluso en aquellos respondedores a la terapia con corticosteroides de acuerdo con la puntuación de Lille124. Considerando que una de las contraindicaciones para la terapia con corticosteroides es la presencia de infección no controlada y el aumento en la mortalidad consecuente de las infecciones en HA, resulta imperativa la búsqueda sistemática, la oportuna identificación y el tratamiento de las infecciones en pacientes con HA.
- 33.
Los agentes biológicos anti-TNF alfa no están recomendados para el tratamiento de la hepatitis alcohólica. Estos agentes se asocian con altos riesgos de infecciones, sepsis y muerte.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
A pesar de contar con sustento fisiopatológico, debido al papel que se ha demostrado que desempeñan en la HA algunas citocinas como TNF alfa, interleucina-1 e interleucina-8, en la actualidad no se cuenta con evidencia consistente acerca del beneficio de la administración de agentes anti-TNF en pacientes con HA grave. Una revisión sistemática del 2019, que incluyó el análisis de cinco estudios, concluyó que el infliximab puede ser una alternativa de tratamiento para pacientes que cuentan con contraindicación para el uso de corticosteroides. Sin embargo, está basada en series de casos y dos ensayos clínicos. De los ensayos clínicos se desprendió que el uso de tres dosis de infliximab aumentan el riesgo de infección alcanzando 89% y, por consecuencia, la mortalidad125. Se estudió también el efecto de combinación con esteroide, aumentando también el riesgo de infección y complicaciones. A pesar de que se observaron aparentes beneficios en la disminución de marcadores bioquímicos de inflamación y de contar con una tasa de infecciones equiparable a la de la terapia con corticosteroides solos (de 10-20%) cuando el infliximab se administra en una sola dosis no se recomienda su uso rutinario pues ha demostrado mayores efectos adversos y mayor costo en el tratamiento126.
- 34.
Existen nuevos agentes farmacológicos con potencial beneficio para la hepatitis alcohólica. Dentro de los blancos terapéuticos están el eje intestino-hígado, la regeneración hepática, la apoptosis, el estrés oxidativo y la señalización inflamatoria.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
Debido a la carga económica y a la mortalidad asociada, en los últimos años se han realizado ensayos clínicos para evaluar nuevos objetivos y desarrollar opciones de tratamientos viables para el tratamiento de la HA grave. La HA está asociada con disbiosis de la microbiota intestinal debido al consumo continuo de alcohol, esto ha originado que el eje hígado-intestino sea un potencial blanco de tratamiento. Se ha demostrado que la disbiosis relacionada con HA se asocia con un aumento de bifidobacterias, estreptococos y enterobacterias con una disminución de Clostridium leptum o Faecalibacterium prausnitzii127. Existe evidencia de que la suplementación con cinc puede preservar la integridad intestinal, reducir la muerte celular de los hepatocitos al restringir la vía mediada por Fas/FasL y disminuir el estrés oxidativo, la producción de citocinas proinflamatorias y la endotoxemia. El cinc generalmente se administra a una dosis de 220 mg (50 mg de sulfato de cinc elemental) al día junto con el alimento128. El trasplante de microbiota fecal también se ha propuesto como una opción de tratamiento en HA. Un estudio piloto en pacientes con HA grave, que no eran candidatos a tratamiento con esteroides, se les realizó transplante de microbiota fecal que mejoró los índices de pronósticos y la supervivencia de la enfermedad hepática a un año129. En la busqueda de aumentar la posiblidad de éxito terapéutico se han realizado estudios con combinaciones de varios fármacos. Hay estudios que han utilizado la combinación de un antagonista del receptor de interleucina 1 (IL-1) denominado anakinra con pentoxifilina y cinc, otros estudios buscaron ejercer su acción en la microbiota intestinal con probioticos o calostro bovino buscando la reducción de la translocación bacteriana. Sin embargo, aunque los resultados preliminares pueden ser prometedores, no existe evidencia suficiente y sólida para recomendarlos en HA. Otros fármacos que se han evaluado como agentes antinflamatorios diferentes a anakinra son el ácido obeticólico, cenicriviroc, alopurinol con probenecid aún no cuentan con resultados satisfactorios o no se han publicado101.
- 35.
El uso del factor estimulante de colonias de granulocitos ha demostrado una mejoría de la función hepática y de la supervivencia de pacientes con hepatitis alcohólica grave. Su uso rutinario aún no se recomienda.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
El factor estimulante de colonias de granulocitos (G-CSF) es una citocina que normalmente actúa en el microambiente de la médula ósea para estimular la formación de células sanguíneas. Existen varias presentaciones comerciales de este factor estimulante en el mercado farmacéutico130. Un estudio aleatorizado, con una muestra pequeña de pacientes con esteatohepatitis alcohólica documentada con estudio histológico, evaluó los efectos a corto plazo del G-CSF. Los resultados demostraron que un curso de cinco días de G-CSF estimula las células progenitoras hepáticas en pacientes con esteatohepatitis alcohólica con cirrosis e insuficiencia hepática de moderada a grave, efectos que se observan a los siete días de inciada la terapia debido a que el G-CSF promueve la movilización de células CD34+ y aumenta el factor de crecimiento de los hepatocitos131, hallazgos que también se han documentado en pacientes tratados con G-CSF, con insuficiencia aguda sobre crónica de etiología alcohólica132. En años recientes se han publicado resultados de un estudio aleatorizado que son favorables sobre la mortalidad al utilizar tratamiento con G-CSF en HA aguda. En este ensayo clínico se demostró que G-CSF, a dosis de 5 μg/kg vía subcutánea, cada 12 horas durante cinco días, aumentó la supervivencia a 90 días comparado con aquellos con tratamiento estandár (p = 0.001)133. También se ha utilizado G-CSF para los pacientes que no responden a esteroides. En un estudio que inicio en 2015 y que se proyecta termine en 2020 (ClinicalTrials.gov, NCT02442180) se está evaluando la eficacia del G-CSF en pacientes con HA grave que tienen respuesta parcial o nula a los esteroides. Este estudio, denominado GRACIAH, es aleatorizado y tiene la hipotesis de que la terapia puede ayudar a prolongar la supervivencia134. Por la evidencia actual, por el momento, el uso rutinario no es considerado en todos los pacientes con HA.
- 36.
La metadoxina es un agente antioxidante que puede ser utilizado como terapia adyuvante; combinada con corticoesteroides ha demostrado mejoría en la supervivencia.
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 95.5%, totalmente en desacuerdo el 4.5%.
La metadoxina es un compuesto formado por cristalización, in vitro, de dos moléculas: vitamina B6 y ácido piroglutámico135. La metadoxina es un fármaco antioxidante que ha demostrado, en modelos experimentales, prevenir la disminución de glutatión y la peroxidación lipídica causada por el etanol y el acetaldheído; adicionalmente, en células estelares previene el aumento de colágeno y de secreción de factor de necrosis tumoral alfa inducida por el acetaldhéido136. Además de mejorar la disponibilidad de glutatión, la metadoxina inhibe la esteatosis hepática en pacientes con HA127.
Existen varios estudios clínicos sobre el uso de metadoxina en enfermedad hepática asociada con el consumo de alcohol. Un estudio aleatorizado, realizado por Mao et al. utilizó metadoxina (1.500 mg al día durante 42 días) y, dentro de los principales resultados, se observó mejoría de las pruebas de función hepática y de la relación hígado-bazo evaluada mediante tomografía computada. Otro estudio no aleatorizado también reportó mejoría de la función y el metabolismo hepático con dosis de tan solo 500 mg al dia por 28 días. En ambos estudios los efectos adversos fueron menores136.
Existen dos estudios mexicanos realizados por Higuera-de la Tijera et al. que evaluaron la efectividad de la metadoxina en pacientes con HA. El primer estudio, aleatorizado, abierto, buscaba evaluar la efectividad de metadoxina adicionada a esteroides en el tratamiento de HA grave. Un grupo recibio solo prednisona 40 mg al día (n = 35) y el otro grupo prednisona mas metadoxina 1,500 mg al día vía oral (n = 35) durante 30 días. Se valoró la supervivencia a 30 y 90 días. Los principales resultados observados fueron mejor supervivencia a 30 días (74.3% vs. 45.7%, p = 0.02) y a 90 días (68.6% vs. 20%, p = 0.0001), menor desarrollo o progresión de encefalopatía y de sindrome hepatorenal en el grupo que recibio metadoxina. Ademas, se reportó una respuesta mayor a esteroides en el grupo que recibio metadoxina137. El segundo estudio, aleatorizado, abierto, a diferencia del previo, se realizó con cuatro grupos. En el grupo uno (n = 35) recibierón prednisona 40 mg/día, el grupo dos (n = 35) prednisona + metadoxina 500 mg tres veces al día, el grupo 3 (n = 33) pentoxifilina 400 mg tres veces al día y el grupo cuatro (n = 32) pentoxifilina + metadoxina 500 mg tres veces al día. La duración de tratamiento en todos los grupos fue de 30 días. Los resultados llevaron a la conclusión de que la metadoxina mejora las tasas de supervivencia de tres y seis meses en pacientes con HA grave. Sin embargo, la abstinencia de alcohol es un factor clave para la supervivencia en estos pacientes. Por otro lado, también se observó que los pacientes que recibieron la terapia combinada con metadoxina tenían más probabilidades de mantener la abstinencia que aquellos que recibieron monoterapia con prednisona o pentoxifilina138.
Con base en los resultados de estos estudios en pacientes mexicanos, la metadoxina a dosis de 1,500 mg al día, vía oral, es un agente antioxidante que puede considerarse como un tratamiento adicional en pacientes con HA.
- 37.
El trasplante hepático puede ser considerado como una opción terapéutica en casos seleccionados de HA grave.
Calidad de la evidencia: A1.
Fuerza de la recomendación: fuerte a favor.
Acuerdo alcanzado: totalmente de acuerdo el 100%.
La selección de candidatos para un trasplante hepático siempre demanda una gran responsabilidad para los profesionales que lo realizan. Una de los principales puntos en contra de la utilización de trasplante hepático, para casos seleccionados de hepatitis alcohólica, es el aspecto pronóstico dada la gravedad de la enfermedad; sin embargo, los aspectos psicosociales siempre han tenido un papel fundamental en la toma de decisiones relativas al trasplante hepático en EHA, debido al riesgo de recaída en el consumo de alcohol, que iría en contra del principio fundamental del tratamiento de la HA en cualquiera de sus modalidades. Actualmente, EHA constituye la causa más común para trasplante hepático, con pronósticos a uno y cinco años similares a los de otras indicaciones. El uso de herramientas que permitan predecir el riesgo de recaída en el consumo de alcohol es impreciso, incluyendo la regla de los seis meses de abstinencia de ingesta. Además, existe el riesgo virtual de que si se elimina el intenso escrutinio del trasplante hepático y se extiende su uso indiscriminado para EHA, la tasa de donaciones se vería dismiuida139,140. No obstante, existen otras consideraciones respecto al tiempo de abstinencia y se ha mencionado que cuando se considera agregar pacientes con HA a la lista de espera de trasplante hepático, tres meses de abstinencia de alcohol pueden ser mejores que seis meses. Los pacientes con falta de apoyo social, tabaquismo activo, trastornos psicóticos o de personalidad, o con un patrón de incumplimiento, se deben agregar a la lista de espera solo con reserva. Aquellos que tienen un diagnóstico de abuso de alcohol, en oposición a la dependencia del alcohol, pueden ser mejores candidatos. Los pacientes que tienen citas regulares de tratamiento de adicciones con un psiquiatra o psicólogo también parecen tener un comportamiento más favorable140.
Así, el trasplante hepático constituye actualmente una indicación de tratamiento para la HA grave (Maddrey > 32), en pacientes no respondedores (Lille > 0.45) o no elegibles a corticosteroides, en su primer evento de descompensación hepática, con perfil psicosocial y apoyo social favorables. Los criterios de exclusión para trasplante son: infección descontrolada, enfermedad sistémica comórbida que impida su recuperación, perfil de mal pronóstico en cuanto al consumo de alcohol, falta de apoyo social, eventos de descompensación hepática previos y comorbilidad psiquiátrica no controlada139.
Respecto a la supervivencia y la tasa de recaída en el consumo de alcohol, en pacientes trasplantados por HA aguda que no cumplieron con seis meses de abstinencia de alcohol, un metaanálisis publicado en 2018 concluyó que el trasplante hepático temprano es un tratamiento que salva vidas de pacientes con HA que no responden a tratamiento médico y que la posibilidad de recaída en consumo de alcohol no aumenta después del trasplante en pacientes bien seleccionados141. Otro metaanálisis reciente, donde se analizan 11 estudios para revisar la evidencia disponible sobre el trasplante de hígado en pacientes con HA y evaluar la recaída del alcohol y la supervivencia a los seis meses encontró, usando criterios de selección estrictos, que el 14% de los pacientes con HA grave tienen recaída de alcohol después del trasplante de hígado. El porcentaje de recaída de alcohol de los pacientes trasplantados con HA es similar al de los pacientes con cirrosis alcohólica que se sometieron a un trasplante de hígado electivo142. Otros datos alentadores respecto a supervivencia son los publicados por Lee et al. donde, de acuerdo con un analisis retrospectivo de 147 pacientes que se sometieron a trasplante hepático temprano (antes de seis meses de abstinencia) por HA grave, encontraron que la mayoría de los pacientes sobreviven a un año (94%) y tres años (84%), de forma similar a los pacientes que reciben trasplantes de hígado por otras indicaciones. En este estudio tambien se refuerza que el consumo sostenido de alcohol después del trasplante es poco frecuente pero, cuando ocurre, está asociado con una mayor mortalidad143.
En el contexto de retraso en la toma de la decisión, o en candidatos en lista de espera de trasplante, la terapia MARS ha demostrado mejoría en el perfil bioquímico suficiente como terapia puente; sin embargo, la mejoría a corto o largo plazo en la mortalidad no se ha demostrado144.
ConclusionesLa HA grave es una entidad con alta mortalidad. Este es el primer consenso mexicano sobre HA donde se abordan definiciones sobre los trastornos del consumo de alcohol, el diagnóstico y el tratamiento de la HA emitidas en 37 recomendaciones. Es importante mencionar que la HA es una condicion que va desde un estado asintómatico hasta la maxima expresión de falla hepática. La HA grave es definida por una función modificada de Maddrey ≥ 32 o por un puntaje de MELD igual o mayor a 21. Es una condición donde no existe un biomarcador específico para el diagnóstico, por lo cual es importante apoyarse con estudios de laboratorio. Respecto al tratamiento, la abstinencia sigue siendo la base y el soporte nutricional es importante. Los esteroides permanecen como la opción terapeútica en la HA grave. El uso de antioxidantes como metadoxina combinada con esteroides ha demostrado aumentar la supervivencia. El trasplante es una opción de tratamiento en pacientes seleccionados. Existen nuevos agentes farmacológicos con potencial beneficio en la HA sin embargo, no existe aún evidencia para su uso en la práctica clínica diaria.
FinanciaciónEste consenso se realizó en parte con el apoyo logístico de la Asociación Mexicana de Hepatología y de la Asociación Mexicana de Gastroenterología. Para la reunión presencial este consenso contó con financiamiento del Laboratorio Sanfer. Los autores no recibieron honorarios por su participación.
Conflictos de interésDr. José Antonio Velarde-Ruiz Velasco: es o ha sido ponente para Takeda, Asofarma, Alfa-Wassermann, Abbvie, Abbott, Gilead y MSD.
Dra. María Fátima Higuera de la Tijera: es o ha sido ponente para Gilead, MSD, Medix, Takeda, Liomont y Merz.
Dra. Graciela Elia Castro Narro: es o ha sido ponente para Gilead, Abbvie y Abbott.
Dr. Felipe Zamarripa Dorsey: declara no tener conflicto de intereses.
Dr. Juan Miguel Abdo Francis: es o ha sido ponente para Medix, Takeda, Merz, Abbott y Liomont.
Dr. Ignacio Aiza Haddad: es o ha sido ponente para Abbvie y Takeda.
Dr. Juan Manuel Aldana Ledesma: declara no tener conflicto de intereses.
Dra. María Victoria Bielsa Fernández: es o ha sido ponente para Chinoin, Takeda y Sanfer.
Dra. Eira Cerda Reyes: es o ha sido ponente para Gilead, Abbvie, MSD, Bayer y Sanfer.
Dra. Laura Esthela Cisneros Garza: es o ha sido ponente para Abbvie, Bayer, Bristol y Gilead.
Dr. Raúl Contreras Omaña: es o ha sido ponente para MSD, Bayer y Schwabe.
Dr. Ángel Reyes Dorantes: declara no tener conflicto de intereses.
Dr. Nicolás Joaquín Fernández Pérez: es o ha sido ponente para Takeda, Gilead, MSD, Medix, Mayoli y Grunenthal.
Dr. Edgar Santino García Jiménez: declara no tener conflicto de intereses.
Dra. María Eugenia Icaza Chávez: declara no tener conflicto de intereses.
Dr. David Kershenobich Stalnikowitz: declara no tener conflicto de intereses.
Dr. Marco Antonio Lira Pedrin: declara no tener conflicto de intereses.
Dra. Rosalba Moreno Alcántar: declara no tener conflicto de intereses.
Dr. José Luis Pérez Hernández: declara no tener conflicto de intereses.
Dra. Mayra Virginia Ramos Gómez: declara no tener conflicto de intereses.
Dra. María Teresa Rizo Robles: es o ha sido ponente de Abbvie, Gilead, Merz y MSD.
Dr. Sergio Solana Sentíes: es o ha sido ponente para Asofarma.
Dr. Aldo Torre Delgadillo: declara no tener conflicto de intereses.