Introducción
La hepatopatía por alcohol es una enfermedad muy frecuente en nuestro medio. Los grupos de edad más afectados se encuentran entre la tercera y quinta décadas de la vida.1 La cantidad y duración de la ingesta de alcohol son los factores más importantes en el desarrollo de la enfermedad hepática alcohólica.2 La hepatitis por alcohol (HA) se origina debido a la ingesta abundante de etanol, que aunado a un consumo por tiempo prolongado se puede manifestar por esteatosis hepática moderada a grave con un elevado índice de mortalidad.2,3 La mortalidad en pacientes hospitalizados con diagnóstico de HA es variable, pero se informa que incluso es mayor de 50% en pacientes con HA grave, quienes por lo común casi no responden a ninguna forma de tratamiento.4
La HA grave se caracteriza por la presencia de leucocitosis marcada, fiebre, hepatomegalia e ictericia. Incluso puede presentarse como un cuadro de falla hepática aguda2,5,6 y la presencia de insuficiencia renal empeora el pronóstico.7 Las alteraciones en la función sintética del hepatocito indican una enfermedad de mayor gravedad. Hipoalbuminemia y coagulopatía forman parte frecuente de la enfermedad hepática avanzada.2 El incremento en el número de leucocitos polimorfonucleares circulantes por arriba de las 5 500 células/dL correlaciona con la infiltración de neutrófilos en los lobulillos hepáticos y anticipa la presencia de HA grave cuando el índice discriminativo de Maddrey es superior a 32.2,5 Este índice, que toma en cuenta la función del tiempo de protrombina y la bilirrubina total, muestra un alto valor predictivo positivo para estimar la probabilidad de mortalidad a los 30 días.8 Cuando el resultado es mayor de 32, se puede establecer mal pronóstico con una mortalidad mayor de 50%.1 La escala de Glasgow toma en cuenta bilirrubina y urea sérica, tiempo de protrombina, leucocitosis y edad. Un rango entre 5-7 predice mortalidad de 7% a 28 días y de 12% a 56 días; entre 8-9, de 21% y 33%; de 10-12 se asocia con mortalidad de 67% y 80%, respectivamente.9
El MELD (Mayo Endstage Liver Disease) es un modelo matemático de predicción de sobrevida en pacientes con enfermedad hepática basado en el INR (relación internacional normalizada), bilirrubina total y creatinina sérica.10
Sin embargo, en la actualidad, ninguna escala pronóstica toma en cuenta el desarrollo de complicaciones como la hemorragia de tubo digestivo alto (HTDA) y la encefalopatía hepática (EH). Por tanto, el objetivo de este estudio fue determinar si el desarrollo de HTDA, insuficiencia renal aguda (IRA) y/o EH son factores de riesgo asociados con incremento de la mortalidad.
Material y métodos
Se realizó un estudio observacional, descriptivo, prospectivo y longitudinal de enero de 2005 a diciembre de 2008. La muestra estuvo integrada por pacientes que ingresaron al servicio de hospitalización a cargo de Gastroenterología del Hospital General de México OD con diagnóstico de HA y que cumplían con los siguientes criterios:
Criterios de inclusión: Pacientes mayores de 18 años de edad, tanto hombres como mujeres, con diagnóstico de HA definida por el antecedente de ingesta reciente de alcohol en cantidad mayor a 50 g/día, ictericia, hiperbilirrubinemia, sin evidencia de obstrucción de la vía biliar en el ultrasonido hepático, relación aminotransferasa de aspartato/ aminotransferasa de alanina (AST/ALT) mayor de 2 y leucocitosis sin evidencia de infección activa.2,5,6,11
Criterios de exclusión: Diagnóstico previo de cualquier otra enfermedad crónico-degenerativa (excepto hepatopatía por alcohol), como diabetes, hipertensión arterial sistémica, cardiopatías, neumopatías, nefropatías, hepatopatía de etiología diferente al alcohol. Pacientes que presentaran alguna infección activa al ingreso, infección por síndrome de inmunodeficiencia adquirida (sida), embarazo, consumo de otras drogas (excepto tabaquismo) o cualquier otra sustancia con potencial hepatotóxico. En aquellos pacientes en quienes se recabó la información en forma retroactiva, se excluyeron quienes no contaban con expediente completo ya que ello impedía o dificultaba conocer la evolución y el desenlace del paciente.
Criterios de eliminación: Pacientes que durante el seguimiento hubieran debutado con diagnóstico de diabetes, hipertensión arterial sistémica, hepatopatía crónica por virus de hepatitis C (VHC) o virus de hepatitis B (VHB) demostrado por serología. Pacientes con desarrollo de infección activa pulmonar (demostrada por telerradiografía de tórax) o urinaria (demostrada por examen general de orina y/o urocultivo). Pacientes que solicitaron su alta voluntaria, ya que en ellos no fue posible efectuar el seguimiento.
La información se capturó en un formato de recolección de datos en el que se consignó edad y género, cantidad consumida de alcohol expresada en gramos/día; exámenes de laboratorio (química sanguínea, electrólitos séricos, pruebas de función hepática, tiempos de coagulación y biometría hemática) y de gabinete (ultrasonido de hígado y vías biliares para descartar obstrucción de vías biliares). Con los datos de laboratorio obtenidos, se calcularon el estadio de Child-Pugh, el índice de Maddrey, el MELD y el pronóstico de acuerdo con la escala de Glasgow.
Gravedad de la HA
Índice de Maddrey: Se calculó con la siguiente fórmula: (tiempo de protrombina en segundos del paciente -tiempo de protrombina en segundos del testigo) x 4.6 + bilirrubina total en mg/dL, para estimar el pronóstico. Cuando se registró un Índice de Maddrey mayor de 32 se suministró tratamiento con base en esteroides sistémicos (prednisona, 40 mg al día), excepto en aquellos casos en que estuvo contraindicado (pacientes con insuficiencia renal, HTDA, infección activa). En estos pacientes se empleó pentoxifilina a dosis de 400 mg cada 8 horas, excepto en un caso que refirió alergia conocida a la pentoxifilina y que sólo fue manejado con hidratación parenteral.
MELD: Se calculó con la fórmula (9.57 x loge [creatinina (mg/dl)] + 3.78 x loge [bilirrubina (mg/dl)] + 11.2 x loge (INR) + 6.43).
Escala de Glasgow: Toma en cuenta edad, leucocitos, INR, urea y bilirrubina sérica y asigna a cada uno un valor de 1, 2 o 3 de acuerdo con niveles ya establecidos para esta escala; para finalizar, se suman los puntos obtenidos.
Complicaciones
Durante el tiempo de seguimiento se registró cuántos pacientes desarrollaron una o más de las siguientes complicaciones:
Hemorragia del tubo digestivo alto (HTDA): Definida como aquella que ocurre proximal al ángulo de Treitz y que se caracteriza clínicamente por presencia de hematemesis y/o melena.12 Los pacientes que presentaron dicha complicación se sometieron a videopanendoscopia diagnóstica y terapéutica, en caso necesario, según la causa específica de la hemorragia.
Insuficiencia renal aguda (IRA): Definida como la reducción abrupta (dentro de un lapso de 48 horas) del funcionamiento renal, con demostración de incremento de 0.3 mg/dL en los valores séricos de creatinina.13 En estos pacientes se suspendieron los diuréticos y se inició el tratamiento con soluciones parenterales, se tomaron muestras para cultivos de orina, hemocultivos y telerradiografía de tórax para descartar una infección activa.
Encefalopatía hepática (EH): Desde el punto de vista clínico, se caracteriza por alteraciones neuropsiquiátricas y signos neuromusculares, de acuerdo con los criterios de West-Haven. Se tomaron en cuenta desde el grado I hasta el grado IV.14 Los pacientes fueron tratados con L-ornitina, L-aspartato o lactulosa por vía oral, según la disponibilidad de fármacos que tuviera el hospital y la existencia de contraindicaciones conocidas para cada uno de ellos.
La variable principal fue muerte temprana, ocurrida en los primeros 30 días a partir del inicio del cuadro clínico.
Análisis estadístico
Se utilizaron medidas de tendencia central y dispersión para las variables cuantitativas, las frecuencias se expresan en términos de proporción y se anotan entre paréntesis. Los valores se expresan en medianas ± 1 desviación estándar. Para comparar los grupos de variables categóricas se usaron como pruebas de hipótesis X2 y la probabilidad exacta de Fisher; se aplicó t de Student o U de Mann-Whitney para datos cuantitativos y se estimaron medidas de asociación como el riesgo relativo con sus respectivos intervalos de confianza al 95%. El nivel de significancia se consideró en p < 0.05 (dos colas). Se usó el paquete estadístico SPSS versión 12.0.
Resultados
Se incluyeron 76 pacientes, pero 5 fueron eliminados del estudio debido a que solicitaron su alta voluntaria del servicio y por tal motivo no fue posible conocer el desenlace de su padecimiento.
Se incluyeron 71 pacientes, 61 (86%) hombres y 10 (14%) mujeres. La relación hombre-mujer fue de 6 a 1. El promedio de edad de los pacientes fue de 42.6 años (rango de 24 a 79 años). El promedio de edad en los hombres fue de 43.0 años (rango 24 a 79 años) y en las mujeres de 40.1 años (rango 32 a 65 años).
De acuerdo con la clasificación de Child-Pugh, ningún paciente se encontró en estadio A, 20 pacientes (28.2%) en estadio B, 51 pacientes (71.8%) se encontraron en estadio C.
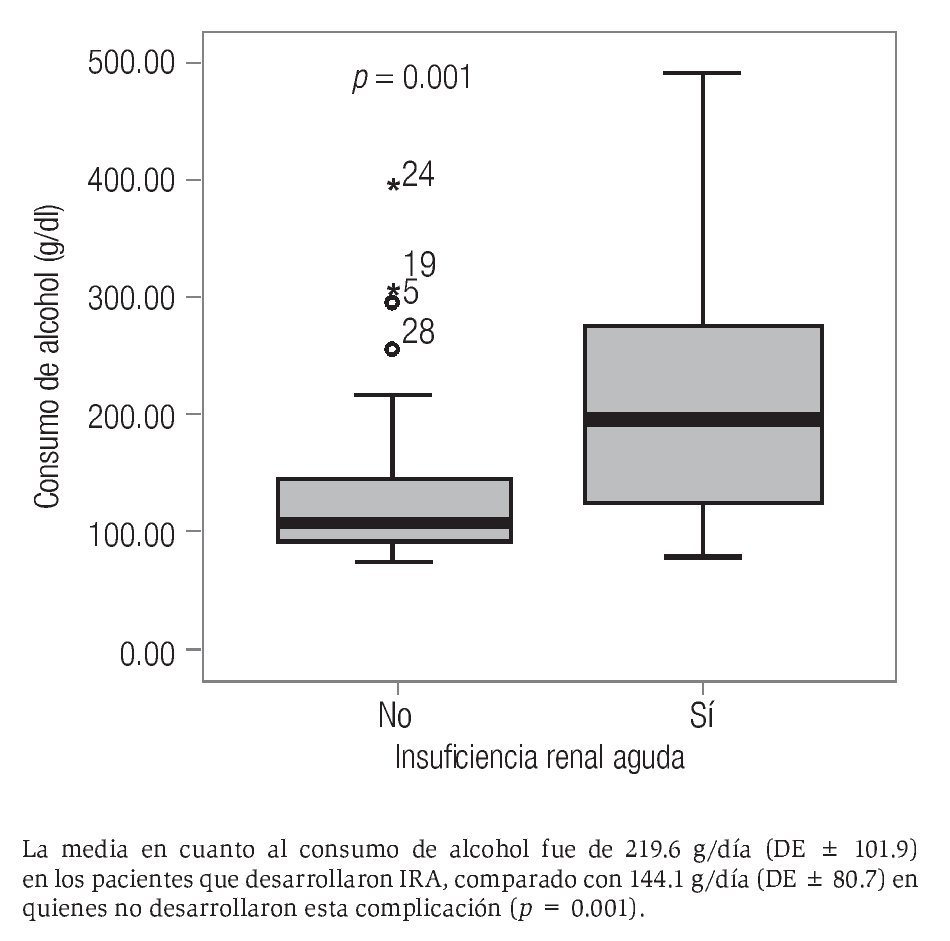
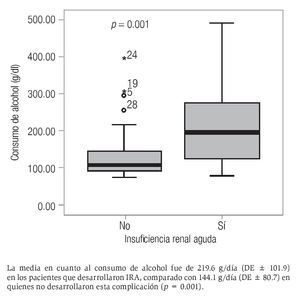
Respecto al consumo de alcohol, los pacientes consumían en promedio 187.7 ± 100.2 g/día (rango de 77 a 496 g/día). Al evaluar el consumo de alcohol se encontró que en promedio los hombres consumían mayor cantidad que las mujeres y que la diferencia era significativa (190.8 ± 105.8 vs. 169 ± 54.3 g/día, p = 0.02). El consumo promedio de alcohol fue mayor en los pacientes que fallecieron en comparación con los que sobrevivieron, aunque la diferencia no fue significativa (220.4 ± 101.6 vs. 140.5 ± 77.8 g/día, p = 0.1). El consumo promedio de alcohol fue mayor en los pacientes que desarrollaron IRA en comparación con quienes no la desarrollaron (219.6 ± 101.9 vs. 144.1 ± 80.7 g/día, p = 0.001) (Figura 1). El consumo promedio de alcohol fue similar en quienes desarrollaron HTDA y quienes no (183.8 ± 79.9 vs. 188.9 g/día ± 105.9, p = 0.8), así como en quienes desarrollaron EH comparado con quienes no (204.3 ± 94.9 vs. 159 ± 104.3 g/día, p = 0.06).
Figura 1. Desarrollo de IRA de acuerdo con la cantidad consumida de alcohol.
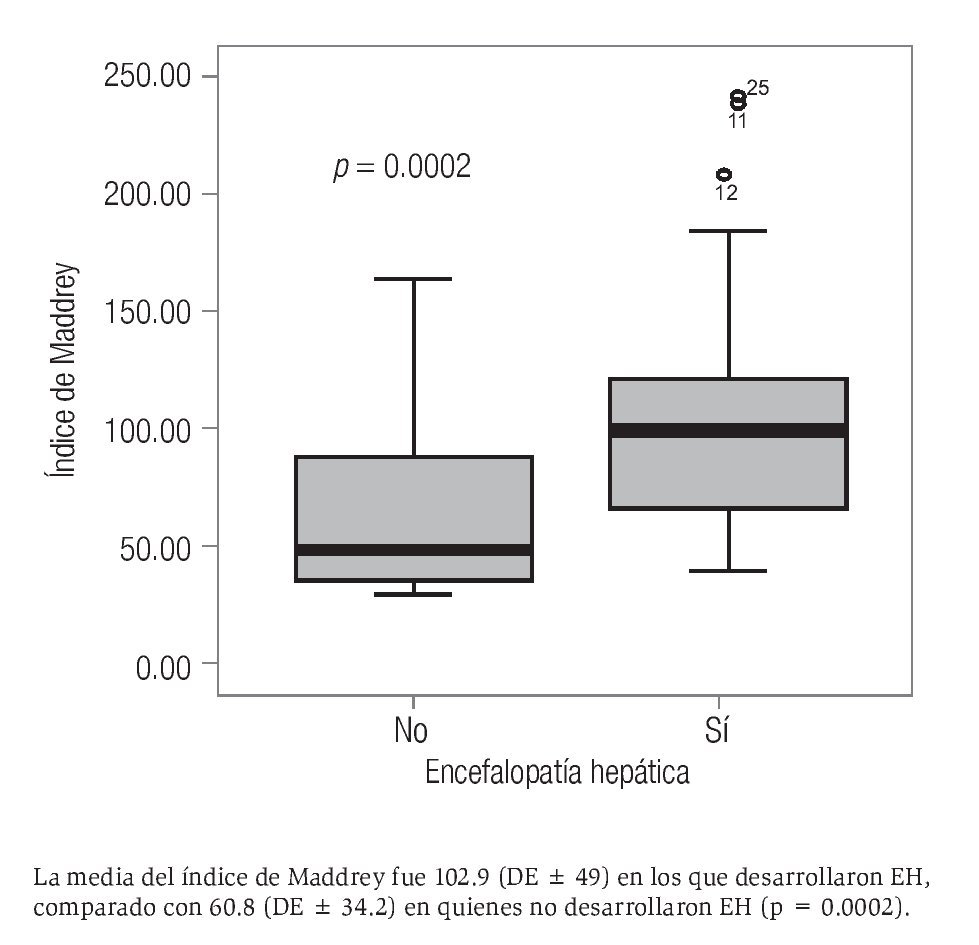
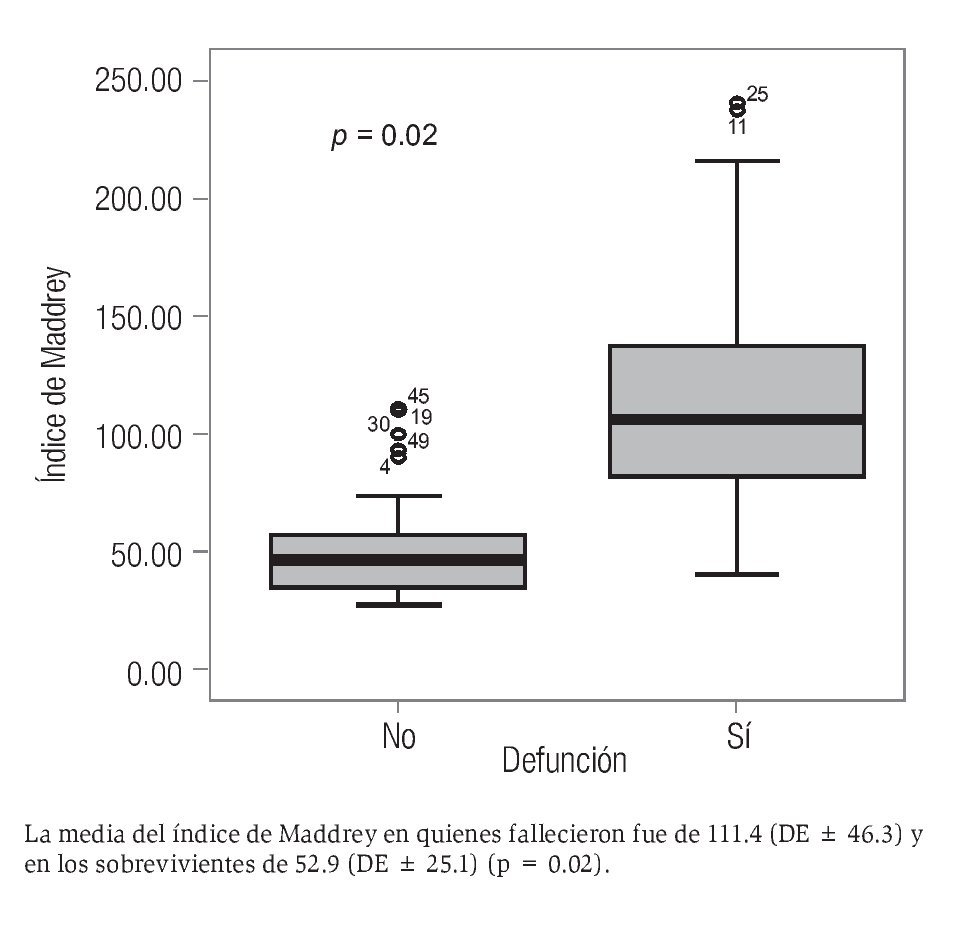
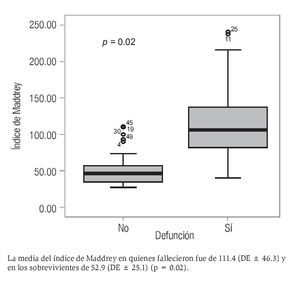
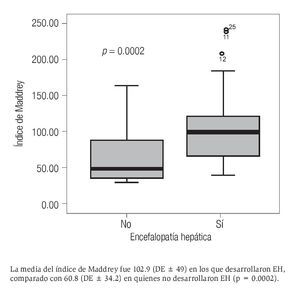
El índice de Maddrey tuvo una media de 87.5 ± 48.4 para esta cohorte (rango 27.6-236.5). Específicamente para el género masculino, la media fue de 92.1 ± 49.7 y para el género femenino de 59.5 ± 27.9. La diferencia de medias entre géneros no resultó significativa (p = 0.12). La media del índice de Maddrey fue significativamente mayor en los pacientes fallecidos que en los sobrevivientes (111.4 ± 46.3 vs. 52.9 ± 25.1, respectivamente, p = 0.02) (Figura 2). La media de este mismo índice fue mayor en pacientes que desarrollaron IRA en comparación con quienes no desarrollaron esta complicación (107.6 ± 48 vs. 60.1 ± 33.7, p = 0.17). También se observó una media del índice de Maddrey mayor en los que desarrollaron HTDA comparada con los pacientes que no la desarrollaron (78.9 ± 37 vs. 89.9 ± 51.3, respectivamente, p = 0.42), y en los que desarrollaron EH comparado con quienes no la desarrollaron (102.9 ± 49 vs. 60.8 ± 34.2, p = 0.0002) (Figura 3).
Figura 2. Comparación entre puntuación de acuerdo con el índice de Maddrey y mortalidad
Figura 3. Diferencia en el índice de Maddrey en relación con el desarrollo de EH.
La puntuación de acuerdo con la escala de Glasgow tuvo una media de 9.0 ± 1.7 para esta cohorte (rango 6-12). La media fue mayor para el género masculino, pero la diferencia de medias entre géneros no resultó significativa (9.2 ± 1.7 vs. 8.3 ± 1.6, p = 0.44). La media de la puntuación de la escala de Glasgow en pacientes fallecidos fue mayor que en los sobrevivientes sin alcanzar significancia estadística (10 ± 1.1 vs. 7.6 ± 1.3, p = 0.1). Las medias de este mismo índice fueron mayores en los pacientes que desarrollaron IRA comparado con quienes no la desarrollaron (10.2 ± 1.1 vs. 7.5 ± 1.1, p = 0.7); fueron mayores en los que desarrollaron HTDA en comparación con quienes no la desarrollaron (8.8 ± 1.5 vs. 9.1 ± 1.8, p = 0.4); y mayores en los que desarrollaron EH comparado con quienes no la presentaron (9.8 ± 1.4 vs. 7.8 ± 1.5, p = 0.84).
De acuerdo con el MELD, la puntuación tuvo una media de 31.4 ± 7.8 para esta cohorte (rango 19 a 40). La media fue mayor para el género masculino, pero la diferencia entre géneros no resultó significativa (31.9 ± 7.9 vs. 28 ± 7.3, p = 0.07). La media de la puntuación del MELD en pacientes fallecidos fue mayor que en los sobrevivientes, sin alcanzar significancia estadística (36.4 ± 4.9 vs. 24.1 ± 4.8, p = 0.4). Las medias de este mismo índice fueron mayores en los pacientes que desarrollaron IRA comparados con quienes no desarrollaron IRA (37 ± 4.1 vs. 23.7 ± 3.9, p = 0.2); fueron similares en los que desarrollaron HTDA en comparación con quienes no la presentaron (31.6 ± 7.9 vs. 31.3 ± 7.8, p = 0.9); y fueron mayores entre quienes desarrollaron EH en comparación con quienes no la presentaron (35.2 ± 6.1 vs. 24.77 ± 5.4, p = 0.19).
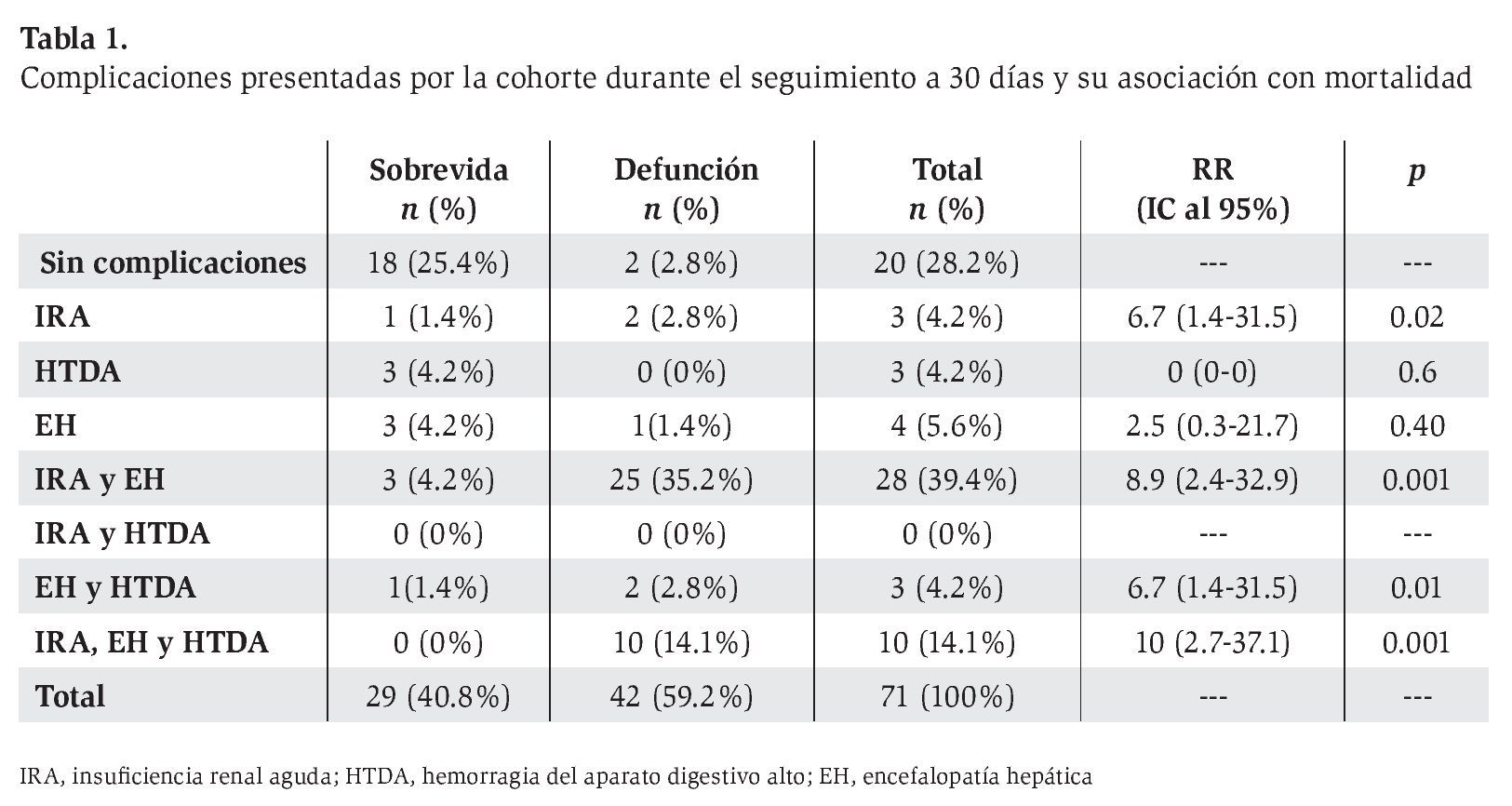
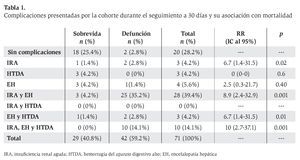
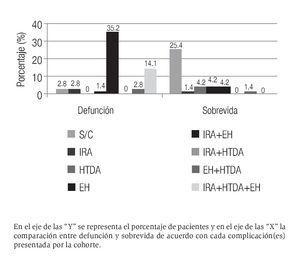
De los 71 pacientes totales que conformaron la cohorte, 42 (59.2%) fallecieron en los primeros 30 días y 29 (40.8%) pacientes sobrevivieron. Respecto de la asociación entre el desarrollo de complicaciones (IRA, HTDA y EH) y muerte en los primeros 30 días de seguimiento, se encontró lo siguiente (Tabla 1):
Sin complicaciones: Veinte pacientes (28.2%) no presentaron ninguna de las tres complicaciones de interés; de ellos, 2 (2.8%) fallecieron y 18 (25.4%) sobrevivieron.
Desarrollo de complicaciones: Durante el seguimiento, la IRA se presentó en 41 pacientes (57.7%), de los cuales 37 (52.1%) fallecieron y sólo 4 (5.6%) sobrevivieron. En total, la HTDA se presentó en 16 (22.5%) pacientes, de los cuales 12 (16.9%) fallecieron y 4 (5.6%) sobrevivieron. La EH se presentó en 45 (63.4%) pacientes, de los cuales 38 (53.5%) fallecieron y sólo 7 (9.9%) sobrevivieron. La distribución en subgrupos de la cohorte de acuerdo con la complicación(es) presentada(s) fue la siguiente:
Una complicación
IRA: Hubo 3 pacientes (4.2%) que desarrollaron IRA como única complicación. De ellos, 2 (2.8%) fallecieron y 1 (1.4%) sobrevivió. Al comparar con el subgrupo de la cohorte que no presentó complicaciones de interés, se estimó un RR = 6.7 (IC 5% = 1.4-31.5, p = 0.02). HTDA: Hubo 3 pacientes (4.2%) que presentaron HTDA como única complicación. De ellos, ninguno falleció y comparado con el subgrupo de la cohorte que no presentó complicaciones de interés se estimó un RR = 0 (IC 95% = 0, p = 0.6).
EH: Hubo 4 pacientes (5.6%) que presentaron EH como única complicación. De éstos, 1 (1.4%) falleció y 3 (4.2%) sobrevivieron. Al comparar con el subgrupo de la cohorte que no presentó complicaciones de interés, se estimó un RR = 2.5 (IC 95% = 0.3-21.7, p =0.40).
Dos complicaciones
IRA y EH: Hubo 28 pacientes (39.4%) que presentaron ambas complicaciones. De ellos, 25 (35.2%) fallecieron y 3 (4.2%) sobrevivieron. Al comparar con el subgrupo de la cohorte que no presentó complicaciones de interés, se estimó un RR = 8.9 (IC 95% = 2.4-32.9, p = 0.001).
EH y HTDA: Hubo 3 pacientes (4.2%) que presentaron ambas complicaciones. De ellos, 2 (2.8%) fallecieron y 1 (1.4%) sobrevivió. Comparado con el subgrupo de la cohorte que no presentó complicaciones de interés, se estimó un RR = 6.7 (IC 95% = 1.4-31.5, p = 0.01).
Tres complicaciones
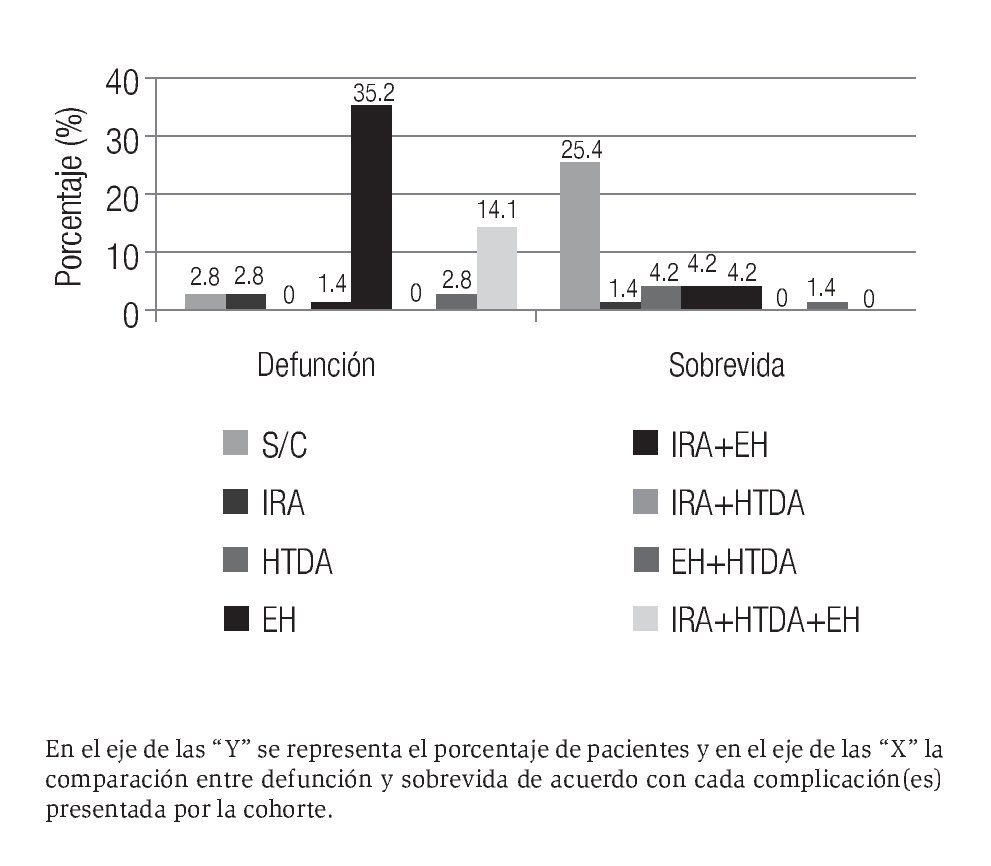
IRA, HTDA y EH: Hubo 10 pacientes (14.1%) que presentaron las tres complicaciones de interés, todos ellos fallecieron. Al comparar con el subgrupo de la cohorte que no presentó complicaciones de interés, se estimó un RR = 10 (IC 95% = 2.7-37.1, p = 0.001) (Figura 4).
Figura 4. Desenlace de la cohorte de acuerdo con las complicaciones presentadas
Discusión
Este estudio demuestra que la cantidad consumida de alcohol se acompaña con el desarrollo de IRA, que la IRA es el factor que guarda relación más estrecha con la muerte y que la presencia de dos o tres complicaciones incrementa significativamente el riesgo de morir por HA.
En la cohorte de enfermos que aquí se presenta, el consumo de alcohol fue significativamente mayor en el género masculino. Esta cantidad consumida de alcohol no tuvo relación directa con la mortalidad, pero sí correlacionó de forma significativa con el desarrollo de IRA y mostró tendencia a la significancia estadística respecto al desarrollo de EH.
En el presente estudio se encontró que la IRA es un factor de riesgo asociado a la elevada mortalidad que se produce en pacientes con HA. Cuando la HTDA y la EH se presentaron como complicaciones únicas no incrementaron la mortalidad de pacientes con HA. Sin embargo, cuando la EH se asoció con IRA, sí se convirtió en un factor de riesgo significativo asociado al incremento en la mortalidad. Asimismo, el hecho de que las tres complicaciones coexistieran fue seguido de un aumento significativo de la mortalidad. Theodossi y colaboradores ya habían señalado que la presencia de encefalopatía, hiperbilirrubinemia e insuficiencia renal son factores que empeoran el pronóstico de la HA.15 Quizá en este estudio no se encontró una asociación significativa entre HTDA y mortalidad debido a que se dispuso de pocos casos en la cohorte con esta complicación; por tanto, resultaría de utilidad evaluar un tamaño de muestra mayor con HTDA como complicación en el curso de la HA.
La mortalidad encontrada en el presente estudio fue mayor de 50%, lo que concuerda con lo informado por otros autores. Mathurin y colaboradores16 informaron que los pacientes con HA no tratada presentaron una mortalidad elevada, y tras 1 año de seguimiento encontraron que la sobrevida fue de alrededor de 41%. Boetticher y colaboradores17 también encontraron una mortalidad de 22.7% a los 6 meses de seguimiento en pacientes con HA.
La prevalencia de HA de este estudio fue mayor en el género masculino, con una relación hombre-mujer de 6 a 1. La mayor frecuencia de pacientes se registró entre los 31 y los 50 años de edad, que representó más de la mitad de la cohorte. Ello concuerda con datos previos informados por Rodríguez y colaboradores,1 donde los grupos de edad más afectados se encontraron entre la tercera y quinta décadas de la vida.
Respecto a los índices y escalas pronósticas validadas disponibles en la actualidad, sólo el índice de Maddrey correlacionó significativamente con mortalidad y un puntaje elevado correlacionó con el desarrollo de EH, no obstante que estudios previos demuestran la baja sensibilidad y especificidad de este índice como predictor de mortalidad. Respecto al índice de Maddrey, Kulkarni y colaboradores18 informaron una sensibilidad de 66.7% y una especificidad del 61.5% como predictor de mortalidad a corto plazo. En el presente estudio no hubo correlación significativa entre la escala de Glasgow y el MELD ni con la mortalidad a 30 días o el desarrollo de complicaciones. Tl vez será necesario realizar un estudio con una cohorte más numerosa para evaluar la correlación entre la escala de Glasgow y el MELD con mortalidad y desarrollo de complicaciones. El estudio de Forrest y colaboradores9 demostró que la escala de Glasgow es mucho más precisa como predictor de mortalidad que el índice de Maddrey, ya que según ellos la escala de Glasgow tuvo una precisión predictiva de 81% a 28 días de seguimiento, comparada con el 49% que arrojó el índice de Maddrey. En un estudio retrospectivo de Altamirano-Gómez y colaboradores19 evaluaron el MELD, la escala de Glasgow y el Índice de Maddrey, y el resultado consistió en que la c-estadística para MELD fue de 0.72, para la escala de Glasgow de 0.75 y para el índice de Maddrey de 0.64. En el análisis de sobrevida, las tres escalas mostraron significancia estadística (log rank < 0.05).
El trabajo que aquí se presenta exhibe algunas limitantes que lleva a los autores a considerar la realización de estudios adicionales en el futuro. El número de pacientes incluido fue relativamente pequeño y la cohorte se siguió por un periodo breve de tiempo. Se está de acuerdo con que la prueba patrón para el diagnóstico de HA es la biopsia hepática, la que no resultó posible de practicar en el grupo de pacientes estudiados. Por lo tanto, los autores consideran que sería deseable contar con una cohorte más amplia, con estudio histopatológico de todos los casos, y seguirlos por un tiempo más prolongado. Pese a las limitaciones mencionadas, el estudio aporta información importante sobre la población mexicana, ya que demuestra que la cantidad consumida de alcohol es un factor asociado al desarrollo de IRA y que esta complicación es el evento cardinal para el mayor riesgo de muerte. Ellos mismos consideran que en el futuro es importante desarrollar un modelo de predicción que permita determinar cuáles pacientes afectados por HA están en riesgo de desarrollar IRA y de esta forma poner en práctica estrategias de prevención que disminuyan la mortalidad en forma global.
Los autores concluyen que, en esta cohorte de pacientes con HA, la cantidad consumida de alcohol se asocia al desarrollo de IRA y que esta complicación es el factor más decisivo vinculado a la muerte. La presencia de dos o tres complicaciones (IRA, HTDA y/o EH) incrementa de manera significativa el riesgo de muerte en esta enfermedad.
Correspondencia: Dra. María de Fátima Higuera de la Tijera,
Hospital General de México OD., Servicio de Gastroenterología, Unidad 107.
Calle Dr. Balmis N° 148, Col. Doctores, Delegación Cuauhtémoc, C.P. 06726, México D. F. Teléfono: 27892000.
Correo electrónico: fatimahiguera@yahoo.com.mx