La infección por Clostridium difficile (ICD) en las últimas décadas se ha convertido en un problema de salud mundial. Nuestro país no es la excepción, y por ello la Asociación Mexicana de Gastroenterología reunió a un grupo multidisciplinario (gastroenterólogos, endoscopistas, internistas, infectólogos y microbiólogos), para que realizaran el «Consenso sobre prevención, diagnóstico y tratamiento de la infección por Clostridium difficile» y se establecieran recomendaciones (dirigidas a población adulta) de utilidad para la comunidad médica.
Las recomendaciones emitidas se presentan en este documento. Se reconoce que la ICD debe sospecharse en sujetos con diarrea con antecedente de uso de antibióticos y/o inmunosupresión, pero que también puede adquirirse en la comunidad. Se propone seguir un algoritmo de dos pasos para el diagnóstico, utilizando una primera prueba de alta sensibilidad como la glutamato deshidrogenasa (GDH) y, en caso de resultado positivo, se debe confirmar mediante detección de toxinas por técnica de inmunoensayo o con pruebas de detección de ácidos nucleicos. Se recomienda categorizar la ICD con base en la evaluación clínica en leve-moderada, grave o grave complicada, ya que esto permite una mejor decisión terapéutica. En la ICD leve-moderada la vancomicina oral es el medicamento de elección, y se recomienda usar metronidazol como tratamiento alternativo. El trasplante de microbiota fecal se reconoce como una opción eficaz ante las recurrencias o los casos más graves, y la cirugía debe reservarse a pacientes con colitis grave (megacolon tóxico) que han fallado a todo tratamiento médico.
In recent decades, Clostridium difficile infection (CDI) has become a worldwide health problem. Mexico is no exception, and therefore the Asociación Mexicana de Gastroenterología brought together a multidisciplinary group (gastroenterologists, endoscopists, internists, infectious disease specialists, and microbiologists) to carry out the “Consensus on the prevention, diagnosis, and treatment of Clostridium difficile infection”, establishing useful recommendations (in relation to the adult population) for the medical community.
Said recommendations are presented herein. Among them, it was recognized that CDI should be suspected in subjects with diarrhea that have a history of antibiotic and/or immunosuppressant use, but that it can also be a community-acquired infection. A 2-step diagnostic algorithm was proposed, in which a highly sensitive test, such as glutamate dehydrogenase (GDH), is first utilized, and if positive, confirmed by the detection of toxins through immunoassay or nucleic acid detection tests. Another recommendation was that CDI based on clinical evaluation be categorized as mild-moderate, severe, and complicated severe, given that such a classification enables better therapeutic decisions to be made. In mild-moderate CDI, oral vancomycin is the medication of choice, and metronidazole is recommended as an alternative treatment. In addition, fecal microbiota transplantation was recognized as an efficacious option in patients with recurrence or in the more severe cases of infection, and surgery should be reserved for patients with severe colitis (toxic megacolon), in whom all medical treatment has failed.
La epidemiología de la infección por Clostridium difficile (ICD) ha cambiado espectacularmente en las últimas décadas y se ha convertido en un importante problema de salud mundial. La aparición de cepas cada vez más virulentas, el uso inadecuado de antibióticos y el envejecimiento de una población afectada por mayor número de enfermedades crónicas y debilitantes son factores que han incrementado la incidencia de esta infección, con el consecuente aumento en la morbilidad, en la mortalidad y en los costos de atención. Así, la ICD ha pasado de ser una infección estrictamente nosocomial a un problema frecuentemente adquirido en la comunidad que muestra un amplio espectro en su presentación clínica. México no es la excepción: diversos estudios han llamado la atención de la comunidad médica sobre este problema de salud, y varios de ellos han sido publicados en la Revista de Gastroenterología de México.
En octubre de 2017, la Asociación Mexicana de Gastroenterología se dio a la tarea de integrar un grupo multidisciplinario de profesionales de la salud conformado por gastroenterólogos, endoscopistas, internistas, infectólogos y microbiólogos para que realizaran el «Consenso sobre prevención, diagnóstico y tratamiento de la infección por Clostridium difficile» y se establecieran recomendaciones de utilidad para la comunidad médica. Es importante mencionar que estas recomendaciones van dirigidas a pacientes adultos y no a población pediátrica.
De manera específica, el objetivo de este consenso fue preparar un documento actualizado sobre la epidemiología, el diagnóstico, el tratamiento y la prevención de la ICD con aplicación práctica en México. Las recomendaciones incluidas están basadas en una extensa revisión de la literatura y en la opinión consensuada de los especialistas participantes.
MétodosSe utilizó el proceso Delphi para el desarrollo del consenso tal y como se ha descrito previamente1. Se designaron tres coordinadores y un coordinador general (ATAA, MRZS, JAVRV) y se invitaron 18 expertos de las especialidades de Gastroenterología e Infectología. Los coordinadores realizaron una búsqueda exhaustiva en las siguientes bases de datos: CENTRAL (The Cochrane Central Register of Controlled Trials), MEDLINE (PubMed), EMBASE (Ovid), LILACS, CINAHL, BioMed Central y World Health Organization International Clinical Trials Registry Platform (ICTRP). La búsqueda comprendió el período del 1 de enero de 2008 al 28 de octubre de 2017. Los criterios de búsqueda incluyeron los siguientes términos: «Clostridium difficile» combinado con los siguientes términos: «epidemiology», «incidence», «prevalence», «Mexico», «pathophysiology», «diarrhea», «microbiota», «diagnosis», «differential diagnosis», «treatment», «antibiotics», «therapy», «management», «review», «guidelines» y «meta-analysis», y sus equivalentes en español. Toda la bibliografía se puso a disposición de los miembros del consenso.
Posteriormente, los coordinadores elaboraron 55 enunciados, los cuales se sometieron a una primera votación anónima vía electrónica (1 a 8 de noviembre de 2017) cuya finalidad fue evaluar la redacción y el contenido de los enunciados. Los participantes del consenso emitieron su voto considerando las siguientes respuestas: a)totalmente de acuerdo; b)parcialmente de acuerdo; c)incierto; d)parcialmente en desacuerdo, y e)totalmente en desacuerdo.
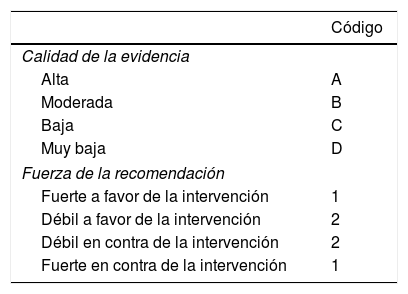
Terminada la primera votación, los coordinadores realizaron las modificaciones correspondientes. Los enunciados que alcanzaron un acuerdo total >75% se mantuvieron y los que tuvieron un desacuerdo total >75% se eliminaron. Los enunciados que tuvieron ≤75% de acuerdo total y ≤75% de desacuerdo total se revisaron y reestructuraron. Los enunciados revisados se sometieron a una segunda votación anónima por vía electrónica (1 a 8 de diciembre de 2017). A partir de los comentarios de la segunda votación los enunciados revisados se sometieron para una tercera votación (16 a 23 de enero de 2018), donde, además de la redacción, se estableció un grado de recomendación para cada uno de los enunciados y se evalúo la calidad de la evidencia para sustentar dicha recomendación empleando el sistema Grading of Recommendations Assessment, Development and Evaluation (GRADE)2. En el sistema GRADE la calidad de la evidencia no se califica únicamente con base en el diseño o la metodología de la investigación, sino que se juzga en función de una pregunta claramente planteada en relación con una variable de desenlace también claramente formulada3. Sobre estas bases, la evidencia puede ser alta, moderada, baja o muy baja. El sistema GRADE también establece la fuerza de las recomendaciones en fuerte o débil, a favor o en contra de la intervención o del enunciado. Es importante mencionar que el sistema GRADE se utilizó en el caso de pruebas diagnósticas e intervenciones terapéuticas. Como se muestra en la tabla 1, el sistema GRADE se expresa empleando un código que usa letras mayúsculas para hablar de la calidad de la evidencia, seguidas de un índice numérico para indicar la fuerza de la recomendación a favor o en contra de la intervención o enunciado.
Código del sistema GRADE
| Código | |
|---|---|
| Calidad de la evidencia | |
| Alta | A |
| Moderada | B |
| Baja | C |
| Muy baja | D |
| Fuerza de la recomendación | |
| Fuerte a favor de la intervención | 1 |
| Débil a favor de la intervención | 2 |
| Débil en contra de la intervención | 2 |
| Fuerte en contra de la intervención | 1 |
Adaptado de Oñate-Ocaña y Ochoa-Carrillo3.
Los resultados de la tercera votación se presentaron el día 31 de enero de 2018 en una reunión presencial realizada en las oficinas de la Asociación Mexicana de Gastroenterología, en la ciudad de México. En esta reunión, los enunciados que obtuvieron un acuerdo >75% fueron ratificados. Los enunciados que no alcanzaron un 75% de acuerdo en las votaciones previas se discutieron con la finalidad de tratar de llegar a un consenso o, en caso contrario, eliminarlos, y se volvieron a votar. Una vez establecidos todos los enunciados del consenso, los coordinadores elaboraron el presente manuscrito, el cual fue revisado y aprobado por todos los miembros del consenso.
ResultadosDe forma inicial, los coordinadores propusieron 55 enunciados. En la primera votación 24 enunciados (44%) fueron eliminados por no alcanzar consenso. La segunda votación se realizó sobre 31 enunciados y de acuerdo con los resultados de la segunda votación se presentaron 35 enunciados para la tercera votación. Para la reunión presencial se presentaron un total de 32 enunciados, 26 (82%) para ratificarse y 6 (18%) para volver a ser votados. Al final de esta reunión presencial se decidió dejar un total de 27 enunciados una vez revisados, eliminados y fusionado varios enunciados. A continuación se presentan los enunciados finales y los resultados de la votación.
Aspectos generales, epidemiología y factores de riesgo- 1.
En las últimas décadas se ha reportado un incremento en la incidencia de infección porClostridium difficileen múltiples poblaciones tanto en ambiente hospitalario como en la comunidad
Acuerdo alcanzado: 91% totalmente de acuerdo, 9% parcialmente de acuerdo
Desde la década de 1970 la ICD se asocia con el uso de antibióticos y se considera un patógeno nosocomial. La ICD se presenta hasta en el 8% de los pacientes hospitalizados y es la causa de diarrea nosocomial más común a escala mundial4-6. Es el agente causal del 15-25% de los casos de diarrea asociada a antibióticos, del 50-75% de colitis asociada a antibióticos y del 90-100% de colitis seudomembranosa asociada a antibióticos5-7. Su incidencia se ha incrementado de forma espectacular desde el año 20008. La epidemiología se ha modificado en el último par de décadas por la aparición de brotes en instituciones de confinamiento como asilos así como en la comunidad8,9. Por otro lado, el Programa de Infecciones Emergentes de los Centros para el Control y la Prevención de Enfermedades (CDC) descubrió que casi el 50% de todos los casos iniciales de ICD habían comenzado en la comunidad8. En México, un estudio retrospectivo en 4 hospitales de 3 ciudades diferentes reportó que de los 487 casos de ICD incluidos, 43 (8.8%) fueron diagnosticados en 2012, 22 (4.5%) en 2013, mostrando un importante aumento en 2014, con 121 casos (24.8%), y 301 casos (61.8%) en 201510. Recientemente, Ochoa-Hein et al. reportaron en un estudio de casos y controles en un hospital de tercer nivel en la Ciudad de México (2015 y 2016) que 155 de 329 casos observados (47.1%) en el periodo fueron casos nuevos adquiridos en el hospital y que 37 casos (11.2%) fueron adquiridos en la comunidad11.
El incremento de casos más graves se ha asociado a un aumento en cepas con mayor virulencia (cepas hipervirulentas) como la cepa PCR-ribotipo 027 o NAP1 (del inglés North American pulsed-field gel electrophoresis type 1) o endonucleasa de análisis de restricción grupo BI, conocida como cepa NAP1/BI/0278,12. Esta cepa se ha asociado con mayor recurrencia y mortalidad en países como Estados Unidos, Canadá, Reino Unido y Europa8,13. Por ejemplo, un estudio que incluyó 15,461 casos de ICD demostró un incremento significativo en la frecuencia de la cepa NAP1/BI/027 en los casos relacionados con atención hospitalaria en comparación con los adquiridos en la comunidad (30.7% vs. 18.8%, p<0.001)14.
En México, la prevalencia de la cepa NAP1/BI/027 varía entre el 28 y el 91%10,14-16. En 2015, Camacho-Ortiz et al.15 demostraron, en un estudio con 22 pacientes, que el 91% de los casos fueron positivos para la cepa NAP1/BI/027. Otro estudio de Morfín-Otero et al.16 examinó los brotes de ICD en un hospital de tercer nivel durante 12meses (n=288): la cepa NAP1/BI/027 se identificó en 31 (39%) de los casos confirmados con ICD y se presentó con mayor frecuencia en pacientes con antecedente de prescripción de quinolonas (39.13% vs. 10.4%, p=0.03) y recaídas (19% vs. 4%, p=0.03). En el estudio realizado por Dávila et al.10 (n=487) el 51.1% de casos correspondía a C.difficile cepa NAP1/BI/027, mientras que en otro estudio más reciente se reportó esta cepa en el 28% de los casos17. El significado clínico de la cepa NAP1/BI/027 en población mexicana aún es incierto, y así, Tamez-Torres et al.17 reportan un desenlace semejante entre los episodios ocasionados por la cepa NAP1/BI/027 en comparación con otros ribotipos en un estudio observacional realizado en un centro hospitalario de tercer nivel entre 2008 y 2015.
- 2.
El espectro de la ICD es variable e incluye desde diarrea leve hasta complicaciones graves como colitis seudomembranosa, megacolon tóxico (colitis fulminante), sepsis y muerte
Acuerdo alcanzado: 91% totalmente de acuerdo, 9% parcialmente de acuerdo
En la ICD con curso clínico leve la diarrea18 es leve-moderada19(>3 y <10 evacuaciones por día), acompañada de cólicos; rara vez hay fiebre y malestar general. Aunque en estos casos ya son detectables las toxinas de C.difficile, la endoscopia y la histología pueden ser normales20. Cuando existen más de 10evacuaciones en 24h se considera que la ICD es grave19. Se puede presentar dolor abdominal de leve a moderado, náusea, anorexia, deshidratación, fiebre y leucocitosis. Si se realiza una sigmoidoscopia se observan regiones eritematosas en parche o difusas, pero sin membranas20. Es importante mencionar que hasta el 20% de los pacientes con ICD grave pueden presentar íleo y no tener diarrea. Algunos autores han definido la gravedad basándose en hallazgos clínicos y de laboratorio18,21,22. Un sistema de puntuación de gravedad de la ICD es el ATLAS, que combina variables clínicas y de laboratorio (tabla 2) y es útil para estratificar a los pacientes23.
Sistema de registro ATLAS y puntaje para cada variable22
| Variable | 0 puntos | 1 punto | 2 puntos |
|---|---|---|---|
| Edad | <60años | 60-70años | >70años |
| Tratamiento con antibióticos sistémicos durante la terapia (>1día) | No | − | Sí |
| Temperatura | <37.5°C | 37.6-38.5°C | >38.6°C |
| Leucocitos totales | <16,000 | 16,000-25,000 | >25,000 |
| Albúmina sérica | >3.5g/dl | 2.6-3.4g/dl | <2.5g/dl |
La colitis seudomembranosa se considera una manifestación típica de la ICD y se presenta hasta en el 40-60% de los casos12. En esta variedad la diarrea generalmente es profusa, con dolor abdominal de moderado a grave. La colonoscopia muestra placas amarillentas. La mayoría de los pacientes tienen afección del colon izquierdo, pero puede abarcar todo el colon. En México, el estudio de Velarde-Ruiz Velasco et al.12 reportó que la colitis seudomembranosa tuvo cierta tendencia a presentarse más frecuentemente con la cepa hipervirulenta (47% vs. 28%), pero sin diferencia estadística (RR:1.62, p=0.23).
Cuando la ICD se presenta con un cuadro grave y se documenta la presencia de distensión del colon (>6cm de diámetro del colon transverso) mediante estudios radiológicos, se considera como «megacolon tóxico»17. A la presencia de una respuesta inflamatoria sistémica grave asociada a megacolon tóxico se le denomina colitis fulminante (véase enunciado 8).
- 3.
La colonización porClostridium difficilees más frecuente en pacientes con antecedente de hospitalización los 2meses previos, inmunosupresión, uso de quimioterapia, antibióticos, inhibidores de la bomba de protones y antagonistas H2
Acuerdo alcanzado: 83% totalmente de acuerdo, 17% parcialmente de acuerdo
No hay una definición consistente de colonización por C.difficile. Sin embargo, de acuerdo con una revisión reciente, se considera colonización cuando el bacilo es detectado y no hay síntomas ni signos de infección24. Probablemente los sujetos estén protegidos de la progresión a infección por una respuesta humoral a las toxinas24. Sin embargo, estos individuos actúan como un reservorio de infección y representan riesgo para otros sujetos25.
La prevalencia de colonización por de C.difficile varía entre diferentes grupos. En individuos sanos varía entre el 0 y el 15%, en neonatos y lactantes entre el 18 y el 90%, en ancianos en asilos entre el 0 y el 54%, y en trabajadores de la salud entre el 0 y el 13%24. El escrutinio de C.difficile para detectar a individuos colonizados no debe realizarse de forma rutinaria, ya que a estos sujetos no se les proporciona tratamiento24,26.
Aunque se desconoce cuál es el mecanismo exacto para la colonización por C.difficile, se han detectado esporas en el ambiente (agua, agua potable, albercas, suelo) y en hospederos intermediarios (animales) así como en alimentos (carne de puerco, res, pavo, mariscos y vegetales listos para comer)5. Sin embargo, no hay reportes de brotes tras el consumo de alimentos contaminados con este patógeno27. Es probable que los humanos ingieran esporas de C.difficile frecuentemente, pero la mayoría permanecen asintomáticos y no colonizados si cuentan con una microbiota intestinal intacta5,28. Las esporas de C.difficile sobreviven al ambiente ácido del estómago y germinan en el intestino6,12,29. Los ácidos biliares primarios en el duodeno se consideran facilitadores del proceso de germinación27. La microbiota intestinal en condiciones normales impide la colonización por patógenos por diferentes mecanismos, como la estimulación del sistema inmunológico del hospedero, la depleción de nutrientes y la inhibición de bacteriocinas13,27.
En los últimos años se ha observado la asociación entre la administración de inhibidores de la bomba de protones (IBP) e ICD, y se asume que la supresión del ácido gástrico prolongada es el mecanismo más importante. Aun cuando esta asociación es controversial, es recomendable una prescripción racional de IBP30,31.
- 4.
Se debe sospechar la ICD en un paciente con diarrea con antecedente de uso de antibióticos y/o inmunosupresión, adquirida en la comunidad o con más de 48h de hospitalización o dentro de las 8semanas posteriores al egreso
Acuerdo alcanzado: 87% totalmente de acuerdo, 9% parcialmente de acuerdo, 4% incierto
Se define ICD como la presencia de diarrea (3o más evacuaciones no formadas en 24h) y resultado positivo en heces de toxinas de C.difficile o detección toxigénica de C.difficile o la presencia de colitis seudomembranosa demostrada por colonoscopia24.
En la mayoría de los pacientes con ICD hay un historial de tratamiento con agentes antimicrobianos o inmunosupresión en las últimas 8semanas26. La definición de ICD adquirida en la comunidad ha variado con el tiempo; sin embargo, en la actualidad y a partir de las definiciones empleadas para clasificación epidemiológica de la ICD de acuerdo con Lessa et al.32 y Martin et al.28, los parámetros de temporalidad en los diferentes escenarios clínicos son:
- •
Adquirido en comunidad. Caso confirmado de ICD adquirido en entorno ambulatorio o ≤3días de la admisión hospitalaria y sin ingresar en un centro hospitalario durante las 12semanas previas. Los casos adquiridos en la comunidad llegan a tener una frecuencia del 10 al 30% y afectan por lo general a pacientes más jóvenes en comparación con los casos adquiridos en medios hospitalarios28.
- •
Inicio comunitario asociado a atención hospitalaria. Caso confirmado de ICD en entorno ambulatorio o ≤3días de la admisión hospitalaria proveniente de una residencia privada, con antecedente de ingresar en un centro hospitalario (o asilo) durante las 12semanas previas.
- •
Intrahospitalario. Caso confirmado de ICD con >3días de admisión hospitalaria.
- •
Inicio en asilo o instituciones de confinamiento. Caso confirmado de ICD de un residente en su entorno ambulatorio en estas instituciones o dentro de los primeros días de su admisión hospitalaria. En algunos países las instituciones de confinamiento, como los asilos, son considerados como centros hospitalarios.
Se considera que el uso de antibióticos es el principal factor de riesgo para que un individuo desarrolle ICD. El mecanismo propuesto es disbiosis, y entre los antibióticos considerados de mayor riesgo están la clindamicina, las fluoroquinolonas, las cefalosporinas de tercera generación y las aminopenicilinas33,34. Los aminoglucósidos, los inhibidores de betalactamasas, los carbapenémicos, la doxiciclina, el linezolid, los macrólidos, la rifampicina, la rifaximina y la tigeciclina se consideran de bajo riesgo.
Una revisión sistemática y metaanálisis que incluyó 12 estudios (n=56,776 pacientes) encontró que la ICD adquirida en comunidad se asoció con el uso de antibióticos y de corticoesteroides, además del hecho de padecer enfermedad inflamatoria intestinal (EII), neoplasia hematológica, falla renal y diabetes mellitus35.
- 5.
La recurrencia de ICD se define por la presencia de un segundo episodio dentro de las 8 semanas posteriores al episodio inicial clínicamente resuelto con el tratamiento
Acuerdo alcanzado: 96% totalmente de acuerdo, 4% parcialmente de acuerdo
Después de un cuadro de ICD, entre el 10 y el 30% de los pacientes presentan recurrencia, definida como la aparición de un segundo episodio dentro de las 8semanas posteriores al episodio inicial20,21. El riesgo de una segunda recurrencia es del 40%, y el de una tercera recurrencia, del 50%21.
La ICD recurrente puede deberse a esporas remanentes que germinan en el colon cuando el tratamiento antibiótico ha cesado o a reinfección adquirida en la comunidad13,20. Los factores de riesgo para recurrencia de ICD son: edad ≥65años, antibióticos adicionales durante el seguimiento, uso de IBP, insuficiencia renal, estancia reciente o prolongada en medio hospitalario, ICD por la cepa NAP1/BI/0275,36.
- 6.
Se ha observado mayor riesgo de ICD en pacientes con edad avanzada, inmunosupresión, en quienes recibieron antibióticos, en pacientes con enfermedad inflamatoria intestinal, hospitalizados y residentes en instituciones de estancia prolongada o confinamiento
Acuerdo alcanzado: 91% totalmente de acuerdo, 9% parcialmente de acuerdo
Los factores de riesgo para ICD se pueden dividir en 3 grupos:
- •
Factores del medio ambiente. Estancia hospitalaria o en instituciones de estancia prolongada o confinamiento, como los asilos4,5,13.
- •
Factores del hospedero. Edad mayor de 65años, EII, inmunodeficiencia, neoplasias hematológicas, desnutrición y albúmina sérica disminuida4,5,13. Los pacientes con EII (colitis ulcerosa crónica idiopática o enfermedad de Crohn) presentan 4.8 veces más riesgo de ICD37, en especial los expuestos a infliximab, esteroides, adalimumab, metronidazol, y con otras comorbilidades37. Además, la ICD complica el curso de la EII, se asocia a mayor estancia hospitalaria, incremento en la tasa de colectomía y mayor mortalidad38. Los estados que favorecen la inmunosupresión, como las neoplasias malignas, la quimioterapia, la infección por el virus de inmunodeficiencia humana, también se asocian a ICD13. Dentro de los pacientes oncológicos presentan mayor riesgo de ICD las mujeres con cáncer de mama. Los pacientes postrasplantados de órganos sólidos tienen un riesgo incrementado de ICD de adquisición hospitalaria 5veces más que el resto de pacientes hospitalizados39. Como se mencionó en el enunciado3, la asociación entre IBP e ICD es controversial40. También resulta controversial el antecedente de apendicectomía, la colocación de sonda nasogástrica y el antecedente de cirugía abdominal para el desarrollo de ICD13.
- •
Factores que inducen disbiosis. Como se menciona en el enunciado4, el uso de antibióticos es el principal factor que predispone al desarrollo de ICD.
- 7.
La edad (más de 65 años), la presencia de cáncer, el deterioro cognitivo y las comorbilidades cardiovasculares, respiratorias y renales son factores de riesgo que se han asociado a mayor morbimortalidad por ICD
Acuerdo alcanzado: 96% totalmente de acuerdo, 4% parcialmente de acuerdo
La morbilidad asociada con ICD incluye la realización de colectomía, ICD recurrente, egreso a instituciones de confinamiento y reingreso hospitalario. Respecto a la mortalidad atribuible a ICD, se consideraba que era menor al 1.5%; sin embargo, a partir del año 2000 se incrementó hasta ser del 4.5-5.7% y alcanzar el 6.9-16.7% durante periodos epidémicos21.
Las enfermedades cardiovasculares (cardiopatía isquémica, insuficiencia cardiaca), la insuficiencia respiratoria y la enfermedad pulmonar crónica y renal preexistentes se asocian con una mayor mortalidad. En un estudio de cohorte realizado en el Reino Unido que incluyó 2,761 pacientes se evalúo el riesgo de comorbilidades para mortalidad a 30días en pacientes con ICD. Contar con enfermedad renal fue el principal predictor de muerte. Padecer algún tipo de neoplasia fue predictor de mortalidad a partir de los 60años31. La enfermedad hepática y el deterioro cognitivo también se consideran predictores de enfermedad grave, aunque no de muerte40,41.
- 8.
Los predictores clínicos para el desarrollo de colitis fulminante porClostridium difficileson la edad (mayor de 70años), la inestabilidad hemodinámica, la hipoalbuminemia, la leucocitosis (mayor de 18,000/mm3), la enfermedad inflamatoria intestinal y el empleo de medicamentos antiperistálticos
Acuerdo alcanzado: 96% totalmente de acuerdo, 4% parcialmente de acuerdo
La progresión de ICD a colitis fulminante es poco frecuente (1-3%); sin embargo, la mortalidad en este grupo es considerable por la evolución a megacolon tóxico y perforación colónica20,21,41. La importancia del diagnóstico de colitis fulminante radica en que del 0.5 al 2.6% de los pacientes requieren colectomía42 y la mortalidad asociada es del 35-80%41.
En general, los datos de respuesta inflamatoria sistémica e inestabilidad hemodinámica, la elevación de creatinina >1.5veces de la basal (o creatinina sérica ≥1.5mg/dl y la leucocitosis >18,000/mm3), el empleo de medicamentos antiperistálticos (como narcóticos y anticolinérgicos), lactato sérico elevado, intervención quirúrgica los 30días previos y EII agregada se consideran factores de mal pronóstico41-43.
Palau-Dávila et al.44 identificaron factores de riesgo en pacientes hospitalizados de población hispana. Entre los factores de riesgo para colectomía se encontraron: índice de Charlson ≥1, estancia en UCI y ≥4días con diarrea antes del diagnóstico de ICD. Para mortalidad general en los primeros 30días los factores asociados fueron: baja concentración de albúmina (<2.00g/dl) y falla al tratamiento42.
Diagnóstico- 9.
El diagnóstico de ICD debe establecerse solo ante sospecha clínica con base en el algoritmo de 2 pasos
Calidad de la evidencia: A1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
El mecanismo exacto por el cual de C.difficile causa una infección sintomática aún no está claro por completo, pero sabemos que el microorganismo no es invasivo y la producción de toxinas es la clave de la patogénesis. Las pruebas de laboratorio por sí solas no pueden distinguir entre colonización asintomática y síntomas clínicos de infección. Por lo anterior, las pruebas diagnósticas para ICD deben realizarse solo en pacientes con sospecha clínica (sintomáticos)45,46.
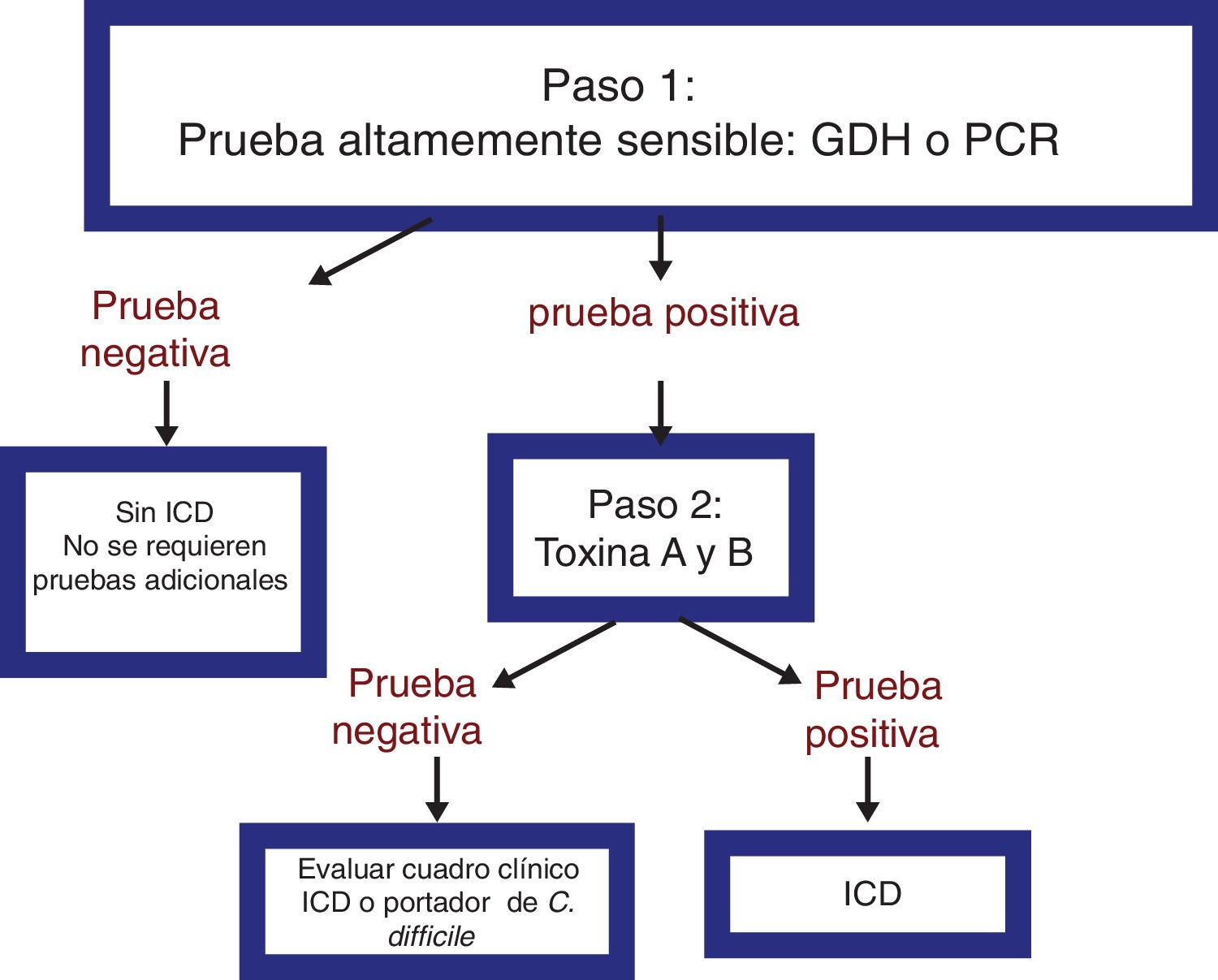
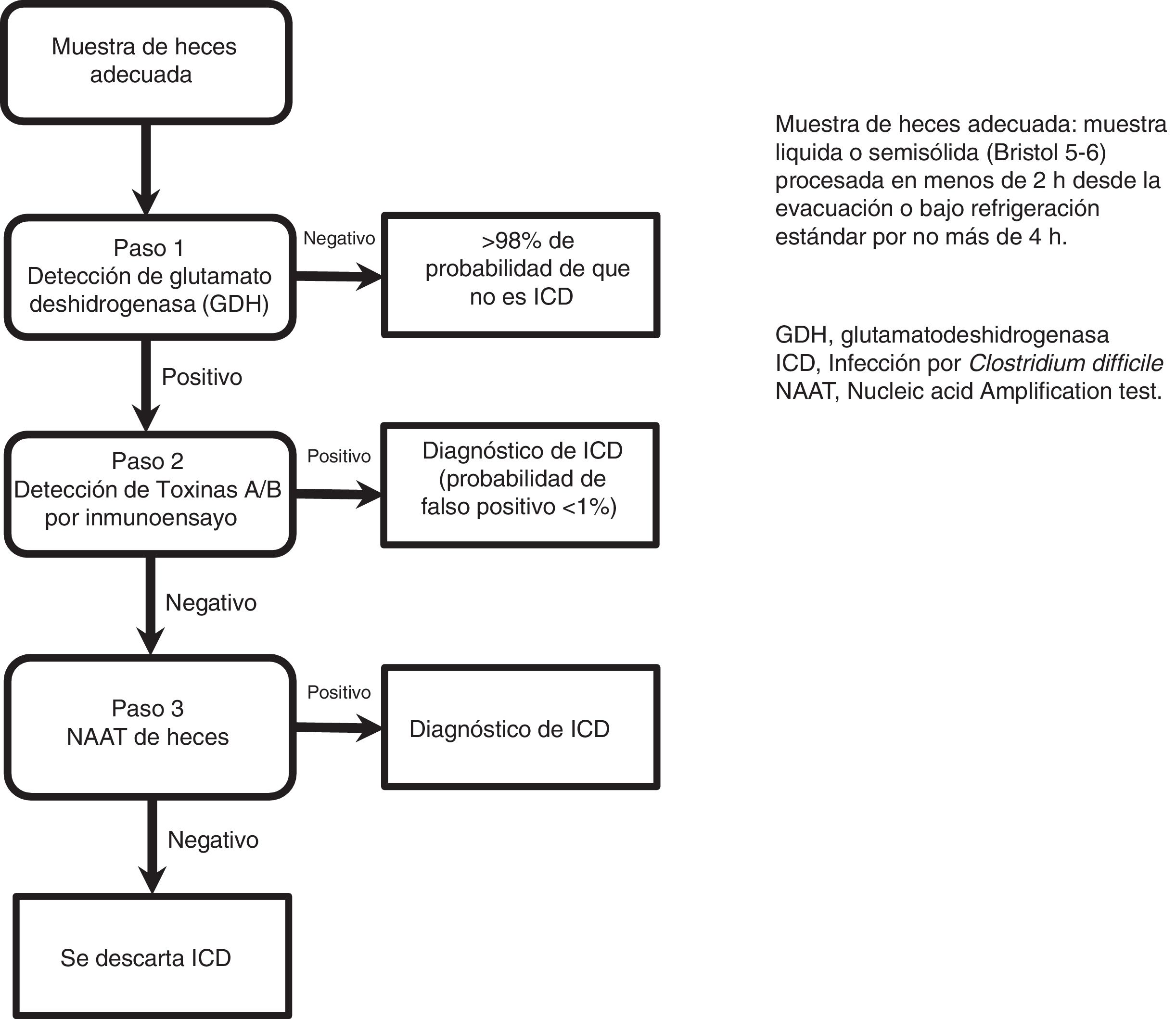
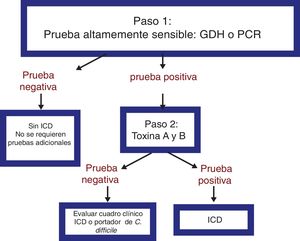
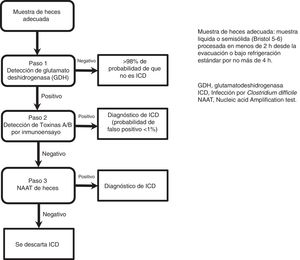
El método más útil para realizar el diagnóstico ante la sospecha clínica de ICD es mediante el algoritmo de 2 pasos (fig. 1). Se recomienda realizar una primera prueba de alta sensibilidad como la glutamato deshidrogenasa (GDH), o pruebas de detección de amplificación de ácidos nucleicos (NAAT) mediante la técnica de reacción en cadena de la polimerasa (PCR); en caso de resultado positivo, se debe confirmar el diagnóstico mediante detección de toxinas por técnica de inmunoensayo47-49. El grupo de consenso propone un algoritmo diagnóstico de 2 pasos. El algoritmo de multipasos, sugerido recientemente en publicaciones y guías internacionales (fig. 2), puede ser de utilidad en un pequeño grupo de pacientes con sospecha diagnóstica pero con detección negativa de toxinas, y puede aplicarse solo en casos de excepción por el costo elevado47-49.
La GDH es una enzima secretada y producida por C.difficile en grandes cantidades en comparación con las toxinasA yB, lo que permite que su detección sea adecuada y altamente sensible para el diagnóstico. La prueba en general tiene un costo accesible, lo que la convierte en una prueba ideal para el abordaje inicial de pacientes con diarrea de inicio reciente y factores de riesgo para ICD47. En un metaanálisis se reporta una alta precisión diagnóstica de GDH para la presencia de C.difficile en las heces, y cuando se compara con el cultivo alcanza una sensibilidad y una especificidad >90%50. La GDH tiene una especificidad del 80-100%, ya que detecta cepas toxigénicas y no toxigénicas del organismo.
La nueva generación de pruebas NAAT amplifica y detecta secuencias de ADN o ARN específicas de patógenos. Las ventajas de NAAT incluyen alta sensibilidad, alta especificidad y velocidad. Debido a que no se necesitan células viables, se simplifican los aspectos de muestreo, manipulación, transporte y almacenamiento. Además, no se requiere cultivo. El papel de NAAT en el proceso de diagnóstico de ICD puede ser de apoyo como parte de un algoritmo de 2 o 3 pasos47,51.
El cultivo toxigénico se considera aún como el estándar de oro para el diagnóstico de ICD52. Se utiliza como la prueba de referencia para comparar el resto de las pruebas diagnósticas, reportándose la detección de toxinas con una sensibilidad y una especificidad variables50. Por otro lado, el ensayo de neutralización de citotoxicidad celular (CCNA) puede tener un rendimiento diagnóstico similar al cultivo toxigénico. En este ensayo, el filtrado de una muestra de heces obtenida recientemente se inocula en varias líneas celulares sensibles para evaluar el efecto citopático de las toxinas de C.difficile, particularmente toxina B (TcdB). El CCNA tiene una sensibilidad del 90.8% y una especificidad del 98.3%47,53. La sensibilidad y la especificidad de las diferentes pruebas de diagnóstico para ICD son variables y se muestran en la tabla 3.
Características de las distintas pruebas de diagnóstico de infección por Clostridium difficile45-50
| Prueba | Blanco de detección | Sensibilidad (%) | Especificidad (%) |
|---|---|---|---|
| Cultivo toxigénico | Esporas o células vegetativas de C.difficile | 87-100 | 94-100 |
| Pruebas de amplificación de ácidos nucleicos | Ácidos nucleicos de C.difficile (genes toxigénicos) | 95-96 | 94-98 |
| Glutamato deshidrogenasa | Antígenos comunes de C.difficile | 75-100 | 80-85 |
| Ensayo de citotoxicidad | Toxinas libres | 90-100 | 98-99 |
| Inmunoensayos de toxinas A/B | Toxinas libres | 53-85 | 91-98 |
Es importante destacar que el algoritmo de 2 pasos es el más adecuado porque: 1)evita el tratamiento innecesario y sus consecuencias, y 2)una evaluación inicial con una prueba de GDH barata permite la identificación rápida de muestras negativas, lo que limita el uso de pruebas de NAAT, más costosas, a solo las muestras que fueron positivas para GDH47,48.
- 10.
Las pruebas de diagnóstico para ICD deben realizarse solamente en pacientes con evacuaciones diarreicas con factores de riesgo, excepto en aquellos con íleo en quienes puede ser útil el hisopado rectal para realizar PCR
Calidad de la evidencia y fuerza de la recomendación:
Pacientes con factores de riesgo: A1 fuerte a favor
Pacientes con íleo: C1 fuerte a Acuerdo alcanzado: 100% totalmente de acuerdo
Totalmente de acuerdo: 100%
El personal médico puede aumentar la eficacia de las pruebas de diagnóstico al solicitarlas en pacientes con probabilidad clínica de tener ICD; esto incluye no realizarlas de manera rutinaria en pacientes que hayan recibido laxantes en las últimas 48h y también puede aumentar la especificidad rechazando muestras fecales no diarreicas (Bristol1-5)18,47,54. Si un paciente tiene diarrea no claramente atribuible a las condiciones subyacentes (EII, síndrome de intestino irritable [SII], SII postinfeccioso, alimentación por sonda enteral, quimioterapia o laxantes), entonces está indicado realizar pruebas para diagnóstico de ICD, más aún si tiene los factores de riesgo descritos en el enunciado647. En la minoría de pacientes en quienes la ICD ocurre como íleo y la obtención de material fecal es complicada, el Colegio Americano de Gastroenterología recomienda la utilización de un hisopo («hisopado rectal») para la obtención de heces y realizar NAAT47. Esta recomendación está basada en un estudio prospectivo en donde se reporta una sensibilidad del 95.7% y una especificidad del 100% para diagnóstico de ICD mediante hisopado rectal55.
- 11.
La determinación de las toxinas A y B por técnica de inmunoensayo tiene una sensibilidad variable. Una prueba negativa no excluye el diagnóstico
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 78% totalmente de acuerdo, 22% parcialmente de acuerdo
Desde la identificación de la toxina que produce C.difficile en la década de 1970 se han utilizado varios métodos de diagnóstico para detectar la infección. La mayoría de las pruebas se basan en la detección de la toxina C.difficile56. Así, es importante recordar que el proceso patogénico se inicia con la germinación de las esporas de CD y la multiplicación de las formas vegetativas, mientras que la segunda fase del proceso patogénico es la producción de toxinas. Las cepas de interés clínico son las productoras de toxinas: A (TcdA) o B (TcdB), o ambas. Las toxinasA yB están codificadas por los genes tcdA y tcdB, que están localizados en el locus PaLoc (19.6kb)48,56. Aunque tradicionalmente se ha considerado que la toxinaA es enterotóxica y la toxinaB es citotóxica, ambas son citotóxicas para diversos tipos celulares, inducen un aumento de la permeabilidad vascular y causan hemorragia. Además, las dos toxinas actúan sinérgicamente en la destrucción de las células del tubo digestivo. A pesar de esto, existe controversia sobre cuál es papel individual de cada una de las toxinas47,48,57-59.
Existen múltiples pruebas comerciales para C.difficile que detectan objetivos diferentes: los análisis de inmunoensayo (ELISA) de toxinas y CCNA (EIA de membrana y toxinas) detectan toxinas libres, y las pruebas de GDH y NAAT detectan la presencia de todas las cepas de C.difficile toxigénicas56. Durante varios años la determinación de las toxinas de C.difficile por técnica de inmunoensayo fue un análisis económico, rápido y fácil de realizar, por lo que estos métodos fueron los más comunes en la mayoría de los laboratorios para realizar el diagnóstico de ICD60,61. Como algunas cepas de C.difficile no producen toxinaA, se recomienda que los inmunoensayos de toxinas detecten ambas toxinas, A yB. Las muestras de heces se pueden conservar a 4°C durante días o semanas antes de analizarse para detectar toxinas sin perder su capacidad diagnóstica62.
Las pruebas de EIA de toxinas han reportado sensibilidad y especificidad variables. La sensibilidad oscila entre el 58 y el 99% y la especificidad entre el 90 y el 100%51,63-72.
La sensibilidad inconsistente de los EIA puede deberse a varios factores, tales como variación antigénica entre las toxinas de diferentes cepas circulantes, almacenamiento y transporte inadecuados de las muestras, ciclos de congelación-descongelación y variación técnica entre laboratorios y diferencias entre fabricantes, entre otros46.
Por lo anterior, debido al bajo rendimiento general de los EIA de toxinas, el grupo de consenso recomienda la prueba en dos pasos descrita en el enunciado9.
- 12.
La prueba de la enzima glutamato deshidrogenasa debe ser la prueba inicial ante sospecha clínica de ICD
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
Los EIA de GDH detectan la GDH, una enzima constitutiva que se detecta fácilmente en heces y es producida en grandes cantidades tanto por cepas toxigénicas y como por cepas no toxigénicas de C.difficile, lo cual hace que sea un buen marcador de detección46-49. La prueba de GDH es de elección inicial en algoritmos de 2 y 3pasos que lo combinan con una prueba de toxina y/o una prueba molecular para detectar el gen de la toxina, y además se considera prueba relativamente sencilla46-49. Es importante mencionar que las técnicas modernas para detección de GDH utilizan anticuerpos monoclonales producidos contra la GDH específica de C.difficile, con lo cual se evita así cualquier reactividad cruzada con la GDH producida por otras bacterias anaeróbicas49. Como se menciona en el enunciado9, la GDH tiene una excelente concordancia cuando se compara con el cultivo, y dada su alta sensibilidad (>90%), se ha considerado como la prueba inicial en el algoritmo de 2pasos50.
- 13.
La colonoscopia solo es útil para establecer diagnóstico diferencial de otras enfermedades (por ejemplo: enfermedad inflamatoria intestinal) o en casos refractarios, pero no se recomienda como una prueba de diagnóstico inicial
Calidad de la evidencia: C1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 87% totalmente de acuerdo, 13% parcialmente de acuerdo
Aunque se ha establecido que para el diagnóstico de ICD se requiere la presencia de un contexto clínico de diarrea (>3 evacuaciones no formadas en 24h) o evidencia radiográfica de íleo o megacolon tóxico, así como resultados positivos de las pruebas de diagnóstico ya mencionadas previamente, algunas publicaciones consideran la evidencia colonoscópica o histopatológica de colitis seudomembranosa45. Sin embargo, ninguna de las guías internacionales recientes menciona que la colonoscopia es útil para el diagnóstico de ICD18,47-49. El rendimiento diagnóstico de la colonoscopia en el contexto de ICD sigue siendo controversial. Los trabajos al respecto coinciden en que, aunque no se recomienda como una herramienta de detección primaria, la colonoscopia puede agregar información valiosa en la ICD cuando pueden existir otras patologías colónicas como EII, colitis isquémica o neoplasias73-75. Además, la colonoscopia tiene aún un papel en el diagnóstico y tratamiento de la ICD, ya que en casos más complicados permite descomprimir el intestino y representa una ruta para administrar medicamentos o terapia de trasplante fecal entre pacientes con ICD refractario76.
En nuestro país existen un par de estudios respecto a los hallazgos endoscópicos en ICD. En el estudio de Velarde-Ruiz Velasco et al.12 se encontraron anormalidades endoscópicas en el 87%, y específicamente colitis seudomembranosa en el 38%. Pérez-Topete et al.77 reportaron en 306 pacientes los hallazgos de colonoscopia de 55casos, encontrando datos indicativos que se correlacionaron con C.difficile por biopsia y cultivo en 35 pacientes (64%).
- 14.
Se recomienda categorizar de acuerdo a criterios de gravedad a los pacientes con ICD confirmada como leve-moderada, grave o grave complicada, ya que esto permite una mejor decisión terapéutica
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
Las guías de práctica clínica para la ICD en adultos en su actualización 2010 realizada por la Sociedad de Salud Epidemiológica de Norteamérica (SHEA, por sus siglas en inglés) y la Sociedad de Enfermedades Infecciosas de Norteamérica (IDSA, por sus siglas en inglés) en conjunto con las guías para el diagnóstico, tratamiento y prevención de las infecciones por C.difficile publicadas en 2013 por el Colegio Americano de Gastroenterología (ACG, por sus siglas en inglés; tabla 4) estratifican a la enfermedad basándose en la gravedad, y esta estratificación útil para dirigir la terapéutica26,47,48.
Clasificación de la gravedad de la ICD
| Leve o moderada |
| Diarrea y cualquier signo o síntoma adicional que NO cumpla los criterios de diarrea grave o complicada |
| Grave |
| Albúmina sérica <3g/dl +UNO de los siguientes: |
| Leucocitos ≥15,000μl |
| Dolor abdominal |
| Grave complicada |
| Ingreso a unidad de cuidados intensivos |
| Hipotensión con o sin uso de vasopresores |
| Fiebre ≥38.5°C |
| Íleo o distensión abdominal significativa |
| Cambios en el estado mental |
| Leucocitos ≥35,000μl o <2,000μl |
| Niveles de lactato sérico >2.2mmol/l |
| Falla orgánica (ventilación mecánica, falla renal…) |
Adaptado de Martínez-Meléndez et al.46.
Finalmente, cabe señalar que en las últimas guías 201848 la estratificación para normar el tratamiento cambia solo un poco en la definición clínica pero no hay cambios en los parámetros, y las categorías son definidas de la siguiente manera:
- a)
Episodio inicial no grave: leucocitos <15,000/μl y creatinina sérica <1.5mg/dl.
- b)
Episodio inicial grave: leucocitos >15,000/μl o creatinina sérica >1.5mg/dl.
- c)
Episodio inicial fulminante: presencia de hipotensión o estado de choque, íleo o megacolon.
- 15.
Ante la confirmación clínica de la ICD, la primera medida para controlar la infección y disminuir el riesgo de progresión es el retiro, en lo posible, de todo tratamiento antimicrobiano, así como de medicamentos que por su mecanismo de acción incrementen el riesgo de recurrencia de ICD
Calidad de la evidencia: A1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 83% totalmente de acuerdo, 17% parcialmente de acuerdo
Un metaanálisis de 12 ensayos clínicos controlados (ECC)78 y un estudio retrospectivo79 han mostrado una asociación independiente entre el uso de antimicrobianos, indicados para una infección diferente a C.difficile, y una mayor recurrencia de la ICD. Por ello, se recomienda suspender los antibióticos durante o después de una ICD a menos de que exista una indicación absoluta para continuar con su uso.
- 16.
El tratamiento médico de la ICD está indicado solo ante la presencia de síntomas. La selección de antibióticos se debe realizar con base en los criterios de gravedad considerando si es un cuadro inicial o una recurrencia
Calidad de la evidencia: A1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 83% totalmente de acuerdo, 17% parcialmente de acuerdo
El tratamiento de la ICD solo está indicado en pacientes con diarrea y en los cuales se ha establecido el diagnóstico de ICD por C.difficile toxigénico. No deben tratarse los pacientes portadores de este microorganismo48. Para la selección de antibióticos es importante diferenciar una infección inicial o una recurrencia (ver enunciados4 y5). Toda ICD debe estratificarse de acuerdo con la gravedad del cuadro clínico, tal como se menciona en el enunciado14.
- 17.
En los casos de infección inicial leve-moderada porClostridium difficilese recomienda utilizar la vancomicina por vía oral en dosis de 125mg cada 6h como tratamiento de elección. En caso de no tener acceso a la vancomicina, se recomienda usar metronidazol como tratamiento alternativo
Calidad de la evidencia: A1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 96% totalmente de acuerdo, 4% parcialmente de acuerdo
El metronidazol y la vancomicina administrados por vía oral son los antibióticos más utilizados en el manejo de la ICD leve-moderada. Dos ECC mostraron que la eficacia del metronidazol es similar a la de la vancomicina80,81. En un estudio reciente se mostró una eficacia para curar la infección moderada del 90% con metronidazol y del 98% con vancomicina7. En otro ECC82 se ha demostrado que la vancomicina es superior al metronidazol en la infección grave. Nosotros recomendamos el uso de metronidazol como alternativa de manejo en la ICD leve-moderada en caso de no tener acceso a la vancomicina. Adicionalmente tiene la ventaja de ser significativamente más barata que la vancomicina y estar ampliamente disponible en nuestro medio. El metronidazol se prescribe a dosis de 500mg tres veces al día por 10días. En pacientes que no toleran la vía oral puede emplearse la vía intravenosa para la administración de este antibiótico47. La falta de respuesta al metronidazol después de 5días de haber iniciado el tratamiento es una indicación para el cambio de antibiótico a vancomicina oral a dosis de 125mg cada 6h por 10días47,48.
- 18.
En la ICD inicial grave se deberá emplear siempre vancomicina por vía oral por 14días
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
La vancomicina por vía oral es el antibiótico de elección en la ICD grave. Varios ECC han mostrado la superioridad de este antibiótico en comparación con metronidazol7,81,82. Se debe emplear a dosis de 125 a 250mg cada 6h por 10 a 14días, dependiendo de la respuesta clínica del paciente. En México no existe la presentación oral, solo está disponible en ampolletas para administración intravenosa. Esta presentación, pero usada para tratamiento oral, ha mostrado ser efectiva en el manejo de la ICD, ya que casi no se absorbe, por lo que alcanza elevadas concentraciones en el colon. Se recomienda agregar 10ml de agua inyectable estéril a la ampolleta de 500mg y darle al paciente 2.5ml (125mg) cada 6h y administrarla con jugo de manzana, de pera o de otra fruta para mejorar su tolerancia. Recientemente, en un estudio preclínico en nuestro país se demostró que la biodisponibilidad de la vancomicina administrada vía oral en agua inyectable es más estable en el tiempo y alcanza en el colon concentraciones más altas que cuando se administra en solución salina y jugo de naranja83.
- 19.
En la ICD grave complicada se deberá emplear vancomicina oral asociada a metronidazol intravenoso
Calidad de la evidencia: A1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 87% totalmente de acuerdo, 13% parcialmente de acuerdo
El tratamiento combinado de vancomicina oral a dosis de 250 a 500mg cada 6h combinada con metronidazol 500mg cada 8h por vía intravenosa es el tratamiento de elección en la ICD grave complicada26,47. No hay ensayos clínicos que permitan evaluar el esquema de dosis de antibióticos en ICD grave complicada, y el esquema terapéutico señalado se basa en recomendaciones de expertos26,47,48. Sin embargo, recientemente en un estudio clínico se observó que la adición de metronidazol intravenoso a la vancomicina disminuyó la mortalidad de los pacientes en un 50%84.
En los casos graves-complicados de ICD que cursen con gran distensión abdominal o íleo se recomienda administrar la vancomicina a dosis de 500mg a través de sonda rectal cada 6h26.
- 20.
Otras alternativas de tratamiento antimicrobiano para la ICD son: fidaxomicina, rifaximina-alfa y nitazoxanida
Calidad de la evidencia: B1 para fidaxomicina, C1 para rifaximina y nitazoxanida
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 78% totalmente de acuerdo, 18% parcialmente de acuerdo; 4% incierto
El tratamiento con fidaxomicina a dosis de 200mg dos veces al día por 10días es una alternativa a la vancomicina. Ensayos clínicos recientes han mostrado la no inferioridad de la fidaxomicina en comparación con la vancomicina, e incluso en análisis post hoc se ha sugerido que la fidaxomicina tiene menor tasa de recurrencia que la vancomicina85,86. Este antibiótico aún no está disponible en nuestro país.
El polimorfa alfa de la rifaximina es un antimicrobiano no absorbible que alcanza altas concentraciones en heces. Se han estudiado la eficacia y la seguridad con dosis de 400mg cada 8h durante 20días sola o en combinación con la terapia de primera línea y en recurrencias de ICD. Sus resultados son modestos y la evidencia sugiere que puede utilizarse como un co-adyuvante en los esquemas que incluyen vancomicina para el manejo de la ICD recurrente18,48,87. La nitazoxanida se ha comparado con esquemas de tratamiento con metronidazol y vancomicina. A dosis de 500mg dos veces al día por 7 a 10días la nitazoxanida mostró mejoría clínica similar al metronidazol y a la vancomicina. La respuesta sostenida a 31días fue similar con los tres antibióticos88. Se requiere un mayor número de estudios bien diseñados para conocer la eficacia de este antibiótico.
- 21.
Para el tratamiento de la primera recurrencia de ICD se recomienda utilizar vancomicina si el paciente recibió metronidazol. Si recibió vancomicina se recomienda volver a tratar con vancomicina, seguida de un esquema de dosis decrecientes y pulsos al final
Calidad de la evidencia: C2
Fuerza de la recomendación: débil a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
La recurrencia de la ICD después de un episodio inicial es del 10 al 20%, pero cuando un paciente presenta una primera recurrencia la posibilidad de futuras recidivas de la infección se eleva al 40 y al 65%, como se menciona en el enunciado547,89.
Para el tratamiento de la primera recurrencia de ICD se recomienda el empleo de la vancomicina a dosis de 125mg cada 6h por vía oral, si el antibiótico inicial fue el metronidazol. Si el tratamiento inicial fue con vancomicina, se recomienda repetir el mismo tratamiento, seguido de un esquema con dosis decrecientes y pulsos al final, bajo el siguiente esquema: 125mg cada 12h por una semana, luego 125mg al día por una semana y después 125mg cada 2 o 3días por dos a ocho semanas.
- 22.
Ante la segunda recurrencia se recomienda el uso de vancomicina vía oral por 14 días y uso decreciente con pulsos al final
Calidad de la evidencia: C2
Fuerza de la recomendación: débil a favor
Acuerdo alcanzado: 96% totalmente de acuerdo, 4% parcialmente de acuerdo
En los episodios de ICD después de la primera recidiva se recomienda emplear la vancomicina a dosis de 125mg cada 6h por 10 a 14días, seguida de dosis decrecientes de vancomicina con pulsos al final, bajo el mismo esquema presentado en el enunciado anterior, a pesar de que no existen ensayos clínicos controlados que apoyen el uso de un régimen de este tipo.
Otras alternativas son la vancomicina 125mg cada 6h por 10 a 14días, seguida de rifaximina 400mg cada 8h por 20días o fidaxomicina 200mg cada 12h por 10días si se llega a tener disponibilidad en el futuro.
- 23.
La evidencia para recomendar probióticos en la prevención o recurrencia de la ICD está limitada a algunas cepas
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
Los estudios que evalúan la utilidad de los probióticos en el tratamiento de la ICD inicial son muy escasos, y por ello no hay datos suficientes para apoyar el uso de probióticos como adyuvantes en el tratamiento con antibióticos de una infección activa47,48.
Por otro lado, diferentes metaanálisis han evaluado la utilidad de los probióticos en la prevención de la diarrea por C.difficile asociada a antibióticos (DCDAA). Una revisión Cochrane90 reciente evaluó 39 estudios en 9,955 participantes adultos y niños. En 31 de los estudios los resultados sugieren que los probióticos reducen el riesgo de DCDAA en un 60%. La incidencia de DCDAA fue del 1% en los tratados con probióticos y del 4% en los que recibieron placebo. En el análisis post hoc los autores demuestran que la reducción de la DCDAA fue significativamente mayor con probióticos que con placebo (3.1% versus 11.6%; NNT=12) en la población con un riesgo basal >5% para desarrollar ICD. Este efecto no se observó en los sujetos con un riesgo basal <5% para tener esta infección.
Diversos ECC, revisiones sistemáticas y guías de manejo han publicado resultados controversiales respecto a la utilidad de los probióticos en la prevención de la ICD en pacientes adultos hospitalizados que reciben antibióticos91-93. En un metaanálisis reciente que evalúo 19 estudios en 6,261 adultos admitidos al hospital en tratamiento con antibióticos se demostró que la incidencia de ICD en la cohorte que recibió probióticos fue del 1.6%, significativamente menor que en los controles, cuya incidencia fue de 3.9% (p<0.001)91. El riesgo relativo acumulado en los tratados con probióticos fue de 0.42 (IC95%: 0.30-0.57). El análisis de meta-regresión demostró que los probióticos fueron significativamente más efectivos si estos son administrados cerca de la primera dosis de antibióticos93. Los probióticos administrados dentro de los dos primeros días de iniciados los antibióticos produjeron una mayor reducción en el riesgo de ICD (riesgo relativo: 0.32; IC95%: 0.22-0.48) que una administración tardía (riesgo relativo: 0.70; IC95%: 0.40-1.23). No se demostró un mayor número de eventos adversos con los probióticos. Esta revisión sistemática con metaanálisis muestra que el uso de probióticos administrados cerca de la primera dosis de antibióticos reduce el riesgo de ICD en >50% en pacientes adultos hospitalizados tratados con antibióticos93.
Las cepas de probióticos más estudiadas y que han mostrado beneficios en la prevención de la recurrencia de ICD son Lactobacillus acidophilus CL1285 +L. casei LBC8OR; Saccharomyces boulardii CNCM I-745 Lactobacillus rhamnosus HN002 +Lactobacillus acidophilus NCFM; Lactobacillus acidophilus +Bifidobacterium bifidum (cepas Cultech)90-93.
- 24.
El trasplante de microbiota fecal es una opción segura y efectiva en pacientes con ICD con dos recurrencias o en episodios graves con falla a tratamiento antimicrobiano
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
El trasplante de microbiota fecal (TMF) consiste en la infusión de heces (que contienen la comunidad completa de la microbiota intestinal) de un donador sano en el tubo digestivo de un enfermo para curar o mejorar una enfermedad. El objetivo del TMF en la ICD es restaurar la diversidad de microorganismos en la microbiota colónica y eliminar el crecimiento del C.difficile. Las series de casos, ECC y diversos metaanálisis han mostrado que el TMF es efectivo en curar las recurrencias en el 85 al 90% de los casos tratados94,95. Las indicaciones del TMF son:
- •
Infección recidivante por Clostridium difficile.
- ∘
Por lo menos 3 episodios de ICD leve o moderada (uno inicial y 2 recurrencias) con falla al tratamiento de 6 a 8 semanas con vancomicina con o sin otro antibiótico alterno (fidaxomicina, rifaximina, nitazoxanida).
- ∘
Por lo menos 2 episodios de ICD con admisión al hospital y morbilidad significativa.
- •
ICD grave o fulminante que no responde al tratamiento estándar en 48h.
La selección del donador es un paso muy importante para el éxito y la seguridad del TMF. Los estudios han mostrado que puede usarse la microbiota fecal de un donador conocido (familiar, amigo, cónyuge) o de un donador universal (anónimo). El sujeto donante debe estar sano sin comorbilidades digestivas o extradigestivas y sin riesgo de transmitir un agente infeccioso y no haber usado antibióticos en los últimos 3meses. La estrategia de selección del donador ha sido descrita en varios artículos96,97. Las vías de administración del TMF incluyen la sonda nasogástrica, por colonoscopia, por enemas o en cápsulas; todas han mostrado ser efectivas98. Así mismo, la eficacia del TMF es similar usando microbiota fecal fresca o congelada99,100.
En pacientes con ICD grave el TMF también es efectivo en más del 80% de los casos tratados. La detección de colitis seudomembranosa durante una ICD es una indicación para realizar TMF de manera secuencial, con o sin la administración de vancomicina, hasta lograr la remisión clínica100,101. Aunque la evidencia es limitada, el TMF ha mostrado ser también efectivo en pacientes inmunocomprometidos con ICD102.
Los efectos adversos a corto plazo son menores e incluyen fiebre transitoria, malestar o dolor abdominal. Se ha descrito la transmisión de norovirus y rotavirus y algunos casos de muerte asociados a la vía de infusión del TMF, como broncoaspiración, con la administración por sonda nasogástrica o perforación asociada a la colonoscopia. En general se acepta que el TMF es un procedimiento seguro. Los efectos a largo plazo aún se desconocen, pero existe el riesgo potencial de desarrollo de alergias, enfermedades autoinmunes, enfermedad inflamatoria intestinal, obesidad y otros trastornos metabólicos o la transmisión de alguna enfermedad del donador. Por ello, el tratamiento con TMF solo debe usarse en pacientes con ICD con las indicaciones previamente señaladas48,99-102.
- 25.
La cirugía debe reservarse a pacientes con colitis grave (megacolon tóxico) que han fallado a todo tratamiento médico, falla del TMF, peritonitis generalizada o los casos raros de perforación colónica, siendo la colectomía subtotal con ileostomía el procedimiento de elección
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 91% totalmente de acuerdo, 9% parcialmente de acuerdo
El tratamiento quirúrgico está indicado en pacientes que desarrollen hipotensión que requiera aminas vasoconstrictoras, signos clínicos de sepsis o de falla orgánica múltiple con evidencia clínica de megacolon tóxico, peritonitis o perforación. La cirugía también debe considerarse en los pacientes con ICD grave que no respondan al tratamiento con antibióticos o con TMF. El procedimiento quirúrgico de elección es la colectomía subtotal con ileostomía terminal. Las colectomías segmentarias tienen peor pronóstico que la colectomía subtotal12. Otras modalidades terapéuticas incluyen la ileostomía en asa con lavado intraoperatorio con polietilenglicol e infusión postoperatoria anterógrada de vancomicina. En un ensayo aleatorio este procedimiento contribuyó a la preservación del colon en el 90% de los casos y a una menor mortalidad operatoria comparada con controles históricos (19% vs. 50%)103.
- 26.
Existen medidas de prevención y control de la ICD que van dirigidas a la interrupción del mecanismo de transmisión de la bacteria a través de manos de pacientes, del personal sanitario y del manejo de superficies o dispositivos médicos contaminados por las esporas bacterianas
Calidad de la evidencia: B1.
Fuerza de la recomendación: fuerte a favor
Acuerdo alcanzado: 100% totalmente de acuerdo
La higiene de manos es la piedra angular en la prevención de infecciones nosocomiales. El lavado apropiado de manos con agua y jabón, no con alcohol, antes y después de visitar enfermos con ICD es efectivo para remover las esporas del C.difficile en el personal médico. El aislamiento de pacientes con ICD en un cuarto con baño privado es recomendable y debe continuarse hasta después de 48h de la resolución de la diarrea. El personal en contacto con pacientes infectados debe usar guantes y bata para visitar a un enfermo con ICD. Los instrumentos o dispositivos diagnósticos usados en pacientes con ICD deben ser desinfectados con agentes esporicidas. La limpieza y la desinfección de habitaciones con agentes esporicidas es recomendable en los casos de un brote hospitalario de ICD48.
- 27.
La implementación de programas de optimización y educación en el empleo de antibióticos(stewardship), así como controles epidemiológicos intrahospitalarios, descontaminación ambiental y de lavado de manos son medidas que han demostrado una reducción de la incidencia de ICD
Calidad de la evidencia: B1
Fuerza de la recomendación: fuerte a favor del enunciado
Grado de acuerdo: 100% totalmente de acuerdo
La reducción en la frecuencia de uso, la duración y el número de antibióticos de alto riesgo en el paciente hospitalizado reduce el riesgo de ICD. Los antibióticos de uso hospitalario deben basarse en la epidemiología local y en el resultado de los cultivos tomados. La restricción de fluoroquinolonas, clindamicina y cefalosporinas debe ser considerada como una medida muy importante en la solución y prevención del problema en las instituciones médicas. Además, la implementación de un programa de optimización de antibióticos (stewardship) es obligada, sobre todo en las instituciones de tercer nível48.
ConclusionesLas recomendaciones emitidas fueron a través de 27 enunciados que se presentan en este documento dirigido a médicos que tratan población adulta. Se reconoce que la ICD debe sospecharse en sujetos con diarrea con antecedente de uso de antibióticos y/o inmunosupresión, pero que también puede adquirirse en la comunidad. Se propone seguir un algoritmo de 2pasos para el diagnóstico utilizando una primera prueba de alta sensibilidad como la glutamato deshidrogenasa (GDH) y, en caso de resultado positivo, se debe confirmar mediante detección de toxinas por técnica de inmunoensayo o con pruebas de detección de ácidos nucleicos. Se recomienda categorizar a la ICD con base a la evaluación clínica en leve-moderada, grave o grave complicada, ya que esto permite una mejor decisión terapéutica. En la ICD leve-moderada la vancomicina por vía oral se considera el medicamento de elección, mientras que el metronidazol puede ser una alternativa. El trasplante de materia fecal se reconoce como una opción eficaz ante las recurrencias o los casos más graves y la cirugía debe reservarse a pacientes con colitis grave (megacolon tóxico) que han fallado a todo tratamiento médico.
FinanciaciónEste consenso se realizó con el apoyo de la Asociación Mexicana de Gastroenterología, que permitió la participación, transportación y hospedaje durante la votación presencial. No se recibieron honorarios.
Conflicto de interesesDra. Ana Teresa Abreu y Abreu: es o ha sido ponente para Takeda, Sanofi, Mayoli-Spindler, Alfa-Wassermann y Carnot.
Dr. José Antonio Velarde-Ruiz Velasco: es o ha sido ponente para Takeda, Asofarma, Alfa-Wassermann, Abbvie, Abbott, Gilead y MSD.
Dra. Mónica Rocío Zavala-Solares: es o ha sido ponente para Takeda.
Dr. José María Remes-Troche: es miembro del consejo asesor de Takeda Pharmaceuticals, Alfa-Wassermann y Almirall. Recibió fondos para la investigación por Sanfer. Ponente para Takeda, Asofarma, Alfa-Wassermann, Carnot, Almirall y Astra-Zeneca.
Dr. Ramón Isaías Carmona-Sánchez: es o ha sido ponente para Asofarma, Astra-Zeneca y Chinoin.
Dr. Juan Manuel Aldana Ledesma: declara no tener conflicto de intereses.
Dr. Adrián Camacho-Ortiz: declara no tener conflicto de intereses.
Dr. Raúl Contreras Omaña: declara no tener conflicto de intereses.
Dr. Raymundo Díaz Seoane: declara no tener conflicto de intereses.
Dra. Carolina Tatiana Elizondo Vázquez: declara no tener conflicto de intereses.
Dra. Elvira Garza-González: declara no tener conflicto de intereses.
Dr. Octavio Gómez-Escudero: es o ha sido ponente para Takeda.
Dra. Janett Sofía Jacobo Karam: declara no tener conflicto de intereses.
Dr. Sergio A. Lazo de la Vega Jasso: declara no tener conflicto de intereses.
Dr. Miguel Morales Arámbula: es o ha sido ponente para Takeda y Asofarma.
Dra. Laura Ofelia Olivares Guzmán: declara no tener conflicto de intereses.
Dr. José Sifuentes Osornio: declara no tener conflicto de intereses.
Dra. Ana Guadalupe Siu Moguel: declara no tener conflicto de intereses.
Dr. Rodrigo Soto Solís: es o ha sido ponente para Ferring, Novartis y UCB.
Dr. Luis Raúl Valdovinos García: declara no tener conflicto de intereses.
Dr. Miguel Ángel Valdovinos Díaz: es miembro del consejo asesor de Takeda, Menarini, Sanofi, Biocodex. Ponente para Takeda, Sanofi, Menarini, Biocodex y Carnot.
Dr. Genaro Vázquez Elizondo: es o ha sido ponente para Takeda, Asofarma y Sanfer.
Dr. G. Grajales Figueroa declara no tener conflictos de interés.