La disfagia orofaríngea (DOF) ocurre en niños con parálisis cerebral. Es importante investigar su relación con algunas variables, y el objetivo de este estudio fue identificar factores asociados con la DOF.
Material y métodosEstudio de casos y controles en pacientes con parálisis cerebral de 8meses a 15años de edad, de noviembre de 2018 a noviembre de 2019, aprobado por el Comité de Ética. El diagnóstico de DOF se realizó por videofluoroscopia cuando hubo reflujo nasofaríngeo, estancamiento en valécula, en senos piriformes, penetración y aspiración. Las variables independientes fueron tipo de parálisis cerebral, afectación motora gruesa clasificada en cinco niveles, estado nutricional y comorbilidades. Se incluyó un caso con DOF, y el siguiente sin alteraciones en la videofluoroscopia fue control. Las variables se compararon con chi cuadrado (χ2) y t de Student. La asociación se midió con odds ratio. El intervalo de confianza fue del 95%.
ResultadosSe estudiaron 30 pacientes con DOF y 30 sin DOF. El sexo, la edad, el peso al nacer y la edad gestacional tuvieron distribución similar en los dos grupos. De los datos percibidos por las madres al momento de la alimentación, la mayor frecuencia de la dificultad en el traslado del bolo alimenticio en el grupo con DOF mostró diferencia estadística significativa (p<0.001); de los factores estudiados, el nivelV de la afectación motora gruesa se asoció con mayor frecuencia de DOF (OR: 5.7; IC95%: 1.8-17.5).
ConclusionesLa DOF se asoció con el nivelV de afectación motora gruesa.
Oropharyngeal dysphagia (OPD) occurs in children with cerebral palsy and its relation to certain variables is important to evaluate. The aim of the present study was to identify factors associated with OPD.
Materials and methodsA case-control study, conducted within the time frame of November 2018 to November 2019 and approved by the Ethics Committee, analyzed patients with cerebral palsy that were 8months to 15years of age. OPD was diagnosed by videofluoroscopy when there was nasopharyngeal reflux, stagnation in the valleculae and the pyriform sinuses, penetration, and aspiration. The independent variables were type of cerebral palsy, gross motor function classified in five levels, nutritional status, and comorbidities. Cases (cerebral palsy patients with an altered VFS) and controls (cerebral palsy patients with an unaltered VFS) were consecutively included. The variables were compared using the chi-square test and the Student’s t test. Associations were measured using odds ratios. A 95% confidence interval was employed..
ResultsThirty patients with OPD and 30with no OPD were studied. Sex, age, birthweight, and gestational age were similarly distributed in the two groups. From the data perceived by the mothers at the time of feeding, difficulty in food bolus transport was more frequent in the OPD group, with a statistically significant difference (<0.001). Of the factors analyzed, levelV gross motor function was more frequently associated with OPD (OR 5.7; 95% CI 1.8-17.5).
ConclusionsOPD was associated with level V gross motor function.
La parálisis cerebral (PC) es un grupo de trastornos neuromotores no progresivos que afectan el desarrollo del cerebro fetal, inician desde el nacimiento y persisten durante toda la vida. La prevalencia es de 2.1 por 1,000 nacidos vivos1.
La PC comprende limitaciones con el desarrollo del movimiento, de la postura y de la función motora; además puede acompañarse de epilepsia, discapacidad intelectual, visual, trastornos cognitivos, del lenguaje, conductuales y alteraciones en la deglución2.
La deglución es un proceso complejo que involucra músculos de la boca, de la laringe y del esófago, con la participación de diferentes niveles del sistema nervioso central; está constituida por tres fases que ocurren de manera secuencial: oral, faríngea y esofágica3.
La disfagia es la dificultad para deglutir. Puede clasificarse como disfagia orofaríngea (DOF), debida a disfunción de la faringe y del esfínter esofágico superior, o como disfagia esofágica, por disfunción del esófago inferior4.
La prevalencia agrupada de DOF en pacientes con PC documentada en un metaanálisis fue de 50.4% y aumentó de manera gradual con la gravedad de la PC5. La DOF en los pacientes con PC favorece la aparición de complicaciones infecciosas, respiratorias y nutricionales que incrementan la mortalidad6.
La videofluoroscopia (VFS) es el mejor examen radiológico para diagnosticar DOF, ya que permite visualizar la anatomía de la cavidad oral, faringe, laringe y esófago superior, así como la función e integración de las fases de la deglución7-8.
En nuestra institución, Quiñones-Pacheco et al.9, en un estudio descriptivo en 25 pacientes con PC a quienes se les practicó VFS para diagnosticar DOF, encontraron que el 64% tuvieron residuo en la valécula y estasis en los senos piriformes; la aspiración pulmonar ocurrió en el 52%.
La relación de algunas variables que ocurren en niños con PC y DOF ha sido estudiada en algunos países desarrollados10-12, pero la frecuencia y la interacción de las variables pueden ser diferentes en distintas regiones, por lo que el objetivo de este estudio fue determinar cuáles son los factores asociados con DOF diagnosticada mediante VFS en niños con PC.
Material y métodosPoblación de estudioSe realizó un estudio de casos y controles13 en pacientes con PC con edades entre 8meses y 15años atendidos en los servicios de gastroenterología y neurología pediátrica del Nuevo Hospital Civil de Guadalajara «Dr. Juan I. Menchaca» entre noviembre de 2018 y noviembre de 2019.
Se incluyeron pacientes con diagnóstico de PC confirmado por el servicio de neurología pediátrica, a quienes se les evaluó la coordinación y la sincronía de la deglución con diferentes texturas de alimentos (líquido, néctar y puré) por VFS usando bario como medio de contraste.
Se excluyeron pacientes con malformaciones congénitas faciales, esofágicas, traqueales y enfermedades degenerativas del sistema nervioso central.
Se conformaron dos grupos de estudio: uno con DOF y otro sin DOF. Los pacientes se incluyeron de manera consecutiva: tras identificar a un paciente con alteraciones en la VFS sugestiva de DOF, el cual se consideró caso, el siguiente sujeto con PC sin alteraciones en la VFS fue considerado control.
El tamaño de la muestra se calculó con error alfa 0.05%, error beta 20%, razón de un control por cada caso, proporción hipotética de pacientes con DOF y grado de afectación motora gruesa nivelIV yV14,15 del 92%6, proporción hipotética de pacientes sin DOF con grado de afectación motora gruesa nivelIV yV14,15, del 37%6, a lo que se añadió un 20% por posibles exclusiones; así, el cálculo sugirió 15casos y 15controles, cifra que se incrementó al doble debido que el valor del razón de momios (OR, siglas en inglés) menos extremo a ser detectado fue muy elevado.
VariablesLa variable dependiente fue DOF, que se consideró presente cuando mediante VFS se detectó al menos uno de los siguientes signos: reflujo nasofaríngeo, residuo en valécula, residuo en senos piriformes, penetración y aspiración; lo anterior, de forma independiente de los datos clínicos.
Las variables independientes fueron: tipo de PC según su clasificación topográfica, que pudo ser espástica, discinética, atáxica, hipotónica/flácida o mixta; grado de afectación motora gruesa de acuerdo con el sistema de clasificación de la función motora gruesa (SCFMG) que comprende cinco niveles14-15, además de otras variables, como comorbilidades y estado nutricional.
Otras variables de estudio fueron: sexo, edad al momento de la investigación, edad gestacional al nacimiento y datos clínicos percibidos por las madres de los pacientes con PC durante la alimentación en el hogar.
ProcedimientosA los padres de los niños con diagnóstico de PC del servicio de gastroenterología y neurología pediátrica se les invitó a participar en el estudio, previa explicación de los motivos de la investigación y en qué consiste la VFS, un procedimiento incluido dentro del protocolo de diagnóstico y tratamiento del servicio de gastroenterología pediátrica en los pacientes con PC de la institución sede.
La VFS fue practicada en el servicio de radiología por un mismo radiólogo certificado (JJCA) mediante fluoroscopia y un equipo de sistema de imagen Multix Fusion Max Marca Siemens Icons 2008, previa colocación del paciente de forma lateral entre la fuente emisora de rayosX y el chasis con el equipo en posición vertical; a los niños en los que no fue posible esta posición se les colocó sobre una silla con su tutor. Las texturas se prepararon para que sus consistencias fueran similares a las administradas con la alimentación oral rutinaria de los niños; la preparación se administró con cuchara de material plástico, ofreciéndose de dos a tres degluciones por textura, que oscilaron entre 1 y 5ml previa adición de bario como medio de contraste. La primera consistencia fue tipo néctar, luego consistencia líquida y al final consistencia tipo puré. El registro de las imágenes se realizó de forma dinámica. Se utilizó un espesante comercial Enterex® con la finalidad de obtener los tipos de texturas y se preparó de la siguiente forma: textura líquida: 90ml de agua más 13.5g de bario en polvo; textura néctar: 90ml de agua más 9g de bario más 2.25g de espesante Enterex®; textura consistencia puré: 90ml de agua más 9g de bario más 9g de espesante Enterex®. Durante el estudio se permitió el acompañamiento de los padres, quienes permanecieron en la sala de radiología desde el inicio hasta el final del procedimiento y participaron en la realización de la VFS para simular la alimentación habitual administrada en casa. Los hallazgos de la VFS se recolectaron durante el procedimiento en un formato diseñado para esta investigación.
Uno de los investigadores (NGR) obtuvo la información de primera mano, mediante entrevistas directas a los padres, acerca de datos clínicos observados durante la alimentación en el hogar. De forma simultánea se extrajeron de los expedientes clínicos los hallazgos durante la evaluación de neurología pediátrica que permitieron clasificar de forma topográfica si existía monoplejía, diplejía, cuadriplejía y hemiplejía; con respecto al tono muscular, si la PC era espástica, discinética, atáxica, hipotónica/flácida o mixta; y en relación con el grado de afectación motora gruesa, de acuerdo con el SCFMG14-15 se clasificó en cinco niveles, que van desde el nivelI, en el que el niño camina sin limitaciones, hasta el nivelV, en el que la movilidad propia está severamente limitada y se usan dispositivos de asistencia.
La clasificación topográfica de la PC fue diagnosticada por el neurólogo pediatra que participó en esta investigación.
El diagnóstico del estado de nutrición fue llevado a cabo por un nutriólogo certificado con la medición del peso, de la talla y del índice de masa corporal (IMC), que se calculó con la fórmula peso (kg)/talla (m2). Las medidas se obtuvieron con los niños en ropa interior ligera con los instrumentos calibrados.
El peso se midió en los pacientes con incapacidad de bipedestación o sedestación independiente en posición de decúbito en un infantómetro marca Seca (precisión 50g), y a los que pudieron mantenerse en bipedestación independiente se les pesó en balanza marca Seca (precisión 0.1kg). El niño se colocó en el centro de la balanza (de pie o en decúbito supino) con los brazos a ambos lados del cuerpo y con vista al frente; el peso de los que no pudieron sostenerse se calculó restando el peso de la madre16.
Para la medición de la talla los pacientes se colocaron de pie sobre un plano horizontal en posición de firmes con la cabeza, la espalda, los glúteos y los gemelos pegados a la barra vertical del instrumento. La cabeza (colocada en el plano de Frankfurt) se puso en contacto con la barra móvil del equipo de medición y se aplicó ligera tracción por las mastoides. La medición se realizó con estadímetro de Harpenden fabricado por Seca (precisión 0.1cm); los niños que por su condición no pudieron ser medidos fueron evaluados mediante las fórmulas para estimar la talla: longitud de la tibia (cm) y altura de la rodilla (cm)16.
Se estimaron los índices antropométricos peso/edad (P/E), talla/edad (T/E), peso/talla (P/T) y el IMC de acuerdo con las tablas de crecimiento en niños portadores de PC infantil16 para clasificar el estado nutricional de acuerdo con la Organización Mundial de la Salud (OMS)17,18.
La información de la investigación se recolectó en un formato diseñado para esta investigación. Antes de la prueba definitiva se efectuó una prueba piloto de recolección y captura de los datos para corregir errores.
Análisis estadísticoA las variables cuantitativas se les calcularon índices de curtosis y de asimetría. Si la distribución fue simétrica, se determinó media y desviación estándar y se compararon con prueba t de Student para dos muestras independientes. Las variables cualitativas se expresaron en porcentajes y se contrastaron con chi cuadrado (χ2) o prueba exacta de Fisher. La asociación entre DOF y los factores de estudio se midió con OR.
El intervalo de confianza fue del 95%. El análisis estadístico se realizó con el programa estadístico para ciencias sociales (SPSS Statistics for Macintosh, versión 22.0, Armonk, NY, IBM Corp.).
Consideraciones éticasSe solicitó a los responsables de los pacientes el consentimiento informado para participar en la investigación descrita.
La investigación cumple con la normativa vigente en investigación bioética y se obtuvo la autorización del Comité de Ética de la institución sede (Folio 000138).
ResultadosSe invitó a participar en la investigación a 64 pacientes con PC con edades entre 8meses y 15años. Se excluyeron cuatro pacientes: tres debido a falta de cooperación de los niños y uno debido a que el padre no aceptó la administración de bario, lo que resultó en una muestra de 60 sujetos: 30 pacientes con DOF y 30 sin DOF.
En los 30 casos los signos de DOF identificados por VFS fueron residuo en valécula, estancamiento en senos piriformes, reflujo nasofaríngeo, penetración, aspiración y aspiración silente; 26 pacientes tuvieron más de un signo (87%), y se identificaron tres signos de forma simultánea por paciente en promedio; la frecuencia máxima de signos en un mismo paciente fue de seis (20%) y la mínima con un signo en cuatro (13%).
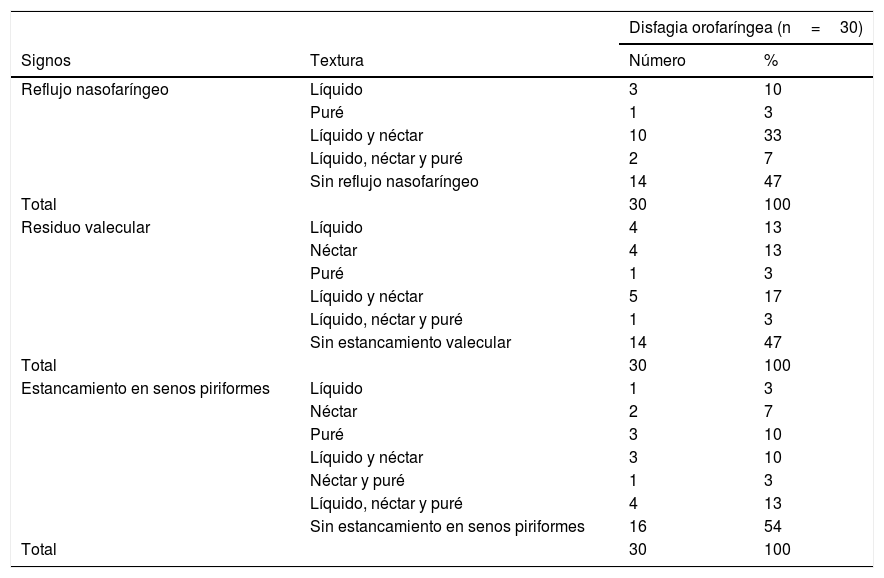
Cuando se realizó la VFS la textura néctar fue la más frecuente y ocurrió con reflujo nasofaríngeo, residuo en valécula y estancamiento en senos piriformes, aunque debe señalarse que la textura líquida, cuando se incluyó en las combinaciones de texturas, fue la más común en todos los signos evaluados (tabla 1).
Frecuencia de reflujo nasofaríngeo, estancamiento valecular y estancamiento en senos piriformes, en los pacientes con disfagia orofaríngea
| Signos | Textura | Disfagia orofaríngea (n=30) | |
|---|---|---|---|
| Número | % | ||
| Reflujo nasofaríngeo | Líquido | 3 | 10 |
| Puré | 1 | 3 | |
| Líquido y néctar | 10 | 33 | |
| Líquido, néctar y puré | 2 | 7 | |
| Sin reflujo nasofaríngeo | 14 | 47 | |
| Total | 30 | 100 | |
| Residuo valecular | Líquido | 4 | 13 |
| Néctar | 4 | 13 | |
| Puré | 1 | 3 | |
| Líquido y néctar | 5 | 17 | |
| Líquido, néctar y puré | 1 | 3 | |
| Sin estancamiento valecular | 14 | 47 | |
| Total | 30 | 100 | |
| Estancamiento en senos piriformes | Líquido | 1 | 3 |
| Néctar | 2 | 7 | |
| Puré | 3 | 10 | |
| Líquido y néctar | 3 | 10 | |
| Néctar y puré | 1 | 3 | |
| Líquido, néctar y puré | 4 | 13 | |
| Sin estancamiento en senos piriformes | 16 | 54 | |
| Total | 30 | 100 | |
De la comparación de los pacientes con DOF y sin DOF resultó que 17 pacientes con DOF (57%) y 16 sin DOF (53%) fueron del sexo femenino (p=0.795).
La edad de los pacientes de los dos grupos de estudio al momento de la investigación mostró distribución simétrica y osciló entre 8meses y 15años de edad.
La edad de los pacientes con DOF fue de 6.7±1.7años y en los sin DOF fue de 7.8±1.1años (p=0.972). Además, tuvieron entre 2 y 12años 26 pacientes con DOF (86%) y 20 sin DOF (66%); fueron menores de 2años de edad dos casos (7%) y dos controles (7%), y mayores de 12años, dos con DOF (7%) y ocho sin DOF (27%).
Con respecto al nivel socioeconómico, el estado socioeconómico medio bajo se documentó en 15 pacientes con DOF (50%) y en 22 sin DOF (73%) (p=0.063). Los demás pacientes, en los dos grupos de estudio, pertenecieron al grupo socioeconómico medio.
La edad gestacional al nacimiento mostró distribución normal; en los pacientes con DOF fue de 34.7±3.7meses y en los recién nacidos sin DOF fue de 35.2±2.9meses (p=0.517).
El peso al nacer también tuvo distribución simétrica: en los casos fue de 2,299±829g y en los controles de 2,330±572g (p=0.863).
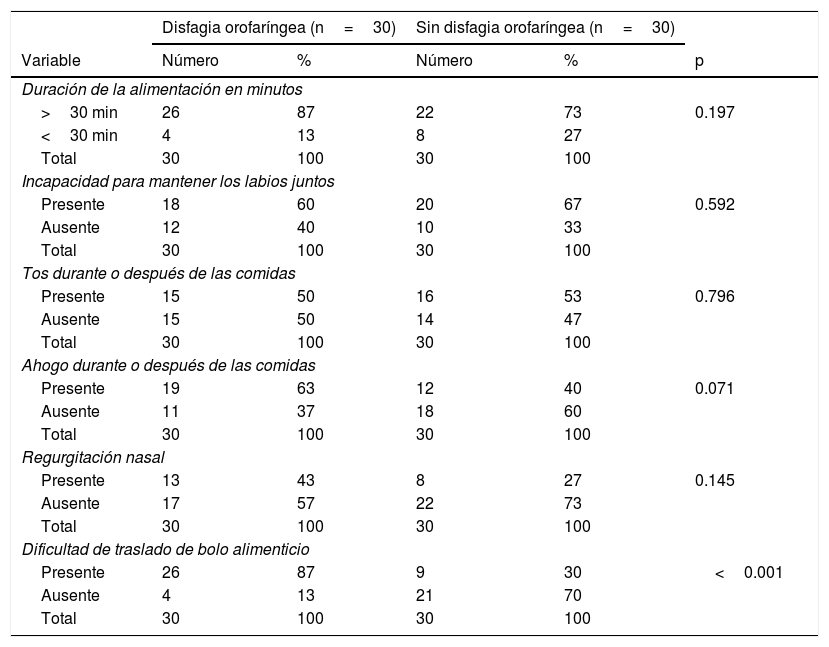
La frecuencia de los datos percibidos por las madres durante la alimentación en el hogar, como duración de la alimentación mayor de 30min, incapacidad para mantener los labios juntos, tos durante o después de las comidas y ahogo durante o después de las comidas, se distribuyó de manera semejante en los dos grupos de estudio; solo la mayor frecuencia de la dificultad en el traslado del bolo alimenticio en el grupo con DOF tuvo diferencia estadística significativa (tabla 2).
Datos percibidos por las madres de los pacientes con y sin disfagia orofaríngea durante la alimentación en el hogar
| Variable | Disfagia orofaríngea (n=30) | Sin disfagia orofaríngea (n=30) | p | ||
|---|---|---|---|---|---|
| Número | % | Número | % | ||
| Duración de la alimentación en minutos | |||||
| >30 min | 26 | 87 | 22 | 73 | 0.197 |
| <30 min | 4 | 13 | 8 | 27 | |
| Total | 30 | 100 | 30 | 100 | |
| Incapacidad para mantener los labios juntos | |||||
| Presente | 18 | 60 | 20 | 67 | 0.592 |
| Ausente | 12 | 40 | 10 | 33 | |
| Total | 30 | 100 | 30 | 100 | |
| Tos durante o después de las comidas | |||||
| Presente | 15 | 50 | 16 | 53 | 0.796 |
| Ausente | 15 | 50 | 14 | 47 | |
| Total | 30 | 100 | 30 | 100 | |
| Ahogo durante o después de las comidas | |||||
| Presente | 19 | 63 | 12 | 40 | 0.071 |
| Ausente | 11 | 37 | 18 | 60 | |
| Total | 30 | 100 | 30 | 100 | |
| Regurgitación nasal | |||||
| Presente | 13 | 43 | 8 | 27 | 0.145 |
| Ausente | 17 | 57 | 22 | 73 | |
| Total | 30 | 100 | 30 | 100 | |
| Dificultad de traslado de bolo alimenticio | |||||
| Presente | 26 | 87 | 9 | 30 | <0.001 |
| Ausente | 4 | 13 | 21 | 70 | |
| Total | 30 | 100 | 30 | 100 | |
Valor de p al comparar las frecuencias con χ2 o prueba exacta de Fisher.
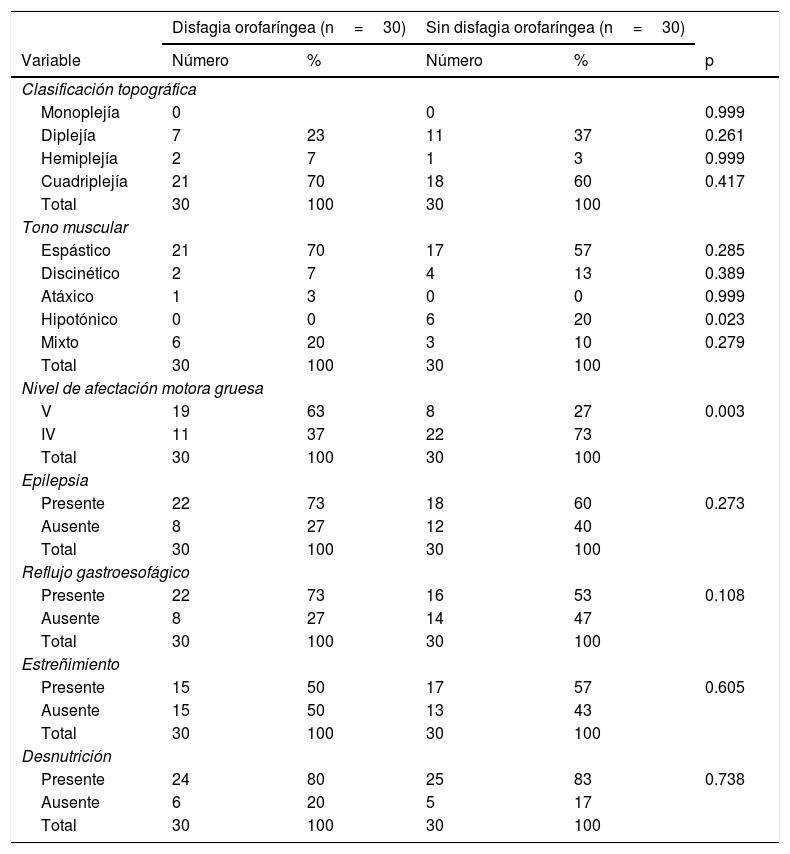
En cuanto a los factores que podrían tener relación con DOF, como la frecuencia de las manifestaciones relacionadas con la clasificación topográfica de la PC (monoplejía, diplejía, hemiplejía y cuadriplejía), los tipos de tono muscular (espástico, discinético, atáxico y mixto), así como las comorbilidades (epilepsia, reflujo gastroesofágico, estreñimiento y desnutrición), se distribuyeron de manera similar en los dos grupos de estudio; por otra parte, el nivelV de afectación motora gruesa medido con el SCFMG13-14, comparado con el nivelIV, mostró diferencia estadística significativa a favor de los pacientes con DOF (p=0.003) (tabla 3) y se asoció con mayor frecuencia de DOF (OR: 5.7; IC95%: 1.8-17.5).
Factores neurológicos y comorbilidades con posible relación con disfagia orofaríngea diagnosticada por videofluoroscopia en los dos grupos de estudio
| Disfagia orofaríngea (n=30) | Sin disfagia orofaríngea (n=30) | ||||
|---|---|---|---|---|---|
| Variable | Número | % | Número | % | p |
| Clasificación topográfica | |||||
| Monoplejía | 0 | 0 | 0.999 | ||
| Diplejía | 7 | 23 | 11 | 37 | 0.261 |
| Hemiplejía | 2 | 7 | 1 | 3 | 0.999 |
| Cuadriplejía | 21 | 70 | 18 | 60 | 0.417 |
| Total | 30 | 100 | 30 | 100 | |
| Tono muscular | |||||
| Espástico | 21 | 70 | 17 | 57 | 0.285 |
| Discinético | 2 | 7 | 4 | 13 | 0.389 |
| Atáxico | 1 | 3 | 0 | 0 | 0.999 |
| Hipotónico | 0 | 0 | 6 | 20 | 0.023 |
| Mixto | 6 | 20 | 3 | 10 | 0.279 |
| Total | 30 | 100 | 30 | 100 | |
| Nivel de afectación motora gruesa | |||||
| V | 19 | 63 | 8 | 27 | 0.003 |
| IV | 11 | 37 | 22 | 73 | |
| Total | 30 | 100 | 30 | 100 | |
| Epilepsia | |||||
| Presente | 22 | 73 | 18 | 60 | 0.273 |
| Ausente | 8 | 27 | 12 | 40 | |
| Total | 30 | 100 | 30 | 100 | |
| Reflujo gastroesofágico | |||||
| Presente | 22 | 73 | 16 | 53 | 0.108 |
| Ausente | 8 | 27 | 14 | 47 | |
| Total | 30 | 100 | 30 | 100 | |
| Estreñimiento | |||||
| Presente | 15 | 50 | 17 | 57 | 0.605 |
| Ausente | 15 | 50 | 13 | 43 | |
| Total | 30 | 100 | 30 | 100 | |
| Desnutrición | |||||
| Presente | 24 | 80 | 25 | 83 | 0.738 |
| Ausente | 6 | 20 | 5 | 17 | |
| Total | 30 | 100 | 30 | 100 | |
Valor de p al comparar las frecuencias con χ2 o prueba exacta de Fisher.
La frecuencia del tipo de tono muscular hipotónico también mostró diferencia estadística significativa a favor de los pacientes sin DOF (tabla 3).
Cabe comentar que otras comorbilidades, como estreñimiento, problemas ortopédicos, auditivos y endocrinos, se distribuyeron de manera similar en los dos grupos de estudio.
En lo que respecta al estado nutricional, se observó algún grado de desnutrición en 24 pacientes con DOF (80%) y en 25 niños sin DOF (83%); la diferencia en las frecuencias de desnutrición leve, moderada y grave entre los dos grupos de estudio no fue significativa: cabe resaltar que seis pacientes (20%) tuvieron desnutrición grave en el grupo con DOF y cinco en el sin DOF (15%), y en la mayoría de los sujetos de los dos grupos de estudio se diagnosticó desnutrición moderada.
Discusión y conclusionesEl presente estudio demostró que la DOF se asoció con el nivelV del grado de afectación motora gruesa clasificada en cinco niveles14-15. Asimismo, la dificultad del traslado del bolo alimenticio percibido por las madres de los pacientes durante la alimentación en el hogar mostró diferencia estadística significativa a favor de los pacientes con DOF.
La asociación de DOF con mayor severidad en la afectación de la función motora gruesa medida por el SCFMG propuesto por Palisano et al.14-15 encontrada en esta investigación también ha sido reportada por otros autores que documentaron DOF por cuestionarios19-21 y por investigadores que diagnosticaron DOF por VFS6,22,23.
En relación con el diagnóstico de DOF por cuestionarios, Calis et al.19, en los Países Bajos, en 166 niños de 2 a 19años de edad con PC nivelIV yV del SCFMG encontraron que el nivelV del SCFMG fue más frecuente en pacientes con mayor severidad de DOF (p<0.001); Parkes et al.20, en Irlanda del Norte, documentaron que los pacientes con nivelIV según el SCFMG tuvieron cerca de cinco veces más probabilidad de DOF (OR: 4.8, p<0.001), y con nivelV alrededor de 15 veces DOF (OR: 15.7, p<0.001), y Benfer et al.21, en Australia, reportaron una relación gradual de la severidad de DOF con el nivel de la afectación motora gruesa, y los niños en nivelV del SCFMG comparados con los de nivelI tuvieron cerca de 17 veces más probabilidades de tener DOF (OR: 17.9, p=0.036).
Asimismo, investigaciones que diagnosticaron DOF por VFS han documentado relación de la DOF con severidad en la afectación de la función motora: Kim et al.6, en Corea del Sur, encontraron alteraciones en las fases oral y faríngea de la deglución en el 20% de los sujetos en nivelI yII, en el 28.6% en nivelIII y en el 91.7% en los nivelesIV yV del SCFMG (p<0.001); Asgarshirazi et al.22, en Irán, hallaron que el 73% de los pacientes con nivelIV yV del SCFMG tuvieron síntomas importantes de DOF, en comparación con el 21% en los nivelesI yII (p<0.001); y Benfer et al.23, en Australia y Bangladesh, reportaron que la probabilidad de tener DOF fue cerca de 1.9-3.5 veces mayor con cada aumento en un nivel del SCFMG en niños de 18 a 36meses con PC de todos los grados.
Cabe comentar que, en relación con los estudios previos6,19,20,22, la edad de los sujetos de estudio fue semejante al de la presente investigación; solo Benfer et al.21,23 incluyeron pacientes de menor edad (18 a 36meses). Por su parte, la intensidad de la asociación de DOF diagnosticada por VFS con la mayor severidad de afectación de la función motora solo fue cuantificada por Benfer et al.23 (OR: 3.8; IC95%: 3.2-4.3), cifra menor a la encontrada en la presente investigación (OR: 5.7; IC95%: 1.8-17.5).
Las alteraciones en la fase oral de la deglución, en gran parte voluntarias, son por daño en las redes neuronales corticales y por problemas en la fase faríngea de la deglución debido a trastornos en los componentes automáticos de deglución; en ambas situaciones pueden surgir por daño cerebral subcortical y en los ganglios basales24, por lo que es probable que la asociación de la severidad de la DOF con mayores niveles de afectación de la función motora gruesa sea debida a que cuando existe un mayor daño neurológico por la PC también ocurre menor control de los movimientos voluntarios e involuntarios de los músculos bucofaciales y de la lengua.
La frecuencia de la dificultad del traslado del bolo alimenticio percibido por las madres de los pacientes durante la alimentación en el hogar (87% en los casos y 30% en los controles) documentada en esta investigación es superior a la reportada por otros investigadores6,12, que encontraron en los pacientes con DOF una frecuencia que va del 33 al 52%. Estas diferencias pueden ser debidas a las distintas maneras de recabar este dato y a la heterogeneidad de los distintos grados de severidad de la PC y de la DOF, entre otros factores.
Por la gravedad que representa la aspiración a la vía área, cabe resaltar que en este estudio el 87% de los pacientes con DOF presentaron dos o más signos de alteración a nivel faríngeo, lo que se traduce en una alta probabilidad de presentar este problema.
Los resultados de esta investigación son importantes debido a que, a nuestro conocimiento, en América Latina no existen estudios que en niños con PC investiguen factores asociados a DOF diagnosticada por VFS. Asimismo, el diseño de casos y controles permitió hacer grupos de estudio más parejos, medir mejor las diferencias de las frecuencias de variables entre los grupos de estudio y explorar la posible asociación de una variable dependiente con las variables independientes. Los trabajos realizados en otros países6,8,10-12,19-23 utilizaron estudios descriptivos y transversales.
Como limitaciones de esta investigación cabe mencionar que los datos clínicos percibidos por las madres de los pacientes se obtuvieron por medio de cuestionarios, como también ocurrió en algunos de los estudios revisados19-21; sin embargo, hubiese sido deseable haber obtenido videograbaciones de los momentos de la alimentación de los pacientes en casa. Asimismo, un mayor tamaño de muestra hubiera permitido analizar el efecto sobre la DOF de otros factores distintos al grado de afectación motora gruesa, que se presentaron con menor frecuencia, y de este modo poder medir su efecto sobre la DOF.
A pesar de las limitaciones mencionadas, el presente estudio permite concluir que existe asociación de la DOF documentada por VFS con mayor severidad en el grado de afectación motora gruesa, lo cual puede ser debido a la relación del mayor daño neurológico con el incremento de la alteración del control de los movimientos voluntarios e involuntarios de los músculos bucofaciales y de la lengua.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
AutoríaTodos los autores declaramos que cada uno ha cumplido con los requisitos de autoría y ha revisado y aprobado la última versión del trabajo.
Conflicto de interesesCada uno de todos los autores manifestamos que en la realización de la presente investigación en ningún caso existe conflicto de intereses.