La colitis ulcerosa crónica idiopática (CUCI) es una condición crónica caracterizada por una inflamación que afecta al colon. Para medir objetiva e integralmente la actividad de la enfermedad en pacientes con CUCI y en consecuencia optimizar el tratamiento farmacológico, se creó un nuevo índice integral de enfermedad que incluye las características clínicas, bioquímicas, endoscópicas e histológicas necesarias para lograr dicho fin. El objetivo del presente estudio fue validar el nuevo índice integral de enfermedad en pacientes con CUCI.
Materiales y métodosSe realizó un estudio de cohorte con un total de 222 pacientes con confirmaciones histológicas de CUCI. Las variables incluidas en el índice de enfermedad fueron: número de evacuaciones por día; valores de hemoglobina, proteína C-reactiva de alta sensibilidad y albúmina en suero; hallazgos endoscópicos e histológicos medidos por medio de las puntuaciones en las subescalas de puntuación de Mayo y Riley respectivamente. El análisis de datos fue realizado con el programa de estadística STATA SE 11.1.
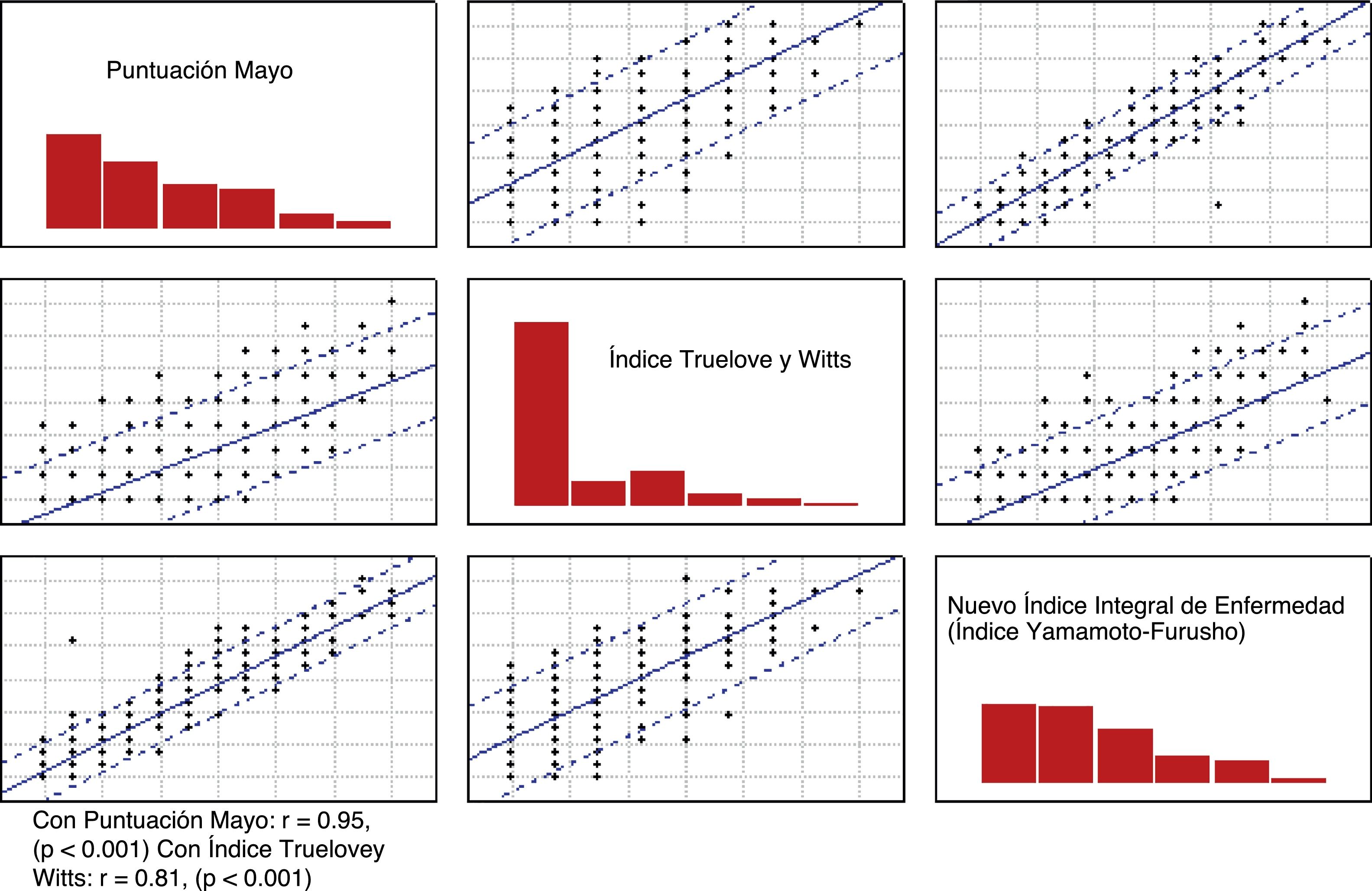
ResultadosLa correlación del nuevo índice de enfermedad fue muy bueno (r=0.817, p<0.001 con los criterios de Truelove y Witts y r=0.957, p <0.001 con puntuación de Mayo). Se encontró buena consistencia interna con un coeficiente de alfa de Cronbach de 0.78 y una media de correlación interelemento aceptable (r=0.47, p <0.05). La eficacia total del nuevo índice fue de 87.2% pacientes correctamente clasificados, con un área bajo la curva de 0.93, 0.92 y 0.96 respectivamente, de acuerdo a los tres escenarios descritos.
ConclusionesEl nuevo índice integral en enfermedad o índice Yamamoto-Furusho proporciona una visión integral de la actividad de la enfermedad en pacientes con CUCI y es útil para optimizar el tratamiento farmacológico.
Ulcerative colitis is a chronic condition characterized by inflammation affecting the colon. To objectively and integrally measure disease activity in patients with ulcerative colitis and thus optimize pharmacologic treatment, a novel integral disease index was created that includes the clinical, biochemical, endoscopic, and histologic characteristics necessary for achieving that task. The aim of the present study was to validate the novel integral disease index in patients with ulcerative colitis.
Materials and methodsA cohort study on a total of 222 patients with histologic confirmations of ulcerative colitis diagnosis was conducted. The variables included in the disease index were: number of bowel movements per day; values for hemoglobin, high-sensitivity C-reactive protein, and serum albumin; and endoscopic and histologic findings measured through the subscales of the Mayo and Riley scores, respectively. The data analysis was performed utilizing the STATA SE 11.1 statistics program.
ResultsThe correlation of the novel disease index was very good (r=0.817, p <.001 with the Truelove and Witts criteria and r=0.957, p <.0001 with the Mayo score, respectively). Good internal consistency was found with a Cronbach's alpha coefficient of 0.78 and an acceptable mean inter-item correlation (r=0.47, p <.05). The total efficacy of the novel index was 87.2% correctly classified patients, with an AUC according to the three scenarios described of 0.93, 0.92, and 0.96, respectively.
ConclusionsThe novel integral disease index (Yamamoto-Furusho Index) provides an integral view of disease activity in patients with ulcerative colitis and is useful for optimizing pharmacologic treatment.
La enfermedad inflamatoria intestinal (EII) es un grupo de enfermedades del tracto gastrointestinal que incluye la enfermedad de Crohn y la colitis ulcerosa crónica idiopática (CUCI)1. La etiología de la EII permanece desconocida, pero los pacientes con EII podrían presentar una respuesta inmune aberrante que ocurre generalmente en individuos susceptibles genéticamente como resultado de una compleja interacción de los factores ambientales, microbianos e inmunológicos2.
La CUCI es una condición inflamatoria crónica que causa una continua inflamación de mucosa del colon, usualmente sin presentar granulomas en biopsia. Afecta al recto y en diferente medida al colon, de manera continua, y se caracteriza por un curso de remisiones y exacerbaciones, con características clínicas, bioquímicas e histológicas heterogéneas. Un curso de enfermedad severo está relacionado con desenlaces pobres, como calidad de vida inferior, discapacidad y mortalidad, y también podría estar relacionado con costos de salud más altos3.
Los avances terapéuticos en el manejo médico han modificado las metas de tratamiento para la EII3. Las recomendaciones de los consensos para la práctica clínica y para la determinación de las metas de tratamiento (objetivo primario) en los estudios clínicos no solo buscan resolver la sintomatología, sino también la curación endoscópica de la mucosa. Sin embargo, estos resultados no necesariamente reflejan una enfermedad microscópica quiescente. La presencia persistente de inflamación microscópica en pacientes con CUCI ha sido asociada con una mayor tasa de recaída, hospitalización, colectomía y riesgo para el desarrollo de displasia y cáncer colorrectal2,4.
Es importante que el médico esté completamente consciente de la actividad de la enfermedad porque esto influye en las decisiones terapéuticas (si el tratamiento deberá ser oral, tópico o quirúrgico) y proporciona información valiosa sobre el riesgo de complicaciones y el pronóstico del paciente5. La actividad clínica de la enfermedad es un concepto complejo que se basa en herramientas de evaluación clinométricas que pueden ser convertidas a un marcador que puede ser utilizado objetivamente para predecir el riesgo para el paciente individual a través de variables obtenidas en una visita médica de rutina6. Sin embargo, la concordancia de la evaluación clínica utilizando resultados obtenidos con los índices actuales y los hallazgos obtenidos por medio de herramientas de diagnóstico objetivas como son los biomarcadores serológicos, colonoscopia e histología, puede ser pobre7. Se ha demostrado que la suma de esos parámetros mejora la estratificación de riesgo y la respuesta al tratamiento. Hace cincuenta años, Sidney Truelove describió un índice que incluía metas clínicas y bioquímicas en ensayos sobre CUCI8 y se convirtió en uno de los índices de mayor uso en la práctica clínica para medir la actividad de la enfermedad. Sin embargo, no incluye integralmente elementos importantes para describir la actividad de la enfermedad objetivamente, tales como los parámetros endoscópicos e histológicos, y no pasó por un proceso correcto de validación.
La evaluación objetiva de la actividad de la enfermedad es un prerrequisito importante para ensayos clínicos que midan la eficacia de nuevos fármacos o estrategias de tratamiento médico9. Al tiempo que se desarrollan nuevos objetivos para el manejo global de la CUCI; lo cual lleva a nuevas estrategias de tratamiento que buscan mejorar el control de la enfermedad, se hace esencial la disponibilidad de herramientas objetivas y de uso fácil para evaluar la actividad de la enfermedad y ayudar al clínico a tomar decisiones respecto al tratamiento. La actividad de la enfermedad en pacientes con CUCI debería ser evaluada de manera integral con parámetros clínicos, bioquímicos, histológicos y endoscópicos7,10. Sin embargo, los expertos están de acuerdo en que aún es necesario crear un índice que incluya la actividad histológica, en conjunto con los otros parámetros. Una mejor estrategia de clasificación podría mejorar las decisiones clínicas y los abordajes terapéuticos11.
El objetivo del presente estudio fue el de validar el nuevo índice integral de enfermedad (NIIE) o índice Yamamoto-Furusho, para medir la actividad en CUCI por medio de hallazgos clínicos, bioquímicos, endoscópicos e histopatológicos; y evaluar el desempeño general de diagnóstico del NIIE en pacientes mexicanos con CUCI.
Materiales y métodosSe realizó un estudio de cohorte que incluyó a 222 pacientes con un diagnóstico definitivo de CUCI confirmado por medio de histopatología. Se analizó un total de 546 evaluaciones en línea base y como mínimo en una visita de seguimiento por cada paciente. Todos los pacientes fueron atendidos en la Clínica de Enfermedad Inflamatoria Intestinal del Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán y fueron evaluados dentro de las fechas de enero del 2014 a julio del 2016. El diagnóstico de CUCI se basó en la historia médica (diarrea crónica con moco y heces sanguinolentas, pérdida de peso y dolor abdominal), hallazgos endoscópicos (úlceras, friabilidad de mucosa, pérdida de partón vascular y extensión), hallazgos histológicos (infiltrado linfoplasmocitario en lámina propia, criptitis, abscesos crípticos, destrucción y ulceración del patrón glandular) y los marcadores bioquímicos de velocidad de sedimentación globular (ESR por sus siglas en inglés), hemoglobina, proteína C-reactiva de alta sensibilidad (hs-CRP por sus siglas en inglés), albúmina en suero y cuenta de leucocitos y plaquetas. Los criterios de exclusión fueron: diagnóstico de colitis indeterminada, enfermedad de Crohn, pacientes de CUCI con proctocolectomía, infecciones concomitantes y pacientes con datos incompletos en los registros clínicos de al menos dos visitas a la clínica.
Medición de la actividad clínicaCada paciente fue evaluado al menos en dos ocasiones, utilizando el NIIE o Yamamoto-Furusho, la puntuación de Mayo12, y el índice Truelove y Witts8. La evaluación incluyó hallazgos clínicos, bioquímicos, colonoscópicos e histopatológicos. Todos los parámetros fueron medidos para evaluar la actividad de la enfermedad en un lapso de una semana. La puntuación de Mayo12 incluye cuatro componentes: 1) número de evacuaciones sobre la frecuencia normal; 2) presencia de sangrado rectal; 3) evaluación médica global y 4) apariencia endoscópica. El índice de severidad de Truelove y Witts incluye varios parámetros: 1) número de evacuaciones por día; 2) cantidad de sangrado rectal; 3) frecuencia cardiaca; 4) temperatura corporal; 5) severidad de la anemia y 6) velocidad de sedimentación globular (ESR).
Parámetros bioquímicosLos marcadores bioquímicos fueron determinados dentro de 7 días posteriores a la colonoscopia y la evaluación histopatológica para determinar la presencia de actividad de CUCI. Los biomarcadores utilizados fueron: hemoglobina (Hb), albúmina, hs-CRP, velocidad de sedimentación globular (ESR) y conteo de plaquetas y glóbulos blancos. Los resultados fueron evaluados durante al menos dos visitas de seguimiento en la clínica de EII.
Hallazgos endoscópicosTodas las colonoscopias fueron realizadas dentro de los 7 días previos a la evaluación después de que los participantes firmaron los consentimientos informados de acuerdo con la Declaración de Helsinki. Todos los pacientes recibieron preparación intestinal estándar con poletilenglicol (solución de lavado) anterior a la colonoscopia. Los hallazgos endoscópicos estuvieron basados en el submarcador endoscópico de la puntuación de Mayo13.
Evaluación histológica de CUCISe tomaron al menos dos biopsias de colon de 6 segmentos que incluyeron el ciego, el colon ascendente, el colon transverso, el colon descendente, el colon sigmoide y el recto. Cada biopsia fue evaluada de acuerdo al índice de Riley14,15, el cual se compone de 6 variables: 1) infiltración inflamatoria aguda (células polimorfonucleares en lámina propia); 2) infiltración inflamatoria crónica (infiltración linfocítica en lámina propia); 3) criptitis (abscesos); 4) pérdida de integridad epitelial; 5) depleción de mucinas y 6) irregularidades en la arquitectura de criptas. Cada variable es graduada en una escala de 4 puntos (sin actividad, leve, moderada y severa) y el resultado es un promedio de dos evaluaciones realizadas por observadores independientes.
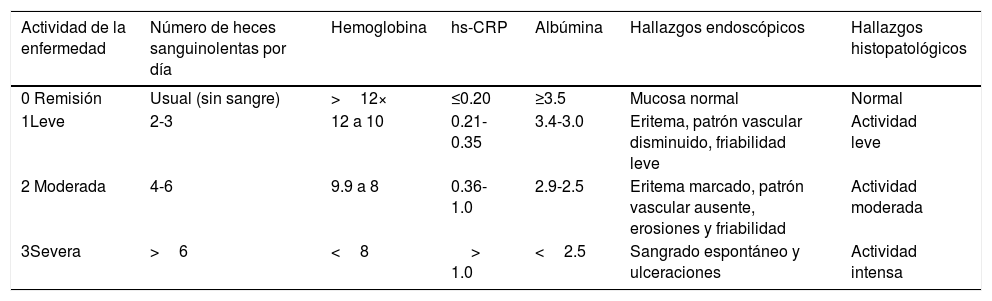
El nuevo índice integral de enfermedad de actividad de colitis ulcerosa crónica idiopática (NIIE) o índice Yamamoto-FurushoEl NIIE, o índice Yamamoto-Furusho, toma en consideración seis categorías: 1) el número de evacuaciones sanguinolentas por día; 2) hemoglobina; 3) proteína C-reactiva de alta sensibilidad; 4) albúmina; 5) hallazgos endoscópicos y 6) hallazgos histológicos. Cada variable es medida en una escala de 0 a 3 puntos como se muestra en la tabla 1. El rango en el NIIE (índice Yamamoto-Furusho) va de 0 a 18 puntos y se distribuye en cuatro categorías: 1) remisión (0 a 3 puntos); 2) actividad leve (4 a 6 puntos); 3) actividad moderada (7 a 12 puntos) y 4) actividad severa (13 a 18 puntos).
Nuevo índice integral de enfermedad para actividad en CU (NIIE) o índice Yamamoto-Furusho
| Actividad de la enfermedad | Número de heces sanguinolentas por día | Hemoglobina | hs-CRP | Albúmina | Hallazgos endoscópicos | Hallazgos histopatológicos |
|---|---|---|---|---|---|---|
| 0 Remisión | Usual (sin sangre) | >12× | ≤0.20 | ≥3.5 | Mucosa normal | Normal |
| 1Leve | 2-3 | 12 a 10 | 0.21- 0.35 | 3.4-3.0 | Eritema, patrón vascular disminuido, friabilidad leve | Actividad leve |
| 2 Moderada | 4-6 | 9.9 a 8 | 0.36-1.0 | 2.9-2.5 | Eritema marcado, patrón vascular ausente, erosiones y friabilidad | Actividad moderada |
| 3Severa | >6 | <8 | > 1.0 | <2.5 | Sangrado espontáneo y ulceraciones | Actividad intensa |
Se realizó un análisis descriptivo de las variables demográficas y clínicas. Se establecieron correlaciones con el coeficiente de Pearson entre el NIIE (índice Yamamoto-Furusho) y tanto el índice Truelove y Witts como la puntuación de Mayo. Los análisis de validación y confiabilidad fueron llevados a cabo utilizando el análisis de componente principal y el coeficiente de alfa de Cronbach para consistencia interna y el promedio de correlación de los elementos individuales. Finalmente, probamos y comparamos todos los resultados de los índices con un análisis basado en característica operativa del receptor (ROC por sus siglas en inglés) para definir su sensibilidad, especificidad, valor predictivo positivo (VPP), valor predictivo negativo (VPN), tasa de verosimilitud positiva (TV+), tasa de verosimilitud negativa (TV-) y área bajo la curva ROC, con intervalos de confianza de 95%. Evaluamos el desempeño del NIIE (índice Yamamoto-Furusho) en escenarios clínicos severos y el espectro de la enfermedad se enfocó en enfermedad grave de acuerdo con los hallazgos histopatológicos, los cuales fueron utilizados como estándar de oro.
Clasificamos nuestros hallazgos de acuerdo con tres escenarios posibles de actividad severa definida de la siguiente manera: 1) actividad severa definida solo por hallazgos colonoscópicos, 2) actividad severa definida solo por hallazgos histopatológicos y 3) actividad severa definida solo cuando ambas condiciones estuvieron presentes. El desempeño de elementos individuales también fue puesto a prueba. La respuesta del NIIE fue evaluada por medio de la sensibilidad al cambio en las 3 evaluaciones realizadas por cada paciente, utilizando t de Student para muestras apareadas y el análisis test-retest para evaluar el coeficiente de correlación interclase.
Consideramos un nivel de valor de p de dos colas de <0.05 para todas las pruebas de hipótesis. El análisis estadístico fue realizado utilizando el software STATA SE 11.1.
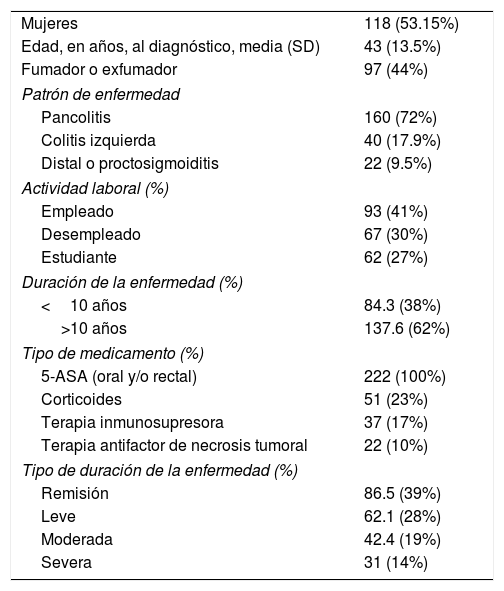
ResultadosCaracterísticas demográficas y de línea baseIncluimos los datos obtenidos de 546 evaluaciones iniciales y de seguimiento de 222 pacientes mexicanos con diagnóstico definitivo de CUCI. Las características clínicas y demográficas se muestran en la tabla 2.
Resumen de características demográficas y de línea base (n=222)
| Mujeres | 118 (53.15%) |
| Edad, en años, al diagnóstico, media (SD) | 43 (13.5%) |
| Fumador o exfumador | 97 (44%) |
| Patrón de enfermedad | |
| Pancolitis | 160 (72%) |
| Colitis izquierda | 40 (17.9%) |
| Distal o proctosigmoiditis | 22 (9.5%) |
| Actividad laboral (%) | |
| Empleado | 93 (41%) |
| Desempleado | 67 (30%) |
| Estudiante | 62 (27%) |
| Duración de la enfermedad (%) | |
| <10 años | 84.3 (38%) |
| >10 años | 137.6 (62%) |
| Tipo de medicamento (%) | |
| 5-ASA (oral y/o rectal) | 222 (100%) |
| Corticoides | 51 (23%) |
| Terapia inmunosupresora | 37 (17%) |
| Terapia antifactor de necrosis tumoral | 22 (10%) |
| Tipo de duración de la enfermedad (%) | |
| Remisión | 86.5 (39%) |
| Leve | 62.1 (28%) |
| Moderada | 42.4 (19%) |
| Severa | 31 (14%) |
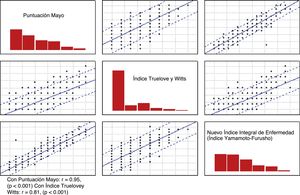
Se evaluó la correlación del NIIE (índice Yamamoto-Furusho) con el índice Truelove y Witts y la puntuación total de Mayo (r=0.817, p <0.001 y r=0.957, p <0.001 respectivamente) como se muestra en la figura 1.
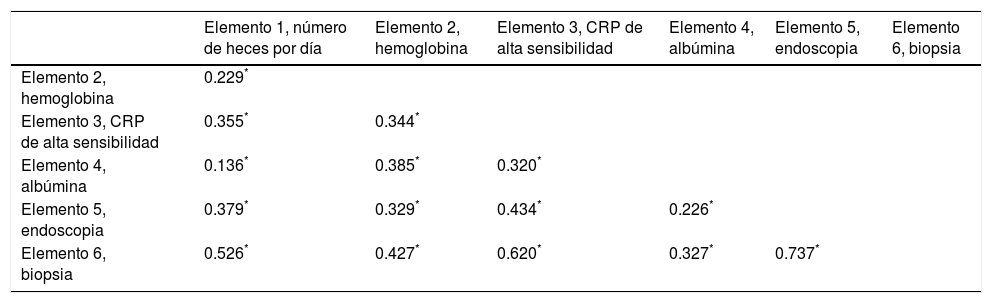
Análisis de validación de los elementos y desarrollo del NIIEEl análisis del componente principal de los seis elementos incluidos en el NIIE (índice Yamamoto-Furusho) reveló una probable escala unidimensional, con 49.9% de la varianza explicada por un único componente. Se observó una adecuada consistencia interna con alfa de Cronbach de 0.78 y una correlación de promedio interelemento aceptable (r=0.47, p <0.05). La matriz de correlación se muestra en la tabla 3. Decidimos conservar todos los elementos incluidos en nuestro índice, ya que la corrección mínima para el alfa de Cronbach fue 0.02 cuando no se retiró ningún ítem elemento.
Matriz de correlación interelementos
| Elemento 1, número de heces por día | Elemento 2, hemoglobina | Elemento 3, CRP de alta sensibilidad | Elemento 4, albúmina | Elemento 5, endoscopia | Elemento 6, biopsia | |
|---|---|---|---|---|---|---|
| Elemento 2, hemoglobina | 0.229* | |||||
| Elemento 3, CRP de alta sensibilidad | 0.355* | 0.344* | ||||
| Elemento 4, albúmina | 0.136* | 0.385* | 0.320* | |||
| Elemento 5, endoscopia | 0.379* | 0.329* | 0.434* | 0.226* | ||
| Elemento 6, biopsia | 0.526* | 0.427* | 0.620* | 0.327* | 0.737* |
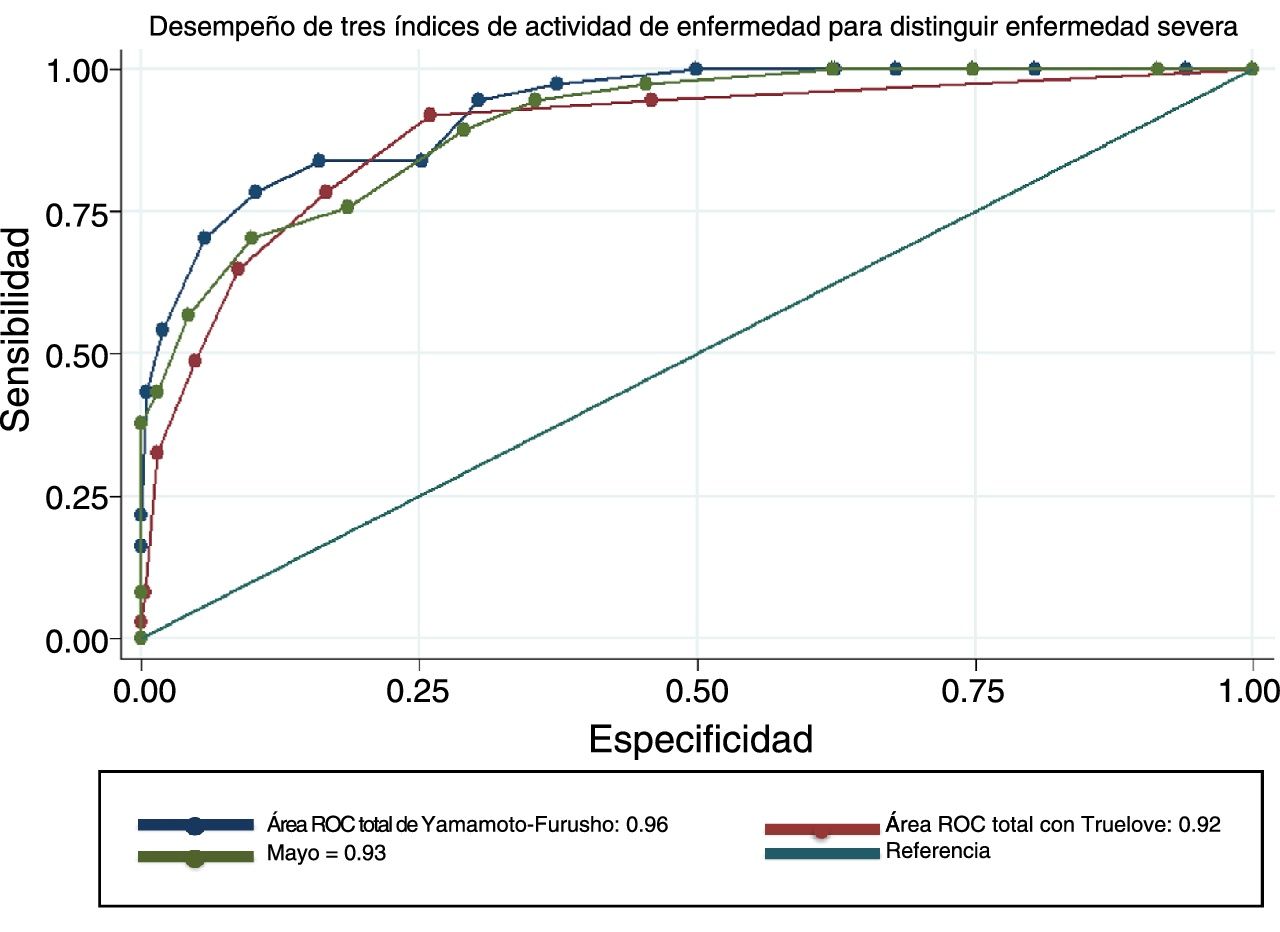
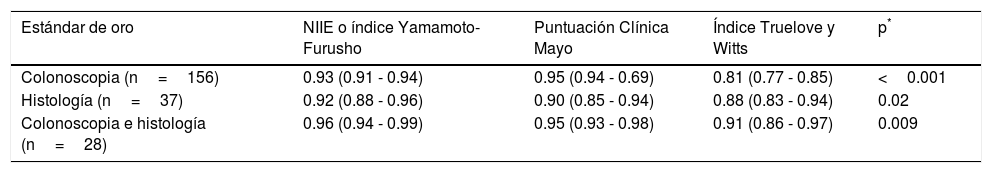
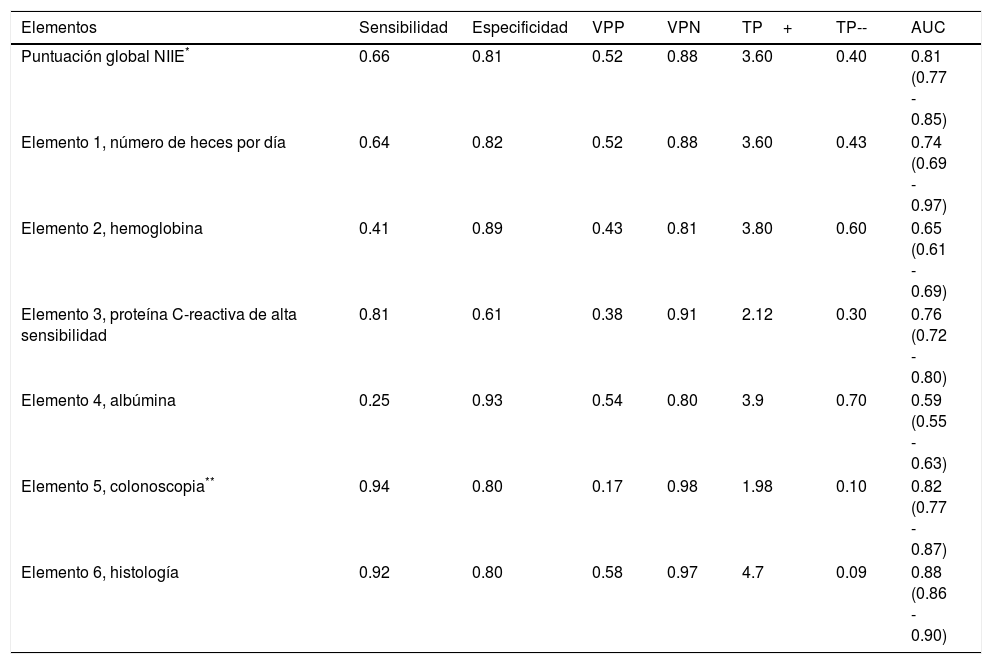
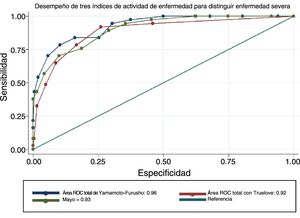
La eficacia general del NIIE (índice Yamamoto-Furusho) fue de 87.2% de los pacientes clasificados correctamente. El AUC de acuerdo a los tres escenarios descritos fue de 0.93, 0.92 y 0.96 respectivamente. Los resultados de comparación entre las tres puntuaciones fueron similares, pero la puntuación que propusimos mostró un mejor desempeño respecto a las definiciones de severidad histológicas y endoscópicas, con un AUC=0.96, como se muestra en la figura 2, en comparación con Truelove y Witts y la puntuación total de Mayo, cuyas AUC fueron 0.95 y 0.91 respectivamente (p=0.0009). Todos los elementos analizados tuvieron una buena capacidad discriminatoria con un rango de especificidad entre 0.61 y 0.93 y un rango de sensibilidad de 0.25 a 0.94. El elemento más preciso fue el parámetro histopatológico, produciendo un AUC de 0.88. La comparación en detalle se muestra en las tablas 4 y 5.
Desempeño de la puntuación de actividad en la detección de enfermedad severa definida en varios escenarios clínicos
| Estándar de oro | NIIE o índice Yamamoto-Furusho | Puntuación Clínica Mayo | Índice Truelove y Witts | p* |
|---|---|---|---|---|
| Colonoscopia (n=156) | 0.93 (0.91 - 0.94) | 0.95 (0.94 - 0.69) | 0.81 (0.77 - 0.85) | <0.001 |
| Histología (n=37) | 0.92 (0.88 - 0.96) | 0.90 (0.85 - 0.94) | 0.88 (0.83 - 0.94) | 0.02 |
| Colonoscopia e histología (n=28) | 0.96 (0.94 - 0.99) | 0.95 (0.93 - 0.98) | 0.91 (0.86 - 0.97) | 0.009 |
Desempeño del NIIE o índice Yamamoto-Furusho y sus elementos individuales para distinguir actividad severa
| Elementos | Sensibilidad | Especificidad | VPP | VPN | TP+ | TP-- | AUC |
|---|---|---|---|---|---|---|---|
| Puntuación global NIIE* | 0.66 | 0.81 | 0.52 | 0.88 | 3.60 | 0.40 | 0.81 (0.77 - 0.85) |
| Elemento 1, número de heces por día | 0.64 | 0.82 | 0.52 | 0.88 | 3.60 | 0.43 | 0.74 (0.69 - 0.97) |
| Elemento 2, hemoglobina | 0.41 | 0.89 | 0.43 | 0.81 | 3.80 | 0.60 | 0.65 (0.61 - 0.69) |
| Elemento 3, proteína C-reactiva de alta sensibilidad | 0.81 | 0.61 | 0.38 | 0.91 | 2.12 | 0.30 | 0.76 (0.72 - 0.80) |
| Elemento 4, albúmina | 0.25 | 0.93 | 0.54 | 0.80 | 3.9 | 0.70 | 0.59 (0.55 - 0.63) |
| Elemento 5, colonoscopia** | 0.94 | 0.80 | 0.17 | 0.98 | 1.98 | 0.10 | 0.82 (0.77 - 0.87) |
| Elemento 6, histología | 0.92 | 0.80 | 0.58 | 0.97 | 4.7 | 0.09 | 0.88 (0.86 - 0.90) |
AUC: área bajo la curva; VPN: valor predictivo negativo; VPP: valor predictivo positivo; TV+: tasa de verosimilitud positiva, TV-: tasa de verosimilitud negativa.
Para medir la respuesta por medio de sensibilidad al cambio, comparamos la primera medición, tanto con la segunda medición como con la tercera. En la comparación de la primera medición con la segunda medición la sensibilidad al cambio fue -0.7 (OF=3.5, p <0.05) y en la comparación de la primera medición con la tercera, la sensibilidad al cambio fue de -1.2 (OF=4.4, p=0.027). El coeficiente de correlación interclase de la primera medición contra la segunda medición fue 0.640 (95% CI=0.52-0.73, p <0.05).
DiscusiónHasta donde llega nuestro conocimiento, el presente estudio proporciona la primera validación de un índice integral para evaluar el grado de actividad de enfermedad en pacientes mexicanos con CUCI, que incluya características clínicas, bioquímicas, endoscópicas e histopatológicas. Las escalas anteriores no han sido validadas formalmente8,12,16 debido a los diseños metodológicos de ensayo clínico que se utilizaron, y en consecuencia no pasaron por un proceso de validación. De la misma manera, la mayoría de las escalas no incluyen todas las variables para cuantificar la actividad de CUCI (clínica, bioquímica, endoscópica e histopatológica)17. Es importante mencionar que la mayoría de ellas fueron desarrolladas solo como parte de la evaluación en ensayos clínicos y no con el propósito de evaluar y validar un instrumento que específicamente midiera la actividad de la enfermedad. En consecuencia, los índices no fueron estudiados cabalmente en el contexto clínico de la práctica clínica cotidiana18.
Es esencial tener resultados validados de CUCI disponibles para proporcionarles a los gastroenterólogos una evaluación global y objetiva que incluya parámetros clínicos, bioquímicos, endoscópicos e histológicos. Como se mencionó previamente, existen numerosos índices de actividad que se utilizan rutinariamente para clasificar pacientes de acuerdo a la actividad de la enfermedad. Ejemplos de estos son el índice Truelove y Witts8, la puntuación Mayo12, el índice Rachmilewitz19, el índice Lichtiger20, el índice Seo16, el índice Montreal21 y el índice de actividad de colitis ulcerosa pediátrica22, entre otros, pero ninguno de ellos incluye la histología como un componente de su índice de evaluación.
El NIIE (índice Yamamoto-Furusho) tiene una ventaja sobre las otras puntuaciones porque proporciona una evaluación global y objetiva de la actividad de la enfermedad que incluye aspectos clínicos, bioquímicos, endoscópicos e histológicos en pacientes con CUCI. Dicho índice integral ayuda a diferenciar y clasificar objetivamente la actividad de la enfermedad lo que ayuda a optimizar el tratamiento médico. Decidimos comparar el NIIE (índice Yamamoto-Furusho) con el índice Truelove y Witts8 y la puntuación de Mayo12 porque son los dos índices de uso más común en la práctica clínica y en ensayos. Sin embargo, la puntuación Mayo solo utiliza parámetros clínicos y endoscópicos y el índice Truelove y Witts solamente evalúa aspectos clínicos y bioquímicos.
La ventaja del NIIE (índice Yamamoto-Furusho) es su evaluación objetiva de la CUCI, la cual incluye evaluación histológica, además de hallazgos clínicos, bioquímicos y endoscópicos. Recientemente se ha descrito la importancia de la actividad histológica en la evaluación de pacientes con CUCI en relación con la predicción de riesgo de recaída a los 6 meses, un peor pronóstico y el verdadero grado de actividad de CUCI23–24.
Basados en la necesidad de tener una evaluación que incluyera las cuatro áreas para evaluar objetivamente a los pacientes, decidimos y diseñamos las variables que serían incluidas en el NIIE (índice Yamamoto-Furusho). La correlación de nuestro índice integral, en comparación con Truelove y Witts8 y la puntuación de Mayo12, fue altamente significativa (r=0.817, p <0.001 y r=0.957, p <0.001 respectivamente) utilizando la evaluación histológica como el estándar de oro25. Con relación a la puntuación de Mayo, obtuvimos una correlación cercana a 1, lo cual fue muy bueno para la clasificación de pacientes en estado de remisión, o con actividad de enfermedad ligera, moderada o severa (r=0.95).
El impacto de agregar la evaluación endoscópica ha sido demostrado, en comparación con índices simples que solo evalúan síntomas y señas. En un estudio realizado por Osada et al.9, reportaron una correlación positiva significativa entre los resultados endoscópicos e histológicos (r=0.738), actividad clínica y resultados endoscópicos (r=0.444) y resultados clínicos e histológicos (r=0.557) concluyendo que una colonoscopia total puede ser indicada cuando CRP o ESR están elevados en pacientes con CUCI en remisión clínica.
En el presente estudio, el NIIE (índice Yamamoto-Furusho) correlacionó muy bien (r=0.767, p <0.001) con la actividad endoscópica de CUCI. La mayoría de los índices endoscópicos que se utilizan en la práctica clínica o en los ensayos clínicos, tales como la puntuación del índice de severidad endoscópica en colitis ulcerosa26, la puntuación Baron27, el índice de severidad colonoscópica en colitis ulcerosa28, el índice endoscópico Rachmilewitz19, el índice Sutherland29, la puntuación Matts30 y el índice Blackstone31, comparten variables endoscópicas similares.
En nuestro estudio, decidimos incluir la actividad histológica como un estándar de oro10,24 porque fue la única variable que demostró con mayor precisión la actividad de la enfermedad (r=0.954, p <0.001). La adición de dicho parámetro, el cual no se incluye en ningún otro índice, permite una mejor estimación de la actividad de la enfermedad, en comparación con otros índices que subestiman la severidad de la CUCI. Esto es especialmente cierto si el resultado de los hallazgos endoscópicos encubre el grado de actividad como «Mayo 0», en el caso de los índices que incluyen un índice subendoscópico, o peor aún, uno no invasivo.
Consideramos a la hs-CRP como una variable porque mostró una buena correlación con la actividad histológica en pacientes con CUCI32–34. Finalmente, la severidad de anemia fue tomada en consideración en el NIIE (índice Yamamoto-Furusho) porque refleja de manera objetiva la pérdida sistemática de sangre en el paciente con CUCI35–37.
La Administración de Alimentos y Fármacos (FDA, por sus siglas en inglés) inició una evaluación de índices compuestos en ensayos clínicos y propuso que existiera guía por parte de la industria para el desarrollo de resultados relacionados al paciente (PRO por sus siglas en inglés) y medidas PRO (PROM por sus siglas en inglés)38 para cuantificar las percepciones de los pacientes de su propio estado funcional y bienestar. Un PRO es cualquier reporte que viene directamente de un paciente respecto a su salud o a su tratamiento sin interpretación de la respuesta del paciente por parte de un clínico o de alguien más. Sin embargo, existe consenso respecto a que el grado de inflamación debería ser medido utilizando instrumentos objetivos tales como la endoscopia, histología y/o imágenes de corte transversal. Es necesario correlacionar los hallazgos del examen físico y de los estudios endoscópicos y de laboratorio para poder hacer modificaciones al tratamiento. La utilización de PROM puede ser una herramienta de apoyo para obtener conocimiento de la percepción que tiene el paciente del tratamiento, pero nunca para llegar a conclusiones absolutas acerca de la actividad de la enfermedad basados solamente en desenlaces clínicos. El objetivo del NIIE fue crear una escala integral de actividad de la enfermedad para pacientes diagnosticados con CUCI, medida a través del análisis global de las herramientas objetivas de los parámetros clínicos, histológicos, endoscópicos y bioquímicos, y de esta forma lograr un abordaje más preciso a la actividad de la enfermedad.
ConclusiónEl NIIE o índice Yamamoto-Furusho proporciona una evaluación objetiva e integral de la actividad de la enfermedad que incluye parámetros clínicos, bioquímicos, endoscópicos e histopatológicos en pacientes mexicanos con CUCI. Es probable que el NIIE (índice Yamamoto-Furusho) pueda optimizar el tratamiento médico en pacientes que no presentan evidencia clínica de actividad de la enfermedad, pero que presentan actividad bioquímica, endoscópica e histopatológica en CUCI.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo respecto a la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que cuentan con el consentimiento informado de los pacientes.
FinanciaciónNo se recibió patrocinio de ningún tipo para llevar a cabo este artículo.
Conflicto de interesesEl Dr. Jesús Kazuo Yamamoto Furusho es un ponente, líder de opinión y miembro de comités directivos de asesoría para los siguientes laboratorios nacionales e internacionales: Abbvie, Ferring, Hospira, Janssen, Pfizer y Takeda. Ha sido ponente con Almirall, Danone, Farmasa, Grunenthal, y laboratorios UCB. Él es o ha sido un investigador líder en proyectos internacionales con Abbvie, Allergan, Bristol, Ferring, Pfizer, Roche, Shire y laboratorios Takeda. Actualmente es el presidente de la Organización Panamericana de Crohn y Colitis (PANCCO por sus siglas en inglés).
Los autores K.E. Bozada-Gutiérrez, A. Sánchez-Rodríguez, F. Bojalil-Romano, R. Barreto-Zuñiga, y B. Martínez-Benitez declaran no tener ningún conflicto de intereses.